红外吸收光谱
红外吸收光谱原理

红外吸收光谱原理
红外吸收光谱原理是一种分析技术,用于研究物质的结构、组成和化学性质。
它基于物质分子对红外光的吸收特性进行分析。
红外光谱是由红外辐射区域的电磁波组成的。
红外光的频率范围通常从1×10^12 Hz到3×10^14 Hz,对应的波长范围从0.8
微米到1000微米。
物质分子在这个频率范围内对特定波长的
红外光有吸收的能力,这与分子结构和化学键的特性有关。
原理上,红外吸收光谱是通过测量红外光通过待测物质后的强度变化来进行的。
当红外光通过物质时,分子会吸收与其振动和转动相对应的能量。
物质中的不同化学键和功能团会产生不同的吸收峰,这样就能通过红外光谱图谱来确定物质的结构和组成。
红外光谱仪通常由光源、样品室、光谱仪和检测器组成。
光源产生红外光束,经过样品室后,光束中的红外光被样品吸收或透射,然后进入光谱仪。
光谱仪将红外光根据其波长分解成不同的频率,并将其转换为电信号。
最后,检测器测量电信号的强度,形成红外光谱图。
红外吸收光谱原理的优势在于其非破坏性和高分辨率的特点。
它可以应用于各种领域,如化学、材料科学、生物科学等。
通过对物质的红外吸收光谱进行分析,可以快速得到物质的结构信息和组成成分,为研究和实际应用提供有价值的信息。
红外吸收光谱的原理及应用

红外吸收光谱的原理及应用一、红外吸收光谱的原理红外吸收光谱(Infrared Absorption Spectroscopy)是一种常见的光谱分析技术,它利用物质分子对红外辐射的吸收特性进行分析和研究。
红外光谱的原理基于分子的振动和转动引起的能量变化。
在红外辐射的作用下,分子会吸收特定波长或频率的光,从而发生能级跃迁并产生吸收峰。
根据不同的吸收峰位置和强度,可以推断物质的结构、组成和化学环境等信息。
红外吸收光谱的原理主要包括以下几个方面: 1. 分子的振动和转动:分子在吸收红外辐射时,会发生振动和转动。
振动包括拉伸、弯曲和扭转等不同形式,每个分子都有特定的振动模式和频率,使其能够吸收不同波长的红外辐射。
2. 分子吸收特定波长的光:分子在特定波长范围内吸收红外辐射,产生吸收峰。
根据吸收峰的位置和强度,可以确定分子的化学键、官能团和分子结构等信息。
3. 光谱图的解读:通过测量物质对红外辐射的吸收情况,可以得到红外光谱图。
光谱图通常以波数为横轴,吸收峰强度为纵轴,常用峰位和峰形进行分析和判断。
二、红外吸收光谱的应用红外吸收光谱具有广泛的应用领域,主要包括以下几个方面:1. 化学分析红外光谱在化学分析中起着重要作用,可以用于鉴定和分析各种有机和无机化合物。
通过测量样品的红外光谱,可以获得化学键和官能团的信息,从而判断物质的结构和组成。
红外光谱被广泛应用于有机化学、药物分析、环境监测等领域。
2. 药物研发红外光谱在药物研发中具有重要的应用价值。
通过红外光谱分析药物的结构和成分,可以判断药物的稳定性、纯度和相态等性质。
红外光谱还可以用于药物的质量控制和检验,确保药物的安全有效。
3. 材料科学在材料科学领域,红外光谱可以用于材料的表征和分析。
不同材料的红外光谱具有独特的特征,可以用于识别和鉴别材料,评估材料的结构、质量和性能。
红外光谱被广泛应用于聚合物材料、无机材料、涂层材料等领域。
4. 生物医学研究红外光谱在生物医学研究中有着重要的应用。
红外吸收光谱产生的条件
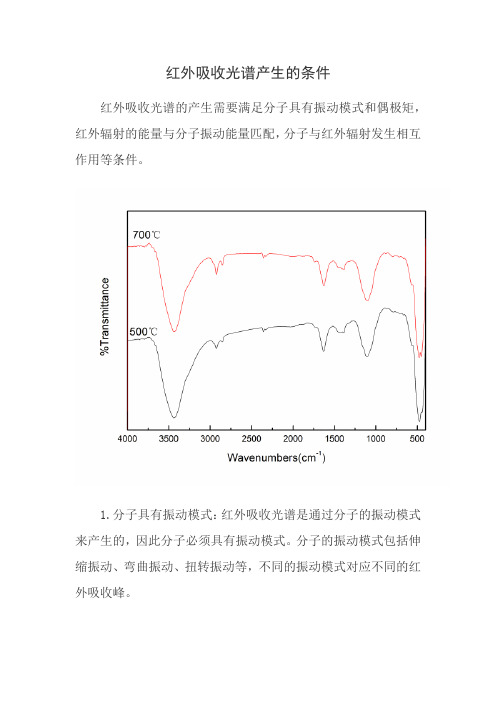
红外吸收光谱产生的条件
红外吸收光谱的产生需要满足分子具有振动模式和偶极矩,红外辐射的能量与分子振动能量匹配,分子与红外辐射发生相互作用等条件。
1.分子具有振动模式:红外吸收光谱是通过分子的振动模式来产生的,因此分子必须具有振动模式。
分子的振动模式包括伸缩振动、弯曲振动、扭转振动等,不同的振动模式对应不同的红外吸收峰。
2.分子具有偶极矩:红外吸收光谱是通过分子的偶极矩来产生的,因此分子必须具有偶极矩。
偶极矩是由分子中正负电荷分布不均引起的,具有偶极矩的分子可以吸收红外辐射。
3.红外辐射的能量与分子振动能量匹配:红外辐射的能量与分子振动能量之间必须存在匹配关系,才能产生红外吸收光谱。
红外辐射的能量通常在4000-400 cm-1范围内,对应着分子的不同振动模式。
4.分子与红外辐射的相互作用:分子必须与红外辐射发生相互作用,才能产生红外吸收光谱。
分子与红外辐射的相互作用通常是通过分子中的振动模式来实现的,分子吸收红外辐射后,分子的振动模式发生变化,产生红外吸收峰。
红外吸收光谱

迈克尔逊干涉仪
吸收池
分 束 器
干涉图 检测器
傅里叶变换
红外吸收光谱 图
数据处理 仪器控制
压片法
光散射现象较严重
KCl、KBr在加压下呈现所谓冷胀现象并变为可塑物,在中红外光区 完全透明,因此常用作固体样品的稀释剂。
稀释剂的比例:样品/稀释剂≈ 1/100
稀释剂的要求:纯度高、粒度小于2.5μm、不含水分。
在测定样品前,常用此红外来进行仪器校正。
红外吸收的基本原理
一、红外光谱的形成、条件和分子的运动 1、红外光谱的形成和产生条件 当一定波长的红外光照射样品时,如果分子中某个基团 的振动频率和它的一样,二者就会发生共振,此时光的能量 通过分子偶极距的变化传递给分子,这个基团就会吸收该频 率的红外光而发生振动能级的跃迁,产生红外吸收峰。 物质吸收红外光发生振动和转动能级的跃迁须满足两个 条件: (1)红外辐射光量子具有的能量等于分子振动能级的 能量差; (2)分子振动时,偶极距的大小和方向必须有一定的 变化。
两个基团相邻且振动基频相差不大时会产生振动耦合,振动耦 合引起的吸收频率称为耦合频率。耦合频率偏离基频,一个移向高 频,一个移向低频。
(c)费米共振 红外基频和倍频,还有组合频。 组合频为基频及倍频的和或差。即 v1 + v2、 2v1 + v2、 v1 - v2等。 费米共振:当一个振动的倍频或组合频与某一个强的基 频有接近的频率时,这两个振动相互作用发生偶合,弱的倍 频或组合频被强化,振动偶合后出现两个谱带。 两谱带中均含有基频和倍频的成份,倍频和组合频明显 被加强,这种现象叫费米共振。 费米共振是普遍现象,它不仅存在于红外光谱中,也存 在于拉曼光谱中。
红外吸收光谱图 中的假谱带:
红外光谱吸收

第六章红外吸收光谱法基本要点:1.红外光谱分析基本原理;2.红外光谱与有机化合物结构;3.各类化合物的特征基团频率;4.红外光谱的应用;5.红外光谱仪.学时安排:3学时第一节概述分子的振动能量比转动能量大,当发生振动能级跃迁时,不可避免地伴随有转动能级的跃迁,所以无法测量纯粹的振动光谱,而只能得到分子的振动-转动光谱,这种光谱称为红外吸收光谱。
红外吸收光谱也是一种分子吸收光谱。
当样品受到频率连续变化的红外光照射时,分子吸收了某些频率的辐射,并由其振动或转动运动引起偶极矩的净变化,产生分子振动和转动能级从基态到激发态的跃迁,使相应于这些吸收区域的透射光强度减弱。
记录红外光的百分透射比与波数或波长关系曲线,就得到红外光谱。
一、红外光区的划分红外光谱在可见光区和微波光区之间,波长范围约为0.75 ~ 1000µm,根据仪器技术和应用不同,习惯上又将红外光区分为三个区:近红外光区(0.75 ~ 2.5µm),中红外光区(2.5 ~25µm ),远红外光区(25 ~ 1000µm)。
近红外光区(0.75 ~ 2.5µm)近红外光区的吸收带主要是由低能电子跃迁、含氢原子团(如O—H、N—H、C—H)伸缩振动的倍频吸收等产生的。
该区的光谱可用来研究稀土和其它过渡金属离子的化合物,并适用于水、醇、某些高分子化合物以及含氢原子团化合物的定量分析。
中红外光区(2.5 ~ 25µm)绝大多数有机化合物和无机离子的基频吸收带出现在该光区。
由于基频振动是红外光谱中吸收最强的振动,所以该区最适于进行红外光谱的定性和定量分析。
同时,由于中红外光谱仪最为成熟、简单,而且目前已积累了该区大量的数据资料,因此它是应用极为广泛的光谱区。
通常,中红外光谱法又简称为红外光谱法。
远红外光区(25 ~1000µm)该区的吸收带主要是由气体分子中的纯转动跃迁、振动-转动跃迁、液体和固体中重原子的伸缩振动、某些变角振动、骨架振动以及晶体中的晶格振动所引起的。
红外吸收光谱分析法

红外吸收光谱分析法
一、红外吸收光谱分析法概述
红外吸收光谱分析法是一种利用物质的红外光吸收能力来探测它们的物质组成的技术。
它特别适用于有机化合物和无机化合物的光谱分析。
通过分析红外吸收光谱,可以检测物质中的有机键、C-H键、C-O键或N-H 键的存在和位置,从而鉴定出物质的化学结构和性质。
红外光吸收法的原理是,物质中的分子、晶体或其他结构会在不同的波长处吸收光,产生光谱,这些吸收光谱是物质的独特特征,反映出物质的特性。
根据这种特性,分析用不同波长的光照射样品,并从所得到的光谱中提取出电子激发、分子振动等信息,从而得到物质的结构和性质。
二、红外吸收光谱分析法基本原理
红外吸收光谱分析法的原理是,当物质受到红外幅射的照射时,它的分子会产生振动和旋转,这些振动和旋转的能量会转化为更高能量的电子跃迁。
这些电子跃迁会引起物质材料吸收一些具有特定波长的红外光,从而产生在不同波长的吸收光谱,通过分析这些吸收光谱,就可以求取物质分子的结构和性质。
红外吸收光谱
第三章红外吸收光谱(Infrared Absorption Spectroscopy)3.1 概述红外光谱又称为分子振动光谱或分子振转光谱1、特点:特征性强,适应范围广。
有机、无机、高分子化合物;固态、液态、气态样品都可以进行测定红外分为三个区域,近红外区(0.76μm~2.5μm,12820~4000cm-1)、中红外区(2.5μm~25μm, 4000~400cm-1)和远红外区(25μm~1000μm, 400~33cm-1)。
绝大多数有机化合物的基团震动频率处于中红外区。
2、表示方法:红外光谱多用透光率T%为纵坐标,表示吸收强度,以波数ζ(cm-1)为横坐标,表示吸收峰的位置。
也有用吸光度A为纵坐标,出反峰。
波数是频率的一种表示方法(每厘米长的光波中的波的数目)ζ(cm-1)=波数(cm-1)=1/波长(λcm)=104/波长(μm)=1/λ(cm);ζ·λ=1cm 3、红外光谱产生的基本条件1)E红外光=△E分子振动或υ红外光=υ分子振动2)分子振动时其偶极矩(μ)必须发生变化,即△μ≠0,μ=δr3.2 红外光谱与分子结构的关系3.2.1分子的振动形式*基频:分为两大类:伸缩振动和弯曲(变型)振动。
用υs表示对称伸缩,用υas 表示不对称伸缩,δ表示面内弯曲振动,γ表示面外弯曲振动。
以亚甲基为例:此外,还有一些其它的振动吸收峰存在:*倍频:由振动能级基态跃迁到第二,第三激发态时所产生的,不是整数倍。
*组合频:一种频率红外光,同时被两个振动所吸收。
倍频和组合频统称为泛频,在谱图中均显示为弱峰。
*振动偶合:当相同的两个基团相邻,且振动频率相近时,会发生振动偶合裂分,成为两个峰。
*费米共振:基频与泛频之间发生的振动偶合。
当泛频峰与某基峰相近时,发生相互作用,使原来很弱的泛频吸收峰增强。
图3-12费米共振和倍频。
3.2.2 红外光谱的分区(1)基团结构与振动频率的关系表3-1 基团振动频率与化学键力常数的关系(化学键种类)基团化学键力常数(K/N·cm-1) 键长(Â)振动频率(cm-1)C—C(三键)12~18 1.27 2262~2100C—C(双键)8~12 1.40 1600~1800C—C(单键)4~6 1.54 1000~1300(弱)表3—2基团振动频率与原子折合质量的关系(原子种类)基团折合质量键长(Â)振动频率cm-1C—H 0.9 1.12 2800~3100C—C 6 1.54 约1000C—Cl 7.3 1.77 约625C—I 8.9 2.31 约5000—H N—H 0.971.0336003300-3500(2)基团频率区的划分(表3-3)前三个区域(氢键区、叁键及累积双键区、双键区,即4000——1500 cm-1)称为特征频率区,小于1500 cm-1的区域称为指纹区(单键区,有些文献中以1350 cm-1作为二者的界限)。
简述红外吸收光谱产生的条件
简述红外吸收光谱产生的条件
红外吸收光谱是一种用于分析物质的非破坏性技术,它基于物质分子吸收红外辐射的特性。
产生红外吸收光谱需要满足以下条件:
1.源辐射:产生红外辐射的源,如红外灯或者激光等。
这些源产生的辐射通常在红外波段具有
强度和稳定性。
2.样品:样品应该是纯净、干燥、透明的,以保证所测得的吸收谱是样品本身的特征。
3.模拟:样品与红外辐射相互作用后,辐射会被吸收、散射或透射。
通过测量透射或吸收的辐
射强度,可以得到样品的红外吸收光谱。
4.检测:需要使用红外光谱仪进行测量。
红外光谱仪通常由光源、光栅或者干涉仪、检测器等
组成。
需要注意的是,红外吸收光谱产生的条件也受限于样品的性质和所研究的波长范围。
某些物质在红外波段吸收较弱或者不吸收,因此可能无法产生明显的红外吸收光谱。
此外,样品的形态、浓度、厚度等因素也会对红外吸收光谱的表现产生影响。
红外吸收光谱简介
分子间氢键 分子间氢键是否能够形成以及缔合程度有多大与该化合物
的浓度有密切关系
例如: 环己醇
浓度<0.01mol/L的CCl4稀溶液中------不形成分子间氢键 浓 度<0.1mol/L的CCl4溶液中------ 形成二聚体和多聚体的吸收 浓 度<1.0mol/L的CCl4溶液中------几乎都是多聚体
强, 宽而散
νN-H /cm-1 :3500~33001
强, 尖峰(单或双峰)
分子内氢键
H OO
O1 νC=O(游离) 1675cm-1 νO--H(缔合) 2843cm-1
形成分子内氢键
O
νC=O(游离) 1676cm-1 νC=O(游离) 1673cm-1 νO--H(游离) 3615~3606cm-1
未形成分子内氢键
氢键对氢键给体的影响较大, 对氢键受体的影响相对较小.
强度
很强 强 中等 弱 很弱
符号
VS S M W VW
红外吸收峰形状
宽峰 尖峰
肩峰 双峰
二.红外光谱的应用
1.通过红外光谱图的比较,可以判断是否是同一种化合物. 2.可以获取分子中各种结构信息, 特别是官能团信息.
例如: 3000±150cm-1区域的任何吸收, 都可以归结为C-H伸缩振动. 1715±100cm-1区域的任何强吸收, 基本上都可以归结为C=O 伸缩振动.
Y=Z伸缩振动区 (C=O, C=N, C=C)
红外吸收光谱中各种主要基团的大致分布图
不仅要注意特征官能团的位置. 而且还要注意观察峰的形状和强度.
例如 例如
νC=O /cm-1 ----1850~1630
强
νC=C /cm-1 ---- 1680~1620
红外吸收光谱和红外反射光谱
红外吸收光谱和红外反射光谱
红外吸收光谱和红外反射光谱都是利用红外光进行光谱分析的技术,但它们在应用方向和检测方式上存在明显的区别。
1. 红外吸收光谱:
红外吸收光谱是利用红外光通过样品时,样品对红外光的吸收作用进行的光谱分析技术。
其主要是研究分子振动能级跃迁而产生的吸收光谱,只有引起分子偶极矩变化的振动才能产生红外吸收。
红外吸收光谱主要用于结构分析、定性鉴别及定量分析。
其优点在于可以获得分子基团的特征吸收峰,从而推断出分子结构式。
例如,在1300cm-1附近的特征吸收峰对应于亚甲基和甲基的伸缩振动,而在1650cm-1附近出现的特征吸收峰对应于C=O的伸缩振动等。
2. 红外反射光谱:
红外反射光谱是一种利用红外反射光研究吸附薄层的光谱分析技术,其与吸附薄层和金属载体的光学常数、入射角及入射光的极化性质有关。
这种技术主要被用于研究表面的吸附特性,如催化剂表面吸附、生物薄膜的形成等。
虽然红外反射光谱不直接给出有关分子基团的信息,但它可以提供关于表面结构、化学组成以及物理性质(如粗糙度、吸附层厚度等)的信息。
总的来说,红外吸收光谱主要适用于分析样品的内部结构和化学组成,而红外反射光谱则主要用于研究表面的结构和化学组成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
UV——分子外层价电子能级的跃迁(电子光谱) IR——分子振动和转动能级的跃迁 (振转光谱)
三、红外光谱的作用 1.可以确定化合物的类别(芳香类) 2.确定官能团: 例:—CO—,—C=C—,—C≡C— 3.推测分子结构(简单化合物) 4.定量分析
四、红外光谱的表示方法
T~λ曲线 →前密后疏
(cm1 ) 10 4 ( m)
当r re U 0 当r re 或r re U 0
分子振动总能量 EV U T
U 位能 T 动能
当 r re U 0 ,EV T 当(r re)最大 T 0 ,EV U
A、B两原子 距平衡位置最
远
量子力学证明:
分子振动总能量 EV
(V
1 ) h
2
分子振动频率
(1)伸缩振动(stretching vibration):指键长沿键轴方向发生周 期性变化的振动,分两种:
1).对称伸缩振动(symmetrical stretching vibration) :键长 沿键轴方向的运动同时发生
AX
型分子
2
AX 3型分子
s CH 2
~
2850cm 1
s CH 3
~
2870cm1
例: CH CC CO 2) 同类原子:u '一定,K , (光谱区左端)
不同类原子:要看K或 u ' 哪一个起主导作用
K影响大,K , (光谱区左端)
u ' 影响大,u ' , (光谱区右端)
例: CC
CC
CC
K 15N / cm K 10 N / cm K 5N / cm
内摇动
AX
型分子
2
CH 2 ~ 720cm 1
L 红外光的照射频率 分子的振动频率
2 振动频率(vibration frequency):由Hooke定律推导出的简
谐振动公式计算:
K为化学键力常数,即将化学键两端的原子
由平衡位置拉长0.1nm后的恢复力,单键、
双键及三键的力常数K分别近似为5、10及
1 K 2 u
每厘米长 度中波动 的数目
2).反称伸缩振动(asymmetrical stretching vibration):键长 沿键轴方向的运动交替发生
AX 2型分子
AX
型分子
3
as CH 2
~
2925cm1
as CH 3
~
2960cm1
(2) 弯曲振动(bending vibration)(变形振动denformation vibration):
~ 2060 cm1 ~ 1680 cm1 ~ 1190 cm1
例: CC CH
3) 同一基团的振动形式不同 峰位不同
例:
as CH
s CH
CC的K 3倍
于C-H,而u '
却6倍于C-H
3 振动形式(vibration style) :多原子分子的振动形式较多,但 基本上包括两大类,即伸缩振动和弯曲振动。
principle of IR
红外分光光度法——研究物质结构与红外光谱之间关系 红外光谱——由吸收峰位置和吸收峰强度共同描述
一、分子振动能级和振动形式 二、红外吸收光谱产生的条件和吸收峰强度 三、吸收峰的位置 四、特征峰和相关峰
一、分子振动能级和振动形式 1.振动能级(vibrational level):为了讨论方便,以双原子 分子(或基团)的纯振动光谱为例予以探索。
r 原子间实际距离 re 原子间平衡距离 K 化学键力常数(N / cm)
把A、B两个不同质量的原子近似地看作 两个小球,把连接两者的化学键看成质量 可以忽略不计的弹簧,则两个原子间的 伸缩振动可近似地看成沿键轴方向的简谐 振动,双原子分子可近似地看作为谐振子
简谐振动位能
U
1 2
K
(r
re
)
2
15N/cm(1N=1×105g.cm/s2);
u为折合质量,即u m A .mB mA mB
其中mA及mB分别为化学键两端原子 A和B的质量;
因为
1 c
每秒内 的波动 数目
所以 1 K 2c u
将原子A和B的折合相对原子质量(简称原子量)u ' 代替折合
质量 u得:
1K
1
6 .0 2 123 K 0 3 /c N m
一、红外光的区划 红外线:波长在0.76~500μm (1000μm) 范围内的电磁波。
近红外区:0.76~2.5μm —OH和—NH倍频吸收区
中红外区:2.5~25μm
振动、伴随转动光谱
远红外区:25~500μm 纯转动光谱
二、红外吸收过程 分子中基团的振动 和转动能级跃迁产 生:振-转光谱 辐射→分子振动能 级跃迁→红外光谱 →官能团→分子结 构
V 分子振动量子数
V 0 ,1 ,2 ,3
分子振动总能量 EV
(V 1 ) h
2
a
当V=0时,分子处于基态,Ev = 1/2hν,
即振动体系的能量仍不为零。当V 0
时,分子处于激发态。
分子振动能级差 E振 V h
光子照射能量 EL h L
产生红外光谱前提 E振 EL
b
即 L V
指键角发生周期性变化、而键长不变的振动。
1).面内(in-plane)弯曲振动β:弯曲振动发生在由几个原子 构成的平面内,有以下两种情况: ·剪式振动(scissoring vibration)δ:振动中键角的变 化类似剪刀的开闭.
AX 2型分子
CH2 ~ 1465 20cm1
·面内摇摆(in-plane rocking)ρ:基团作为一个整体在平面
T ~σ曲线 →前疏后密
五、IR与 转动能级跃迁
适用
所有红外吸收的 有机化合物
特征性 特征性强
用途
鉴定化合物类别
鉴定官能团
推测结构
UV 分子外层价电能级跃迁
具n-π*跃迁有机化合物 具π-π*跃迁有机化合物 简单、特征性不强 定量 推测有机化合物共轭骨架
第一节 红外分光光度法基本原理
()
2cu 2 3 .14 3 .0 1 0 1 610 c 0 0/m s u '(g )
1N110 5g.cm /s2
( ) 1302 K (cm1 )
u'
注: 与K 和u '有关
化学键力常数K越大,折合相对原子质量 u ' 越小,则谐振 子的振动频率越大,即振动吸收峰的波数越大。
讨论: ( ) 1302 K (cm1 ) 1) K相近,u ' ,u ' (光谱区右端)
