化学平衡及影响因素转化率练习题(附答案)
高中化学考点40 化学平衡常数及转化率

考点40 化学平衡常数及转化率1.化学平衡常数(1)定义在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,这个常数就是该反应的化学平衡常数(简称平衡常数),用K表示。
(2)表达式对于一般的可逆反应:m A(g)+n B(g)p C(g)+q D(g),K=(C)(D) (A)(B)p qm nc cc c⋅⋅。
(3)应用①判断反应进行的限度K值大,说明反应进行的程度大,反应物的转化率高。
K值小,说明反应进行的程度小,反应物的转化率低。
K <10−510−5~105>105反应程度很难进行反应可逆反应可接近完全②判断反应是否达到平衡状态化学反应a A(g)+b B(g)c C(g)+d D(g)在任意状态时,浓度商均为Q c=(C)(D) (A)(B)c da bc cc c⋅⋅。
Q c>K时,反应向逆反应方向进行;Q c=K时,反应处于平衡状态;Q c<K时,反应向正反应方向进行。
③利用平衡常数判断反应的热效应若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
2.转化率对于一般的化学反应:a A+b B c C+d D,达到平衡时反应物A的转化率为α(A)=A AA的初始浓度-的平衡浓度的初始浓度×100%=0(A)(A)(A)c cc-×100%[c0(A)为起始时A的浓度,c(A)为平衡时A的浓度]反应物平衡转化率的变化判断判断反应物转化率的变化时,不要把平衡正向移动与反应物转化率提高等同起来,要视具体情况而定。
常见有以下几种情形:反应类型条件的改变反应物转化率的变化有多种反应物的可逆反应m A(g)+n B(g)p C(g)+q D(g) 恒容时只增加反应物A的用量反应物A的转化率减小,反应物B的转化率增大同等倍数地增大(或减小)反应物A、B的量恒温恒压条件下反应物转化率不变恒温恒容条件下m+n>p+q反应物A和B的转化率均增大m+n<p+q反应物A和B的转化率均减小m+n=p+q反应物A和B的转化率均不变只有一种反应物的可逆反应m A(g)n B(g)+p C(g) 增加反应物A的用量恒温恒压条件下反应物转化率不变恒温恒容条件下m>n+p反应物A的转化率增大m<n+p反应物A的转化率减小m=n+p反应物A和B的转化率不变考向一 化学平衡常数及影响因素典例1 下列关于化学平衡常数的说法中,正确的是A .在任何条件下,化学平衡常数都是一个定值B .化学平衡常数K 可以推断一个可逆反应进行的程度C .化学平衡常数K 只与温度、反应物浓度、体系的压强有关D .当改变反应物的浓度时,化学平衡常数会发生改变 【答案】B【解析】A .在给定的反应方程式中,化学平衡常数只受温度的影响,温度改变则化学平衡常数改变,故错误;B .任何时刻Q c >K ,说明平衡向逆反应方向进行,Q c <K ,说明平衡向正反应方向进行,Q c =K ,说明反应达到平衡,故正确;C .化学平衡常数只受温度影响,故错误;D .根据选项C 分析,故错误。
2024届全国高考(新高考)化学复习历年真题好题专项(化学平衡常数及转化率计算)练习(附答案)

2024届全国高考(新高考)化学复习历年真题好题专项(化学平衡常数及转化率计算)练习1.[2022ꞏ广东卷]恒容密闭容器中,BaSO 4(s )+4H 2(g )⇌BaS (s )+4H 2O (g )在不同温度下达平衡时,各组分的物质的量(n )如图所示。
下列说法正确的是( )A.该反应的ΔH <0B.a 为n (H 2O )随温度的变化曲线C.向平衡体系中充入惰性气体,平衡不移动D.向平衡体系中加入BaSO 4,H 2的平衡转化率增大2.[2022ꞏ海南卷]某温度下,反应CH 2===CH 2(g )+H 2O (g )⇌CH 3CH 2OH (g )在密闭容器中达到平衡。
下列说法正确的是( )A.增大压强,v 正>v 逆,平衡常数增大B.加入催化剂,平衡时CH 3CH 2OH (g )的浓度增大C.恒容下,充入一定量的H 2O (g ),平衡向正反应方向移动 D.恒容下,充入一定量的CH 2===CH 2(g ), CH 2===CH 2(g )的平衡转化率增大3.[2023ꞏ专题模块测试]K 、K a 、K w 分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是( )A.在500 ℃、20 MPa 条件下,在5 L 密闭容器中进行合成氨的反应,使用催化剂后K 增大B.室温下K (HCN )<K (CH 3COOH ),说明CH 3COOH 的电离程度一定比HCN 的大 C.25 ℃时,pH 均为4的盐酸和NH 4I 溶液中K w 不相等D.2SO 2+O 2 催化剂△2SO 3达平衡后,改变某一条件时K 不变,SO 2的转化率可能增大、减小或不变4.[2023ꞏ湖南师大附中高三月考]N 2O 5是一种新型硝化剂,一定温度下发生反应2N 2O 5(g )⇌4NO 2(g )+O 2(g ) ΔH >0,T 1温度下的部分实验数据如下表所示。
t /s 0 500 1 000 1 500c (N 2O 5)/(molꞏL -1) 5.00 3.52 2.50 2.50下列说法正确的是( )A .该反应在任何温度下均能自发进行B .T 1温度下的平衡常数为K 1=125,1 000 s 时N 2O 5(g )转化率为50%C .其他条件不变时,T 2温度下反应到1 000 s 时测得N 2O 5(g )浓度为2.98 molꞏL -1,则T 1<T 2D .T 1温度下的平衡常数为K 1,T 2温度下的平衡常数为K 2,若T 1>T 2,则K 1<K 25.[2023ꞏ福建福州质检]在1 L 的密闭容器中充入2 mol N 2和7 mol H 2,发生反应N 2+3H 2⇌2NH 3,保持其他条件不变,相同时间内测得NH 3的浓度与温度的关系如图所示。
高中化学平衡移动及影响因素练习题(附答案)
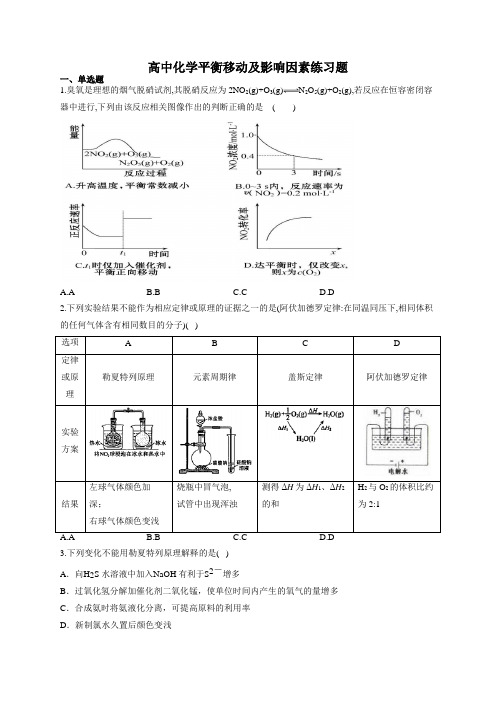
高中化学平衡移动及影响因素练习题一、单选题1.臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()A.AB.BC.CD.D2.下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)( )左球气体颜色加烧瓶中冒气泡, 测得ΔH为ΔH、ΔH H与O的体积比约3.下列变化不能用勒夏特列原理解释的是( )A.向H2S 水溶液中加入N aOH 有利于S2-增多B.过氧化氢分解加催化剂二氧化锰,使单位时间内产生的氧气的量增多C.合成氨时将氨液化分离,可提高原料的利用率D.新制氯水久置后颜色变浅4.下列不能能用勒夏特烈原理解释的是( ) A .对2HI====H 2+I 2平衡体系增加压强使颜色变深B .在溴水中存在如下平衡:Br 2+H 2O===HBr+HBrO ,当加入NaOH 溶液后颜色变浅C .反应2NO+2CO===2CO 2+N 2正反应放热,升高温度使平衡向逆方向移动D .合成氨反应:N 2+3H 2===2NH 3正反应放热,为使氨的产率提高,理论上应采取低温高压的措施5.下列事实不能..用勒夏特列原理解释的是( ) A .光照新制的氯水时,溶液的pH 逐渐减小 B .高温,使2N 和2H 转化为更多的3NH (△H <0) C .可用浓氨水和氢氧化钠固体快速制取氨气 D .增大压强,有利于2SO 和2O 反应生成3SO6.某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)2C(g)达到平衡时,各物质的物质的量之比为n (A):n (B):n (C)=2:2:1。
保持温度不变,以2:2:1的物质的量之比再充入A 、B 、C,则( ) A.平衡不移动B.再次达到平衡时,n (A):n (B):n (C)仍为2:2:1C.再次达到平衡时,C 的体积分数增大D.正反应速率增大,逆反应速率减小7.下列事实不能用勒夏特列原理解释的是( ) ①工业合成氨,反应条件选择高温②实验室可以用排饱和食盐水的方法收集氯气 ③使用催化剂可加快SO 2转化为SO 3的速率④硫酸工业中,增大O 2的浓度有利于提高SO 2的转化率 A.②③B.②④C.①③D.①④8.在某密闭容器中,反应a A(g)+b B(g)c C(g)+d D(g)达到平衡时,B 的浓度为0.6mol/L,若保持温度不变,将容器的容积扩大到原来的3倍,达新平衡时B 的浓度降为0.3mol/L 。
高三化学化学平衡试题答案及解析

高三化学化学平衡试题答案及解析1.可逆反应mA(g)+nB(s)rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分含量和温度T 或压强P关系如图所示,下列叙述中正确的是A.温度降低,化学平衡向正反应方向移动B.使用催化剂,D的物质的量分数增加C.化学方程式系数m+n = r+qD.物质B的颗粒越小,反应越快,有利于平衡向正反应方向移动【答案】A【解析】A.由左图知,温度T2为先到达平衡,故T2>T1,升高温度,升高温度,D%减小,则平衡向逆反应移动,A正确;B.使用催化剂,缩短到达平衡时间,平衡不移动,D%的不变,B错误;C、由右图可知,压强为P2先到达平衡,故P2>P1,增大压强,D%不变,则平衡不移动,反应中B为固体,故m=r+q,C错误;D.B为固体,物质B的颗粒越小,接触面积越大,反应越快,但对平衡移动没有影响,D错误.【考点】考查化学平衡的移动,化学平衡的影响因素,化学评横的图像等知识。
2.(14分)中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要为燃煤、机动车尾气等。
因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
请回答下列问题:(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:NH SO NO-5-5-5根据表中数据计算PM2.5待测试样的pH =。
(2) NOx 是汽车尾气的主要污染物之一。
汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:① N2(g)+O2(g)2NO(g)△H=。
②当尾气中空气不足时,NOx 在催化转化器中被还原成N2排出。
写出NO被CO还原的化学方程式。
③汽车汽油不完全燃烧时还产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,该设想能否实现?。
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:①用离子方程式表示反应器中发生的反应。
化学平衡(习题及答案)解析

101kPa大气平衡的水中此c(O2)。[大气中p(O2)=21.0kPa]
解:
K ceq (O2 ) / c pO2 / p
20℃时: K 1.38 103 1.38 103 1
K
ceq (O2 ) / c pO2 / p
ceq (O2 ) / c 21.0 /101
1.38103
ceq(O2)=2.87×10-4(mol·dm-3)
对于放热反应, ΔrHm⊙ <0,温度升高, K⊙减小, Q> K⊙,平衡向逆向移动。
对于吸热反应, ΔrHm⊙ >0,温度升高, K⊙增大, Q <K⊙,平衡向正向移动。
2.反应3H2(g)+N2(g)=2NH3(g) △rHmθ>0,在密闭容器该反应达 到平衡时,若降低温度,平衡 向逆反应方向移动;若恒容条 件下,充入惰性气体,增加系统的总压力,则平衡 不移动。
A、K1θ+K2θ
B、K1θ-K2θ
C、K1θ×K2θ
D、K1θ/K2θ
6.合成氨反应3H2(g)+N2(g)=2NH3(g)在恒压下进
行时,若向体系中加入Ar,则氨的产率( A )
A、减小 B、增大 C、不变 D、无法判断
2
General Chemistry
Chapter 5 Homework
二、填空题 1.对放热反应,化学平衡常数K值随温度升高而 减小 随温 度降低而 增大 。
C、小于35%
D、无法知道
3.反应CO2(g)+H2(g)=CO(g)+H2O(g) △rHmθ>0,若要提高 CO的产率,可采用的方法是 ( )C
A、增加总压力
B、加入催化剂
化学平衡经典试题(附答案).doc

化学平衡经典试题(附答案)1.恒温、恒压下, a mol A 和 b mol B 在一个容积可变的容器中发生如下反应:A(g) +2B(g) 2C(g) ,一段时间后达到平衡,生成n mol C .则下列说法中正确的是( )A.物质 A、 B 的转化率之比为a∶bnB.起始时刻和达到平衡后容器中的压强比为(a +b) ∶(a + b- )2C.若起始时放入2a mol A和2b mol B,则达到平衡时生成2n mol CD.当 v 正 (A) = 2v 逆 (B) 时,可确定反应达到平衡解析:生成 n mol C 时参加反应的A、 B 的物质的量分别为n/2 mol 、 n mol ,转化率之比为n n bC 的量也成倍地增加;反应∶ =;恒温、恒压过程成倍地增大反应物的量,则平衡时2a b 2a速率之比等于化学计量数之比,当2v 正 (A) = v 逆(B) 时,可确定反应达到平衡.答案: C2.在一个容积为 VL 的密闭容器中放入:2L A(气 ) 和 lL B(气 ), 在一定条件下发生下列反应:13A( 气 )+B( 气 ) nC(气 )+2D( 气 ) 达到平衡后, A 物质的量浓度减少2,混合气体的平均摩1尔质量增大8,则该反应的化学方程中n 的值是( )A. 1 B . 2 C . 3 D . 43. ( 2011 四川)可逆反应① X(g)+2Y(g) 2Z(g) 、② 2M( g)N( g)+P(g) 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。
反应开始和达到平衡状态时有关物理量的变化如图所示:下列判断正确的是A.反应①的正反应是吸热反应B. 达平衡( I )时体系的压强与反应开始时体系的压强之比为14:15C.达平衡( I )时, X 的转化率为511D. 在平衡(I )和平衡(II )中M的体积分数相等4.反应 mA(固) +nB(气)pC(气)+Q在一定温度下的关系如图2-11 所示,下列叙述中正确的是()B 的体积分数(B%)与压强变化①m+n> P;②x 点表示该反应的正反应速率大于逆反应速率;③n>p;④x 点比y 点时的反应速率慢。
2025届高考化学复习:历年优质真题、模拟题专项(化学平衡的移动及影响因素)阶梯练习(附答案)

2025届高考化学复习:历年优质真题、模拟题专项(化学平衡的移动及影响因素)阶梯练习1.[2022ꞏ浙江1月]在恒温恒容条件下,发生反应A(s)+2B(g)⇌3X(g),c(B)随时间的变化如图中曲线甲所示。
下列说法不正确的是( )A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率C.在不同时刻都存在关系:2v(B)=3v(X)D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙所示2.[2022ꞏ江苏卷]用尿素水解生成的NH3催化还原NO,是柴油机车辆尾气净化的主要方法。
反应为4NH3(g)+O2(g)+4NO(g)⇌4N2(g)+6H2O(g)下列说法正确的是( )A.上述反应ΔS<0B.上述反应平衡常数K=c4(N2)ꞏc6(H2O)c4(NH3)ꞏc(O2)ꞏc4(NO)C.上述反应中消耗1 mol NH3,转移电子的数目为2×6.02×1023D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小3.[2024ꞏ贵州贵阳监测]已知可逆反应a A(g)+b B(s)⇌c C(g)+d D(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图,根据图像判断下列说法正确的是( )A.平衡常数K:K(T1)>K(T2),K(p1)=K(p2)B.反应达到平衡后,添加合适的催化剂,D的百分含量增加C.e、f点对应的化学反应速率:v正(e)>v逆(f)D.T1>T2,p1>p24.[角度创新]一定温度下,在一密闭容器中发生反应:2SO2(g)+O2(g)⇌2SO3(g),c(SO2)随时间(t)变化如图所示。
400 ℃时压强对SO2的转化率的影响如表。
压强0.1 MPa 0.5 MPa 1 MPa 10 MPaSO2的转化率99.2% 99.6% 99.7% 99.9% 下列说法正确的是( )A.a点的v逆大于b点的v逆B.t2时刻改变的条件一定是增大c(SO2)C.化学平衡常数d点与e点相等D.硫酸工业中,SO2催化氧化制SO3时采用高压提高生产效益5.[2024ꞏ广州市综合测试]反应R(g)⇌P(g)在有水和无水条件下,反应历程如图。
2023版高考化学微专题小练习专练36化学平衡的移动及影响因素(含答案)

高考化学微专题小练习:专练36 化学平衡的移动及影响因素1.[2022·广东卷]恒容密闭容器中,BaSO4(s)+4H2(g)⇌BaS(s)+4H2O(g)在不同温度下达平衡时,各组分的物质的量(n)如图所示。
下列说法正确的是( )A.该反应的ΔH<0B.a为n(H2O)随温度的变化曲线C.向平衡体系中充入惰性气体,平衡不移动D.向平衡体系中加入BaSO4,H2的平衡转化率增大2.[2021·辽宁卷]某温度下,在恒容密闭容器中加入一定量X,发生反应2X(s)⇌Y(s)+Z(g),一段时间后达到平衡。
下列说法错误的是 ( )A.升高温度,若c(Z)增大,则ΔH>0B.加入一定量Z,达新平衡后m(Y)减小C.加入等物质的量的Y和Z,达新平衡后c(Z)增大D.加入一定量氩气,平衡不移动3.[2021·江苏卷]NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。
工业尾气中NH3可通过催化氧化为N2除去。
将一定比例NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、N2的选择性[2n生成(N2)n总转化(NH3)×100%]与温度的关系如图所示。
下列说法正确的是( )A.其他条件不变,升高温度,NH3的平衡转化率增大B.其他条件不变,在175~300 ℃范围,随着温度的升高,出口处氮气、氮氧化物的量均不断增大C.催化氧化除去尾气中的NH3应选择反应温度高于250 ℃D.高效除去尾气中的NH3,需研发低温下NH3转化率高和N2选择性高的催化剂4.[2022·哈尔滨师大青冈实验中学月考]已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列叙述正确的是( )①生成物的体积分数一定增加②生成物的产量一定增加③反应物的转化率一定增加④反应物的浓度一定降低⑤正反应速率一定大于逆反应速率A.①②④⑤ B.①②③⑤C.②③ D.②⑤5.[角度创新]一定温度下,在一密闭容器中发生反应:2SO2(g)+O2(g)⇌2SO3(g),c(SO2)随时间(t)变化如图所示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学平衡及影响因素转化率练习题一、单选题1.在一定温度时,将1mol A 和2mol B 放入容积为5L 的某密闭容器中发生如下反应:A(s)+2B(g)C(g)+2D(g),经5min 后,测得容器内B 的浓度减少了0.2mol·L -1。
下列叙述不正确的是( ) A.在5min 内该反应用C 的浓度变化表示的反应速率为 0.02mol·L -1·min -1 B.5min 时,容器内D 的浓度为0.2mol·L -1C.该可逆反应随反应的进行,容器内压强逐渐增大D.5min 时容器内气体总的物质的量为3mol2.实验室用30%左右的24H SO 溶液(浓度约为3.7-1mol L )与锌粒反应制取氢气。
下列措施不可能加快反应速率的是( )A.适当升高温度B.将锌粒改为锌粉C.将所用硫酸加适量水稀释D.加入合适的催化剂 3.H 2O 2分解速率受多种因素影响。
实验测得70 ℃时不同条件下H 2O 2 浓度随时间的变化如图所示。
下列说法正确的是( )A.图甲表明,其他条件相同时,H 2O 2浓度越小,其分解速率越快B.图乙表明,其他条件相同时,溶液pH 越小,H 2O 2分解速率越快C.图丙表明,有少量Mn 2+存在时,溶液碱性越强,H 2O 2分解速率越快D.图丙和图丁表明,碱性溶液中,Mn 2+对H 2O 2分解速率的影响大4.酸性条件下,KMnO 4与H 2C 2O 4可发生氧化还原反应,用0.1mol·L -1的KMnO 4溶液与过量的H 2C 2O 4反应,测得Mn 2+的生成速率v 与时间t 的变化如图所示,下列说法正确的是( )A.该反应中每生成1mol CO 2转移电子10molB.方程式配平后,H 2O 的系数为6C.反应开始很短一段时间内v 减小是因为反应物浓度减小,后来突然增大是因为生成的Mn 2+对该反应有催化作用D.t 0时,Mn 2+的浓度最大 5.设C+ 2CO 2CO(正反应为吸热反应)的反应速率为1v ; 22N +3H 32NH (正反应为放热反应)的反应速率为2v ,对于上述反应,当温度升高时, 1v 和2v 的变化情况为( ) A.都增大B.都减小C. 1v 增大, 2v 减小D. 1v 减小, 2v 增大6.在温度相同、容积均为2L 的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下。
下列说法正确的是( ) 容器 甲乙丙 反应物投入量 1mol N 2、3mol H 2 2mol N 2、6mol H 2 2mol NH 3 NH 3的浓度/(mol·L -1) c 1 c 2 c 3 反应的能量变化 放出Q 1 kJ 放出Q 2 kJ 吸收Q 3 kJ 体系压强/Pa p 1 p 2 p 3 反应物转化率 α1α2α3已知N 2(g)+3H 2(g)2NH 3(g) ΔΗ=-92.4 kJ·mol -1。
A.2p 1=2p 3<p 2B.达到平衡时丙容器中NH 3的体积分数最大C.α2+α3<1D.Q 1+Q 3=92.47.某化学科研小组研究在其他条件不变时,改变某一条件对反应A 2(g)+3B 2(g)2AB 3(g)的化学平衡状态的影响,得到如图所示的变化规律(图中T 表示温度,n 表示物质的量),根据图象得出的结论正确的是( )①正反应一定是放热反应②达到平衡时A2的转化率大小为b>a>c③若T2>T1,则正反应一定是吸热反应④b点时,平衡体系中A、B原子数之比接近1:3A.①②B.①③C.②④D.③④8.—定温度下,在一定容积的密闭容器中充入N2和H2,发生反应N2(g)+3H2(g)2NH3(g),达到平衡时N2的转化率为c%,向平衡混合物中再次充入N2,重新达到平衡后N2的转化率将( )A.增大B.减小C.不变D.无法确定9.反应a M(g)+ b N(g) c P(g)+d Q(g)达到平衡时,M的体积分数φ(M)与反应条件的关系如图所示。
其中z表示反应开始时N的物质的量与M的物质的量之比。
下列说法正确的是( )A.同温同压同z时,加入催化剂,平衡时Q的体积分数增大B.同压同z时,升高温度,平衡时Q的体积分数增大C.同温同z时,增大压强,平衡时Q的体积分数增大D.同温同压时,增大z,平衡时Q的体积分数增大10.已知可逆反应4NH3(g)+5O2(g)4NO(g)+6H2O(g),下列叙述正确的是( )A.反应达到化学平衡状态时,4v正(O2)=5v逆(NO)B.若单位时间内生成x mol NO的同时消耗x mol NH3,则反应达到平衡状态C.反应达到化学平衡状态时,若增大容器体积,则正反应速率减小,逆反应速率增大D.化学反应速率关系:2v正(NH3)=3v正(H2O)11.相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)2NH3(g) ΔΗ=-92.6kJ·mol-1。
实验测得该反应起始、平衡时的有关数据如下表所示:容器编号起始时物质的物质的量/mol达平衡时体系能量的变化N 2H 2 NH 3 ① 1 3 0 放出热量:23.15kJ ②0.92.70.2放出热量:Q 下列叙述错误的是( )A.容器①、② 中反应的平衡常数相等B.平衡时,两个容器中NH 3的体积分数均为14.3%C.容器② 中反应达平衡时,放出的热量Q =23.15kJD.若容器① 的体积为0.5L,则平衡时放出的热量小于23.15kJ12.25℃ 时,密闭容器中X 、Y 、Z 三种气体的初始浓度和平衡浓度如下表所示:物质 X Y Z 初始浓度/(mol·L -1) 0.1 0.2 0.0 平衡浓度/(mol·L -1) 0.050.050.1下列说法错误的是( )A.反应达到平衡时,X 的转化率为50%B.该反应可表示为X(g)+3Y(g)2Z(g),其平衡常数为1600C.增大压强使平衡向生成Z 的方向移动,平衡常数增大D.改变温度可以改变该反应的平衡常数13.在一定温度下的密闭容器中,加入1mol CO 和1mol H 2O 发生反应CO(g)+H 2O(g)CO 2(g)+H 2(g),达到平衡时测得n (H 2)=0.5mol,下列说法不正确的是( )A.在该温度下,反应的平衡常数K =1B.平衡常数与反应温度无关C.CO 的平衡转化率为50%D.平衡时n (H 2O)=0.5mol14.下列反应在任何温度下都不能自发进行的是( ) A.2O 3(g)=3O 2(g) ΔH <0 B.2CO(g)=2C(s)+O 2(g) ΔH >0 C.N 2(g)+3H 2(g)=2NH 3(g) ΔH <0D.CaCO 3(s)=CaO(s)+CO 2(g) ΔH >015.反应CH 3OH(l)+NH 3(g)=CH 3NH 2(g)+H 2O(g)在某温度下自发向右进行,若反应的|ΔΗ|=17kJ·mol -1,|ΔΗ-T ΔS |=17kJ·mol -1,则下列判断正确的是( )A.ΔΗ>0,ΔΗ-T ΔS <0B.ΔΗ<0,ΔΗ-T ΔS >0C.ΔΗ>0,ΔΗ-T ΔS >0D.ΔΗ<0,ΔΗ-T ΔS <016.在一个不传热的恒容密闭容器中,可逆反应N 2(g)+3H 2(g)2NH 3(g)达到平衡的标志是( )①反应速率223N H NH ::1:3:2v v v ②各组分的物质的量不变③体系的压强不再发生变化④混合气体的密度不变(相同状况)⑤体系的温度不再发生变化⑥2v正(N2)=v逆(NH3)⑦单位时间内3mol H-H键断裂参加反应,同时2mol N-H键也断裂参加反应A.①②③⑤⑥B.②③④⑤⑥C.②③⑤⑥D.②③④⑥⑦17.已知反应2H2(g)+CO(g)CH3OH(g)的平衡常数如下表,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,下列大小比较正确的是( )温度/℃500 700 800平衡常数K 2.50 0.34 0.15A.平衡常数:K(a)>K(c),K(b)=K(d)B.正反应速率:v(a)>v(c),v(b)=v(d)C.达到平衡所需时间:t(a)=t(c),t(b)>t(d)D.平均相对分子质量:()(),()()=>M a M c M b M d18.可逆反应:2NO2(g)2NO(g)+O2(g)在密闭容器中反应,达到平衡状态的标志是( )①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时,生成2n mol NO③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的平均相对分子质量不再改变的状态A.①④⑥B.②③⑤C.①③④D.①②③④⑤⑥19.某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )A.若T 2>T 1,则正反应一定是放热反应B.在T 2和n(A 2)不变时达到平衡,AB 3的物质的量大小为c>b>aC.若T 2>T 1,达到平衡时b,d 两点的反应速率:v d >v bD.达到平衡时A 2的转化率:b>a>c20.下列叙述中一定能判断某化学平衡发生移动的是( ) A.混合物中各组分的浓度改变 B.正、逆反应速率改变 C.混合物中各组分的含量改变D.混合体系的压强发生改变21.2COCl 俗名光气,是有毒气体。
在一定条件下,可发生的化学反应为:()()22COCl (g)CO g +Cl g ,0H ∆<。
下列有关说法正确的是( )A.在一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率B.当反应达平衡时,恒温恒压条件下充入Ar,能提高2COCl 的转化率C.单位时间内生成CO 和2Cl 的物质的量之比为1:1时,反应达到平衡状态D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大22.一定量的锌粉和6mol/L 的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,但不影响产生2H 的总量的是( )①石墨粉 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 A.①②⑤ B.①③⑤ C.③④⑤ D.①③④ 23.其他条件一定时,发生反应2A(g)+B(g)2C(g),B 的平衡转化率α(B)与温度T 的关系如图所示,图中4个点中表示未达到平衡状态且v 正<v 逆的点是( )A.aB.bC.cD.d 24.下列不能用勒夏特列原理解释的事实是( )A.棕红色的NO 2加压后颜色先变深后变浅B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深C.黄绿色的氯水光照后颜色变浅D.合成氨工业使用高压以提高氨的产量 25.下列说法正确的是( )A.凡是放热反应都是自发的,因为吸热反应都是非自发的B.自发反应的现象一定非常明显,非自发反应的熵一定减小C.常温下,反应C(s)+CO 2(g)2CO(g)不能自发进行,则该反应的ΔΗ>0D.反应2Mg(s)+CO 2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔΗ>0参考答案1.答案:D解析:经5min 后测得容器内B 的浓度减少了0.2mol ⋅L −1,则消耗的B 的物质的量为5L×0.2mol ⋅L −1=1mol ,则 A(s)+2B(g)C(g)+2D(g)起始:1mol 2mol 0 0 转化:0.5mol 1mol 0.5mol 1mol 平衡:0.5mol 1mol 0.5mol 1molA. 在5min 内该反应用C 的浓度变化表示的反应速率为110.5mol0.02mol L min 5L 5min--=⋅⋅,故A 正确; B. 5min 时,容器内D 的浓度为11mol=0.2mol L 5L-⋅,故B 正确; C. 反应前后气体的体积不等,反应过程中气体物质的量增大,容器内压强逐渐增大,故C 正确; D. 5min 时容器内气体总的物质的量为1mol+0.5mol+1mol=2.5mol ,故D 错误。
