螯合剂的概念
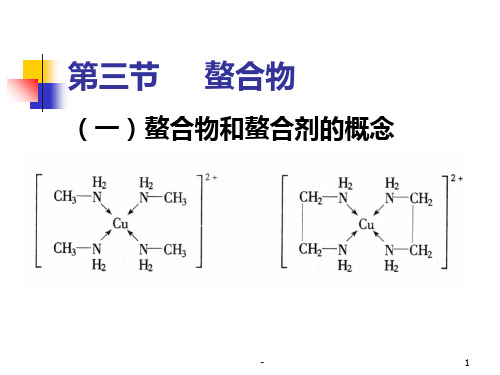
(一)螯合物和螯合剂的概念

二、氨羧螯合剂及氨羧 螯合滴定
(一)氨羧螯合剂的结构和特点 氨羧螯合剂中最重要同时应用最 广的是乙二氨四乙酸( 广的是乙二氨四乙酸(EDTA)及其 ) ),统称为 二钠盐 (EDTA-2Na),统称为 ), EDTA。结构如下: 。结构如下:
EDTA在水中溶解度小,故配制 在水中溶解度小, 在水中溶解度小 标准溶液时,常用它的二钠盐。 标准溶液时,常用它的二钠盐。 EDTA的分子或离子中含有 个氨基 的分子或离子中含有2个氨基 的分子或离子中含有 氮和4个羧基氧可与金属离子配合, 氮和4个羧基氧可与金属离子配合, 个羧基氧可与金属离子配合 生成具有5个五元环的稳定性很高的 生成具有 个五元环的稳定性很高的 螯合物。如下图: 螯合物。如下图:
溶液中螯合物的稳定性除决定于螯 合物稳定常数的大小外, 合物稳定常数的大小外,还与溶液 值有关。 的pH值有关。不同的金属离子与 值有关 EDTA生成的螯合物的稳定性不同, 生成的螯合物的稳定性不同, 生成的螯合物的稳定性不同 滴定时所需溶液的pH值也不同 值也不同。 滴定时所需溶液的 值也不同。因 此,在两种以上金属离子的混合溶 液中,常可以通过调节溶液的pH值 液中,常可以通过调节溶液的 值, 进行选择滴定。 用EDTA进行选择滴定。 进行选择滴定
例如, 离子和Zn 例如,在Mg2+离子和 2+离子的混合 溶液中,调节溶液的pH ≈ 6.8, 这时 溶液中,调节溶液的 , EDTA仍可与 Zn2+离子完全螯合,而与 离子完全螯合, 仍可与 Mg2+离子则完全不螯合,即Mg2+离子 离子则完全不螯合, 的存在不会干扰EDTA 对Zn2+离子的螯 的存在不会干扰 合滴定。 合滴定。 由于滴定时不断有离子的生成, 由于滴定时不断有离子的生成,为了 保持合适的pH值 使反应进行完全, 保持合适的 值,使反应进行完全,滴 定前必须加入合适的缓冲溶液控制溶液 的pH值。 值
edta滴定原理

edta滴定原理EDTA滴定原理。
EDTA(乙二胺四乙酸)是一种常用的配位试剂,广泛应用于化学分析和工业生产中。
其滴定原理是基于EDTA与金属离子形成稳定的络合物,从而实现对金属离子的定量分析。
本文将介绍EDTA滴定原理的基本概念、反应机制和实验操作。
1. 基本概念。
EDTA是一种螯合剂,具有四个羧基和两个氨基,可以形成六个配位键。
在水溶液中,EDTA以其阴离子形式存在,可以与金属离子形成络合物。
由于EDTA与金属离子的络合物都是无色的,因此可以利用指示剂来指示滴定终点。
常用的指示剂有压定胆碱蓝、黑色氧化铁等。
2. 反应机制。
在EDTA滴定中,EDTA与金属离子之间发生的反应是配位反应。
当EDTA与金属离子形成络合物时,金属离子的配位数和配位几何结构会发生改变。
这种络合物的形成是可逆的,在EDTA的作用下,金属离子会逐渐与EDTA形成络合物,直至金属离子全部与EDTA反应完毕。
通过滴定,可以确定金属离子的浓度。
3. 实验操作。
进行EDTA滴定实验时,首先需要准备好标准溶液和待测溶液。
然后将待测溶液加入滴定瓶中,加入适量的指示剂。
接下来,使用标准溶液滴定待测溶液,直至出现指示剂的颜色变化。
记录滴定所需的标准溶液的体积,根据滴定反应的化学方程式,计算出待测溶液中金属离子的浓度。
4. 应用领域。
EDTA滴定广泛应用于水质分析、食品检测、医药制剂、环境监测等领域。
例如,可以利用EDTA滴定法测定水中钙、镁、锌等金属离子的含量;在食品工业中,可以使用EDTA滴定法测定食品中重金属的残留量;在医药制剂中,可以利用EDTA滴定法测定药品中金属离子的含量。
总之,EDTA滴定原理是一种重要的化学分析方法,通过与金属离子形成络合物,实现对金属离子的定量分析。
在实验操作中,需要严格控制滴定条件,选择合适的指示剂,并进行准确的数据记录和计算。
EDTA滴定法在化学分析和工业生产中具有广泛的应用前景,对于推动化学技术的发展和进步具有重要意义。
过多金属螯合剂

过多金属螯合剂
过多金属螯合剂,又称过量金属螯合剂,是一种在化学反应中起到螯合金属离子的作用的化合物。
金属螯合剂可以通过配位键与金属离子形成稳定的配合物,从而改变金属离子的性质和活性。
过多金属螯合剂在许多领域都有广泛的应用。
在医学领域,金属螯合剂被用作治疗某些金属中毒的药物。
例如,EDTA是一种常用的金属螯合剂,可以与重金属离子形成稳定的配合物,从而促进这些金属离子的排出。
在环境保护领域,金属螯合剂也被用来处理含有重金属的废水,以减少对环境的污染。
金属螯合剂还被广泛应用于农业领域。
例如,一些金属螯合剂可以与植物根系中的金属离子结合,从而增加植物吸收这些金属离子的能力。
这对于修复受到金属污染的土壤非常重要。
除了医学、环境保护和农业领域,金属螯合剂还在化学合成、材料科学和能源领域得到了广泛应用。
例如,一些金属螯合剂可以作为催化剂,促进化学反应的进行。
另外,金属螯合剂还可以用于制备新型的功能材料,如金属有机骨架材料和金属聚合物。
尽管金属螯合剂在许多领域都有重要应用,但是过多的金属螯合剂使用可能会对环境和人类健康造成潜在的风险。
因此,在使用金属螯合剂时,需要仔细控制剂量和使用方法,以确保安全性和有效性。
过多金属螯合剂在各个领域都有广泛的应用。
它们可以改变金属离
子的性质,用于治疗金属中毒、处理废水、修复受污染的土壤,以及在化学合成、材料科学和能源领域中发挥重要作用。
然而,我们也需要注意金属螯合剂的使用安全性,以避免对环境和人类健康造成潜在的风险。
离子螯合剂

离子螯合剂是一类能够与金属离子结合的化合物,它们在化学、生物学、医学和环境科学等领域中有着广泛的应用。
离子螯合剂通过与金属离子形成稳定的配合物,从而有效地清除金属离子对生物体系和环境的影响。
离子螯合剂的种类繁多,包括柠檬酸、EDTA(乙二胺四乙酸)、DTPA(二乙基三胺五乙酸)等。
这些化合物可以通过与金属离子发生配位反应,形成具有高度稳定性的螯合物,从而有效地抑制金属离子的氧化、还原、毒害等作用。
在生物学和医学领域,离子螯合剂的应用尤为广泛。
例如,许多蛋白质、酶等生物大分子中含有的金属离子对于生物体系的正常功能至关重要。
然而,当这些金属离子浓度过高时,它们可能会对细胞产生毒害作用,甚至引发疾病。
因此,离子螯合剂在生物医学领域中扮演着重要的角色,它们能够有效地清除体内的有害金属离子,从而防止金属离子导致的疾病的发生。
在环境保护领域,离子螯合剂也被广泛应用。
许多工业废水、生活污水等水中含有高浓度的金属离子,这些金属离子会对环境造成污染。
离子螯合剂可以通过与金属离子形成螯合物,将金属离子从水中分离出来,从而有效地净化废水,保护环境。
此外,离子螯合剂在食品工业、石油工业等领域中也发挥着重要的作用。
它们可以用于食品添加剂中,提高食品的口感和稳定性;也可以用于石油工业中,清除油污和金属离子,提高石油产品的质量。
总之,离子螯合剂在许多领域中都有着广泛的应用,它们通过与金属离子形成螯合物,有效地清除金属离子对生物体系和环境的影响,为科学研究和实际应用提供了重要的支持。
(一)螯合物和螯合剂的概念PPT课件
-
6
CaY2-的结构
-
7
EDTA与金属离子的配合有以下特点:
1.螯合能力强 除碱金属以外,能与 几乎所有的金属离子形成稳定的螯 合物。
2.与金属离子形成的螯合物大多带 有电荷,因此易溶于水。
-
8
3.简单的螯合比 不论几价的金属离子, 它们与EDTA总是1:1螯合。例如:
M2++H2Y2--MY2 - +2H + M3++H2Y2--MY - +2H + M4++H2Y2--MY +2H +
-
12
(二)EDTA螯合滴定的基本原理
EDTA螯合滴定就是基于EDTA与
金属离子螯合反应的一种重要的滴定分 析方法,常用于测定溶液中金属离子的 含量。
EDTA螯合滴定的原理和基本过程:
滴定时使用的指示剂叫做金属指示剂。 它们是一类能与金属离子形成有色配合 物的水溶性有机染料。
-
13
作为金属指示剂必须具备以下条件: 1.与金属离子形成的配合物的颜色 与其本身(即未配合时)的颜色有 明显不同;
Ca2++H2Y2- ⇌ CaY2- +2H+ Mg2+ + H2Y2- ⇌MgY2- +2H+
滴定终点时:
MgIn-+ H2Y2- ⇌MgY2- +HIn- +H+
紫红
蓝
-
21பைடு நூலகம்
水的总硬度按下式计算:
总硬度= 式中:
CEDTVAEDTA V水样 1000
CEDTA: EDTA 标准溶液的浓度( mol ·L-1 ) VEDTA : 消耗EDTA标准溶液的体积(L) V: 滴定时水样的体积(L)
金属离子螯合

金属离子螯合金属离子螯合是化学中的一个重要概念,指的是金属离子与配体之间的配位作用,形成稳定的配合物。
金属离子螯合具有广泛的应用领域,包括催化剂、药物、环境修复等。
本文将从金属离子螯合的定义、配位键的形成、螯合剂的选择以及应用领域等方面进行论述。
一、金属离子螯合的定义金属离子螯合是指金属离子与配体发生配位作用,通过配位键的形成,形成稳定的配合物。
金属离子通常是电子亏损或电子富集的离子,而配体则是能够提供电子对的分子或离子。
金属离子与配体之间的配位作用可以通过共价键、离子键或者范德华力等方式来实现。
二、配位键的形成金属离子与配体之间的配位键的形成是金属离子螯合的关键步骤。
常见的配位键包括配位键、共价键和范德华力。
配位键是指金属离子与配体中的一个或多个原子之间形成的化学键。
共价键是指金属离子与配体之间通过共用电子对形成的化学键。
范德华力是指金属离子与配体之间的非共有电子间的相互作用力。
三、螯合剂的选择选择合适的螯合剂对于金属离子螯合的成功非常重要。
螯合剂通常是能够提供多个配位位点的化合物或离子。
常见的螯合剂包括有机酸、有机胺和配位聚合物等。
有机酸是一类能够提供羧基或羧酸根离子的化合物,例如乙二酸、草酸等。
有机胺是一类能够提供氨基或胺根离子的化合物,例如乙二胺、三乙矽胺等。
配位聚合物是一类具有多个配位位点的大分子化合物,例如聚乙烯亚胺、聚丙烯酰胺等。
金属离子螯合在催化剂、药物和环境修复等领域具有广泛的应用。
在催化剂领域,金属离子螯合可以提高催化剂的活性和选择性,加速化学反应的进行。
在药物领域,金属离子螯合可以增强药物的稳定性和生物活性,提高药物的疗效。
在环境修复领域,金属离子螯合可以用于重金属离子的去除和土壤污染的修复。
金属离子螯合是指金属离子与配体之间的配位作用,通过配位键的形成,形成稳定的配合物。
金属离子螯合具有广泛的应用领域,包括催化剂、药物、环境修复等。
选择合适的螯合剂对于金属离子螯合的成功非常重要,常见的螯合剂包括有机酸、有机胺和配位聚合物等。
金属离子螯合剂的作用

金属离子螯合剂的作用金属离子螯合剂是一种能够与金属离子形成稳定的络合物的化合物。
它们在许多领域中都有广泛的应用,包括医学、环境保护、工业生产等。
本文将探讨金属离子螯合剂的作用及其在不同领域中的应用。
金属离子螯合剂在医学领域中起着重要的作用。
它们可以与金属离子结合,形成稳定的络合物,从而减少金属离子对生物体的毒性。
例如,EDTA(乙二胺四乙酸)是一种常用的金属离子螯合剂,可以与重金属离子形成络合物,如铅、汞等,从而降低它们对人体的危害。
此外,金属离子螯合剂还可以用于治疗某些疾病。
例如,某些螯合剂可以与铁离子结合,形成稳定的络合物,用于治疗缺铁性贫血。
金属离子螯合剂在环境保护中也发挥着重要的作用。
许多金属离子在自然界中存在,但它们的过量释放会对环境造成污染。
金属离子螯合剂可以与这些过量的金属离子结合,形成不溶于水的络合物,从而减少金属离子对环境的危害。
例如,EDTA可以与重金属离子结合,形成不溶于水的络合物,从而减少重金属离子在水中的浓度,保护水体的生态环境。
金属离子螯合剂在工业生产中也有广泛的应用。
许多工业过程中需要使用金属离子作为催化剂或反应物。
然而,金属离子的活性往往不稳定,容易发生氧化或还原反应。
金属离子螯合剂可以与金属离子形成络合物,增加其稳定性,从而提高催化剂的效果或减少反应的副产物。
例如,某些有机合成反应需要使用钯离子作为催化剂,但钯离子很容易被氧化。
通过加入适量的金属离子螯合剂,可以稳定钯离子,提高催化剂的使用寿命。
总体而言,金属离子螯合剂在医学、环境保护和工业生产中都有重要的作用。
它们可以减少金属离子对生物体的毒性,保护环境免受金属离子污染,提高催化剂的效果和稳定性。
随着科技的不断发展,金属离子螯合剂的应用领域还将不断扩大。
我们有理由相信,在未来的研究中,金属离子螯合剂将发挥更加重要的作用,为人类带来更多的福祉。
生活垃圾飞灰螯合反应

生活垃圾飞灰螯合反应
首先,生活垃圾焚烧是一种常见的处理方式,它可以将垃圾转化为能量,并减少垃圾的体积。
然而,焚烧过程会产生飞灰,其中包含了一些有害物质,如重金属和有机物。
为了减少这些有害物质的释放,可以采用螯合剂来进行控制。
其次,螯合剂是一种能够与金属离子形成稳定络合物的物质。
在生活垃圾焚烧过程中,添加适量的螯合剂可以与飞灰中的重金属离子发生螯合反应,形成稳定的络合物。
这些络合物具有较低的溶解度和较高的稳定性,可以减少重金属的释放和迁移,从而降低对环境和人体的危害。
此外,飞灰螯合反应还可以改善垃圾焚烧过程中的燃烧效果。
螯合剂的添加可以促进垃圾的燃烧,提高燃烧温度和燃烧效率,减少有机物的生成和排放。
同时,螯合剂还可以抑制飞灰的粒径增长和聚结,减少飞灰的飘散和扩散,有利于飞灰的后续处理和利用。
此外,需要注意的是,螯合剂的选择和使用需要综合考虑多个因素,如螯合剂的稳定性、成本、环境友好性等。
不同的垃圾焚烧设施和飞灰特性可能需要不同的螯合剂和添加方式。
因此,在实际
应用中,需要进行充分的实验和研究,以确定最佳的螯合剂和添加条件。
总结起来,生活垃圾飞灰螯合反应是一种通过添加螯合剂来控制飞灰中重金属离子的释放和迁移的方法。
它可以减少对环境和人体的危害,改善垃圾焚烧过程中的燃烧效果。
然而,螯合剂的选择和使用需要综合考虑多个因素,并进行实验和研究来确定最佳的应用条件。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
双功能螯合剂(bifunctional chelator,BFC)既有很强的金属
螯合基团,又能与生物分子以共价键的形式连接。
生物分子
接上BFC 后,既能与金属牢固结合,又可以保证引入的金属
元素远离生物分子以保证其生物活性不受损失[1 - 3]。
BFC 包
含3 部分:螯合单元,结合基团和配体构架。
理想的BFC 应
该能够在BFC-生物分子低浓度条件下,与放射性核素牢固结
合,并且有很高的标记速度[2]。
N2S2
类BFC 由于其结构、性质的特殊性(骨架结构体积
小;易于形成稳定络合物;与生物分子连接时,较好地保持
了其原有的生化性质),成为BFC 领域研究的重点[4 - 21]。
其
中,单胺单酰胺二硫醇(monoamino-monoamide dithiol,MAMA)等
类联接剂近年来备受关注,并已经被广泛应用于联接受体配
基、多肽、蛋白质、单克隆抗体等[13 - 21];但在合成路线以及改
善其稳定性方面,尚待进一步探索[12 - 16],以符合现今环境及
绿色化学发展的要求。
本文以半胱胺盐酸盐为起始原料,将其巯基用对甲氧苄
基保护后与溴乙酰溴经“one-pot reaction”合成MAMA 联接剂
前体,N-(2"-对甲氧苄巯乙基)-2-[(2'-对甲氧苄巯乙基)氨基]
乙酰胺,并将其制成更稳定且易于保存的盐酸盐。
螯合剂,是一类能与金属离子形成多配位络合物的交联功能有机材料,其组成是由一个简单正离子和几个中性分子或离子结合而成的复杂离子,称为配离子(又称络离子),含有配离子的化合物叫配位化合物[18]。
它能与重金属离子强力螯合,形成絮凝,达到去除各种重金属目的。
与传统去除水中重金属污染的方法相比,螯合剂具有可处理低重金属离子浓度废水、可同时去除多种重金属离子、可去除胶质重金属、不受共存盐类的影响、可在较宽pH范围内反应等许多优点[19]。
螯合剂大致可分为无机和有机两类,以多聚磷酸盐为代表的无机螯
合剂, 如三聚磷酸钠等,其缺点是高温下易分解,使螯合能力降低甚至消失,而且只适用于碱性介质,只能用于硬水的软化。
这类螯合
剂容易造成水体富营养化,已逐渐被淘汰。
目前,天然高分子和人
工合成母体的高分子螯合吸附剂是主要研究方向,可根据配位原子
对其进行分类,因为从配位原子的种类很容易预测螯合吸附剂对重
金属离子的选择性,并指导其合成过程。
螯合吸附剂中可作为配位
原子的有第五族至第七族元素,以O、N、S、P、As、Se为主[20]
二硫代胺基甲酸盐类是目前实际应用最广泛的重金属螯合剂,主要
为有机伯胺或仲胺与CS2在碱性条件下反应生成,它能捕捉阳离子
并趋向成键,而生成难溶的相对分子质量可达数百万甚至上千万的
二硫代氨基甲酸盐,可起到絮凝沉淀效果[21]。
刘新梅等[22]以二乙
烯三胺、二硫化碳为原料合成了二硫代氨基甲酸盐类重金属捕集剂DTC(BETA),研究最佳合成工艺,并用DTC(BETA)处理单一含铜废水,结果表明,它对单一含铜废水的有较好的捕集效果。
令玉林,戴友芝等[23]利用环氧氯丙烷将二乙烯三胺接枝到氰尿酸
分子上,然后加入NaOH和CS2,在仲胺上引入二硫代氨基甲酸(DTC)基团,合成了一种新的二硫代氨基甲酸盐类重金属螯合剂CDTC,并对其处理游离Cu2+、EDTA络合铜和柠檬酸络合铜废水的性能进行了研究。
实验结果表明:CDTC能直接去除已络合的铜,
对不同形态的Cu2+去除率均达99%以上,在废水pH=3-12范围内,CDTC对Cu2+的去除率高且稳定;处理废水产生的絮体沉降性能好,
不需额外添加其他絮凝剂;螯合沉淀物在弱酸性和碱性条件下很稳定,不会产生二次污染。
Nuri Unlu等[24]研究通过两步合成新型改
性螯合剂,首先将乙二胺接枝到孢粉素上(DAE-S),然后用CS2将二
硫代氨基甲酸盐与DAE-S接枝,并利用合成的螯合吸附剂处理含
Cu2+、Pb2+、Cd2+的废水,研究其对重金属离子的螯合吸附性能。
结果表明,该螯合吸附剂的吸附过程符合朗格缪尔吸附等温方程,
符合伪二阶动力方程,对Cu2+、Pb2+、Cd2+的最大吸附量分别为
0.2734、0.4572和0.0631 mmol·g-1。
以螯合剂为基本组成的环境功能材料还有高分子螯合剂和螯合树脂,高分子螯合剂对不同价态、不同几何构型的金属离子有选择性形成
螯合物的能力,它能与水体中重金属离子快速络合,生成良好的絮凝,沉降快速。
因此,研究合成新型螯合吸附剂,使其功能化和稳
定化,提高其处理水体重金属污染物的效率,找到一种最合理去除
水体重金属污染物的方法。
例如,G.R.Kiani等[25]用聚丙烯腈和二
乙烯三胺在一定条件下反应制得PAN-DTC树脂,根据二乙烯三胺
的浓度不同分为PAN-DTC50和PAN-DTC150,研究其对Zn2+和
Fe3+的吸附作用。
结果表明,该螯合树脂的吸附性能随着pH值的
增加而增加,PAN-DTC150对Zn2+和Fe3+的最大吸附量分别为
1.38和1.42mmol·g-1。
Lan Bai等[26]研究首先用聚醚酰亚胺和CS2
一定条件下反应合成高分子MDTC,再与氯功能化硅胶反应合成新
型螯合吸附剂Si-DTC,并处理含Pb2+、Cd2+、Cu2+、Hg+的废水。
研究了不同条件对Si-DTC螯合吸附性能的影响,分别用不同吸附等温线表征该螯合吸附剂的吸附过程,对Pb2+、Cd2+、Cu2+、Hg+最大吸附量分别为0.34、0.32、0.36和0.40mmol·g-1。
汤红仙等[27]采用悬浮聚合方法,以丙烯酸和苯乙烯为共聚单体,二乙烯苯为交联
剂,甲苯和环己烷为混合致孔剂,引入多胺基团,合成了一系列多
胺型螯合树脂。
研究结果表明,在n(AA)∶n(St)=2.17、交联剂用量(占共聚单位质量)15%、致孔剂用量(占共聚单位质量)50%的条件下
合成的树脂外观规整。
以二乙烯三胺为螯合基团,在pH=5时,树
脂吸附Ni2+的性能最佳,吸附容量达37.7mg·g-1,优于目前的离子交换树脂。
根据目前的研究进展,有机高分子螯合吸附剂的制备方法主要分为
两种合成方法,一种是将含螯合功能基的单体经过加聚、缩聚、开
环聚合或逐步聚合等方法制取。
这种合成途径由于功能基来自单体,因而制成的螯合树脂的吸附容量大,螯合功能基在分子链上分布均匀,合成过程较为困难。
该方法合成的多为有机类螯合剂,发展迅速,品种逐年增加, 成为螯合剂的发展主流,其种类众多,如氨基羧酸类、有机磷酸类、羟基羧酸类和聚羧酸类等。
另一种是利用天然
高分子物质或者合成的母体,通过化学反应将具有螯合功能的侧基
引入其中,反应形成新的具有吸附性质的物质,通过吸附作用去除
水中污染物。
这种螯合剂由于引入天然高分子物质,具有合成简便、价格低廉、吸附容量大、易洗脱、干扰少和稳定性好等优点,与离
子交换树脂相比,与重金属离子的结合能力更强,选择性也更好。
Wang等[28]利用微乳液法制备包裹了纳米零价铁的聚合物,应用于水体中三氯乙烯的降解。
研究讨论了pH值、三氯乙烯的起始浓度、纳米零价铁含量和离子强度等影响降解速率的因素。
实验研究表明,载入聚合物后不仅能够阻止纳米零价铁被环境介质过度氧化,还能
促使三氯乙烯和被包裹后的纳米颗粒有效互溶。
Vítor S.Amaral等[29]研究用硅胶包覆磁性赤铁矿,再用二硫代氨基甲酸盐(DTC)功能化,合成一种兼具螯合和吸附功能的新型材料,研究该新型材料对重金
属离子的处理效果。
研究结果表明,该功能化材料处理含痕量汞离
子的废水,对Hg+的吸附去除率达74%,由于磁性分离和螯合性能
共同作用,该材料在去除重金属离子方面有很大的潜能。
