第一节共价键
第一节 共价键

单位:kJ/mol
【例如】形成l mol H—H键释放的最低能量为436.0 kJ, 则 H—H键能为436.0 kJ/mol 形成1 molN三N键释放的最低能量为946 kJ 则 N三N键能为946 kJ/mol
键
键能
键
键能
F-F
Cl-Cl Br-Br I-I C-C C=C C≡C
157
242.7 193.7 152.7 347.7 615 812
常见的等电子体:
⑴N2 ⑵O3
CO SO2
CN- NO2N 2O
C22AlO2SiO32-
⑶CO2 CS2
⑷SO3 NO3⑸NH3 H3O+
CO32-
⑹CH4
NH4+
-NO2
(7) NO2
科学视野: 用质谱仪测定分子结构
现代化学常利用质谱仪测定分子的结构。它的基本 原理是在质谱仪中使分子失去电子变成带正电荷的分子 离子和碎片离子等粒子。由于生成的分子离子、碎片离 子具有不同的相对质量,它们在高压电场加速后,通过 狭缝进入磁场分析器得到分离,在记录仪上呈现一系列 峰,化学家对这些峰进行系统分析,便可得知样品分子 的结构。例如,图2—7的纵坐标是相对丰度(与粒子的 浓度成正比),横坐标是粒子的质量与电荷之比(m/e) ,简称质荷比。化学家通过分析得知,m/e=92的峰是 甲苯分子的正离子(C6H5CH3+),m/e=91的峰是丢失一 个氢原子的的C6H5CH2+ ,m/e=65的峰是分子碎片…… 因此,化学家便可推测被测物是甲苯。
π键的电子云
键特点:两个原子轨道以平行或“肩并肩” 方式重
叠;原子重叠的部分分别位于两原子核构成平面的两 侧,如果以它们之间包含原子核的平面为镜面,它们 互为镜像,称为镜像对称 由于键重叠程度要比键小,所以键的强度要 比键大。
第二章分子结构与性质第一节共价键

第二章分子结构与性质第一节共价键共价键是指两个原子通过共用电子对来结合在一起的化学键。
在分子化合物中,共价键是最常见的键类型,它对于分子的结构和性质起着决定性的作用。
一、共价键的形成共价键的形成是由于原子之间存在着相互吸引力,这种相互吸引力是由于原子之间互相排斥的静电力降低而产生的。
具体来说,当两个原子靠近到一定距离时,它们的外层电子会发生重叠,从而形成一个电子对。
这个电子对同时属于两个原子,使得两个原子之间形成了一个共享电子对的区域,即共价键。
共价键的形成是一种动态的过程。
在共价键形成的过程中,原子的电子云发生了重新排布,电子从原子的一个轨道转移到另一个轨道,从而形成了共价键。
在共价键形成后,原子成为了一个整体,形成了一个稳定的分子结构。
二、共价键的性质共价键具有一些特殊的性质,这些性质决定了共价键的稳定性和键能。
1.共价键的稳定性共价键的稳定性取决于原子之间的相互作用力的强弱。
一般来说,原子的价电子数越多,形成共价键的能力越强。
也就是说,原子的电负性越大,形成的共价键越稳定。
此外,共价键的稳定性还受到原子之间的距离的影响。
在共价键中,原子之间的距离越近,共价键越稳定。
2.共价键的键能共价键的强度可以用键能来表示。
键能是指在断裂共价键时需要输入的能量的大小。
键能的大小取决于共享电子对的稳定性。
一般来说,共价键的键能越大,其共享电子对越稳定,键越难被断裂。
共价键的键能可以通过一定的实验方法(如光合成实验)来测定。
三、共价键的类型根据共享电子对的数目和电子云的排布形式,共价键可以分为单键、双键和三键。
1.单键单键是由两个原子共享一个电子对形成的。
单键的键能较低,容易被断裂。
常见的单键有C—C键、C—H键等。
单键也是化学反应中最常见的键类型。
2.双键双键是由两个原子共享两个电子对形成的。
双键的键能比单键高,比较稳定。
常见的双键有C=C键、O=O键等。
3.三键三键是由两个原子共享三个电子对形成的。
三键的键能最高,非常稳定。
第一节 共价键

第一节共价键1.了解共价键的主要类型σ键和π键,知道σ键和π键的明显差别和一般规律。
2.理解键能、键长、键角等键参数的概念,并能应用键参数说明简单分子的某些性质。
3.了解等电子原理,结合实例说明等电子原理的应用。
共价键1.本质和特征(1)本质:在原子之间形成共用电子对。
(2)特征:饱和性——决定分子的组成;方向性——决定分子的立体构型。
2.类型(按成键原子的原子轨道的重叠方式分类)(1)σ键形成由两个原子的s轨道或p轨道“头碰头”重叠形成类型ss型H—H的s-s σ键的形成s-p型H—Cl的s-p σ键的形成p-p型Cl—Cl的p-p σ键的形成特征以形成化学键的两原子核的连线为轴做旋转操作,共价键电子云的图形不变,这种特征称为轴对称;σ键的强度较大形成由两个原子的p轨道“肩并肩”重叠形成pp π键pp π键的形成特征π键的电子云具有镜面对称性,即每个π键的电子云由两块组成,分别位于由两原子核构成平面的两侧,如果以它们之间包含原子核的平面为镜面,它们互为镜像;π键不能旋转;不如σ键牢固,较易断裂(3)判断σ键、π键的一般规律共价单键为σ键;共价双键中有一个σ键、一个π键;共价三键由一个σ键和两个π键组成。
1.正误判断(正确的打“√”,错误的打“×”,并阐释错因或列举反例)。
语句描述正误阐释错因或列举反例(1)原子轨道在空间都具有方向性(2)一般来说,σ键比π键强度大,更稳定(3)N2分子中σ键与π键的个数之比是2∶1(4)σ键和π键都只存在于共价分子中(5)两个原子间可以只形成σ键,但不能只形成π键(2)√(3)×应为1∶2(4)×离子化合物中也存在,如CaC2(5)√2.(2020·铜川高二检测)下列说法中正确的是()A.乙烷分子中,既有σ键,又有π键B.Cl2和N2的共价键类型相同C.由分子构成的物质中一定含有σ键D.HCl分子中含一个s-p σ键解析:选D。
第一节 共价键
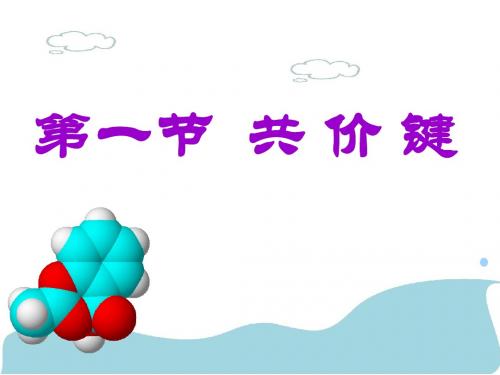
①s-s σ键的形成
H H
氢原子形成氢分子的电子云描述
②s-p σ键的形成
H H-Cl Cl
H-Cl的s-pσ键的形成
③p-p σ键的形成
Cl Cl
Cl
Cl
Cl-Cl的p-pσ键的形成
(2)π键的形成
π键的电子云由两块组成,分别位于由两原子 核构成平面的两侧,如果以它们之间包含原 子核的平面为镜面,它们互为镜像,这种特 征为镜像对称。
4、共价半径:
相同原子的共价键键长的一半称为共价半径
思考与交流P32
1、形成2mo1HCl释放能量: 2×431.8 kJ -(436.0kJ+242.7kJ)= 184.9 kJ 形成2mo1HBr释放能量: 2×366kJ -(436.0kJ+193.7kJ)= 102.97kJ HCl释放能量比HBr释放能量多,因而生成 的HCl更稳定,即HBr更容易发生热分解生 成相应的单质.
p-pπ键的形成
小结 项目
键型 成键方向
σ键
沿轴方向 “头碰头” 轴对称 强度大, 不易断裂
π键
平行方向 “肩并肩” 镜像对称 强度较小, 易断裂
电子云形状 牢固程度
成键判断 规律
共价单键是σ键,共价双键中一个 是 σ键,另一个是π键,共价三键 中一个是σ键,另两个为π键。
1、氮气分子中原子轨道重叠方式如何?
z y
z y
x
2.钠和氯通过得失电子同样也是形成电子对, 为什么这对电子不被钠原子和氯原子共用形 成共价键而形成离子键呢?你能从原子的电 负性差别来理解吗?讨论后请填写表2-2: Na Cl H Cl C O 原子 电负性 3.5 0.9 3.0 2.1 3.0 2.5
第二章第一节共价键(第一课时)
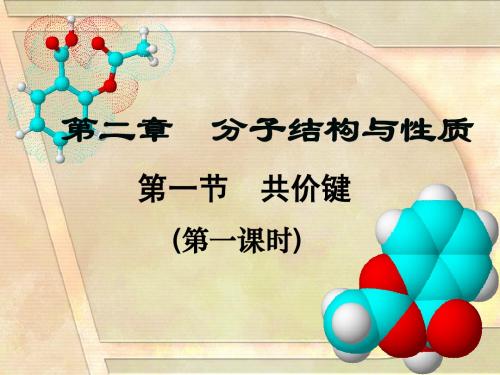
科学探究
键组成。 别是由几个σ键和几个π键组成。 3、乙烷、乙烯、乙炔分子中的共价键分 乙烷、乙烯、
乙烷: 键一个π 乙烷 : 7 个 σ 键 乙烯 : 5 个 σ 键一个 π 键 乙炔: 键两个π 乙炔:3个σ键两个π键
总结: 总结:共价键的类型
σ键:“头碰头” 键 头碰头”
形成σ 形成σ键的电子 电子云形状呈轴对称 称为σ电子。 称为σ电子。
电子重叠形成的σ键 ③ p—p σ键:由两个 电子重叠形成的 键,如Cl—Cl。 键 由两个p电子重叠形成的 。
Cl Cl Cl Cl
小结: 键成键方式 头碰头” 小结 σ键成键方式 “头碰头”
S-S重叠 S-S重叠
S-P重叠
P-P重叠 P-P重叠
注意: 键成键方式采用“头碰头” 注意: σ键成键方式采用“头碰头”式,以取得 原子轨道的最大重叠,从而使体系能量降至最低, 原子轨道的最大重叠,从而使体系能量降至最低, 达到稳定状态。 达到稳定状态。
用电子云来描述共价键的形成过程
π键形成过程 p-p π键形成过程
“肩并肩” 肩并肩”
2、π键 键 (1)定义:两个p轨道除了“头碰头”重叠 定义:两个p轨道除了“头碰头” 形成σ键外, 轨道还可以“肩并肩” 形成σ键外,p—p轨道还可以“肩并肩”的 方式发生轨道重叠,这种键称为π 方式发生轨道重叠,这种键称为π键。
(3)类型 )
电子重叠形成的σ键 ① s—s σ键:由两个 电子重叠形成的 键,如H—H。 键 由两个s电子重叠形成的 。 H
H H
H
电子和一个p电子重叠形成的 ② s—p σ键:由一个 电子和一个 电子重叠形成的 键, 键 由一个s电子和一个 电子重叠形成的σ键 如H—Cl。 。
精选 《共价键》参考完整教学课件PPT

三键:如N≡N键
2按共用电子对是否偏移
非极性键:如C-C键 极性键:如H-C键
3按原子轨道的重叠方式 σ键
π键
观察以以下图中乙烷、乙烯和乙炔分子的球棍模型,答复相关问题。
问题思考: 1乙烯和乙炔分子中的碳原子间,既存在σ键,又存在π键,σ键和π键的成键方式 有何不同 提示:σ键是原子轨道以“头碰头〞方式发生重叠成键;π键是轨道与轨道以“ 肩并肩〞方式发生重叠成键。
- σ键
氢原子形成氢分子的电子云描述〔两个轨道重叠〕
H
H
H
H
电子云
σ键
↑
↓
1s
1s
原子轨道在两个原子核间重叠,意味着电子出现在核间的概率增大,因此可以说,核 间电子好比在核间架起一座带负电的桥梁,把带正电的两个原子核“黏结〞在一起了。
相互靠拢
H2中的共价键称为σ键。H2中的σ键是由两个轨道重叠形成的。 σ键的特征是:以形成化学键的两原子核的连线为轴旋转,共价键电子云 的图形不变,这种特征为轴对称。 H2中的σ键是由两个轨道重叠形成的,可称为- σ键。轨道和轨道,轨道和轨 道重叠是否也能形成σ键呢?我们看一看HC和C2中的共价键。
水分子的空间充填模型
过氧化氢分子的空间充填模型
1水分子中的共价键是哪些原子形成的哪类共价键为什么水分子中的三个原子不 在一条直线上 提示:水分子中的共价键是由O原子与H原子形成的σ键;共价键的方向性导致水 分子中的三个原子不在一条直线上。
、H元素的化合价分别是多少?为什么 提示:过氧化氢分子中O、H元素的化合价分别是-1价、1价。 过氧化氢分子中有两类共价键,O—O间的共价键是非极性键,共用电子对不偏 移;O—H键是极性键,氧的电负性较H大,共用电子对偏向氧。 3共价键可以存在于哪些物质中?举例说明。 提示:共价键可以存在于共价单质中,如H2、O2、N2等;可以存在于共价化合 物中,如H2O、H2O4、CH4等;也可以存在于离子化合物中,如NaOH、NH4C 、Na2O2等。
2.1共价键

(4)键能和键长决定共价键的稳定性,键长和键角决定 分子的立体结构。
(5)等电子体具有相似的化学键特征,它们的许多性质 是相近的。
3
面正三角形结构,B项正确;H3O+和PCl3价电子总数不相
等,不是等电子体,C项不正确;CO2和CS2是等电子体,
D项正确。故答案为B、D项。
[答案] BD
常见等电子体的推断
(1)同主族元素的价电子数相等,可将元素符号变换。
如CO2和CS2;CCl4和SiCl4;SO2和O3;PCl3和NCl3。 (2)同周期相邻元素的原子序数相差1,元素符号变换时,
[解析] 本题主要考查σ键和π键的形成。由于π键的键 能小于σ键的键能,所以反应时易断裂,A项正确;在分子 形成时为了使其能量最低,必然首先形成σ键,根据形成 的原子的核外电子排布来判断是否形成π键,所以B项正确, D项错误;像H原子跟Cl原子只能形成σ键,所以C项正确。
[答案] D
两个原子形成共价键时,一定有σ键,可能有π键;共 价双键有一个是σ键,一个是π键;共价三键有一个是σ键, 两个是π键。
一、共价键 1.本质 在原子之间形成 共用电子对 。 2.类型 按照原子轨道 重叠 的方式共价键分为σ键和 π 键。 (1)σ键。 ①形成:成键原子的原子轨道“头碰头”重叠而形成。
a.ss σ键: 由两个 s 轨道重叠形成的σ键,如H—H。
b.sp σ键: 由一个 s 轨道和一个 p轨道重叠形成的σ键,如H—Cl。
(2)方向性: 除s轨道是球形对称外,其他的原子轨道都具有一定的 空间取向。在形成共价键时,原子轨道重叠得愈多,电子 在核间出现的概率越大,所形成的共价键就越牢固,因此 共价键将尽可能沿着电子出现概率最大的方向形成,所以 共价键具有方向性。
第一节 共价键
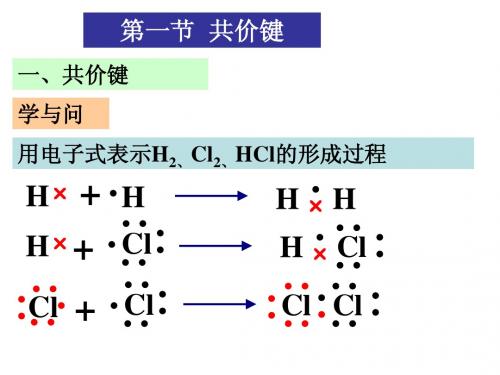
1、下列各组表述中,两种粒子不属于同种元素 原子的是 A、3p能级有一个空轨道的基态原子和核外电子 排布为1s22s2 2p6 3s2 3p2的原子 B、2p能级无空轨道,且有一个未成对电子的基 态原子和最外层电子排布为2s2 2p5的原子 C、M层全充满而N层为4s2 的原子和核外电子 排布为1s22s2 2p6 3s2 3p6 4s2的原子 D、最外层电子数是核外电子总数的1/5的原子 和最外层电子排布为4s2 4p5的原子
键长的长短,与化学键的键能大小有什么关系
稳定。
键长的大小与化学键的稳定性又有什么联系?
3.键角:在原子数超过2的分子中,两个共价键之间 的夹角称为键角。
多原子分子的键角一定,表明共价键具有方向性。
三、等电子原理
CO分子和N2分子的某些性质
分子
沸点/℃ 在水中的 分子解 分子的 溶解度 离能 价电子 (室温) kJ/mol 总数 CO -205.05 -191.49 2.3mL 1075 10 熔点 /℃
键 H-Cl H-Br H-I
键能 /kJ · -1 mol 431.8 366 298.7
思考与交流
2.已知键能: N≡N 键能是946KJ/mol,H-H 键能是 436KJ/mol, H-N键能是391KJ/mol N2(g) +3H2(g)
催化剂 高温高压
2NH3(g),
从理论上计算这个反应是放热反应还是吸热反应。 并计算生成1molNH3放出(或吸收)的热量是多少?
5、某元素原子的核电荷数是电子层数的5倍,其 质子数是最外层电子数的3倍,该元素的原子结 构示意图为________________ ,轨道表示式为 __________________。
3、下列原子构成的单质中既能与硫酸反应,又 能与烧碱反应,且都产生氢气的是 A、核内无中子的原子 B、价电子构型为3s2 3p1 C、最外层电子数等于倒数第三层上的电子数的 原子 D、N层中无电子,最外层上的电子数等于电子 层数的原子
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
用电子式表示离子键、共价键的形成过程要注意 两点: (1)要搞清楚成键原子间形成 的是离子键还是 共价键。 (2)不要混淆“用电子式表示结构”和“用电子 式表示分子的形成 过程 ”。 一个化学反应的过程 ,本质上就是旧化学键断裂 和新化学键形成的过程。
极性共价键、非极性共价键?
化学键 相邻的原子之间强烈的相互作用叫做化学键。 注: A、化学键是存在于分子内相邻的原子之间“强烈 的相互作用” B、不要把“强烈的相互作用”说成是结合力。
π键:电子云分布的界面图好象两个长圆 形的冬瓜,是对于通过键轴的一个平面对 称的。电子云采用“肩并肩”的方式重叠, 由两块组成,分别位于由两原子核构成平 面的两侧,互为镜象,不可以围绕成键的 两原子核的连线旋转。比σ键重叠程度小很 多,。所以π键的键能比σ键的键能要小些, π键电子的能量较高,易活动,是化学反应 的积极参与者。 一般规律:共价单键是σ键;而共价双键 中有一个σ键,另一个是π键;共价三键由 一个σ键和两个π键组成。
第二章分子结构与性质
第一节 共价键
学习重点: σ键和π键的特特征性质; 用键能、键长、键角等说明简单分子的某些性质。 学习难点: σ键和π键的特征;键角。 第一节 共价键
一、共价键 [问](1)两个H在形成H2时,电子云如何重叠? (2)在HCl、Cl2中,电子云如何重叠? 1、价键理论的基本要点: (1)自旋方向相反的成单电子相互接近时,核 间电子云密度较大,可形成稳定的化学键。 (2)共价键有饱和性。一个原子有几个未成对 电子,便可和几个自旋方向相反的电子配对成键。 按照价键理论,未成对电子的电子数,就是原子 的化合价,它应等于形成共价目键的数目。 (3)共价键有方向性。共价键尽可能沿着原子 轨道最大重叠的方向形成。
什么是离子化合物?
表示离子化合物的形成过程常出现错误: A、离子漏标电荷数 B、离子所带正负电荷数与元素的化合价表 示 法分辨不清 C、阴离子未加括号 D、把相同离子归在一起, E、把“→”写成“=”。
二、共价键 1、定义:原子之间通过共用电子对所形成的 相互作用,叫做共价键。 2、形成 条件: 成键的粒子:原子 成键的性质:共用电子对。 3、表示方法 单键: H2 双键: CO2 叁键: N2 4.结构式: 化学上常用一根短线表示一对共用电子。
从原子轨道的角度认识σ键和π键的特征
二、键参数——键能、键长与键角 表面2-1思考:(1)键能是共价键强度的一 种标度,键能的大小与键的强度有什么样关系? (2)键能与化学反应的能量变化有什么联系? 怎样利用键能的数据计算反应的热效应?1、 键能:气态基态原子形成1mol化学键释放的 最低能量。 是衡量化学键强弱的物理量。通常为正值。 对于双原子分子,键能就等于键的离解能, 其大小等于气态原子生成气态分子的能量,而 符号相反。 键能越大,即形成化学键时放出的能量越多, 意味着这个化学键越稳定,越不容易被打断。
σ键:电子云密度分布,对于两个原子核 的联线——“键轴”呈圆柱形对称。 特征:以形成化学键的两原子核的连线 为轴作旋转操作。共价键电子云的图形不 变,这种特征称为轴对称,可以围绕成键 的两原子核的连线旋转。 成键时,电子云采取“头碰头”的方式 重叠形成的——能量最低。 类型:S-Sσ键、S-Pσ键、P-Pσ键
旧知识回顾
化学键 一、离子键 1、定义:使阴、阳离子结合成化合物的静电 作用,叫做离子键。 2、形成条件:活泼金属(ⅠA、ⅡA)与活泼 非金属(ⅥA、ⅦA) 二、电子式 1、定义:在元素符号周围用小黑点(或×号) 来表示原子的最外层电子。这种式子叫做电子 式。
2、书写方法: 原子:离子:阳离子 阴离子: 离子化合物:XY型:X2Y型:XY2型
2、键长:形成共价键两个原子之间的核 间距。 键长越短,往往键能越大,表明共价键越 稳定。 怎样知道多原子分子的形状? 3、键角:分子中键和键之间的夹角。 键角是描述分子空间立体结构的重要参数。 各种分子的构形。
分子 CO2 H2O
共价键的夹角 分子的立体结 构
图示
NH3CBiblioteka 4规律:一般说来,如果知道某个分子中的键长和键 角数据,那么这个分子的几何构型就确定了。 键能越大,键长越短,化学键就越牢固,含有该键 的分子就越稳定,越不易发生化学反应。反之然。 三、等电子原理 1、等电体 氮气、为同核双原子,一氧化碳为异核双原子,但 它们具有相等的价电子总数。 2、等电子原理及等电子体 原子总数相同、价电子总数相同的分子具相似的化 学键特征,它们的许多化学性质是相近的,,这条 规律称之为等电子原理,这样的分子叫等电子体。
