安徽高考化学试题及答案
安徽省阜阳市化学高考试卷及答案指导(2025年)

2025年安徽省阜阳市化学高考复习试卷及答案指导一、单项选择题(本大题有16小题,每小题3分,共48分)1、下列物质中,既能与盐酸反应又能与氢氧化钠溶液反应的是:A、Na2CO3B、Al(OH)3C、Fe2O3D、CuSO4答案:B 解析:本题考查的是物质的两性性质。
选项中,只有氢氧化铝(Al(OH)3)是一种典型的两性氢氧化物,既可以表现出碱性,与强酸如盐酸反应生成铝盐和水;也可以表现出酸性,与强碱如氢氧化钠反应生成偏铝酸盐和水。
而其他选项,碳酸钠(Na2CO3)只能与酸反应,三氧化二铁(Fe2O3)只能与碱反应,硫酸铜(CuSO4)既不是酸也不是碱,因此它不会与强碱发生显著的反应。
所以正确答案是 B、Al(OH)3。
2、下列物质中,不属于电解质的是()A. 氢氧化钠(NaOH)B. 硫酸铜(CuSO4)C. 氯化钠(NaCl)D. 二氧化硅(SiO2)答案:D解析:电解质是指在水溶液中或熔融状态下能导电的化合物。
选项A、B、C均为离子化合物,在水溶液中可以电离出离子,因此是电解质。
而选项D二氧化硅是共价化合物,在水溶液中不电离,因此不属于电解质。
3、下列关于乙醇和乙酸的说法中,正确的是 ( )A. 乙醇和乙酸都含有碳氧双键B. 乙醇和乙酸都能与钠反应生成氢气C. 乙醇和乙酸都能使紫色石蕊试液变红D. 乙醇和乙酸之间能发生酯化反应,酯化反应属于加成反应答案:B解析:A选项:乙醇的分子式为C2H6O,结构简式为CH3CH2OH,从结构简式可以看出,乙醇分子中只含有单键,包括碳碳单键、碳氢单键和碳氧单键,并不含有碳氧双键。
而乙酸的分子式为C2H4O2,结构简式为CH3COOH,从结构简式可以看出,乙酸分子中含有一个碳氧双键。
因此,A选项错误。
B选项:乙醇和乙酸都可以与金属钠反应,生成对应的钠盐和氢气。
这是因为乙醇分子中的羟基(−OH)和乙酸分子中的羧基(−COOH)中的氢原子都具有一定的活性,可以与钠发生置换反应。
高考安徽化学答案及解析
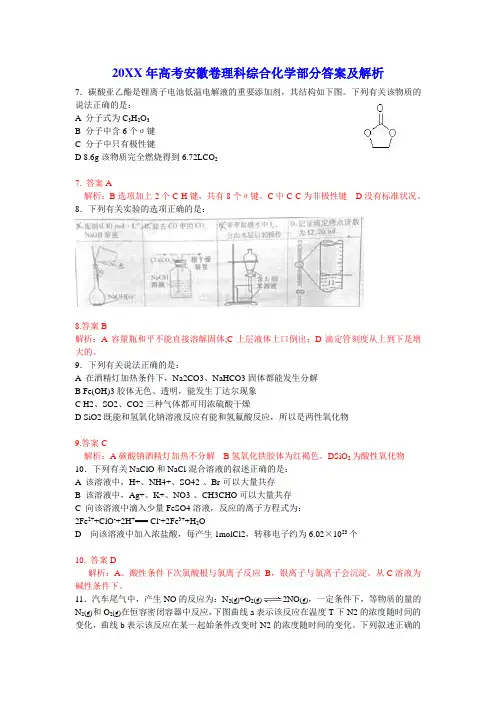
20XX年高考安徽卷理科综合化学部分答案及解析7.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如下图。
下列有关该物质的说法正确的是:A 分子式为C3H2O3B 分子中含6个σ键C 分子中只有极性键D 8.6g该物质完全燃烧得到6.72LCO27. 答案A解析:B选项加上2个C-H键,共有8个σ键。
C中C-C为非极性键D没有标准状况。
8.下列有关实验的选项正确的是:8.答案B解析:A容量瓶和平不能直接溶解固体;C上层液体上口倒出;D滴定管刻度从上到下是增大的。
9.下列有关说法正确的是:A 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解B Fe(OH)3胶体无色、透明,能发生丁达尔现象C H2、SO2、CO2三种气体都可用浓硫酸干燥D SiO2既能和氢氧化钠溶液反应有能和氢氟酸反应,所以是两性氧化物9.答案C解析:A碳酸钠酒精灯加热不分解B氢氧化铁胶体为红褐色。
DSiO2为酸性氧化物10.下列有关NaClO和NaCl混合溶液的叙述正确的是:A 该溶液中,H+、NH4+、SO42-、Br-可以大量共存B 该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存C 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+=== Cl-+2Fe3++H2OD 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个10. 答案D解析:A。
酸性条件下次氯酸根与氯离子反应B,银离子与氯离子会沉淀。
从C溶液为碱性条件下。
11.汽车尾气中,产生NO的反应为:N2(g)+O2(g)2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。
下列叙述正确的是:A 温度T下,该反应的平衡常数K=B 温度T下,随着反应的进行,混合气体的密度减小C 曲线b对应的条件改变可能是加入了催化剂D 若曲线b对应的条件改变是温度,可判断该反应的△H<011. 答案A解析:B密度不变;C使用催化剂平衡不移动;D温度改变氮气浓度减小说明正反应为吸热反应。
安徽高考化学试题及答案

安徽高考化学试题及答案一、选择题(每题3分,共30分)1. 下列元素中,属于金属元素的是:A. 碳B. 氧C. 铁D. 硫答案:C2. 化学反应速率与反应物浓度的关系是:A. 无关B. 正比C. 反比D. 无关答案:B3. 下列物质中,属于电解质的是:A. 酒精B. 蔗糖C. 硫酸D. 植物油答案:C4. 根据元素周期表,下列元素中属于同一主族的是:A. 钠和钾B. 氧和硫C. 氢和氦D. 镁和铝答案:B5. 根据勒夏特列原理,下列操作中不能使平衡向正反应方向移动的是:A. 增加反应物浓度B. 减少生成物浓度C. 增加生成物浓度D. 降低温度答案:D6. 下列化合物中,属于共价化合物的是:A. NaClB. HClC. CaOD. MgO答案:B7. 根据化学平衡移动原理,下列物质中,加入催化剂会改变平衡位置的是:A. 氮气和氢气合成氨B. 碳酸钙分解C. 铁和盐酸反应D. 水的电离答案:C8. 下列反应中,属于氧化还原反应的是:A. 氯化钠和硝酸银反应B. 碳酸钙分解C. 氢气和氧气反应D. 硫酸铜和氢氧化钠反应答案:C9. 下列物质中,具有两性的是:A. 氢氧化钠B. 硫酸C. 氢氧化铝D. 硝酸答案:C10. 根据酸碱中和反应原理,下列物质中,可以和盐酸发生中和反应的是:A. 氢氧化钠B. 碳酸钠C. 氯化钠D. 硫酸钠答案:A二、填空题(每题5分,共20分)1. 写出下列物质的化学式:- 水:H2O- 二氧化碳:CO2- 氧化铁:Fe2O3- 硫酸:H2SO42. 根据质量守恒定律,化学反应前后元素的种类不变,质量不变。
请写出下列化学反应的化学方程式:- 镁在氧气中燃烧:2Mg + O2 → 2MgO- 氢气和氧气反应生成水:2H2 + O2 → 2H2O3. 写出下列物质的离子方程式:- 硫酸铜和氢氧化钠反应:Cu2+ + 2OH- → Cu(OH)2↓- 碳酸钙和盐酸反应:CaCO3 + 2H+ → Ca2+ + CO2↑ + H2O4. 根据反应速率的定义,下列物质中,反应速率最快的是:- 在相同条件下,反应速率与反应物浓度成正比,浓度越大,反应速率越快。
2023年安徽高考化学真题及答案
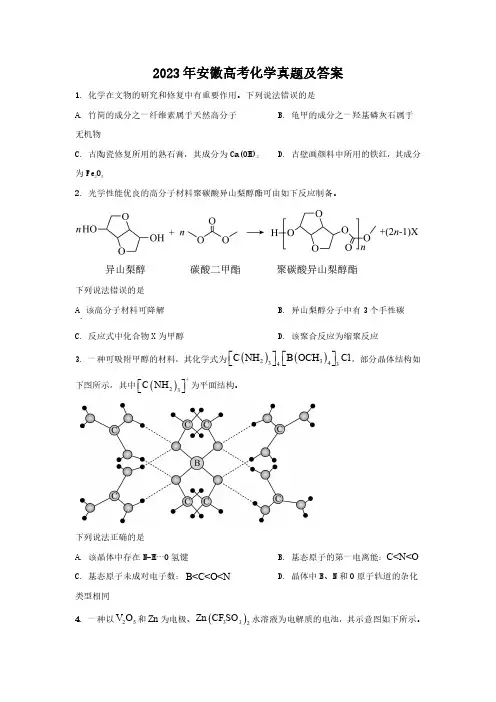
2023年安徽高考化学真题及答案1.化学在文物的研究和修复中有重要作用。
下列说法错误的是A.竹简的成分之一纤维素属于天然高分子 B.龟甲的成分之一羟基磷灰石属于无机物C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)2D.古壁画颜料中所用的铁红,其成分为Fe 2O 32.光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是A .该高分子材料可降解B.异山梨醇分子中有3个手性碳C.反应式中化合物X 为甲醇D.该聚合反应为缩聚反应3.一种可吸附甲醇的材料,其化学式为()()233434C NH B OCH Cl ⎡⎤⎡⎤⎣⎦⎣⎦,部分晶体结构如下图所示,其中()+23C NH ⎡⎤⎣⎦为平面结构。
下列说法正确的是A.该晶体中存在N-H…O 氢键B.基态原子的第一电离能:C<N<OC.基态原子未成对电子数:B<C<O<ND.晶体中B、N 和O 原子轨道的杂化类型相同4.一种以25V O 和Zn 为电极、()332Zn CF SO 水溶液为电解质的电池,其示意图如下所示。
放电时,2+Zn 可插入25V O 层间形成x 252Zn V O nH O ⋅。
下列说法错误的是A.放电时25V O 为正极B.放电时2+Zn 由负极向正极迁移C .充电总反应:252x 252xZn+V O +nH O=Zn V O nH O⋅D.充电阳极反应:-2+x 252252Zn V O nH O-2xe =xZn +V O +nH O ⋅5.根据实验操作及现象,下列结论中正确的是选项实验操作及现象结论A常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象稀硝酸的氧化性比浓硝酸强B取一定量23Na SO 样品,溶解后加入2BaCl 溶液,产生白色沉淀。
加入浓3HNO ,仍有沉淀此样品中含有2-4SO C将银和3AgNO 溶液与铜和24Na SO 溶液组成原电池。
安徽化学高考试题及答案

安徽化学高考试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于混合物的是()。
A. 氧气B. 蒸馏水C. 空气D. 纯碱答案:C2. 根据质量守恒定律,化学反应前后不变的量是()。
A. 元素种类B. 原子数目C. 质量总和D. 物质种类答案:C3. 以下化合物中,属于共价化合物的是()。
A. NaClB. NaOHC. HClD. CaO答案:C4. 金属钠在空气中燃烧,产物是()。
A. Na2OB. Na2O2C. NaOHD. NaCl答案:B5. 实验室中,用于鉴别NaOH和NaCl溶液的试剂是()。
A. 酚酞试液B. 石蕊试液C. 硝酸银溶液D. 稀硫酸答案:C6. 根据酸碱中和反应的实质,下列说法不正确的是()。
A. 酸中的氢离子与碱中的氢氧根离子结合B. 酸中的氢离子与碱中的氢离子结合C. 酸中的氢离子与碱中的氢氧根离子结合成水D. 酸中的氢离子与碱中的氢氧根离子结合成盐答案:B7. 下列金属中,活动性最强的是()。
A. 钾B. 钠C. 铁D. 铜答案:A8. 实验室中,用浓硫酸配制稀硫酸时,正确的操作是()。
A. 将浓硫酸倒入水中B. 将水倒入浓硫酸中C. 将浓硫酸与水同时倒入烧杯中D. 将浓硫酸与水同时倒入试管中答案:A9. 根据元素周期表,下列元素中,属于非金属元素的是()。
A. 钠B. 氧C. 铁D. 钙答案:B10. 下列化学反应中,属于氧化还原反应的是()。
A. CO2 + H2O → H2CO3B. 2H2 + O2 → 2H2OC. Na2CO3 + 2HCl → 2NaCl + H2O + CO2D. NaOH + HCl → NaCl + H2O答案:B二、填空题(每空2分,共20分)1. 根据元素周期表,元素的原子序数为11的元素是______。
答案:钠2. 化学反应方程式2H2 + O2 → 2H2O中,反应物的总质量等于生成物的总质量,这是因为______。
安徽高考化学试题及答案

安徽高考化学试题及答案安徽省2024年高考化学试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于混合物的是A. 氧气B. 碳酸钠C. 矿泉水D. 氯化钠答案:C2. 化学反应中,下列哪种物质是催化剂A. 反应物B. 生成物C. 反应条件D. 改变反应速率的物质答案:D3. 根据化学方程式2H2 + O2 → 2H2O,下列说法正确的是A. 氢气和氧气反应生成水B. 2个氢气分子和1个氧气分子反应生成2个水分子C. 氢气和氧气的摩尔比为2:1D. 以上说法都正确答案:D4. 下列哪种物质不属于碱A. NaOHB. KOHC. HClD. Ba(OH)2答案:C5. 根据质量守恒定律,下列说法错误的是A. 化学反应前后物质的总质量不变B. 化学反应前后元素的种类不变C. 化学反应前后原子的种类和数量不变D. 化学反应前后原子的质量不变答案:D6. 下列哪种元素的原子结构中,最外层电子数为4A. 碳B. 硅C. 氧D. 硫答案:B7. 下列哪种物质属于非电解质A. NaClB. HClC. H2OD. SO2答案:D8. 根据pH值判断,下列哪种溶液呈碱性A. pH=3B. pH=7C. pH=10D. pH=14答案:C9. 下列哪种物质属于氧化物A. CO2B. H2OC. NaClD. CH4答案:A10. 下列哪种物质不属于有机化合物A. CH4B. C2H6C. CO2D. C6H12O6答案:C二、填空题(每空2分,共20分)11. 写出下列物质的化学式:- 水:H2O- 二氧化碳:CO2- 硝酸:HNO3- 硫酸:H2SO412. 写出下列化学反应的离子方程式:- 碳酸钙与盐酸反应:CaCO3 + 2H+ → Ca2+ + CO2↑ + H2O - 氢氧化钠与硫酸反应:OH- + H+ → H2O13. 写出下列物质的电子式:- 氢气:H:H- 氯气:Cl:Cl- 钠离子:Na+[Ne]- 氯离子:Cl-[Ne]三、计算题(每题10分,共20分)14. 计算100g 10%的NaOH溶液中,NaOH的质量是多少?解:100g × 10% = 10g15. 计算在标准状况下,22.4L氧气的质量是多少?解:22.4L ÷ 22.4L/mol × 32g/mol = 32g四、实验题(每题15分,共30分)16. 实验目的:验证质量守恒定律实验步骤:- 步骤一:准确称量反应前各物质的质量- 步骤二:进行化学反应- 步骤三:准确称量反应后各物质的质量- 步骤四:比较反应前后物质的总质量,验证质量守恒定律17. 实验目的:探究温度对化学反应速率的影响实验步骤:- 步骤一:准备两组相同浓度的过氧化氢溶液- 步骤二:将一组溶液置于室温下,另一组置于热水中- 步骤三:同时向两组溶液中加入等量的催化剂- 步骤四:观察并记录两组溶液中气泡产生的速度,分析温度对反应速率的影响以上为安徽省2024年高考化学试题及答案,供参考。
2023年安徽省高考化学试卷(1)
2023年安徽省高考化学试卷一、选择题(本卷共20个小题,每小题6分,共120分)1.(6分)CO2地资源化利用是解决温室效应地重要途径,如图是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸地反应:下列有关三聚氰酸地说法正确地是( )A.分子式为C3H6N303B.分子中既含极性键,又含非极性键C.属于共价化合物D.生成该物质地上述反应为中和反应2.(6分)下列有关Fe2(SO4)3溶液地叙述正确地是( )A.该溶液中,K+、Fe2+、C6H5OH、Br﹣可以大量共存B.和KI溶液反应地离子方程式:Fe3++2I﹣═Fe2++I2C.和Ba(OH)2溶液反应地离子方程式:Fe3++SO42﹣+Ba2++3OH﹣═Fe(OH)3↓+BaSO4↓D.1L O.1mol•L﹣1该溶液和足量地Zn充分反应,生成11.2g Fe3.(6分)为实现下列实验目地,根据下列提供地主要仪器,所用试剂合理地是( )选项实验目地主要仪器试剂A分离Br2和CCl4混合物分液漏斗、烧杯Br2和CCl4混合物、蒸馏水B鉴别葡萄糖和蔗糖试管、烧杯、酒精灯葡萄糖溶液、蔗糖溶液、银氨溶液C实验室制取H2试管、带导管地橡皮塞锌粒、稀HNO3D测定NaOH溶液滴定管、锥形瓶、烧NaOH溶液、0.1000mol•L﹣1盐酸浓度杯A .AB .BC .CD .D 4.(6分)臭氧是理想地烟气脱硝试剂,其脱硝反应为:2NO 2(g )+O 3(g )⇌N 2O 5(g )+O 2(g ),若反应在恒容密闭容器中进行,下列由该反应相关图象作出地判断正确地是( )A B C Dt 1时仅加入催化剂,平衡向正方向移动达平衡时,仅改变x,则x 为c (O 2)从反应开始达平衡气体浓度变化升高温度,平衡常数减小A .A B .B C .C D .D5.(6分)室温下,下列溶液中粒子浓度关系正确地是( )A .Na 2S 溶液:c (Na +)>c (HS ﹣)>c (OH ﹣)>c (H 2S )B .Na 2C 2O 4溶液:c (OH ﹣)=c (H +)+c (HC 2O 4﹣)+2c (H 2C 2O 4)C .Na 2CO 3溶液:c (Na +)+c (H +)=2c (CO 32﹣)+c (OH ﹣)D .CH 3COONa 和CaCl 2混合溶液:c (Na +)+c (Ca 2+)=c (CH 3COO ﹣)+c (CH 3COOH )+2c (Cl ﹣)6.(6分)中学化学中很多"规律"都有其适用范围,下列根据有关"规律"推出地结论正确地是( )选项规律结论A 较强酸可以制取较弱酸次氯酸溶液无法制取盐酸B 反应物浓度越大,反应速率越快常温下,相同地铝片中分别加入足量地浓、稀硝酸,浓硝酸中铝片先溶解完C 结构和组成相似地物质,沸点随NH 3沸点低于PH 3相对分子质量增大而升高D 溶解度小地沉淀易向溶解度更小地沉淀转化ZnS 沉淀中滴加CuSO 4溶液可以得到CuS 沉淀A .AB .BC .CD .D 7.(6分)室温下,在0.2mol•L ﹣1 Al 2(SO 4)3溶液中,逐滴加入1.0mol•L ﹣1 NaOH 溶液,实验测得溶液pH 随NaOH 溶液体积变化曲线如图,下列有关说法正确地是( )A .a 点时,溶液呈酸性地原因是Al 3+水解,离子方程式为:Al 3++3OH ﹣⇌Al (OH )3B .a ﹣b 段,溶液pH 增大,Al 3+浓度不变C .b ﹣c 段,加入地OH ﹣主要用于生成Al (OH )3沉淀D .d 点时,Al (OH )3沉淀开始溶解二、非选择题8.(14分)Na 、Cu 、O 、Si 、S 、Cl 是常见地六种元素.(1)Na 位于元素周期表第 周期第 族;S 地基态原子核外有 个未成对电子;Si 地基态原子核外电子排布式为 .(2)用">"或"<"填空:第一电离能离子半径熔点酸性Si S O 2﹣ Na +NaCl Si H 2SO 4 HClO 4(3)CuCl (s )与O 2反应生成CuCl 2(s )和一种黑色固体.在25℃、101kPa 下,已知该反应每消耗1mol CuCl (s ),放热44.4kJ,该反应地热化学方程式是 .(4)ClO 2常用水地净化,工业上可用Cl 2氧化NaClO 2溶液制取ClO 2.写出该反应地离子方程式,并标出电子转移地方向和数目 .9.(16分)Hagemann 酶(H)是一种合成多环化合物地中间体,可由下列路线合成(部分反映条件略去):(1)(A→B)为加成反应,则B地结构简式是 ;B→C地反应类型是 .(2)H中含有地官能团名称是 ,F地名称(系统命名)是 .(3)E→F地化学方程式是 .(4)TMOB是H地同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有一个吸收峰;②存在甲氧基(CH3O﹣).TMOB地结构简式是 .(5)下列说法正确地是 .a.A能和HCl反应得到聚氯乙烯地单体b.D和F中均含有2个π健c.1mol G完全燃烧生成7mol H2O d.H能发生加成,取代反应.10.(14分)LiPF6是锂离子电池中广泛应用地电解质,某工厂用LiF、PCl3为原料、低温反应制备LiPF6,其流程如下:已知:HCl地沸点是﹣85.0℃,HF地沸点是19.5℃。
高考安徽化学试题及答案
高考安徽化学试题及答案一、选择题(本题共10小题,每小题3分,共30分)1. 下列物质中,属于混合物的是:A. 纯碱B. 食盐C. 蒸馏水D. 空气答案:D2. 化学反应速率与反应物浓度的关系是:A. 无关B. 成正比C. 成反比D. 先快后慢答案:B3. 下列物质中,属于强电解质的是:A. 醋酸B. 酒精C. 蔗糖D. 硫酸答案:D4. 根据质量守恒定律,下列说法正确的是:A. 反应前后原子的种类不变B. 反应前后原子的数目不变C. 反应前后原子的质量不变D. 所有选项都正确答案:D5. 下列化合物中,属于共价化合物的是:A. NaClB. NaOHC. HClD. MgO答案:C6. 根据元素周期表,下列元素中,最外层电子数最多的是:A. 氧B. 硫C. 氯D. 钾答案:B7. 根据酸碱中和反应的实质,下列说法正确的是:A. H+ + OH- → H2OB. H+ + CO32- → HCO3-C. H+ + SO42- → H2SO4D. H+ + Cl- → HCl答案:A8. 下列物质中,属于非金属单质的是:A. 铁B. 硫磺C. 铜D. 氢气答案:B9. 根据氧化还原反应的定义,下列说法正确的是:A. 氧化剂被还原B. 还原剂被氧化C. 氧化剂得电子D. 还原剂失电子答案:C10. 下列物质中,属于弱电解质的是:A. 硫酸B. 醋酸C. 氯化钠D. 碳酸氢钠答案:B二、填空题(本题共5小题,每小题4分,共20分)1. 写出下列物质的化学式:- 水:H2O- 二氧化碳:CO2- 硫酸:H2SO42. 根据元素周期表,第ⅢA族元素的最外层电子数为__3__。
3. 写出下列化学反应方程式:- 铁与稀盐酸反应:Fe + 2HCl → FeCl2 + H2↑- 碳酸钙与盐酸反应:CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O4. 写出下列物质的名称:- Na2CO3:碳酸钠- CuSO4:硫酸铜5. 根据氧化还原反应的定义,下列反应中,氧化剂是__氯气__。
安徽化学高考试题及答案
安徽化学高考试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于混合物的是:A. 纯水B. 氧气C. 空气D. 氯化钠答案:C2. 根据化学方程式计算,若生成物中有4g水,则反应物中氢气的质量为:A. 1gB. 2gC. 4gD. 8g答案:B3. 以下哪种物质在常温下为液态?A. 氧气B. 氮气C. 铁D. 汞答案:D4. 以下哪种元素的原子序数大于20?A. 钾B. 钙C. 铝D. 钠答案:B5. 以下哪种化合物属于共价化合物?A. NaClB. CaOC. HClD. Fe答案:C6. 以下哪种物质的化学式书写正确?A. 氧化铁:FeOB. 碳酸钠:Na2CO3C. 硫酸铜:CuSO4D. 氢氧化钠:NaOH答案:B7. 在标准状况下,1摩尔气体的体积是:A. 22.4 LB. 22.4 mLC. 22.4 cm³D. 22.4 mm³答案:A8. 以下哪种物质属于碱?A. HClB. NaOHC. H2SO4D. NH4Cl答案:B9. 以下哪种物质属于酸?A. NaOHB. HClC. NaClD. Ca(OH)2答案:B10. 以下哪种物质属于氧化物?A. CO2B. NaClC. H2OD. SO2答案:D二、填空题(每题5分,共20分)11. 写出下列物质的化学式:- 水:H2O- 二氧化碳:CO2- 氢氧化钠:NaOH- 硝酸银:AgNO312. 根据质量守恒定律,化学反应前后物质的总质量不变。
若反应物总质量为10g,生成物总质量为9g,则反应中消耗的氧气质量为1g。
13. 写出下列元素的符号:- 铁:Fe- 铜:Cu- 氧:O- 碳:C14. 根据题目所给的化学方程式,计算生成物的质量。
已知反应物A 的质量为5g,反应物B的质量为10g,生成物C的质量为15g。
根据化学方程式,生成物D的质量为5g。
三、计算题(每题10分,共20分)15. 已知某化学反应方程式为:2A + B → C + 2D,若反应中消耗了10g的A和5g的B,则生成的C的质量为多少?答案:生成的C的质量为10g。
安徽高考化学试题及答案
安徽高考化学试题及答案一、选择题(共40分,每题4分)1. 下列物质中,属于纯净物的是:A. 食盐水B. 蒸馏水C. 空气D. 矿泉水答案:B2. 根据题目所给的化学方程式,计算反应物的摩尔质量:A. 2H2 + O2 → 2H2OB. 2KMnO4 → K2MnO4 + MnO2 + O2C. 2Al + 6HCl → 2AlCl3 + 3H2D. 2HgO → 2Hg + O2答案:D3. 下列关于化学反应速率的描述,正确的是:A. 反应速率与反应物的浓度无关B. 反应速率与反应物的接触面积无关C. 反应速率与反应物的化学性质有关D. 反应速率与温度无关答案:C...(此处省略其他选择题,共10题)二、填空题(共20分,每空2分)1. 根据题目所给的化学方程式,写出下列反应的化学方程式:A. 铁与稀硫酸反应生成硫酸亚铁和氢气答案:Fe + H2SO4 → FeSO4 + H2↑2. 根据题目所给的原子结构示意图,写出元素的名称:A. 原子序数为11的元素答案:钠(Na)...(此处省略其他填空题,共10空)三、简答题(共20分,每题10分)1. 简述电解水实验的实验现象和结论。
答案:电解水实验中,水在通电的条件下分解成氢气和氧气。
实验现象为水逐渐减少,电极附近产生气泡,正极产生氧气,负极产生氢气。
结论是水是由氢元素和氧元素组成的。
2. 说明为什么硫酸铜溶液显蓝色,而硫酸铁溶液显黄色。
答案:硫酸铜溶液显蓝色是因为铜离子在水溶液中形成[Cu(H2O)6]2+络合物,这种络合物吸收可见光中的红光,反射蓝光,因此溶液显蓝色。
硫酸铁溶液显黄色是因为铁离子在水溶液中形成[Fe(H2O)6]3+络合物,这种络合物吸收可见光中的蓝光,反射黄光,因此溶液显黄色。
四、计算题(共20分)1. 根据题目所给的化学方程式和已知量,计算反应物或生成物的质量。
答案:(根据题目所给的具体数据和方程式进行计算)结束语:本套安徽高考化学试题涵盖了化学基础知识点,旨在考查学生对化学概念的理解、化学计算能力以及分析和解决问题的能力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2014年安徽高考理综化学试题解析第Ⅰ卷7.CO2的资源化利用是解决温室效应的重要途径,以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应:NH3+CO2 +H2O下列有关三聚氰酸的说法正确的是A.分子式为C3H6N3O3 B.分子中既含极性键,又含非极性键C.属于共价化合物D.生成该物质的上述反应为中和反应【答案】C【解析】三聚氰酸分子式为C3H3N3O3,分子中只含极性键(碳氮极性键、碳氧极性键和氧氢极性键)。
氰酸的结构为HO—C≡N,3个氰酸分子发生加成生成三聚氰酸。
本题是用NH3捕获CO2在一定条件下生成三聚氰酸,其过程是:NH3先与CO2发生加成反应生成中间产物氨基甲酸H2N—COOH,3个H2N—COOH失去3个水分子生成三聚氰酸。
8.下列有关Fe2(SO4)3溶液的叙述正确的是A.该溶液中,K+、Fe2+、C6H5OH、Br—可以大量共存B.和KI溶液反应的离子方程式:Fe3+ +2I—== Fe2+ +I2C.和Ba(OH)2溶液反应的离子方程式:Fe3+ +SO42—+Ba2+ +3OH—== Fe(OH)3↓+BaSO4↓D.1 L0.1 mol/L该溶液和足量的Zn充分反应,生成11.2 gFe【答案】D【解析】A选项:Fe3+与C6H5OH反应:Fe3++6C6H5OH==[Fe(OC6H5)6]3—+6H+B选项:正确的离子方程式为2Fe3+ +2I—== 2Fe2+ +I2C选项:正确的离子方程式为2Fe3+ +3SO42—+3Ba2+ +6OH—== 2Fe(OH)3↓+3BaSO4↓选项实验目的主要仪器试剂A 分离Br2和CCl4混合物分液漏斗、烧杯Br2和CCl4混合物、蒸馏水B 鉴别葡萄糖和蔗糖试管、烧杯、酒精灯葡萄糖溶液、蔗糖溶液、银氨溶液C 实验室制取H2试管、带导管的橡皮塞锌粒、稀HNO3D 测定NaOH溶液浓度滴定管、锥形瓶、烧杯NaOH溶液、0.1000 mol/L盐酸【解析】A选项:Br2和CCl4是两种互溶的液体,Br2和CCl4混合物是溶液,不能通过分液的方法分离。
B选项:葡萄糖是还原性糖(分子中含—CHO),蔗糖是非还原性糖(分子中不含—CHO)。
C选项:实验室制取H2的试剂通常是用锌粒和稀盐酸或稀硫酸,不是稀硝酸。
锌与稀硝酸反应反应通常不能得到H2,而是低价氮的化合物或氮单质。
D选项:缺少酸碱指示剂。
10.臭氧是理想的烟气脱硝试剂,其反应为:2NO2(g)+O3(g) N2O5 (g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断准确的是A B C D升高温度,平衡常数减小0~3s内,反应速率为:v(NO2)=0.2 mol/Lt1时仅加入催化剂,平衡正向移动达平衡时,仅改变x则x为c(O2)【解析】A选项:该反应是放热反应,温度升高,平衡逆向移动,平衡常数减小。
B选项:0~3s内,反应速率为:v(NO2)=0.2 mol/(L·s)C 选项:加入催化剂,反应速率同等程度加快,平衡不移动。
D选项:NO2转化率增大的措施(其它条件不变)有:增大c(O3)、加压(缩小容器容积)、降温、分离出O2或N2O5。
11.室温下,下列溶液中粒子浓度关系正确的是A.Na2S溶液:c(Na+)>c(HS—)>c(OH—)>c(H2S)B.Na2C2O4溶液:c(OH—) ==c(H+)+c(HC2O4—) + 2c(H2C2O4)C.Na2CO3溶液:c(Na+) +c(H+)==2c(CO32—)+c(OH—)D.CH3COONa和CaCl2混合溶液:c(Na+) +c(Ca2+)==c(CH3COO—)+c(CH3COOH)+2c(Cl—)【答案】B【解析】A选项:Na2S两级水解,则c(Na+)>c(OH—)>c(HS—)>c(H2S)。
B选项:c(OH—) ==c(H+)+c(HC2O4—) + 2c(H2C2O4)是Na2C2O4溶液的质子守恒式。
C选项:Na2CO3溶液的电荷守恒式为c(Na+) +c(H+)==2c(CO32—)+c(OH—)+c(HCO3—)D选项:CH3COONa和CaCl2混合溶液电荷守恒式为c(Na+) +2c(Ca2+)+ c(H+)==c(CH3COO—)+c(OH—)+c(Cl—);CH3COONa和CaCl2混合溶液中有c(Na+) ==c(CH3COO—)+c(CH3COOH)和2c(Ca2+)==c(Cl—),两式相加得:c(Na+) +2c(Ca2+)==c(CH3COO—)+c(CH3COOH)+ c(Cl—)。
选项规律结论A 较强酸制取较弱酸次氯酸溶液无法制取盐酸B 反应物浓度越大,反应速率越快常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完C 结构和组成相似的物质,沸点随相对分子质量增大而升高NH3沸点低于PH3D 溶解度小的沉淀易向溶解度更小的沉淀转化ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀【解析】A 选项:HClO见光分解生成盐酸或发生如下反应也生成盐酸:2HClO+HCHO=CO2↑+2H++2Cl—+H2OB选项:常温下,Al在浓硝酸中钝化。
C选项:NH3分子间存在氢键,分子间作用力较大,沸点比PH3高。
D选项:因为K sp(ZnS)>K sp(CuS),能发生如下反应:ZnS(s)+Cu2+(aq)== CuS(s)+ Zn2+(aq)。
13.室温下,在0.2 mol/LAl2(SO4)3溶液中,逐滴加入1.0 mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是A .a 点时,溶液呈酸性的原因是Al 3+水解,离子方程式为:Al 3+ +3OH —== Al(OH)3↓ B .a ~b 段,溶液pH 增大,Al 3+浓度不变C .b ~c 段,加入的OH —主要用于生成Al(OH)3沉淀 D .d 点时,Al(OH)3沉淀开始溶解 【答案】C【解析】A 选项:a 点时,溶液呈酸性的原因是Al 3+水解,其离子方程式为:Al 3+ +3H 2O Al(OH)3+3H +。
B 选项:溶液pH 增大,Al 3+浓度减小。
D 选项:d 点之前的“平缓线”的拐点处Al(OH)3就开始溶解了,d 点之后Al(OH)3基本溶解完,此后溶液pH 的增大是加入NaOH 溶液所引起的。
第Ⅱ卷25.(14分)Na 、Cu 、O 、Si 、S 、Cl 是常见的六种元素。
(1)Na 位于元素周期表第_____周期第_____族;S 的基态原子核外有____个未成对电子;Si 的基态原子核外电子排布式为____________________。
第一电离能 离子半径 熔点 酸性Si_______SO 2—_______Na +NaCl______SiH 2SO 4______HClO 422耗1 mol CuCl(s),放热44.4 kJ ,该反应的热化学方程式是___________________________。
(4)ClO 2常用于水的净化,工业上可用Cl 2氧化NaClO 2溶液制取ClO 2。
写出该反应的离子方程式,并标出电子转移的方向和数目____________________________________。
【答案】(1)三 IA 2 1s 22s 22p 63s 23p 2 (2)<><<(3)4CuCl(s)+O 2(g)==2CuCl 2(s)+2CuO(s) △H =—177.6 kJ/mol(4) 2e —2ClO — + Cl ==ClO 2+2Cl —26.(16分)Hagemann 酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):G OCH 3 CH 3COOCH 2CH 3 O CH 3 COOCH 2CH 3 2C H≡CH CH 3C ≡CH OCH 3 CH 2=CH —C=CH 2 CH 3C ≡C COOCH 2CH 3 催化剂 A B C D E CH 3OH 催化剂CO 2 一定条件 CH 3CH 2OH 浓H 2SO 4 F H(1)A → B 为加成反应,则B 的结构简式是______________;B C 的反应类型是_____。
(2)H 中含有的官能团名称是____________;F 的名称(系统命名)__________________。
(3)E → F 的化学方程式是__________________________________________________。
(4)TMOB 是H 的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;②存在甲氧基(CH 3O —)。
TMOB 的结构简式是____________________。
(5)下列说法正确的是________________。
a.A 能和HCl 反应得到聚氯乙烯的单体b.D 和F 中均含有2个π键c.1 mol G 完全燃烧生成7 molH 2Od.H 能发生加成、取代反应 【答案】(16分)(1)CH 2=CH —C≡CH 加成 (2)碳碳双键 羰基 酯基 2-丁炔酸乙酯 (3)CH 3C ≡CCOOH+CH 3CH 2OH CH 3C ≡CCOOCH 2CH 3+H 2O(4) OCH 3—C —OCH 3OCH 3 (5)ad【解析】合成路线中涉及了多个加成反应: A B :2C H≡CH CH 2=CH —C≡CHB C :CH 2=CH —C≡CH + CH 3OH D E :CH 3C ≡CH +O=C=O CH 3C ≡C —COOHE F 是酯化反应。
C 和F 生成 G 是烯炔加成成环(环加成):CH 3CH 2COO CH 2 C C —OCH 3 C CH CH 3 CH 2 G H 是在HI 作用下先生成烯醇,烯醇重排生成H :第(4)题H 分子中有10个碳原子3个氧原子不饱和度Ω=4,而TMOB 分子中含有苯环(Ω=4)且核磁共振氢谱只有1个吸收峰就是CH 3O —中氢的吸收峰,除去苯环的6个碳原子,还有4个碳原子和3个氧原子,所以HMOB 分子中还含有3个—OCH 3。
HMOB 的结构:OCH 3—C —OCH 3OCH 3第(5)题b 选项:F 分子中含1个—C ≡C —和1个酯基,分子中含3个π键。
OCH 3CH 3COOCH 2CH 3HI 无水乙醚OCH 3COOCH 2CH 3OHCH 3COOCH 2CH 3分子重排OCH 3CH 3 COOCH 2CH 3催化剂催化剂OCH 3CH 2=CH —C=CH 2一定条件浓H 2SO 4 △c 选项:G 的分子式为C 11H 16O 3即完全燃烧生成8 mol H 2O 。
