产品技术要求变更情况对比表
GB16806《消防联动控制系统》

目录第一章产品标准及市场准入制度 (3)国家认证认可监督管理委员会2007年第4号公告 (3)国家认证认可监督管理委员会2007年第9号公告 (3)公安部消防产品合格评定中心2007年第76文 (5)第二章消防联动控制系统概述 (7)第一节消防联动控制器 (7)一、分类 (7)二、功能和性能 (8)三、组成与工作原理 (9)四、工程应用 (10)第二节气体灭火控制器 (11)一、主要功能 (11)二、组成与工作原理 (12)第三节消防电气控制装置 (12)一、消防电气控制装置的分类 (12)二、消防电气控制装置的功能 (13)三、组成与工作原理 (13)第四节消防设备应急电源 (13)一、分类与型号编制 (14)二、功能要求 (14)三、组成与工作原理 (15)四、主要部件 (16)五、主要技术参数与特性及主要特点 (16)第五节消防应急广播设备 (17)一、功能 (17)二、组成与工作原理 (18)第六节消防电话 (18)一、功能 (18)二、组成与工作原理 (20)第七节传输设备 (20)第八节消防控制室图形显示装置 (21)一、消防控制室图形显示装置的功能 (21)二、组成与工作原理 (22)第九节消防联动模块 (23)一、中继模块 (23)二、输入模块 (23)三、输出模块 (23)四、输入/输出模块 (24)第十节消防电动装置 (24)一、基本功能 (24)二、组成与工作原理 (24)第十一节消火栓按钮 (24)一、功能与性能 (24)消火栓按钮具有以下主要功能与性能: (24)二、组成与工作原理 (24)第三章 GB16806-2006《消防联动控制系统》标准条文解释 (26)第一节一般要求 (26)第二节消防联动控制器 (30)第三节气体灭火控制器 (38)第四节消防电气控制装置 (42)第五节消防设备应急电源 (44)【条文说明】本条规定了直流输出消防设备应急电源的直流电压稳定度和负载稳定度。
变更前后对比表
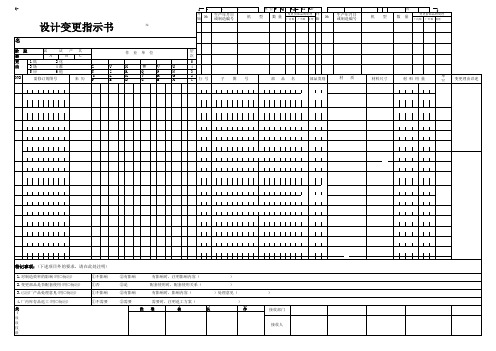
层 次
5 4 3 2 1
行 号
子
图
号
部
品
名
部品类别
材
质
材料尺寸
材 料 用 量
单 位
变更理由详述
特记事项:(下述项目外的要求,请在此处注明)
1.对制造效率的影响(用○标出) 2.变更部品是否配套使用(用○标出) 3.已出厂产品处理意见(用○标出) 4.厂内库存品返工(用○标出) 相关记录(必要时)
《设计变更点可靠性评价表》编号: 《设计变更点说明书》编号: 《设计变更提案书》/《制造变更点管理表》编号: 《技术公告》编号: 关联更改图纸明细
机 型
数 量
E:再加工后使用 变更前部品的处理
厂内数 厂外数 处理
设计变更指示书
品名、型号
阶 段 试作 量试 量产 其他 重要度等级 A B C 变更 1 降低成本 2 优化设计 理由 3 市场需要 4 标准变更 5 供应商需求 6 其他( ) NO 需修订的图号 来 历
作 业 单 位
Z T M F Y S L E X R K D W Q J C V P H B U N G A
HH/Q-Q20002/T2-E 青岛海信日立空调系统有限公司
a:马上 b:从…… c:用完在库
单 位 1:T 2:Kg
开 № 始
№
生产年月日 或制造编号
机 型
数 量
3:g 4:m 5:l 6:㎡ 变更前部品的处理
厂外数 处理
A:退货
B:待定
C:报废
D:用于其他机种
厂内数
开 始
№
生产年月日 或制造编号
①不影响 ①否 ①不影响 ①不需要
②有影响 ②是 ②有影响 ②需要
立卷审查标准介绍

•主要内容–立卷审查–立卷审查标准–申请表填写需要特别注意的事项•立卷审查–什么是立卷审查•立卷审查指按照立卷审查标准对申报资料进行审查,对申报资料进入技术审评环节的完整性、合规性、一致性进行判断的过程。
立卷审查不对产品的安全性、有效性评价的合理性、充分性进行分析,亦不对产品风险受益比进行判定。
•就是受理,对应法规中行政受理的环节。
依照《医疗器械注册管理办法(国家食品药品监督管理总局令第4号)》(以下简称《办法》)中行政受理的相关要求开展,时限为5个工作日。
–与技术审评的关系•立卷主要解决:适用的交没交,资料是不是合规,交的资料和申请的事项是不是一致•审评解决:交的资料能不能证明安全有效/受益大于风险•各立卷审查问题通过规范描述、增加备注等方式明确了尺度,与技术审评要求进行了区分。
•立卷审查–审查人员:•审评部、临床与生物统计部–立卷审查基本定位•服务–审评一次发补,不合格退审–背着抱着一样沉–建议自查•对于立卷审查标准中的问题,若在立卷审查环节未能做出充分判断,导致不应通过立卷审查环节的申报资料通过了立卷审查,在技术审评环节,仍可对立卷审查标准中的问题提出补正意见。
•立卷审查–立卷审查的适用范围:•立卷审查适用于复杂注册申请事项,即产品注册申请和复杂许可事项变更申请。
•复杂许可事项变更的判定准则(注册申请表中包含)–复杂、简单划分主要为了配合中心机构和流程调整–为了方便判断,只将少量项目划分为简单变更•立卷审查标准–为什么要设定立卷审查标准•配合电子申报,调整并明确了受理标准–立卷审查标准设定依据•注册管理办法,说明书管理办法,43、44号等公告,GCP,通知,指导原则(临床评价、临床试验设计、认可境外临床数据、软件等)等等•参考电子申报格式•明确审评基本关注问题•立卷审查标准的明确,未提高任何法规、规定的要求,不提高任何技术审评的要求•立卷审查标准–立卷审查标准编写过程•7稿•中心内部征求意见、试填、公开征求意见•多次多部门范围内研讨•中心办公会定稿–主要内容•医疗器械、IVD•产品注册立卷审查标准、变更注册立卷审查标准、临床立卷审查用表•产品注册和变更注册立卷审查标准主要内容:–相关说明、使用说明、信息/结论、基本审查问题、总体审查问题、适用的注册审查指导原则和强制性标准识别、立卷审查问题•临床立卷审查用表:–免临床目录路径、同品种路径、临床试验路径•申请表填写需要特别注意的事项–分类编码–临床评价路径–变更情形–注册单元划分–联系人手机号(一定填写准确了,联系用,会发短信)–申请表附的word文件会用于出报告,有的信息会用于注册证及其附件,应与电子申报中PDF保持一致结尾页2附件11.为确保医疗器械产品注册项目立卷审查工作的规范开展,制定本审查标准。
GBT28004.1《纸尿裤第1部分∶婴儿纸尿裤》新旧标准比对解析

摘要:从范围、规范性引用文件、术语和定义、产品分类、技术要求和试验方法、原材料要求、检验规则、标志、包装、运输和贮存等方面介绍了G B/T 28004.1-2021《纸尿裤 第1部分:婴儿纸尿裤》的标准要求,并与老版标准G B/T 28004-2011《纸尿裤(片、垫)》进行了内容比较,对新标准中变更内容进行了着重解读,最后给出了4点新标准实施建议,以帮助相关企业及检测人员更准确、全面理解和应用新标准。
关键词:婴幼儿纸尿裤;质量;检测规则;标准;差异Abstract: The standard requirements of the new standard of GB/T 28004.1-2021 Disposable diapers—Part 1: Disposable diapers for baby were introduced, including the scope of application and normative reference file, terms and definitions, product classification, requirements and test methods, requirements of raw materials, judgement rules, mark, as well as packing, transportation and storage. Meanwhile, the main contents of the old standard of GB/T 28004.1-2011 Disposal diapers were compared. Besides, four suggestions were put forward for the implementation of the new standard, which helping the relative enterprise and testing companies to understand and apply the standard correctly.Key words: disposable diapers for baby; quality; detection rules; standards; differencesGB/T 28004.1《纸尿裤 第1部分:婴儿纸尿裤》新旧标准比对解析⊙ 常生1吴波伟2单学蕾1曾双穗3郭爱莲1(1.天纺标检测认证股份有限公司,天津 300308;2.广州检验检测认证集团有限公司,广州 511447;3.绍兴方圆检测科技有限公司,浙江绍兴 312000)Comparison and Analysis between New and Old Standards of GB/T 28004.1Disposable Diapers—Part 1: Disposable Diapers for Baby⊙ Chang Sheng 1, Wu Bowei 2, Shan Xuelei 1, Zeng Shuangsui 3, Guo Ailian 1(1.Tianfang Standard Testing & Certification Co., Ltd., Tianjin 300308, China; 2.Guangzhou Inspection Testing and Certification Group Co., Ltd., Guangzhou 511447, China; 3.Shaoxing Fangyuan Testing Technology Co., Ltd., Shaoxing 312000, Zhejiang, China)中图分类号:TS77; TS761.6文献标志码:B 文章编号:1007-9211(2022)10-0014-05常生 先生硕士,工程师;从事纸制品、纺织品、鞋类、皮革检测研究。
FZT 74001《纺织品 针织运动护具》新旧标准对比

24纺织报告| Textile Reports随着人们生活质量的提高,全民运动逐渐成为一种生活方式。
在参加各种各样的健身活动时,为了避免或减少运动过程中的意外伤害,越来越多的人开始佩戴合适的运动护具。
FZ/T 74001—2013《纺织品 针织运动护具》[1](以下简称“旧标准”),起初由中国纺织工业联合会提出,归口于全国体育用品标准化技术委员会运动服分技术委员会,于2014年3月1日开始实施。
由于近几年市场的快速发展,原版的不足之处逐渐显现。
为了更好地适应市场需求,FZ/T 74001—2020《纺织品 针织运动护具》[2](以下简称“新标准”)于2020年12月9日发布、2021年4月1日实施。
在新标准实施之前,有必要对新旧标准的异同进行全面的比较和分析,以便检测机构和生产企业更好地理解。
1 主要内容1.1 范围新旧标准适用范围的变化见表1。
由表1可知,新标准增加了“抽样规则”“产品使用说明”和“本标准不适用于年龄在36个月及以下的婴幼FZ/T 74001《纺织品 针织运动护具》新旧标准对比裴茹冰,常 过[阿迪达斯(体育)中国有限公司,江苏 苏州 215121]Comparison of old and new standards ofFZ/T 74001 “Textiles-Knitted Sports Protectors ”Pei Rubing, Chang Guo[Adidas (Sports)China Co. Ltd., Suzhou 215121, China]Abstract This paper compares the 2020 edition and 2013 edition of FZ/T 74001 “Textiles-Knitted Sports Protectors” fromthe aspects of scope of application, normative references, terms and definitions, internal quality and product instructions, so as to provide reference for relevant practitioners.Key words knitwear; sports protectors; standard摘 要 文章分别从适用范围、规范性引用文件、术语和定义、内在质量、产品使用说明等方面,对比FZ/T 74001《纺织品 针织运动护具》2020版与2013版,以供相关从业者参考。
关于我国化学药品技术指导原则体系有关问题的探讨_姜典卓

12
要 求 国 际 协 Quality( 质量可控)
46
调会)
Safety( 安全性)
17
INDs( 新药申请)
1
Industry Letters( 企业来信)
10
Labeling( 标签)
19
Modernization Act( 现代化法案)
18
OTC( 非处方药)
19
Pharmacology / Toxicology( 药理 / 毒理)
Chinese Journal of New Drugs 2016,25(13)
·新药申报与审评技术·
关于我国化学药品技术指导原则体系有关问题的探讨
姜典卓 ( 国家食品药品监督管理总局药品审评中心,北京 100038)
[摘要] 通过梳理目前国内外化学药品技术指导原则体系文件,分析了国内与欧美的差异和存在的问 题,并从新药申报及审评角度分析了种种差异带来的误解和疑惑,同时结合实际工作经验提出了关于我国药 品技术指导原则体系建设的思考和建议。
《药品注册管理办法》[1]第二十八条中规定: 药 物研究参照国家食品药品监督管理局发布的有关技 术指导原则进行,申请人采用其他评价方法和技术 的,应当提交证明其科学性的资料。中华人民共和 国药典 2015 年版四部[2]凡例中规定: 指导原则系为 执行药典、考察药品质量、起草与复核药品标准等所 制定的指导性规定。也就是说技术指导原则只是建 议性原则,若能提供其他科学性证明的其他方法和 技术,也可采用。但使用者应尽量采用法定技术指 导原则,以便与监管者统一思路和与其他使用者具
质量标准 对比与生物类似 血液制品 血液主控文件 疫苗 稳定性 制剂 药物研发 产品信息 外源性病毒安全评价 海绵状脑病毒控制 脊髓灰质炎 生物新药研发 基因重组 药理 药代 毒理 单剂量及多剂量给药 基因毒性 致癌性 生殖及发育毒性 局部刺激性 其他 一般准则 植物药
注册标准变更主要研究信息汇总模板
注册标准变更主要研究信息汇总模板一、品种概述1.1 同品种上市背景信息:包括品种国内外上市情况、国家标准和国内外药典收载情况。
1.2申报品种获准上市的信息:包括批准文号、批准时间、执行标准、有效期,以及最近一次再注册的情况等内容。
1.3简述变更事项:简述变更事项。
若非首次申报且未被批准,应简述未获批准的原因。
二、立题合理性根据同品种上市背景信息及本品种最新的研究进展,简述化合物、制剂及剂型的立题合理性。
三、变更内容及变更理由以文字或列表方式说明变更涉及项目、原标准内容、变更后内容、主要变化及原因。
项目原标准内容变更后内容主要变化及原因四、变更研究针对变更事项,提供相应的变更研究综述资料。
如果下述研究内容不适用于变更事项,可在相应的栏目下说明不适用。
4.1.变更风险分析根据《已上市化学药品变更研究的技术指导原则》,基于具体问题具体分析的原则对变更内容进行风险分析。
分析变更对药品质控水平的影响,确定变更的合理性和变更风险。
如变更可能影响药品的安全性、有效性和质量可控性,需结合药品生产过程控制、药品研发过程及药品性质等综合分析和证明标准中该项变更不会引起产品质量控制水平的降低,必要时需要有关安全性和/或有效性试验资料或文献资料的支持。
4.2质量标准对比说明该品种国内外药典收载情况,以文字或列表方式对原质量标准、修订后标准、现行版中国药典以及国外主流药典进行比较。
如重要质控项目的方法和限度存在差异时,提供详细的对比资料。
范例:溶出度及有关物质(HPLC-UV)对比如下:检查项目原质量标准修订后标准现版ChP 现版USP现版BP/EP现版JP溶出度溶出方法溶出介质溶出体积转速溶出时间检测方法供试品溶液处理方法限度有关物质色谱柱流动相检测波长系统适用性试验要求色谱图记录时间供试品溶液浓度已知杂质定位方法已知杂质校正因子杂质定量方法限度对修订后标准是否符合现行技术要求进行评价,如不符合现行要求应进行系统的方法学研究和修订。
《化妆品监督管理条例》新旧对照表
2020年6月29日,《化妆品监督管理条例》发布,自2021年1月1日起施行。
《化妆品监督管理条例》取代了原《化化妆品应当符合强制性国家标准。
鼓励企业制定严于强制性国家标准的企业标准。
第三章生产经营第二十六条从事化妆品生产活动,应当具备下列条件:(一)是依法设立的企业;(二)有与生产的化妆品相适应的生产场地、环境条件、生产设施设备;(三)有与生产的化妆品相适应的技术人员;(四)有能对生产的化妆品进行检验的检验人员和检验设备;(五)有保证化妆品质量安全的管理制度。
第六条化妆品生产企业必须符合下列卫生要求:(一)生产企业应当建在清洁区域内,与有毒、有害场所保持符合卫生要求的间距。
(二)生产企业厂房的建筑应当坚固、清洁。
车间内天花板、墙壁、地面应当采用光洁建筑材料,应当具有良好的采光(或照明),并应当具有防止和消除鼠害和其他有害昆虫及其孳生条件的设施和措施。
(三)生产企业应当设有与产品品种、数量相适应的化妆品原料、加工、包装、贮存等厂房或场所。
(四)生产车间应当有适合产品特点的相应的生产设施,工艺规程应当符合卫生要求。
(五)生产企业必须具有能对所生产的化妆品进行微生物检验的仪器设备和检验人员。
第二十七条从事化妆品生产活动,应当向所在地省、自治区、直辖市人民政府药品监督管理部门提出申请,提交其符合本条例第二十六条规定条件的证明资料,并对资料的真实性负责。
省、自治区、直辖市人民政府药品监督管理部门应当对申请资料进行审核,对申请人的生产场所进行现场核查,并自受理化妆品生产许可申请之日起30个工作日内作出决定。
对符合规定条件的,准予许可并发给化妆品生产第二章化妆品生产的卫生监督第五条对化妆品生产企业实行化妆品生产许可证制度。
化妆品生产许可证由省、自治区、直辖市化妆品监督管理部门批准并颁发。
化妆品生产许可证有效期五年。
未取得化妆品生产许可证的单位,不得从事化妆品生产。
进口化妆品可以直接使用中文标签,也可以加贴中文标签;加贴中文标签的,中文标签内容应当与原标签内容一致。
普源精电DG1022与鼎阳SDG1025技术参数对比表
项目 DG1022
DDS技术
带宽 输出通道 输出幅度范围
采用
20MHz 2 2mVPP ~ 10 VPP (50Ω ) 1μHz ~ 5MHz 通道1:4kpts 通道2:1kpts
任意波最大频率范围
任意波波形长度
输出波形种类
采样率 垂直分辨率 波形长度
AM、AM-DSB、FM、PM、FSK、ASK、PWM、扫频、Burst USB Host&Device标配,GSYWAVE,支持远程命令控制 48种 50Ω +高阻可调
内置频率计 突发 FSK调制波频率 点阵液晶屏显示 调制波形 标配接口
输出5种标准波形+48种任意波行
100MSa/s 通道1:14bit 通道2:10bit 通道1:4kpts 通道2:1kpts
100 mHz ~ 200 MHz(单通道)
计数,无限,门控
2mHz~50KHz 黑白液晶显示器 256水平 x 64垂直
AM、FM、PM、FSK、扫频、Burst
USB Host & Device 配置功能强大的任意波编辑软件UltraWave 48种 50Ω +高阻可调
标配的任意波编辑软件
内建常用任意波形 输出阻抗
鼎阳SDG1025技术参数对比表
SDG1025
采用
25MHz 2 2mVpp-10Vpp(50Ω )
1μ Hz ~ 5MHz
通道1:16kpts 通道2:16kpts,
五种标准波形+内置48种任意波形
125MSa/s 通道1:14bit 通道2:14bit 通道1:16kpts 通道2:16kpts,
2020版与2017版标准化对比机电专业变化情况
排水系统
第9条,增加有电动机及主 要轴承温度和振动监测
9、使用低耗、先进、可靠的电控装置;
第10条,增加“宜:
10、采用集中远程监控,实现无人值守
4、设有水位观测及高、低水位声光报警装置
9、使用低耗、先进、可靠的电控装置,有电动机 及主要轴承温度和振动监测;
10、宜采用集中远程监控,实现无人值守
井下供配电网络第4条 4、中央变电所安装有选择性接地保护装置
理(23分)
第3条。增加变电所有停送 电记录
有设备运转、检修、保护试验、干部上岗、交接班、事 故、外来人员、钢丝绳检查(或其他专项检查)等记录
有设备运转、检修、保护试验、干部上岗、交接班、事 故、外来人员、钢丝绳检查(或其他专项检查)等记 录,变电所有停送电记录
技术管理
第3条,主提升变为提升、 矿井主提升、排水、压风、供热、供水、通讯、井 矿井提升、排水、压风、供热、供水、通讯、井
4、井下变电所高压馈电线上安装有选择性接地保 护装置
第10条删除高压配电点 10、变电所及高压配电点设有与矿调度室直通电话 10、变电所设有与矿调度室直通电话
采掘工作面供电第3条
三、煤矿电 气(30分)
井下供电系统
高压供电装备评分方法有
变化
信号照明系统
1.组织保障
删除本项
(4)作业前进行安全确认
(3)规范作业,无三违行为,作业前进行岗位安 全风险辨识及安全确认
(1)使用被列入国家应予淘汰的煤矿机电设备和 工艺目录的产品或者工艺的;
(2)井下电气设备未取得煤矿矿用产品安全标 志,或者防爆等级与矿井瓦斯等级不符的;
(3)单回路供电的(对于边远地区煤矿另有规定 的除外);
原(13)采用集中远程监控,实现无人值守
