高考化学钠及其化合物综合练习题含答案
高三化学《钠及其化合物》测试卷附参考答案

高三化学《钠及其化合物》测试卷一、选择题1.钠与水反应时的现象与钠的下列性质无关的是()A.钠的熔点低B.钠的密度小C.钠的硬度小D.钠有强还原性2.观察是研究物质性质的一种基本方法。
一同学将一小块金属钠露置于空气中,观察到下列现象:银白色变灰暗变白色出现液滴白色固体,下列说法正确的是()A.①发生了氧化还原反应B.②变白色是因为生成了碳酸钠C.③是碳酸钠吸收空气中的水蒸气形成了溶液D.④只发生物理变化3.焰火“脚印”“笑脸”“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。
下列说法中正确的是()A.非金属单质燃烧时火焰均为无色B.所有金属及其化合物灼烧时火焰均有颜色C.焰色反应均应透过蓝色钴玻璃观察D.NaCl与Na2CO3灼烧时火焰颜色相同4.可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法是()A.加热时无气体放出B.滴加盐酸时有气泡放出C.溶于水后滴加稀BaCl2溶液有白色沉淀生成D.溶于水后滴加澄清石灰水有白色沉淀生成5.钡和钠相似,也能形成O的过氧化物,则下列叙述错误的是()A.过氧化钡的化学式是Ba2O2B.1mol过氧化钠或过氧化钡跟足量水反应都生成0.5mol氧气C.过氧化钡是离子化合物D.过氧化钠和过氧化钡都是强氧化剂6.16.8gNaHCO3和7.8gNa2O2在密闭容器中灼烧,充分反应后,将密闭容器保持温度为500℃。
最后容器内的物质是()A.Na2CO3、Na2O2和O2B.Na2CO3、O2和H2O(g)C.Na2CO3、CO2、O2和H2O(g)D.NaHCO3、Na2CO3和O27.200℃时,11.6g由CO2和H2O组成的混合气体与足量Na2O2充分反应后,固体质量增加3.6g,则原混合气体的平均摩尔质量为(g·mol-1)()A.5.8B.11.6C.23.2D.46.48.下列对Na2O2的叙述中,正确的是()A.Na2O2中氧元素化合价为-1B.Na2O2能与水反应,所以Na2O2可以作气体的干燥剂C.Na2O2与水反应时,Na2O2是氧化剂,水是还原剂D.Na2O2与二氧化碳反应时,Na2O2只作氧化剂9.下列各物质的学名是:Na2S2O3叫硫代硫酸钠;CaS x叫多硫化钙;Na2O2叫过氧化钠;KO2叫超氧化钾。
高考化学知识点复习《钠及其化合物》真题练习含答案

高考化学知识点复习《钠及其化合物》真题练习含答案一、单选题1.(2023年湖北省普通高中学业水平合格性考试)常温下,将一小块下列金属投入盛有水的烧杯中,有气体产生的是A .NaB .AlC .FeD .Cu 【答案】A【解析】Na 能与水反应生成氢氧化钠和氢气,有气体产生,故选A 。
2.(2023年云南普通高中学业水平考试)下列关于钠及其化合物的叙述错误的是A .钠很软,能用小刀切割B .Na 2O 2可作供氧剂C .Na 元素的焰色呈黄色D .钠着火时,可用水灭火 【答案】D【解析】A .钠很软,将钠分成若干小块时,可用小刀切割,A 正确;B .常温下,Na 2O 2能与CO 2、H 2O 反应生成O 2,所以可作供氧剂,B 正确;C .含Na 元素的物质燃烧时,会产生黄色火焰,所以钠元素的焰色呈黄色,C 正确;D .钠在常温下就能与水剧烈反应,所以钠着火时,不能用水灭火,D 错误;故选D 。
3.(2023年7月黑龙江省普通高中学业水平合格性考试)下列有关钠及其化合物的叙述错误..的是 A .碳酸钠是难溶于水的白色粉末B .碳酸氢钠不稳定,受热易分解C .钠着火时,需要用干燥的沙土灭火D .过氧化钠可在呼吸面具中作为氧气的来源 【答案】A【解析】A .碳酸钠在25℃时的溶解度为33g ,为可溶性白色粉末,A 错误;B .碳酸氢钠不稳定,高温下可以分解生成碳酸钠、二氧化碳和水,B 正确;C .钠的化学性质非常活泼,容易与水、二氧化碳发生反应,因此钠着火时需要用干燥的沙土灭火,C 正确;D .过氧化钠可以与二氧化碳反应放出氧气,可以用来做呼吸面具的供氧来源,D 正确;故答案选A 。
4.(2023年湖南省普通高中学业水平考试)下列钠的化合物中,可在呼吸面具中作为氧气来源的是 A .22Na O B .NaCl C .NaOH D .24Na SO【答案】A【解析】过氧化钠能与人体呼出的二氧化碳和水蒸气反应生成氧气,常在呼吸面具中作为氧气来源,故选A。
高考化学钠及其化合物综合练习题含答案

高考化学钠及其化合物综合练习题含答案一、高中化学钠及其化合物1.现有下列物质:①KCl ②CH4③NH4NO3④I2⑤Na2O2⑥HClO4⑦N2⑧CO ⑨SO2⑩金刚石⑪CH3CH2OH ⑫MgO ⑬MgCl2⑭KOH ⑮HCl ⑯Al2O3请回答下列问题。
(1)两性氧化物是___(填序号),其电子式为___。
(2)最简单的有机化合物是___(填序号),用电子式表示其形成过程:___。
(3)属于共价化合物的是___(填序号),含有共价键的离子化合物是___(填序号)。
(4)由两种元素组成,且含有离子键和共价键的化合物为___(填序号),这两种元素的单质反应生成该化合物的化学方程式为___。
【答案】⑯②②⑥⑧⑨⑪⑮③⑤⑭⑤ 2Na+O2点燃Na2O2【解析】【分析】(1)两性氧化物指的是能与碱和酸反应生成盐和水的氧化物;(2)最简单的有机化合物是CH4,甲烷为共价化合物;(3) 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价化合物;(4)由两种元素组成,且离子键、共价键都含有的是Na2O2。
【详解】(1)两性氧化物指的是能与碱和酸反应生成盐和水的氧化物,这里只有Al2O3,Al2O3是离子化合物,其电子式为:,故答案为:⑯;;(2)最简单的有机化合物是CH4,甲烷为共价化合物,用电子式表示其形成过程为:,故答案为:②;;(3)只含共价键的化合物为共价化合物,CH4、HClO4、CO、SO2、CH3CH2OH、HCl中只含共价键,属于共价化合物;含有共价键的离子化合物有:NH4NO3、Na2O2、KOH,故答案为:②⑥⑧⑨⑪⑮;③⑤⑭;(4)由两种元素组成,且离子键、共价键都含有的是Na2O2,钠和氧气反应生成过氧化钠的化学方程式:2Na+O2点燃Na2O2,故答案为:⑤;2Na+O2点燃Na2O2。
全国各地高考化学分类:钠及其化合物综合题汇编含答案解析
全国各地高考化学分类:钠及其化合物综合题汇编含答案解析一、高中化学钠及其化合物1.化学兴趣小组制取Na2O2,并测定制得的Na2O2样品的纯度。
I.制取Na2O2。
查阅资料:①钠与空气在453~473K之间可生成Na2O,迅速提高温度到573~673K之间可生成Na2O2。
②4Na+3CO 22Na2CO3+C。
③加热后,Na不与N2反应。
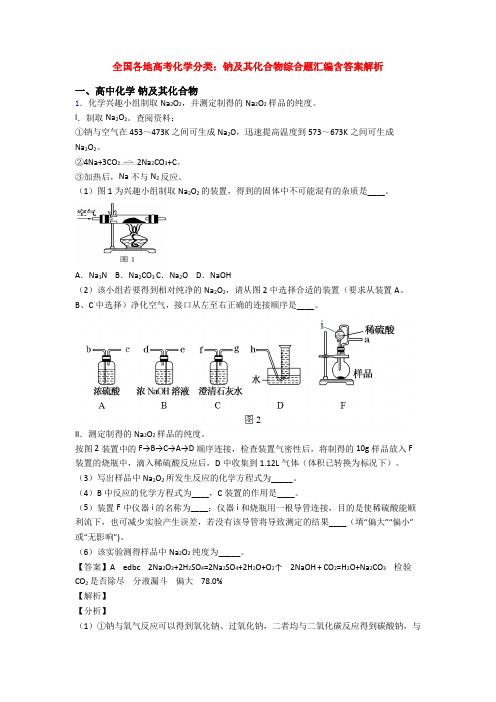
(1)图1为兴趣小组制取Na2O2的装置,得到的固体中不可能混有的杂质是____。
A.Na3N B.Na2CO3 C.Na2O D.NaOH(2)该小组若要得到相对纯净的Na2O2,请从图2中选择合适的装置(要求从装置A、B、C中选择)净化空气,接口从左至右正确的连接顺序是____。
II.测定制得的Na2O2样品的纯度。
按图2装置中的F→B→C→A→D顺序连接,检查装置气密性后,将制得的10g样品放入 F 装置的烧瓶中,滴入稀硫酸反应后,D中收集到1.12L气体(体积已转换为标况下)。
(3)写出样品中Na2O2所发生反应的化学方程式为_____。
(4)B中反应的化学方程式为____,C装置的作用是____。
(5)装置F中仪器i的名称为____;仪器i和烧瓶用一根导管连接,目的是使稀硫酸能顺利流下,也可减少实验产生误差,若没有该导管将导致测定的结果____(填“偏大”“偏小”或“无影响”)。
(6)该实验测得样品中Na2O2纯度为_____。
【答案】A edbc 2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑ 2NaOH+ CO2=H2O+Na2CO3检验CO2是否除尽分液漏斗偏大 78.0%【解析】【分析】(1)①钠与氧气反应可以得到氧化钠、过氧化钠,二者均与二氧化碳反应得到碳酸钠,与水反应会得到氢氧化钠,由信息可知钠与氮气不反应;(2)若要得到相对纯净的过氧化钠,应将空气通过盛有浓氢氧化钠溶液的洗气瓶除去二氧化碳,再通过盛有浓硫酸的洗气瓶除去水蒸气;(3)过氧化钠与稀硫酸反应生成硫酸钠、氧气和水;(4)该实验设计的原理是烧瓶中过氧化钠与硫酸反应生成硫酸钠、氧气与水,用浓氢氧化钠溶液吸收氧气中可能混有二氧化碳,用澄清石灰水检验二氧化碳是否除尽,用排水法收集氧气,根据氧气体积可以计算过氧化钠的质量,进而计算样品中过氧化钠的质量分数; (5)分液漏斗和烧瓶用导管连接可以平衡气压,使稀硫酸顺利流下,还可以抵消滴加硫酸排出空气的体积,若没有该导管,排出的空气按生成氧气的体积计算;(6)依据标况下氧气的体积和反应方程式计算过氧化钠的质量,由题给数据计算过氧化钠的纯度。
高考化学钠及其化合物综合题汇编含详细答案
高考化学钠及其化合物综合题汇编含详细答案一、高中化学钠及其化合物1.化学兴趣小组制取Na2O2,并测定制得的Na2O2样品的纯度。
I.制取Na2O2。
查阅资料:①钠与空气在453~473K之间可生成Na2O,迅速提高温度到573~673K之间可生成Na2O2。
②4Na+3CO 22Na2CO3+C。
③加热后,Na不与N2反应。
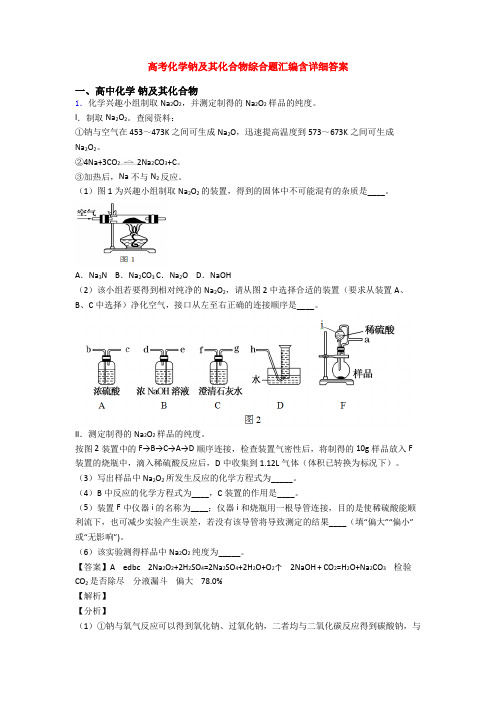
(1)图1为兴趣小组制取Na2O2的装置,得到的固体中不可能混有的杂质是____。
A.Na3N B.Na2CO3 C.Na2O D.NaOH(2)该小组若要得到相对纯净的Na2O2,请从图2中选择合适的装置(要求从装置A、B、C中选择)净化空气,接口从左至右正确的连接顺序是____。
II.测定制得的Na2O2样品的纯度。
按图2装置中的F→B→C→A→D顺序连接,检查装置气密性后,将制得的10g样品放入 F 装置的烧瓶中,滴入稀硫酸反应后,D中收集到1.12L气体(体积已转换为标况下)。
(3)写出样品中Na2O2所发生反应的化学方程式为_____。
(4)B中反应的化学方程式为____,C装置的作用是____。
(5)装置F中仪器i的名称为____;仪器i和烧瓶用一根导管连接,目的是使稀硫酸能顺利流下,也可减少实验产生误差,若没有该导管将导致测定的结果____(填“偏大”“偏小”或“无影响”)。
(6)该实验测得样品中Na2O2纯度为_____。
【答案】A edbc 2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑ 2NaOH+ CO2=H2O+Na2CO3检验CO2是否除尽分液漏斗偏大 78.0%【解析】【分析】(1)①钠与氧气反应可以得到氧化钠、过氧化钠,二者均与二氧化碳反应得到碳酸钠,与水反应会得到氢氧化钠,由信息可知钠与氮气不反应;(2)若要得到相对纯净的过氧化钠,应将空气通过盛有浓氢氧化钠溶液的洗气瓶除去二氧化碳,再通过盛有浓硫酸的洗气瓶除去水蒸气;(3)过氧化钠与稀硫酸反应生成硫酸钠、氧气和水;(4)该实验设计的原理是烧瓶中过氧化钠与硫酸反应生成硫酸钠、氧气与水,用浓氢氧化钠溶液吸收氧气中可能混有二氧化碳,用澄清石灰水检验二氧化碳是否除尽,用排水法收集氧气,根据氧气体积可以计算过氧化钠的质量,进而计算样品中过氧化钠的质量分数; (5)分液漏斗和烧瓶用导管连接可以平衡气压,使稀硫酸顺利流下,还可以抵消滴加硫酸排出空气的体积,若没有该导管,排出的空气按生成氧气的体积计算;(6)依据标况下氧气的体积和反应方程式计算过氧化钠的质量,由题给数据计算过氧化钠的纯度。
全国高考化学钠及其化合物的综合高考真题汇总附答案

全国高考化学钠及其化合物的综合高考真题汇总附答案一、高中化学钠及其化合物1.某兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行试验论证,某同学设计了下列装置进行试验(已知PdCl2能被CO还原为Pd),请回答下列问题:(1)上图装置2中应盛放__________溶液.(2)为了使反应随开随用,随关随停,上图方框内应选用_____装置(填上图字母代号).(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置______(填数字编号)中出现_______________现象时,再点燃酒精灯.(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_________.②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_____________.【答案】饱和碳酸氢钠 C 5 澄清石灰水变浑浊的 2Na+2CO2Na2CO3+CO4Na+3CO22Na2CO3+C【解析】【分析】【详解】(1)根据二氧化碳的实验室制法可知二氧化碳中可能含有HCl气体,所以应除去HCl,则装置B中盛放的溶液是饱和碳酸氢钠溶液;答案为:饱和碳酸氢钠;(2)为了使反应随开随用,随关随停,上图方框内应选用C装置,因为C装置可以达到固液分离的目的,起到随开随用,随关随停的作用;答案为:C;(3)因为该实验是验证二氧化碳与Na的反应,所以应排除空气中的氧气,所以先通入二氧化碳使5中澄清石灰水变浑浊后,再点燃酒精灯;答案为:澄清石灰水变浑浊的;5;(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,说明该固体是碳酸钠,则Na与二氧化碳反应生成CO和碳酸钠,化学方程式是2Na+2CO2Na2CO3+CO;答案为: 2Na+2CO2Na2CO3+CO;②若装置6中溶液无明显现象,说明无CO生成,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则一种固体为碳酸钠,另一种是C单质,化学方程式是4Na+3CO22Na2CO3+C。
高考化学钠及其化合物推断题综合题及答案.docx

高考化学钠及其化合物推断题综合题及答案一、钠及其化合物1.A 为日常生活中常见的化合物, B 为淡黄色固体,C、 G、 H 均为气体,其中C、 H 为单质, G 能使红色石蕊试剂变蓝, E 是一种由两种元素组成的具有耐高温、硬度大的耐热冲击材料,其摩尔质量为 41 g/moL 。
⑴B 的电子式为 _____。
⑵E 的化学式为 _____。
⑶写出反应②的离子方程式(D 足量 ):_____。
⑷写出反应③的化学方程式:_____。
【答案】-22-3322AlN AlN+OH+H O=AlO +NH ↑4NH +3O2N ↑+6H2O【解析】【分析】B 是淡黄色固体, B 与化合物 A 反应产生单质气体C 和化合物 D,则 B 是 Na2O2, C 是 O2,G 能使红色石蕊试剂变蓝,则G 是 NH3,NH3与 O2在高温下发生反应:4NH3+3O22N2↑ +6H2O,可知 A 是 H2O, H 是 N2; D 是 NaOH; E 是一种由两种元素组成的具有耐高温、硬度大的耐热冲击材料,其摩尔质量为41 g/moL ,由于其中一种元素是N 元素, N 相对原子质量是 14,则另一种元素相对原子质量是42-14=27,则另外一种元素是 Al 元素, E 是 AlN, NaOH、 H2 O、 AlN 发生反应,产生NH3和 NaAlO2;则 F 是 NaAlO2,据此解答。
【详解】根据上述分析可知 A 是 H2O, B 是 Na2O2, C是 O2,D 是 NaOH, E是 AlN, F 是 NaAlO2。
(1)B 是 Na2 O2, B 的电子式为;(2)E 是氮化铝, E 的化学式为 AlN;(3)反应②是 NaOH、 AlN、H2O 反应的离子方程式为:AlN+OH- +H2O=AlO2-+NH3↑;(4)反应③是氨气被氧气氧化的反应,该反应的化学方程式是4NH3+3O22N2↑+6H2O。
【点睛】本题考查了物质的推断、物质的结构、离子方程式书写等知识。
高考化学钠及其化合物综合练习题附详细答案

高考化学钠及其化合物综合练习题附详细答案一、高中化学钠及其化合物1.纯碱、烧碱等是重要的化工原料。
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。
将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是______。
若其它操作不变,将A与C连接,可观察到的现象是_______。
(2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3 g白色固体,该白色固体的组成是_______(写化学式)。
设计实验确认该白色固体中存在的阴离子,试完成下列方案。
实验操作实验现象结论①取少量白色固体于试管中,加____________足量水溶解,再加足量BaCl2溶液②过滤,取2 mL滤液于试管____________中,滴加酚酞(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:已知NaHCO3在低温下溶解度较小。
反应I为:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl,处理母液的两种方法如下。
①向母液中加入石灰乳,可将其中_____循环利用,同时得到融雪剂_____。
②向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式:______________。
【答案】水沿导管由广口瓶进入烧瓶广口瓶中的长导管口有气泡产生 NaOH和Na2CO3产生白色沉淀原白色固体中有CO32-存在溶液变红溶液中含有氢氧化钠 NH3 CaCl2 HCO3—+NH3=NH4++H2O【解析】【分析】(1)CO2与NaOH反应生成Na2CO3,烧瓶内压强减小;(2)先根据钠原子守恒,通过极值法确定白色固体的组成;根据题中所给试剂,要首先利用中性溶液BaCl2检验出碳酸钠,并将碳酸根离子全部沉淀,再通过检验溶于的pH来确定是否含有NaOH;(3)①根据流程可知,母液中含有氯化铵,加入石灰乳后可以生成氨气;②碳酸氢钠溶于水,母液为碳酸氢钠饱和溶液,向母液中通入氨气,氨气与碳酸氢钠反应碳酸钠和碳酸铵。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学钠及其化合物综合练习题含答案一、高中化学钠及其化合物1.现有下列物质:①KCl ②CH4③NH4NO3④I2⑤Na2O2⑥HClO4⑦N2⑧CO ⑨SO2⑩金刚石⑪CH3CH2OH ⑫MgO ⑬MgCl2⑭KOH ⑮HCl ⑯Al2O3请回答下列问题。
(1)两性氧化物是___(填序号),其电子式为___。
(2)最简单的有机化合物是___(填序号),用电子式表示其形成过程:___。
(3)属于共价化合物的是___(填序号),含有共价键的离子化合物是___(填序号)。
(4)由两种元素组成,且含有离子键和共价键的化合物为___(填序号),这两种元素的单质反应生成该化合物的化学方程式为___。
【答案】⑯②②⑥⑧⑨⑪⑮③⑤⑭⑤ 2Na+O2点燃Na2O2【解析】【分析】(1)两性氧化物指的是能与碱和酸反应生成盐和水的氧化物;(2)最简单的有机化合物是CH4,甲烷为共价化合物;(3) 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价化合物;(4)由两种元素组成,且离子键、共价键都含有的是Na2O2。
【详解】(1)两性氧化物指的是能与碱和酸反应生成盐和水的氧化物,这里只有Al2O3,Al2O3是离子化合物,其电子式为:,故答案为:⑯;;(2)最简单的有机化合物是CH4,甲烷为共价化合物,用电子式表示其形成过程为:,故答案为:②;;(3)只含共价键的化合物为共价化合物,CH4、HClO4、CO、SO2、CH3CH2OH、HCl中只含共价键,属于共价化合物;含有共价键的离子化合物有:NH4NO3、Na2O2、KOH,故答案为:②⑥⑧⑨⑪⑮;③⑤⑭;(4)由两种元素组成,且离子键、共价键都含有的是Na2O2,钠和氧气反应生成过氧化钠的化学方程式:2Na+O2点燃Na2O2,故答案为:⑤;2Na+O2点燃Na2O2。
【点睛】一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价化合物。
2.现有下列几种物质:①盐酸;②Na2O;③Na2O2;④Al(OH)3;⑤Na2CO3;⑥H2O;⑦CO2;⑧乙醇;⑨Cu;⑩NaOH溶液。
(1)其中属于电解质的有___________(填写序号,下同),属于碱性氧化物的有_______。
(2)④与⑩反应的离子方程式为______________________________________。
(3)Na2O2因能发生下列反应被用作供氧剂:2Na2O2+2CO2=2Na2CO3+O2,该反应中,氧化剂与还原剂的物质的量之比为:______。
(4)如用超氧化钾(KO2)作供氧剂,写出它和CO2反应的化学方程式,并标出电子转移的方向和数目______________________________________________________。
【答案】②③④⑤⑥② Al(OH)3 + OH- = AlO2-+2H2O 1:1 或【解析】【分析】(1)①盐酸为混合物,不属于电解质;②Na2O为离子化合物,属于电解质、碱性氧化物;③Na2O2为离子化合物,属于电解质,过氧化物;④Al(OH)3为离子化合物,属于电解质;⑤Na2CO3为离子化合物,属于电解质;⑥H2O属于电解质、氧化物;⑦CO2不属于电解质,为氧化物;⑧乙醇属于非电解质;⑨Cu为单质,不属于电解质;⑩NaOH溶液为混合物,不属于电解质;(2)NaOH与氢氧化铝反应生成偏铝酸钠和水;(3)过氧化钠中部分氧原子化合价升高为0价,部分降低为-2价,则过氧化钠既是氧化剂,又是还原剂,且物质的量之比为1:1;(4)超氧化钾(KO2)中O2-平均价态为-0.5价,部分氧原子化合价升高为0价,部分降低为-2价,则升高的氧原子数目为降低氧原子数目的3倍。
【详解】(1)①盐酸为混合物,不属于电解质;②Na2O为离子化合物,属于电解质、碱性氧化物;③Na2O2为离子化合物,属于电解质,过氧化物;④Al(OH)3为离子化合物,属于电解质;⑤Na2CO3为离子化合物,属于电解质;⑥H2O属于电解质、氧化物;⑦CO2不属于电解质,为氧化物;⑧乙醇属于非电解质;⑨Cu为单质,不属于电解质;⑩NaOH溶液为混合物,不属于电解质;综上所述,属于电解质的为②③④⑤⑥;碱性氧化物的为②;(2)NaOH与氢氧化铝反应生成偏铝酸钠和水,离子方程式为Al(OH)3 + OH- = AlO2-+2H2O;(3)过氧化钠中部分氧原子化合价升高为0价,部分降低为-2价,则过氧化钠既是氧化剂,又是还原剂,且物质的量之比为1:1;(4)超氧化钾(KO2)中O2-平均价态为-0.5价,部分氧原子化合价升高为0价,部分降低为-2价,则升高的氧原子数目为降低氧原子数目的3倍,则单线桥法为或。
3.化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验。
请你参与并完成对有关问题的解答:(1)甲同学用如图所示装置测定CO2的质量。
实验时稀硫酸是与样品中的__________(填“Na2CO3”或“NaCl”)发生反应,仪器b的名称是______,洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是__________。
(2)乙同学用如图所示装置,取一定质量的样品(m g)和足量稀硫酸反应进行实验,完成样品中Na2CO3质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的______________________________,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的______(填“体积”或“质量”)。
(3)丙同学用下图所示方法和步骤进行实验:①操作Ⅰ涉及的实验名称有:__________、洗涤;操作Ⅱ涉及的实验名称有干燥、__________。
②丙同学测得样品中Na2CO3的质量分数为__________。
【答案】Na2CO3分液漏斗除去CO2中的水蒸气液面上升体积过滤称量106y/197x【解析】【详解】(1)依据装置和试剂分析,硫酸和样品中的碳酸钠反应,仪器b是加入液体的仪器可以控制加入的量,是分液漏斗;反应过程中含有水蒸气,可以利用浓硫酸干燥二氧化碳气体;(2)①使用注射器改变瓶内气体的多少而改变瓶内压强;当将针筒活塞向内推压时,瓶内气体被压缩,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好;②在实验完成时,反应后可以利用注射器读取生成气体的体积,能直接测得的数据是CO2的体积;(3)①流程分析可知,加入氢氧化钡溶液和碳酸钠反应生成碳酸钡沉淀,通过过滤得到沉淀,洗涤后称重得到沉淀碳酸钡质量;②由流程分析判断:碳酸钡沉淀质量为yg,根据原子守恒可知样品中Na2CO3质量为106197yg,因此样品中Na2CO3的质量分数为106197yx。
4.(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g)ΔFe3O4+4H2。
该反应中H2O作__________(填“氧化剂”或“还原剂”);(2)检验某溶液中是否含有SO42-,先加盐酸,再加______(填“BaCl2”或“NaCl;(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。
该沉淀剂是__________(填“生石灰”或“盐酸”)。
(4)过氧化钠可用于呼吸面具中作为氧气的来源。
完成下列化学方程式:2Na2O2 + 2______ = 2Na2 CO3 +O2 ↑;(5)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。
据此他判断汤汁中含有________(填“钠”或“钾”)元素;【答案】氧化剂 BaCl2生石灰 CO2钠【解析】【详解】(1)在3Fe+4H2O(g)ΔFe3O4+4H2中氢元素的化合价从+1价降为0价,则H2O作氧化剂;(2)检验某溶液中是否含有SO42-,先加稀盐酸,可以排除银离子与碳酸根离子等离子的干扰,再加入BaCl2溶液,产生的沉淀是硫酸钡;(3)海水中的Mg2+沉淀是生成Mg(OH)2,沉淀剂是利用生石灰与水反应生成氢氧化钙,从而将Mg2+沉淀;(4)过氧化钠可用于呼吸面具中作为氧气的来源,是利用Na2O2与CO2或水蒸气反应生成氧气,则2Na2O2 + 2CO2= 2Na2 CO3 +O2 ↑;(5)钠元素的焰色反应呈黄色,即可判断汤汁中含有钠元素。
5.在呼吸面具和潜水艇中可用Na2O2作为供氧剂:(1)实验室常用加热钠的方法制备Na2O2,Na2O2是_______色固体,实验室制备Na2O2的化学方程式_______,试写出Na2O2与CO2反应的化学方程式________。
(2)现有mg含有Na2O杂质的Na2O2试样。
(可供选用的反应物只有CaCO3固体,6mol•L﹣1盐酸和蒸馏水)请从如图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度。
请填写下列空白:①写出实验中Na2O2和Na2O分别发生反应的化学方程式__________、__________。
②应选用的装置的连接顺序应是___________。
③若开始时测得样品的质量为2.0g,反应结束后测得生成气体的体积为224mL(标准状况),计算出试样中Na2O2的纯度为:__________。
【答案】淡黄色 2Na+O2Na2O2 2Na2O2+2CO2=2Na2CO3+O22Na2O2+2H2O=4NaOH+O2↑ Na2O+H2O=2NaOH G→A→B→F 78%【解析】【分析】(1)Na与O2在加热条件下反应产生淡黄色的Na2O2,Na2O2能够与CO2反应产生碳酸钠和氧气;(2)根据Na2O与水反应但不产生O2,Na2O2与水反应有O2产生。
在装置⑤中用H2O与样品反应,产生的O2通过A进入到装置①中,通过排水方法收集O2,反应产生的O2的体积通过装置④的量筒读出结合试样质量和有关化学方程式,计算Na2O2的质量和含量。
【详解】(1)Na与O2在加热条件下反应产生Na2O2,Na2O2是淡黄色的固体,制备Na2O2的反应方程式为:2Na+O2Na2O2;Na2O2能够与CO2反应产生碳酸钠和氧气,反应方程式为:2Na2O2+2CO2=2Na2CO3+O2;(2)①在实验中Na2O2与H2O反应产生NaOH和O2,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O与H2O发生反应产生NaOH,反应的化学方程式为:Na2O+H2O=2NaOH;②使用装置⑤(试样与足量水反应的装置)、①和④(量度O2体积的装置)来测定试样中Na2O2的纯度。
