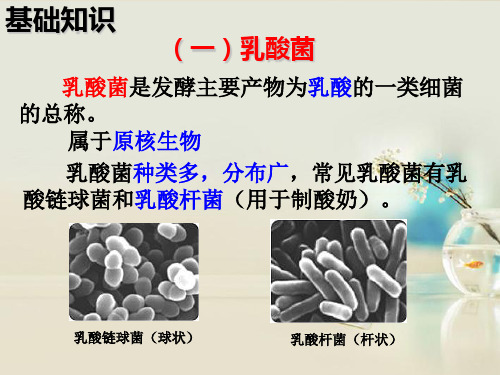
亚硝酸盐与对氨基苯磺酸发生重氮化反应,盐酸萘乙二胺反应方程式
肉制品中亚硝酸盐的测定

急性中毒原因多为: 急性中毒原因多为: 1.将亚硝酸盐误作食盐、面碱等使用和食用。2.投毒。 将亚硝酸盐误作食盐、 投毒。 将亚硝酸盐误作食盐 面碱等使用和食用。 投毒 3.食用了含有大量亚硝酸盐的蔬菜,尤其是不新鲜的 食用了含有大量亚硝酸盐的蔬菜, 食用了含有大量亚硝酸盐的蔬菜 绿叶蔬菜。刚腌不久的蔬菜(暴腌菜 暴腌菜)含有大量亚硝酸 绿叶蔬菜。刚腌不久的蔬菜 暴腌菜 含有大量亚硝酸 温度过高食盐用量不足10%,腌制时间短, %,腌制时间短 盐,温度过高食盐用量不足 %,腌制时间短,易造 成细菌大量繁殖,亚硝酸盐含量增加,一般腌制10天 成细菌大量繁殖,亚硝酸盐含量增加,一般腌制 天 后亚硝酸盐开始下降,腌后20天消失 天消失。 后亚硝酸盐开始下降,腌后 天消失。
5、0.2%盐酸萘乙二胺溶液:称取 克盐酸萘乙二 、 %盐酸萘乙二胺溶液:称取0.2克盐酸萘乙二 溶于100毫升水中,避光保存。 毫升水中, 胺,溶于 毫升水中 避光保存。 6、亚硝酸钠标准溶液:精密称取 、亚硝酸钠标准溶液:精密称取0.1000克于硅胶 克于硅胶 干燥器中干燥24小时的亚硝酸钠 加水溶解移入500 小时的亚硝酸钠, 干燥器中干燥 小时的亚硝酸钠,加水溶解移入 毫升容量瓶中,并稀释至刻度。 毫升容量瓶中,并稀释至刻度。此溶液每毫升相当于 200微克亚硝酸钠。 微克亚硝酸钠。 微克亚硝酸钠 7、亚硝酸钠标准使用液:临用前,吸取亚硝酸钠 、亚硝酸钠标准使用液:临用前, 标准溶液5.00毫升,置于 毫升, 毫升容量瓶中, 标准溶液 毫升 置于200毫升容量瓶中,加水稀 毫升容量瓶中 释至刻度,此溶液每毫升相当于5微克亚硝酸钠 微克亚硝酸钠。 释至刻度,此溶液每毫升相当于 微克亚硝酸钠。 8、分光光度计。 、分光光度计。
亚硝酸盐的测定

盐酸萘乙二胺法测定亚硝酸盐得含量1亚硝酸盐得测定(盐酸萘乙二胺法)1、1原理样品经沉淀蛋白质、除去脂肪后,在弱酸性条件下,亚硝酸盐与对氨基苯磺酸(H 2N —C 6H 4-SO 3H)重氮化,产生重氮盐,此重氮盐再与偶合试剂(盐酸萘乙二胺)偶合形成紫红色染料,其最大吸收波长为550nm,测定其吸光度后,可与标准比较定量。
2HCl+NaNO 2+H 23H 重氮化H 3SO-Cl ---+NaCl 2H +2O2HCl .H 2NH 2CH 2+--N -Cl3H 偶合CHN 2CH 2NH 2H .2HCl -N -H 3SON +HCl盐酸萘乙二胺紫红色1、2仪器与试剂1、2、1仪器①小型粉碎机。
②分光光度计。
③25ml 具塞比色管。
1、2、2试剂①氯化铵缓冲溶液:在1 000ml 容量瓶中加人500ml 水,然后准确加入20、0ml 盐酸,振荡混匀后,再准确加入50ml 氢氧化铵,用水稀释至刻度。
必要时用稀盐酸与稀氢氧化铵调试pH 至9、6~9、7。
②硫酸锌溶液(0、42mol/L):称取120g 硫酸锌(ZnSO 4·7H 2O),用水溶解,并稀释至1000ml 。
③氢氧化钠溶液(20g/L):称取20g 氢氧化钠用水溶解,稀释至1 000ml 。
④对氨基苯磺酸溶液:称取10g对氨基苯磺酸,溶于700ml水与300ml冰乙酸中,置棕色瓶中混匀,室温保存。
⑤盐酸萘乙二胺溶液(1g/L):称职0、1g盐酸萘乙二胺,加60%乙酸溶解并稀释至100ml,混匀后,置棕色瓶中,在冰箱中保存,1周内稳定。
⑥显色剂:临用前,将盐酸萘乙二胺溶液(1g/L)与对氨基苯磺酸溶液等体积混合。
仅供1次使用。
⑦亚硝酸钠标准储备液:准确称取250、0mg于硅胶干燥器中干燥24h得亚硝酸钠,用水溶解后移入500ml容量瓶中,加100ml氯化铵缓冲溶液,用水稀释至刻度,混匀,在4℃避光保存。
此溶液每毫升相当于500μg得亚硝酸钠。
实验室食品中亚硝酸盐的测定盐酸萘乙二胺法亚硝酸盐测定

实验室食品中亚硝酸盐的测定盐酸蔡乙二胺法亚硝酸盐测1范围本标准规定了食品中亚硝酸盐的测定方法。
适用于食品中亚硝酸盐的测定。
亚硝酸盐方法检出限为Img/kg。
2原理试样经沉淀蛋白质、除去脂肪后,在弱酸条件下亚硝酸盐与氨基苯磺酸重氮化后,再与盐酸蔡乙二胺偶合形成紫红色染料,与标准比较定量。
3试剂3.1亚铁氟化钾溶液:称取106.Og亚铁氟化钾[KFe(CN)6・3比0],用水溶解,并稀释至IoOon1.1.。
3.2乙酸锌溶液:称取220.Og乙酸锌[Zn(CHsCOO)2、2⅛0],加30m1.冰乙酸溶于水,并稀释至1000m1.o3.3饱和硼砂溶液:称取5.Og硼酸钠(Na2BQ7∙IOH2O),溶于IOOm1.热水中,冷却后备用。
3.4对氨基苯磺酸溶液(4g∕1.):称取0.4g对氨基苯磺酸,溶于IOOnI1.20%盐酸中,置棕色瓶中混匀,避光保存。
3.5盐酸蔡乙二胺溶液(2g∕1.):称取0.2g盐酸蔡乙二胺,溶解于IOOm1.水中,混匀后,置棕色瓶中,避光保存。
3.6亚硝酸钠标准溶液:准确称取0∙IOOOg于硅胶干燥器中干燥24h的亚硝酸钠,加水溶解移入50OnI1.容量瓶中,加水稀释至刻度,混匀,此溶液每毫升相当于200Ug的亚硝酸钠。
3.7亚硝酸钠标准使用液:临用前,吸取亚硝酸钠标准溶液5.OOm1.,置于20OnI1.容量瓶中,加水稀释至刻度,此溶液每毫升相当于5.Oug亚硝酸钠。
4仪器4.1小型绞肉机。
4.2分光光度计。
5分析步骤5.1试样处理称取5.Og经绞碎混匀的试样,置于50m1.烧杯中,加12.5m1.硼砂饱和液,搅拌均匀,以70。
C左右的水约300m1.将试样洗入50Om1.容量瓶中,于沸水浴中加热15min,取出后冷却至室温,然后一面转动,一面加入5m1.亚铁氟化钾溶液,摇匀,再加入5m1.乙酸锌溶液,以沉淀蛋白质。
加水至刻度,摇匀,放置0.5h,除去上层脂肪,清液用滤纸过滤,弃去初滤液30m1.,滤液备用。
实验 肉制品中亚硝酸盐的测定

实验肉制品中亚硝酸盐的测定(盐酸萘乙二胺法)一、目的与要求:1.熟练掌握样品制备、提取的基本操作技能。
2.明确与掌握盐酸萘乙二胺比色法测定亚硝酸盐的基本原理及操作方法。
二、原理:样品经沉淀蛋白质,除去脂肪后,在弱酸条件下亚硝酸盐与对氨基苯磺酸重氮化后,生成的重氮化合物,再与盐酸萘乙二氨偶合形成紫红色染料,此“染料”颜色的深浅与亚硝酸盐的含量成正比,其最大吸收波长为538nm ,可以测定吸光度并与标准比较定量。
反应式如下:见教材P3161.重氮化反应:2.偶合反应:三、样品、试剂与仪器样品:品名:厂家:试剂:1.蛋白质沉淀剂(公用)(1)饱和硼砂溶液:称取5克硼酸钠(Na2B07·10H20),溶于100毫升热水中,冷却后备用。
(2) 亚铁氰化钾溶液:称取10.6克亚铁氰化钾[K4Fe9(CN)5.3H2O],溶于水后,稀释至100毫升。
乙酸锌溶液:称取11g Zn(CHCOO)2 .2H2O加1.5mL冰乙酸,溶于水定容50mL。
2.显色剂(1)0.4%对氨基苯磺酸溶液:称取0.4克对氨基苯磺酸,溶于100毫升20%的盐酸中,避光保存。
100ml/4组()0.2%盐酸萘乙二胺溶液:称取0.2克盐酸萘乙二胺,溶于100毫升重蒸馏水中,避光保存。
100ml/4组3.亚硝酸钠标准原液:精密称取0.1000克于硅胶干燥器中干燥24小时的亚硝酸钠,加水溶解移入500毫升容量瓶中,并稀释至刻度。
此溶液每毫升相当于200微克亚硝酸钠。
4.亚硝酸钠标准使用液(5μg NaNO2/ml):临用前,吸取亚硝酸钠标准溶液5.00毫升,置于200毫升容量瓶中,加重蒸馏水稀释至刻度,此溶液每毫升相当于5μg亚硝酸钠。
亚硝酸钠标准原液由教师提供。
5.1:4盐酸配制显色剂1用,每4组100ml。
仪器:1. 小型绞肉机。
2. 721分光光度计。
3.25ml比色管每组7支四、操作方法:1.样品处理:称取5.0克经绞碎混匀的样品,置于50毫升干洁的小烧杯中,加入12.5毫升饱和硼砂溶液,以玻璃棒搅拌均匀,以70℃左右的重蒸馏水约300毫升分数次将样品全部洗入500毫升容量瓶中。
亚硝酸盐含量的测定实验
亚硝酸盐含量的测定实验一、实验原理泡菜的制作离不开乳酸菌,乳酸菌是厌氧细菌,在无氧的情况下,将葡萄糖分解成乳酸。
常见的乳酸菌有乳酸链球菌和乳酸杆菌。
在盐酸酸化条件下,亚硝酸盐与对氨基苯磺酸发生重氮化反应后,与N-1-萘基乙二胺盐酸盐结合形成玫瑰色染料。
将显色反应后的样品与已知浓度的标准液进行目测比较,可以大致估算出泡菜中亚硝酸盐的含量。
二、设备及试剂泡菜、三角瓶、量筒、烧杯、pH试纸、玻璃棒、微量可调移液器、试管、亚硝酸盐含量的测定试剂盒。
(试剂盒实验首先利用亚硝酸盐在弱酸条件下可与对氨基苯磺酸重氮化后。
再与N-1-萘基乙二胺偶合形成红色染料的原理,以及利用比色计对红色染料的测定,从而得出标准梯度显色液。
然后将处理后的样品溶液与标准显色液观察比较,就可得出亚硝酸盐的含量。
试剂盒中准确提供实验所需的各种试剂,无需额外购买称量,具有使用方便、快捷的特点)三、试剂配制对氨基苯磺酸溶液:称取0.4g对氨基苯磺酸,溶解于100ml体积分数为20%的盐酸中,避光保存(4mg/ml)。
N-1-萘基乙二胺盐酸盐溶液:称取0.2g N-1-萘基乙二胺盐酸盐,溶解于100ml的水中,避光保存(2mg/ml)。
亚硝酸钠标准溶液:向含有0.025g亚硝酸钠固体的离心管中加入1mL蒸馏水充分溶解,然后将以上溶解液移至50mL容量瓶中,取1mL溶液,移至100mL容量瓶中,加蒸馏水稀释到刻度,即制得5μg/mL亚硝酸钠标准液;提取剂:分别称取50g氯化镉、氯化钡,溶解于1000ml蒸馏水中,用盐酸调节pH至1。
氢氧化铝乳液:取10g氢氧化铝固体,加水100mL配成乳液。
四、实验流程测定亚硝酸盐的含量(1)制备标准显色液:用微量可调移液器吸取0μL,20μL,40μL,60μL,80μL,100μL,150μL 的亚硝酸钠标准溶液,分别置于7支试管中,在各管中分别加入200μL对氨基苯磺酸,混匀,静置3~5min后,再分别各加入100μL N-1-萘基乙二胺盐酸盐溶液,用微量可调移液器添加蒸馏水,使各试管内总体积为5mL,混匀,观察亚硝酸钠溶液颜色的梯度变化;(2)制备样品处理液:取腌制的泡菜40g,用榨汁机粉碎,过滤后得到大约20mL汁液。
亚硝酸盐对氨基苯磺酸
d、亚硝酸盐与人体健康的关系:
膳食中的亚硝酸盐一般不会危害人体健康, 但是,当人体摄入的亚硝酸盐总量达到0.3~ 0.5g时,会引起中毒,达3g时会引起死亡。
膳食中的绝大部分亚硝酸盐随尿排出,只有 在特定的条件下(适宜的pH、温度和一定的
微生物作用)才会转变成致癌物――亚硝胺
e、我国食品卫生标准规定的亚硝酸盐含量:
肉制品中不得超过30mg/kg 酱菜中不超过20mg/kg 婴儿奶粉中不得超过2mg/kg
为什么日常生活中要多吃新鲜蔬菜,不吃 存放时间过长、变质的蔬菜?
答:有些蔬菜,如小白菜和萝卜等,含有 丰富的硝酸盐。当这些蔬菜放置过久发生 变质(发黄、腐烂)或者煮熟后存放太久 时,蔬菜中的硝酸盐会被微生物还原成亚 硝酸盐,危害人体健康。
酶
C6H12O6
2C3H6O3+能量
为什么含有抗生素的牛奶不能发酵为酸奶?
牛奶发酵为酸奶主要依靠乳酸菌的发酵 作用,而抗生素能够杀死或抑制乳酸菌的生 长。
(二)亚硝酸盐
a、性质: 白色粉末,外观与食盐相似,有
咸味,易溶于水
b、在食品生产中的作用: 食品添加剂
c、分布 广泛
,在蔬菜、咸菜和
豆粉中的含量如何?
0.15 0.60 0.20 0.10 0.10
0.15 0.20 0.10 0.05 0.05
0.15 0.80 0.60 0.20 0.20
泡菜腌制过程中亚硝酸盐含量的变化
课题成果评价
(一)泡菜腌制的质量如何
(三)泡菜发酵的阶段
1、发酵前期:
蔬菜刚入坛时,其表面带入的微生物,主要 是以不抗酸的大肠杆菌和酵母菌等较为活跃, 它们产生较多的乳酸、酒精、醋酸和CO2,CO2 以气泡从水槽内放出,逐渐使坛内形成无氧状 态。
[注册环保工程师考试密押题库与答案解析]环境监测与分析(三)
![[注册环保工程师考试密押题库与答案解析]环境监测与分析(三)](https://img.taocdn.com/s3/m/e24cc7ad3b3567ec102d8af2.png)
B.24h
C.36h
D.48h
答案:D[解析] 固体废弃物急性毒性的初筛试验,采用18~24g体重的小白鼠(或200~300g大白鼠),经口染毒,记录48h的动物死亡数。
[解题关键] 本题易于实验前8~12h禁食混淆。
问题:35. 未经任何处理的清洁水样最长存放时间为 。
A.24h
B.48h
问题:1. 在重铬酸钾法化学需氧量COD的测定中硫酸银的加入起到 作用。
A.催化剂
B.掩蔽剂
C.活化剂
D.络合剂
答案:A[解析] 采用重铬酸钾回流法测定化学需氧量COD的过程中加入硫酸银的作用是起到催化剂的作用,掩蔽氯离子用硫酸汞-硫酸溶液。
[解题关键] 解此题的关键是正确区分硫酸银在化学需氧量COD以及高锰酸盐测定过程中的作用不同,硫酸银在高锰酸盐指数测定中起的是沉淀掩蔽氯离子的作用。
注册环保工程师考试密押题库与答案解析环境监测与分析三注册环保工程师考试密押题库与答案解析环境监测与分析三page1numpages1注册环保工程师考试密押题库与答案解析环境监测与分析三环境监测与分析三单项选择题问题
[注册环保工程师考试密押题库与答案解析]环境监测与分析(三)
环境监测与分析(三)
单项选择题
问题:39. 在水质监测中,一个江(河)段应设几个消减断面 。
A.一个
B.两个
C.三个
D.四个
答案:A一般一个河段只设一个消减断面。
问题:40. 微溶化合物Ag2CrO4在O.0010mol·L-1AgNO3溶液中的溶解度比在0.0010mol·L-1K2CrO4溶液中的溶解度( )。
A.较大
B.较小
A.三级
B.Ⅳ类
C.二级
食品分析复习题

食品分析检样--由整批食物的各个部分采取的少量样品称为检样。
检样的量按产品标准的规定。
原始样品--把许多份检样综合在一起称为原始样品。
平均样品--原始样品经过处理再抽取其中一部分作检验用者称为平均样品。
应一式三份,分别供检验、复验及备查使用。
每份样品数量一般不少于0.5公斤。
准确度是指测定值与真实值接近的程度;精密度是指重复测定值之间的接近程度或重现性。
“精密称取”——必须按所列数值称取,精确0.0001g 。
准确度高的方法精密度必然高;而精密度高的方法准确度不一定高。
标准偏差S =√∑d2 / n-1说明数据的分散程度直接法--利用水分本身的物理性质、化学性质测定水分:重量法、蒸馏法(香料)、卡尔²费休法(水和碘、二氧化硫反应)、化学方法。
间接法--利用食品的物理常数通过函数关系确定水分含量:如测相对密度、折射率、电导、旋光率等。
水分活度表示食品中水分存在的状态,反映水与食品的结合或游离程度溶液中水的逸度与纯水的逸度之比值,可近似表示为溶液中水蒸气分压与纯水蒸汽压之比。
食品组分经高温灼烧后,无机成分(主要是无机盐和氧化物)残留下来,这些残留物即为灰分。
通常把食品经高温灼烧后的残留物称为——粗灰分(总灰分)。
总酸度:食品中所有酸性成分的总量,又可称“可滴定酸”。
有效酸度:H+的活度,用pH表示。
挥发酸:食品中易挥发的有机酸,可用蒸馏的方式分离,再用标准碱液来滴定。
挥发酸包含游离的和结合的两部分。
牛乳酸度:1、外表酸度(固有酸度,0.15-0.18%乳酸):新鲜牛乳所具有的酸度,主要成分为酪蛋白、白蛋白、柠檬酸盐、磷酸盐;2、真实酸度(发酵酸度):牛乳的乳糖发酵而产生的乳酸而升高的那部分酸度。
习惯上把含量在0.2%以上的牛乳列为不新鲜牛乳。
牛乳18°T—指滴定100 ml 牛乳样品,消耗0.1 mol/L NaOH 溶液的ml数,或滴定10 ml 样品,结果再乘10。
新鲜牛乳的酸度常为16 ~18°T。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
亚硝酸盐与对氨基苯磺酸发生重氮化反应,盐酸萘乙二胺反应方程式亚硝酸盐与对氨基苯磺酸(俗称苯磺酸)可以发生重氮化反应,生成对硝基苯磺酸钠和水。
这是化学中非常重
要的反应之一,也是有机合成中常用的一种反应。
本文将
详细介绍亚硝酸盐与苯磺酸的反应机理、反应条件以及反
应的应用。
一、反应机理
在反应中,亚硝酸钠首先与苯磺酸反应生成出对氨基苯磺酸钠和水,然后对氨基苯磺酸钠在酸性条件下发生重
氮化反应。
具体反应机理如下:
首先,亚硝酸钠(NaNO2)和苯磺酸(H2C6H4SO3H)反应生成出对氨基苯磺酸钠(NaH2C6H4SO3)和水(H2O):H2C6H4SO3H + NaNO2 + HCl → NaH2C6H4SO3 + H2O + NaCl
然后,对氨基苯磺酸钠在酸性条件下(pH = 3.5-4)发生重氮化反应,生成出对硝基苯磺酸钠
(NaC6H4SO3N=O)和水:
NaH2C6H4SO3 + HCl + NaNO2 → NaC6H4SO3N=O + H2O + NaCl
二、反应条件
1. 反应物的浓度
亚硝酸钠和苯磺酸反应的浓度是影响反应速率的重要因素。
通常情况下,亚硝酸钠的浓度在1-2 mol/L时,苯磺酸浓度为1-3 mol/L时反应速率较快。
2. 反应的酸度
对氨基苯磺酸钠需要在酸性条件下才能发生重氮化反应。
为了使反应中的pH值达到酸性条件,可以加入少量的盐酸或硝酸,使pH降至3.5-4。
3. 反应的温度
反应温度对反应速率直接影响,通常情况下,初始反应温度在0℃-5℃,反应过程中可以升温至10℃-15℃。
三、反应应用
亚硝酸盐与苯磺酸发生重氮化反应的产物——对硝基苯磺酸钠也是一种重要的中间体。
它可以被用于合成染料、药物、香料等有机化合物,具有广泛的应用前景。
例如,对硝基苯磺酸钠可以和萘乙二胺反应,生成出新的染料——香肉碱君主黄。
反应方程式如下:
C10H7NH2 + NaC6H4SO3N=O + HCl →
C10H7N=NC6H4SO3Na + H2O
这种染料在制备纤维素酯人造丝时,可以作为着色剂使用。
同时,在食品工业中也可以用于染色。
对硝基苯磺酸钠还可以和其它的酸性底物反应,生成出具有不同性质的化合物。
例如,它可以和3-氨基-4-甲氧基苯甲酸钠反应,生成出阳离子染料——阳离子茜草红。
这种染料广泛应用于纺织、皮革、木制品等领域。
总之,亚硝酸盐与苯磺酸的重氮化反应是一种非常重要的有机反应。
通过对该反应机制、反应条件以及反应应用的研究,我们可以更深入地理解这种有机反应的本质,同时也可以扩展其在实际应用中的可能性。
