金属及各类晶体配位数计算图总结共140页文档
合集下载
金属晶体配位数计算优秀文档

既有共价键又有金属键和范 1、在晶体学中配位数与晶胞类型有关;
2、离子晶体中指一个离子周围最近的异电性离子的数目;
德华力,属于混合型晶体 它可以描述晶体中粒子排列的紧密程度,粒子排列越紧密,配位数越大,结合能越低,晶体结构越稳定。 C的杂化方式:SP 2
谢谢!
谢谢观看
铜型
采用这种堆 积的典型代
表
空间利用率
配位数
Po
52℅
6
Na K Fe
68℅
8
Mg Zn Ti
74℅
12
Cu Ag Au
74℅
12
混合型晶体
1、在晶体学中配位数与晶胞类型有关; 非密置层堆积——简单立方堆积 配位数:在晶体中与离子(或原子)直接相连的离子(或原子)数。 半径越小,金属键越强 如碱金属 3、配位化学中,化合物中性原子周围的配位原子的数目。 概念:一个粒子周围最近邻的粒子数称为配位数。 半径越小,金属键越强 如碱金属 金属晶体的原子堆积模型 金属晶体的原子堆积模型
在提到配位数时应当分析其所处环境。
• 1、在晶体学中配位数与晶胞类型有关; • 2、离子晶体中指一个离子周围最近的异电性离子的数目; • 3、配位化学中,化合物中性原子周围的配位原子的数目。
配位数:在晶体中与离子(或原子)直接相连的离 子(或原子)数。
金属晶体的原子堆积模型
非密置层,配位 数是4
金属晶体配位数计算
影响金属键强弱的因素
金属阳离子的半径
半径越小,金属键越强
如碱金属
金属阳离子的电荷数 电荷越多,金属键越强;如
Al>Mg>Na 金属阳离子的堆积方式
配位数
概念:一个粒子周围最近邻的粒子数称为配位数。
2、离子晶体中指一个离子周围最近的异电性离子的数目;
德华力,属于混合型晶体 它可以描述晶体中粒子排列的紧密程度,粒子排列越紧密,配位数越大,结合能越低,晶体结构越稳定。 C的杂化方式:SP 2
谢谢!
谢谢观看
铜型
采用这种堆 积的典型代
表
空间利用率
配位数
Po
52℅
6
Na K Fe
68℅
8
Mg Zn Ti
74℅
12
Cu Ag Au
74℅
12
混合型晶体
1、在晶体学中配位数与晶胞类型有关; 非密置层堆积——简单立方堆积 配位数:在晶体中与离子(或原子)直接相连的离子(或原子)数。 半径越小,金属键越强 如碱金属 3、配位化学中,化合物中性原子周围的配位原子的数目。 概念:一个粒子周围最近邻的粒子数称为配位数。 半径越小,金属键越强 如碱金属 金属晶体的原子堆积模型 金属晶体的原子堆积模型
在提到配位数时应当分析其所处环境。
• 1、在晶体学中配位数与晶胞类型有关; • 2、离子晶体中指一个离子周围最近的异电性离子的数目; • 3、配位化学中,化合物中性原子周围的配位原子的数目。
配位数:在晶体中与离子(或原子)直接相连的离 子(或原子)数。
金属晶体的原子堆积模型
非密置层,配位 数是4
金属晶体配位数计算
影响金属键强弱的因素
金属阳离子的半径
半径越小,金属键越强
如碱金属
金属阳离子的电荷数 电荷越多,金属键越强;如
Al>Mg>Na 金属阳离子的堆积方式
配位数
概念:一个粒子周围最近邻的粒子数称为配位数。
晶体配位数_空间利用率计算
解析:
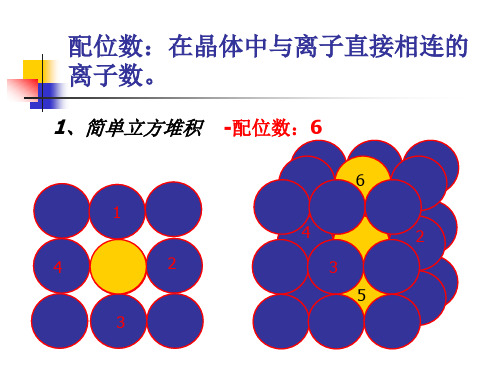
① Ni原子的配位数为: Ni原子的数目为: 8×1/8 + 6×1/2 =4 ②晶体的密度为: m= 4M/NA ; V= a3 ,a2+a2+a2 = (4r)2 3a2=16r2→a=4d/3 p=m/v=4M/NA/4d/3= 3M/dNA
探究3:已知铜晶胞是面心立方晶胞,该晶胞的 边长为3.6210-10m ,每一个铜原子的质量为 1.05510-25kg ,试回答下列问题: (1)一个晶胞中“实际”拥有的铜原子数是多 少? (2)该晶胞的体积是多大? (3)利用以上结果计算金属铜的密度。 (4)计算空间利用率。
探究1:单质晶体中原子的堆积方式
如下图所示,其晶胞特征如下图乙所示,原子之间 相互位置关系的平面图如下图丙所示。
甲
乙
丙
若已知Ni的原子半径为d,NA代表阿伏加德罗常数,Ni的 相对原子质量为M,请回答: ①晶胞中Ni原子的配位数为___ ___ _ ,一个晶胞中Ni 原子的数目为_ _; ②该晶体的密度为______ _ (用字母表示)。
a
3
100 %
晶胞的有关计算
1) 利用晶胞参数可计算晶胞体积(V),根据相对分子 质量(M)、晶胞中粒子数(Z)和阿伏伽德罗NA,可计算 晶体的密度 :M·Z/NA·V 2)已知棱长,求某线段。晶胞中各线段间的关系如下:
3 )空间利用率:指构成晶体的微粒在整个晶体空间中 所占有的体积百分比。 球体积 空间利用率 = ———— 100% 晶胞体积
配位数:在晶体中与离子直接相连的 离子数。
1、简单立方堆积
-配位数:6
6 1 4 3 2 1 4 3 5 2
2、钾型(体心立方堆积)
金属晶体配位数 计算 ppt课件

笨,没有学问无颜见爹娘 ……” • “太阳当空照,花儿对我笑,小鸟说早早早……”
配位数
概念:一个粒子周围最近邻的粒子数称为配位数。
它可以描述晶体中粒子排列的紧密程度,粒 子排列越紧密,配位数越大,结合能越低, 晶体结构越稳定。
在提到配位数时应当分析其所处环境。
• 1、在晶体学中配位数与晶胞类型有关; • 2、离子晶体中指一个离子周围最近的异电性离子的数目; • 3、配位化学中,化合物中性原子周围的配位原子的数目。
配位数:在晶体中与离子(或原子)直接相连的离 子(或原子)数。
金属晶体的原子堆积模型
非密置层,配位 数是4
密置层,配位数 是6
非密置层堆积——简单立方堆积
1、简单立方堆积
-配位数:6
1
4
2
3
6146源自2352.体心立方堆积——钾型
2.体心立方堆积——钾型
5
6
8
7
1
2
4
3
-配位数:8
二.密置层堆积
金属晶体的空间结构
影响金属键强弱的因素
金属阳离子的半径
半径越小,金属键越强
如碱金属
金属阳离子的电荷数 电荷越多,金属键越强;如
Al>Mg>Na 金属阳离子的堆积方式
• 你怎么称呼老师? • 如果老师最后没有总结一节课的重点的难点,你
是否会认为老师的教学方法需要改进? • 你所经历的课堂,是讲座式还是讨论式? • 教师的教鞭 • “不怕太阳晒,也不怕那风雨狂,只怕先生骂我
3. 六方最密堆积——镁型
配位数:12
7 19
8 2
6
3
5
4
10
11
12
4.面心立方最密堆积——铜型
配位数
概念:一个粒子周围最近邻的粒子数称为配位数。
它可以描述晶体中粒子排列的紧密程度,粒 子排列越紧密,配位数越大,结合能越低, 晶体结构越稳定。
在提到配位数时应当分析其所处环境。
• 1、在晶体学中配位数与晶胞类型有关; • 2、离子晶体中指一个离子周围最近的异电性离子的数目; • 3、配位化学中,化合物中性原子周围的配位原子的数目。
配位数:在晶体中与离子(或原子)直接相连的离 子(或原子)数。
金属晶体的原子堆积模型
非密置层,配位 数是4
密置层,配位数 是6
非密置层堆积——简单立方堆积
1、简单立方堆积
-配位数:6
1
4
2
3
6146源自2352.体心立方堆积——钾型
2.体心立方堆积——钾型
5
6
8
7
1
2
4
3
-配位数:8
二.密置层堆积
金属晶体的空间结构
影响金属键强弱的因素
金属阳离子的半径
半径越小,金属键越强
如碱金属
金属阳离子的电荷数 电荷越多,金属键越强;如
Al>Mg>Na 金属阳离子的堆积方式
• 你怎么称呼老师? • 如果老师最后没有总结一节课的重点的难点,你
是否会认为老师的教学方法需要改进? • 你所经历的课堂,是讲座式还是讨论式? • 教师的教鞭 • “不怕太阳晒,也不怕那风雨狂,只怕先生骂我
3. 六方最密堆积——镁型
配位数:12
7 19
8 2
6
3
5
4
10
11
12
4.面心立方最密堆积——铜型
金属晶体配位数计算

8
Mg Zn Ti
74℅
12
Cu Ag Au
74℅
12
混合型晶体
在提到配位数时应当分析其所处环境。
2、离子晶体中指一个离子周围最近的异电性离子的数目;
半径越小,金属键越强 如碱金属
六方最密堆积——镁型
六方最密堆积——镁型
配位数:在晶体中与离子(或原子)直接相连的离子(或原子)数。
电荷越多,金属键越强;
金属晶体配位数计算
影响金属键强弱的因素
金属阳离子的半径
半径越小,金属键越强
如碱金属
金属阳离子的电荷数 电荷越多,金属键越强;如
Al>Mg>Na 金属阳离子的堆积方式
配位数
概念:一个粒子周围最近邻的粒子数称为配位数。 2、离子晶体中指一个离子周围最近的异电性离子的数目;
非密置层堆积——简单立方堆积 概念:一个粒子周围最近邻的粒子数称为配位数。 它可以描述晶体中粒子排列的紧密程度,粒子排列越紧密,配位数越大,结合能越低,晶体结构越稳定。 它可以描述晶体中粒子排列的紧密程度,粒子排列越紧密,配位数越大,结合能越低,晶体结构越稳定。 概念:一个粒子周围最近邻的粒子数称为配位数。 半径越小,金属键越强 如碱金属
2.体心立方堆积——钾型
5
6
8
7
1
2
4
3
-配位数:8
3. 六方最密堆积——镁型
配位数:12
7 19
8 2
6
3
5
4
10
11
12
4.面心立方最密堆积——铜型
堆积模型
简单立方 体心立方 钾型 立方最密 镁型 面心立方最密
铜型
采用这种堆 积的典型代
常见晶体模型及晶胞计算
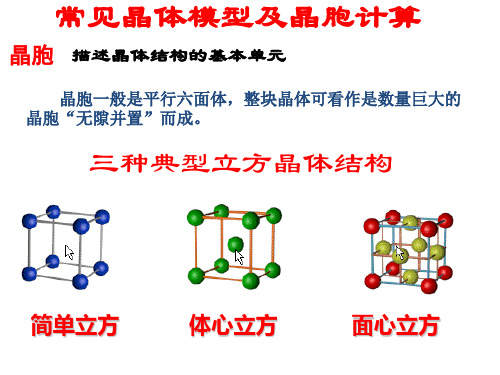
(4)能否 把“NaCl”称为分子式?
练习
-的距离为 a cm,该晶体密度为
(1)设NaCl晶胞的边长为acm,则
示晶为胞中Na+和Cl-的最近距离(( 即小)立
方体的边长)为 a/2 cm,则晶胞中 同种离子的最近距离为 a/2 cm。
(2)晶胞的边长为acm,求NaCl晶 体的密度。
ρ=
M / NA×晶胞所含粒子数 晶胞的体积
镁型[六方密堆积] (Be Mg ⅢB ⅣB ⅦB )
12
6
3
54
12
6
3
54
12
6
3
54
A B A B A
找镁型的晶胞
1200
每个晶胞含原子数: 2 配位数: 12
空间占有率:
六方密堆积(镁型)的空间利用率计算:
四点间的夹角均为60°
先求S
在镁型堆积中取出六方晶胞,平行六面体的底是
平行四边形,各边长a=2r,则平行四边形的面积:
找铜型的晶胞
面心立方最密堆积的空间占有率 =74%
金属晶体的四种堆积模型对比
堆积模型
采纳这种堆积 的典型代表
空间利用率
配位数
简单立方
Po(钋)
52%
6
体心立方 (钾型)
K、Na、Fe
68%
8
六方最密 (镁型)
Mg、Zn、Ti
74%
12
面心立方最密 (铜型)
Cu, Ag, Au
74%
12
晶胞
原子晶体
金刚石
该晶胞实际分摊到的碳原子数为 (4 + 6 ×1/2 + 8 ×1/8) = 8个。
小结:高考常见题型 (一) 晶胞中微粒个数的计算, 求化学式
练习
-的距离为 a cm,该晶体密度为
(1)设NaCl晶胞的边长为acm,则
示晶为胞中Na+和Cl-的最近距离(( 即小)立
方体的边长)为 a/2 cm,则晶胞中 同种离子的最近距离为 a/2 cm。
(2)晶胞的边长为acm,求NaCl晶 体的密度。
ρ=
M / NA×晶胞所含粒子数 晶胞的体积
镁型[六方密堆积] (Be Mg ⅢB ⅣB ⅦB )
12
6
3
54
12
6
3
54
12
6
3
54
A B A B A
找镁型的晶胞
1200
每个晶胞含原子数: 2 配位数: 12
空间占有率:
六方密堆积(镁型)的空间利用率计算:
四点间的夹角均为60°
先求S
在镁型堆积中取出六方晶胞,平行六面体的底是
平行四边形,各边长a=2r,则平行四边形的面积:
找铜型的晶胞
面心立方最密堆积的空间占有率 =74%
金属晶体的四种堆积模型对比
堆积模型
采纳这种堆积 的典型代表
空间利用率
配位数
简单立方
Po(钋)
52%
6
体心立方 (钾型)
K、Na、Fe
68%
8
六方最密 (镁型)
Mg、Zn、Ti
74%
12
面心立方最密 (铜型)
Cu, Ag, Au
74%
12
晶胞
原子晶体
金刚石
该晶胞实际分摊到的碳原子数为 (4 + 6 ×1/2 + 8 ×1/8) = 8个。
小结:高考常见题型 (一) 晶胞中微粒个数的计算, 求化学式
金属晶体配位数计算

非密置层,配位数 是4
密置层,配位数是 6
第5页,本讲稿共15页
非密置层堆积——简单立方堆积
第6页,本讲稿共15页
1、简单立方堆积
-配位数:6
1
4
2
3
6
1
4
6
2
3
5
第7页,本讲稿共15页
2.体心立方堆积——钾型
第8页,本讲稿共15页
2.体心立方堆积——钾型
5
6
8
7
1
2
4
3
-配位数:8
第9页,本讲稿共15页
二.密置层堆积
第10页,本讲稿共15页
3. 六方最密堆积——镁型
配位数:12
7
1
9
6 5
8
2 3
4
10
11
12
第12页,本讲稿共15页
堆积模型
简单立方 体心立方 钾型 立方最密 镁型 面心立方最密
铜型
采用这种堆 积的典型代
表
空间利用率
配位数
第3页,本讲稿共15页
在提到配位数时应当分析其所处环境。
• 1、在晶体学中配位数与晶胞类型有关; • 2、离子晶体中指一个离子周围最近的异电性离子的数目; • 3、配位化学中,化合物中性原子周围的配位原子的数目。
配位数:在晶体中与离子(或原子)直接相连的离子(或 原子)数。
第4页,本讲稿共15页
金属晶体的原子堆积模型
金属晶体配位数计算
第1页,本讲稿共15页
影响金属键强弱的因素
金属阳离子的半径
金属阳离子的电荷数 金属阳离子的堆积方式
半径越小,金属键越强 如碱金属
电荷越多,金属键越强;如 Al>Mg>Na
金属晶体配位数计算

02
越紧密,配位数越大,结合能越低,晶体结构越稳
定。
在提到配位数时应当分析其所处环 境。
配位数:在晶体中与离子(或原子) 直接相连的离子(或原子)数。
1. 在晶体学中配位数与晶胞类 型有关;
2. 离子晶体中指一个离子周围 最近的异电性离子的数目;
3. 配位化学中,化合物中性原 子周围的配位原子的数目。
采用这种堆积的 典型代表
空间利用 率
配位数
简单立方
Po
52℅
6
体心立方 钾型
Na K Fe
68℅
8Байду номын сангаас
立方最密 镁型
Mg Zn Ti
74℅
12
面心立方最密 铜型
Cu Ag Au
74℅
12
混合型晶体
C的杂化方式: SP2
既有共价键又有金属键和范德华力,属于混合型晶体
谢谢!
汇报人姓名
汇报日期
金属晶体的原 子堆积模型
非密置层,配 位数是4
密置层,配位 数是6
非密置层堆积——简单立方堆积
-配位数:6
1、简单立方堆积
1
4
2
3
6
1
4
6
2
3
5
2.体心立方堆积——钾型
2.体心立方堆积——钾型
-配位数:8
二.密置层堆积
3. 六方最密堆积——镁型
配位数:12
面心立方最密 堆积——铜型
堆积模型
金属晶体的空间结 构
金属晶体
单击此处添加正文具体内容
影响金属键强弱的因 素
金属阳离子的堆积方 式
半径越小,金属键越 强 如碱金属
金属阳离子的电荷数
金属晶体配位数计算

金属晶体
金属晶体的空间结构
精选课件
1
影响金属键强弱的因素
金属阳离子的半径
半径越小,金属键越强
如碱金属
金属阳离子的电荷数 电荷越多,金属键越强;如
Al>Mg>Na 金属阳离子的堆积方式
精选课件
2
配位数
概念:一个粒子周围最近邻的粒子数称为配位数。
它可以描述晶体中粒子排列的紧密程度,粒 子排列越紧密,配位数越大,结合能越低, 晶体结构越稳定。
精选课件
3
在提到配位数时应当分析其所处环境。
• 1、在晶体学中配位数与晶胞类型有关; • 2、离子晶体中指一个离子周围最近的异电性离子的数目; • 3、配位化学中,化合物中性原子周围的配位原子的数目。
配位数:在晶体中与离子(或原子)直接相连的离 子(或原子)数。
精选课件
4
金属晶体的原子堆积模型
非密置层,配位 数是4
8 2
6
3
5
4
Hale Waihona Puke 101112
精选课件
11
4.面心立方最密堆积——铜型
精选课件
12
Po
52℅
6
Na K Fe
68℅
8
Mg Zn Ti
74℅
12
Cu Ag Au
74℅
12
精选课件
13
混合型晶体
既有共价键又有金属键和范 德华力,属于混合型晶体 C的杂化方式:SP 2
精选课件
14
谢谢!
精选课件
15
感谢亲观看此幻灯片,此课件部分内容来源于网络, 如有侵权请及时联系我们删除,谢谢配合!
精选课件
密置层,配位数
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
16、业余生活要有意义,不要越轨。——华盛顿 17、一个人即使已登上顶峰,也仍要自强不息。——罗素·贝克 18、最大的挑战和突破在于用人,而用人最大的突破在于信任人。——马云 19、自己活着,就是为了使别人过得更美好。——雷锋 20、要掌握书,莫被书掌握;要为生而读,莫为读而生。——布尔沃
金属及各类晶体配位数计算图总结
1、合法而稳定的权力在使用得当时很 少遇伯克
3、最大限度地行使权力总是令人反感 ;权力 不易确 定之处 始终存 在着危 险。— —塞·约翰逊 4、权力会奴化一切。——塔西佗
5、虽然权力是一头固执的熊,可是金 子可以 拉着它 的鼻子 走。— —莎士 比
END
