金属晶体练习题
材料科学基础习题

查看文本习题一、名词解释金属键; 结构起伏; 固溶体; 枝晶偏析; 奥氏体; 加工硬化; 离异共晶; 成分过冷; 热加工; 反应扩散二、画图1在简单立方晶胞中绘出()、(210)晶面及[、[210]晶向。
2结合Fe-Fe3C相图,分别画出纯铁经930℃和800℃渗碳后,试棒的成分-距离曲线示意图。
3如下图所示,将一锲形铜片置于间距恒定的两轧辊间轧制。
试画出轧制后铜片经再结晶后晶粒大小沿片长方向变化的示意图。
4画出简单立方晶体中(100)面上柏氏矢量为[010]的刃型位错与(001)面上柏氏矢量为[010]的刃型位错交割前后的示意图。
5画图说明成分过冷的形成。
三、Fe-Fe3C相图分析1用组织组成物填写相图。
2指出在ECF和PSK水平线上发生何种反应并写出反应式。
3计算相图中二次渗碳体和三次渗碳体可能的最大含量。
四、简答题1已知某铁碳合金,其组成相为铁素体和渗碳体,铁素体占82%,试求该合金的含碳量和组织组成物的相对量。
2什么是单滑移、多滑移、交滑移?三者的滑移线各有什么特征,如何解释?。
3设原子为刚球,在原子直径不变的情况下,试计算g-Fe转变为a-Fe时的体积膨胀率;如果测得910℃时g-Fe和a-Fe的点阵常数分别为0.3633nm和0.2892nm,试计算g-Fe转变为a-Fe的真实膨胀率。
4间隙固溶体与间隙化合物有何异同?5可否说扩散定律实际上只有一个?为什么?五、论述题τC结合右图所示的τC(晶体强度)—ρ位错密度关系曲线,分析强化金属材料的方法及其机制。
晶须冷塑变六、拓展题1 画出一个刃型位错环及其与柏士矢量的关系。
2用金相方法如何鉴别滑移和孪生变形?3 固态相变为何易于在晶体缺陷处形核?4 画出面心立方晶体中(225)晶面上的原子排列图。
综合题一:材料的结构1 谈谈你对材料学科和材料科学的认识。
2 金属键与其它结合键有何不同,如何解释金属的某些特性?3 说明空间点阵、晶体结构、晶胞三者之间的关系。
《金属学原理》各章习题及解答(晶体的塑性变形)
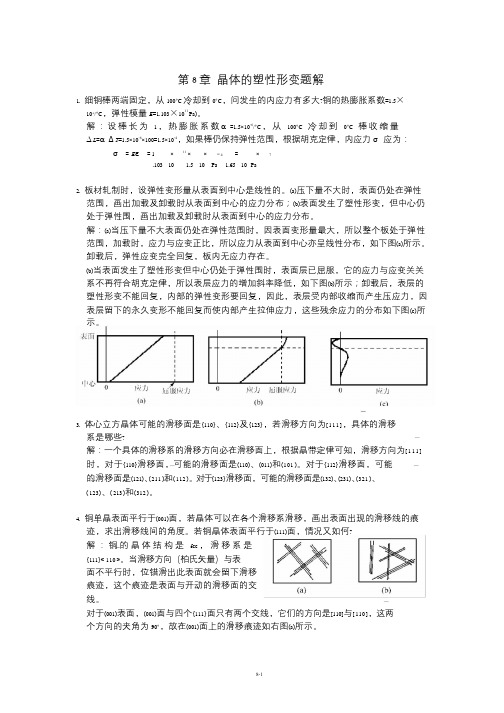
第8 章晶体的塑性形变题解1. 细铜棒两端固定,从100°C 冷却到0°C,问发生的内应力有多大?铜的热膨胀系数=1.5×10-6/°C,弹性模量E=1.103×1011 Pa)。
解:设棒长为 1 ,热膨胀系数α=1.5×10-6/°C ,从100°C 冷却到0°C 棒收缩量∆L=α∆T=1.5×10-6×100=1.5×10-4,如果棒仍保持弹性范围,根据胡克定律,内应力σ应为:σ=Eε=1 ×11 ××−4 =×7.103 10 1.5 10 Pa 1.65 10 Pa2. 板材轧制时,设弹性变形量从表面到中心是线性的。
(a)压下量不大时,表面仍处在弹性范围,画出加载及卸载时从表面到中心的应力分布;(b)表面发生了塑性形变,但中心仍处于弹性围,画出加载及卸载时从表面到中心的应力分布。
解:(a)当压下量不大表面仍处在弹性范围时,因表面变形量最大,所以整个板处于弹性范围,加载时,应力与应变正比,所以应力从表面到中心亦呈线性分布,如下图(a)所示。
卸载后,弹性应变完全回复,板内无应力存在。
(b)当表面发生了塑性形变但中心仍处于弹性围时,表面层已屈服,它的应力与应变关关系不再符合胡克定律,所以表层应力的增加斜率降低,如下图(b)所示;卸载后,表层的塑性形变不能回复,内部的弹性变形要回复,因此,表层受内部收缩而产生压应力,因表层留下的永久变形不能回复而使内部产生拉伸应力,这些残余应力的分布如下图(c)所示。
3. 体心立方晶体可能的滑移面是{110}、{112}及{123},若滑移方向为[111],具体的滑移系是哪些?解:一个具体的滑移系的滑移方向必在滑移面上,根据晶带定律可知,滑移方向为[111] 时,对于{110}滑移面,可能的滑移面是(110)、(011)和(101 )。
金属材料与热处理练习题(含答案)

金属材料与热处理练习题(含答案)一、单选题(共30题,每题1分,共30分)1、面心立方晶格有( )个顶点。
A、6B、10C、8正确答案:C2、45钢的含碳量是()。
A、0.45%B、4.5%C、45%正确答案:A3、铅在常温下的变形属:( ) 。
A、弹性变形B、既有冷变形也有热变形C、冷变形D、热变形正确答案:D4、铁碳合金共晶转变的温度是( )摄氏度。
A、1227B、727C、1148D、1083正确答案:C5、共晶白口铸铁的含碳量为( )%。
A、4.3B、2.11C、6.69正确答案:A6、牌号55的优质碳素用途是哪种( )。
A、轴B、型材C、齿轮D、弹簧正确答案:C7、冷变形时,随着变形量的增加,金属中的位错密度( )。
A、增加B、减小C、无变化D、先增大后减小正确答案:A8、根据材料的主要性能与作用分类,下列复合材料不正确的是( )。
A、功能复合材料B、纤维复合材料C、智能复合材料D、结构复合材料正确答案:B9、常用不锈钢有铁素体不锈钢、奥氏体不锈钢、马氏体不锈钢和( )。
A、铁素体-奥氏体不锈钢B、贝氏体不锈钢C、莱氏体不锈钢D、马氏体-奥氏体不锈钢正确答案:A10、灰铸铁中石墨呈什么状态的存在?( )。
A、球状B、网状C、团絮状D、片状正确答案:D11、原子的最小单元是( )。
A、晶体B、晶胞C、晶格正确答案:B12、实际晶粒度总是( )起始晶粒度。
A、大于B、等于C、小于D、无法确定正确答案:A13、淬火后的钢一般需要进行及时()。
A、退火B、正火C、回火正确答案:A14、按碳的含量分类下列正确的是( )。
A、大碳钢B、超碳钢C、小碳钢D、中碳钢正确答案:D15、合金固溶强化的主要原因是( )。
A、晶格类型发生了变化B、晶格发生了畸变C、晶粒细化D、发生了化学反应正确答案:B16、合金渗碳钢渗碳后需要进行()后才能达到使用要求。
A、淬火+高温回火B、淬火+低温回火C、淬火+中温回火正确答案:B17、球墨铸铁是怎样制作出来的( )。
高中化学晶体结构与性质练习题(含解析)

高中化学晶体结构与性质练习题学校:___________姓名:___________班级:_____________一、单选题1.下列关于晶体的结构,粒子间的相互作用的说法,正确的是()A.分子晶体中只存在范德华力B.离子晶体中只存在离子键C.共价晶体中都存在极性键D.金属晶体中只存在金属键2.某晶体的一部分如图所示,这种晶体中A、B、C三种微粒数之比是()A.3:9:4 B.1:4:2 C.2:9:4 D.3:8:5 3.下列各组物质的晶体中,化学键类型和晶体类型均相同的是()A.NH3和NH4Cl B.HCl和H2OC.KCl和K D.CO2和SiO24.电子表、电子计算器、电脑显示器都运用了液晶材料显示图象和文字。
有关其显示原理的叙述中,正确的是()A.施加电压时,液晶分子沿垂直于电场方向排列B.移去电压后,液晶分子恢复到原来状态C.施加电场时,液晶分子恢复到原来状态D.移去电场后,液晶分子沿电场方向排列5.下列物质的晶体类型与其他几个不同的是()A.Na2S B.MgCl2C.AlCl3D.Al2O36.下列说法中,错误的是()A.只含分子的晶体一定是分子晶体B.碘晶体升华时破坏了共价键C.几乎所有的酸都属于分子晶体D.稀有气体中只含原子,但稀有气体的晶体属于分子晶体7.美国某杂志曾经报道:在40 GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,有关原子晶体干冰的推断错误的是()A.有很高的熔点和沸点B.易汽化,可用作制冷材料C.含有极性共价键D.硬度大,可用作耐磨材料8.化学用语是学习化学的工具和基础。
下列有关化学用语的说法或使用正确的是A.稀有气体的晶体,其组成微粒是原子,晶体中不存在分子间作用力B.核素C—12的原子组成符号为C,二氧化碳分子的结构式为O=C=OC.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2OD.表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-571.6KJ/mol 9.铁元素形成的单质有三种晶胞的结构,如图所示,则下列说法正确的是()A.铁元素基态原子M层上有8对成对电子BC.三种晶胞α、β、θ中铁原子的配位数之比为4:6:3D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体结构相同10.下列说法正确的是()A.晶体一般都是透明的B.金刚石属于混合型晶体C.区分晶体和非晶体最可靠的科学方法是对固体进行X射线衍射实验D.在[Cu(NH3)4]2+配离子中NH3与中心离子Cu2+结合的化学键是非极性键11.金属钛(Ti)与氮形成的某种化合物常被用作高温结构材料和超导材料。
练习题及参考答案

1第一章1-1. 晶体与非晶体的本质区别是什么?单晶体为何有各向异性而实际金属表现为各向同性?(1)晶体中的质点在空间作有规则的排列,而非晶体内部的质点排列不规则 (2)因为不同的晶面及晶向上,原子的排列情况不同,所以晶体表现为各向异性,而实际金属是由很多方向各异的单晶体杂乱排列而成,所以整体表现为各向同性。
1-4. 铜和铁室温下的晶格常数分别为0.286n m 和0.3607n m ,求1c m 3铁和铜中的原子数。
1n m (n a n o m e t e r )=10--99m =10A (a n g s t r o n g ) 铜的晶格常数=0.286 x 10--77c m 铁的晶格常数=0.3607 x 10--77c m1c m 3铜的原子数=3)710286.0(31cm x cm - x 4 = 1.71x 10231c m 3 铁的原子数=3)7103607.0(31cm x cm -x 2 = 4.26x 102221-5. 常见的金属晶体典型结构有哪几种?α-F e , γ-F e , C u , A l , N i , P b , C r , V , M o , M g , Z n , W 各属于何种晶体结构?面心立方结构、体心立方结构、密排六方结构 γ-F e , C u , A l , N i , P b - 面心立方结构 α-F e , C r , V , M o , W - 体心立方结构 M g , Z n - 密排六方结构1 作图表示立方晶系(211)、(112)、(210)、(321)、(223)、(236)晶面与[111]、[111]、[021]、[112]、[211]、[123]晶向。
解:如图所示。
(211)、(112)、(210)、(321)、(223)、(236)晶面:(211) (112) (210)1.2★作图表示立方晶系(211)、(112)、(210)、(321)、(223)、(236)晶面与[111]、[111]、[021]、[112]、[211]、[123]晶向。
《金属学原理》各章习题及解答(第一章晶体题解)

11.某正交晶系单胞中,在如下位置有单原子存在:①(0, 1/2, 0),(1/2, 0, 1/2)两种位置都是同 类原子;②([1/2, 0,0]),(0, 1/2, 1/2)上是 A 原子,(0, 0, 1/2),(1/2, 1/2, 0)是 B 原子。问上两 种晶胞各属于哪一种布喇菲点阵? 解:①右图 a 中黑实线是一个正交单 胞,a 和 b 分别是两个晶轴,两个带影 线的圆代表给定的原子位置,应该注 意到在与此等效的所有位置都有原 子。根据题意,一个单胞含两个原子, 如果把黑线所定的晶轴向-b 平移 b/2, 把现在的 ABCDD'A'B'C'六面体看成 是单胞,可以知道这是 I 点阵。 ②右图 b 中黑实线是一个正交单胞,a 和 b 分别是两个晶轴,两个带影线的圆代表 A 原子 位置,两个黑色的圆代表 B 原子位置,应该注意到在与这些位置等效的所有位置都有相应 的各类原子。如果把黑线所定的晶轴向-a 平移 a/2,把现在的 CDEFF'C'D'E'六面体看成是 单胞,看出这是 I 单胞,其中结构基元由一个 A 原子和一个 B 原子构成。
8. 画出图 1-60 中四种平面点阵(它是无限大的)除平移外的所有对称元素及其所在位置(在 有限个阵点画出就可以了)。 解:把对称元素直接画在图 1-60 中,如下图所示。图 a 中过每个阵点并垂直纸面的轴都 是 2 次轴;根据上题的结果,在平行的 2 次轴中间又有 2 次轴,所以在四个相邻阵点中间 出现新的 2 次轴;因为α=90°,所以过 a1 以及过 a2 轴并垂直纸面的面是镜面,根据上题的 结果,在平行的 2 个镜面中间应是镜面,故在那里又出现新的镜面。图 c 中过每个阵点并 垂直纸面的轴都是 2 次轴;因在平行的 2 次轴中间应是 2 次轴,所以在阵点中间出现新的 2 次轴,在这些新的 2 次轴之间又出现新的 2 次轴;在图中看到一个复式单胞的轴之间夹 角是 90°,所以过复式单胞两根轴并垂直纸面的两个面是镜面,同样在每一组平行镜面之 间又应是新的镜面。图 b 中 a1=a2,并且α=90°,所以过每个阵点并垂直纸面的轴都是 4 次 轴,4 次轴隐含 2 次轴,因在平行的 2 次轴中间应是 2 次轴,故在两个 4 次轴的中间出现
高考化学一轮复习晶体的结构与性质专项训练知识点及练习题含答案
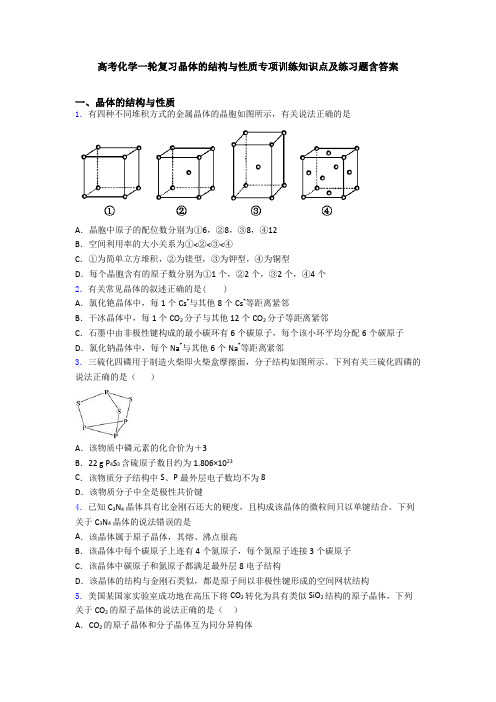
高考化学一轮复习晶体的结构与性质专项训练知识点及练习题含答案一、晶体的结构与性质1.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是A.晶胞中原子的配位数分别为①6,②8,③8,④12B.空间利用率的大小关系为①<②<③<④C.①为简单立方堆积,②为镁型,③为钾型,④为铜型D.每个晶胞含有的原子数分别为①1个,②2个,③2个,④4个2.有关常见晶体的叙述正确的是( )A.氯化铯晶体中,每1个Cs+与其他8个Cs+等距离紧邻B.干冰晶体中,每1个CO2分子与其他12个CO2分子等距离紧邻C.石墨中由非极性键构成的最小碳环有6个碳原子,每个该小环平均分配6个碳原子D.氯化钠晶体中,每个Na+与其他6个Na+等距离紧邻3.三硫化四磷用于制造火柴即火柴盒摩擦面,分子结构如图所示。
下列有关三硫化四磷的说法正确的是()A.该物质中磷元素的化合价为+3B.22 g P4S3含硫原子数目约为1.806×1023C.该物质分子结构中S、P最外层电子数均不为8D.该物质分子中全是极性共价键4.已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合。
下列关于C3N4晶体的说法错误的是A.该晶体属于原子晶体,其熔、沸点很高B.该晶体中每个碳原子上连有4个氮原子,每个氮原子连接3个碳原子C.该晶体中碳原子和氮原子都满足最外层8电子结构D.该晶体的结构与金刚石类似,都是原子间以非极性键形成的空间网状结构5.美国某国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体的说法正确的是()A.CO2的原子晶体和分子晶体互为同分异构体B.在一定条件下,CO2的原子晶体转化为分子晶体是物理变化C.CO2的原子晶体和分子晶体具有相同的物理性质D.在CO2的原子晶体中,每个C原子周围结合4个O原子,每个O原子与2个碳原子结合6.下列叙述正确的是A.离子晶体中,只存在离子健,不可能存在其它化学键B.可燃冰中甲烷分子与水分子之间存在氢键C.Na2O2、NaHSO4晶体中的阴、阳离子个数比均为12D.晶体熔点:金刚石>食盐>冰>干冰7.氟在自然界中常以CaF2的形式存在。
热处理课后练习题

第二章纯金属与合金的基本知识一、填空题:1.根据原子在空间排列的特征不同,固态物质可分为:和。
2.金属中常见的晶格类型有:、和。
3.金属中常见的晶体缺陷有:、和。
4.按合金组元间相互作用不同,合金在固态下的相结构分为和两类。
5.根据溶质原子在溶剂晶格中所占位置的不同,固溶体可分为和。
6.金属的实际结晶温度低于理论结晶温度的现象称为。
7.在纯金属的结晶过程中,理论结晶温度与实际结晶温度之差,称为。
8.金属的结晶过程包括和两个基本过程。
9.为了细化铸件的晶粒,改善其性能,在铸造过程中常采用的方法有:______________________、______________________、______________________。
10.Cu-Ni合金构成的相图是:_____________________。
二、判断题:1.晶体的原子排列有序,并具有各向同性的特点。
2.晶体缺陷越多,实际金属的力学性能一定也越差。
3.间隙固溶体和置换固溶体均可形成无限固溶体。
4.一般情况下,金属的晶粒越细小,其力学性能越好。
5.所谓共晶转变,是指一定成分的液态合金,在一定的温度下同时结晶出两种不同固相的转变。
6.合金是指由两种或两种以上的金属元素组成的,具有金属特性的新物质。
三、选择题:1.位错是一种()。
A. 点缺陷B. 线缺陷C. 面缺陷D. 不确定2.固溶体的晶体结构()A. 与溶剂的相同B. 与溶质的相同C. 与溶剂、溶质的都不相同D. 是两组元各自结构的混合3.合金发生固溶强化的主要原因()。
A. 晶格类型发生变化B. 晶粒细化C. 晶格发生畸变D. 晶界面积发生变化4.实际生产中,金属冷却时,实际结晶温度总是()理论结晶温度。
A. 低于B. 等于C. 高于D. 不能确定5.α-Fe是具有()晶格的铁。
A. 体心立方B. 面心立方C. 密排六方D. 无规则几何形状第三章铁碳合金相图一、填空题:1.金属在态下,随温度的改变,由转变为的现象称为同素异晶转变。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属晶体练习题
1.金属键的实质是( )
A.自由电子与金属阳离子之间的相互作用 B.金属原子与金属原子间的相互作用
C.金属阳离子与阴离子的吸引力 D.自由电子与金属原子之间的相互作用
2.金属的下列性质与金属晶体结构中的自由电子无关的是( )
A.良好的导电性B.良好的导热性 C.良好的延展性 D.密度大小
3.按下列四种有关性质的叙述,可能属于金属晶体的是( )
A.金属阳离子之间存在斥力 B.金属原子半径都较大,价电子较少C.金属中大量自由电子受到外力作用时,运动速度加快
D.金属受到外力作用时,各原子层容易发生相对滑动,但不会改变原来的排列方式,也不会破坏金属键
4.关于晶体的下列说法正确的是( )
A.在晶体中只要有阳离子就一定有阴离子
B.金属镁、金刚石和固体氖都是由原子直接构成的单质晶体
C.金属晶体的熔点可能比分子晶体的低,也可能比原子晶体的高
D.铜晶体中,1个铜离子跟2个价电子间有较强的相互作用
5.金属晶体堆积密度大,原子配位数大,能充分利用空间的原因是( )
A.金属原子价电子数少 B.金属晶体中有自由电子
C.金属原子的原子半径大 D.金属键没有饱和性和方向性
6.下列金属晶体中,金属阳离子和自由电子之间的作用最强的是( )
A.Na B.Mg C.Al D.K
7.铝硅合金(含硅%)凝固时收缩率很小,因而这种合金适合于
铸造。
现有下列三种晶体:①铝;②硅;③铝硅合金。
它们的熔
点从低到高的顺序是( )
A.①②③ B.②①③ C.③②① D.③①②
8.关于体心立方堆积型晶体(如图)结构的叙述中正确的是( )
A.是密置层的一种堆积方式 B.晶胞是六棱柱
C.每个晶胞内含2个原子 D.每个晶胞内含6个原子
9.石墨晶体是层状结构,在每一层内,每一个碳原子都跟其他3个
碳原子相结合。
据图分析,石墨晶体中碳原子数与共价键数之比为
( )
A.2∶3 B.2∶1 C.1∶3 D.3∶2
10.现有5种固态物质:四氯化硅、硼、石墨、锑、氖。
将符合信息的物质名称和所属晶体类型填在表格中。
11.(2012·武汉高二质检)在常温常压下,下列物质中属于金属晶体的是( )
A.铂B.汞 C.水晶 D.金刚石
12.金属的下列性质中,不.能用金属的电子气理论加以解释的是( )
A.易导电 B.易导热 C.易腐蚀D.有延展性
13.按下列四种有关性质的叙述,可能属于金属晶体的是( )
A.由分子间作用力结合而成,熔点低
B.固体或熔融后易导电,熔点在1000 ℃左右
C.由共价键结合成网状结构,熔点高
D.固体和熔融状态不导电,但溶于水后可能导电
13.金属晶体的形成是因为晶体中存在( )①金属原子②金属阳离子③自由电子④阴离子
A.只有① B.只有③ C.②③ D.②④
14.下列不.属于金属晶体的共性的是( )
A.易导电 B.易导热 C.有延展性D.高熔点
15.下列有关金属的叙述正确的是( )
A.金属受外力作用时常常发生变形而不易折断,是由于金属离子之间有较强的作用
B.通常情况下,金属里的自由电子会发生定向移动,而形成电流
C.金属是借助金属离子的运动,把能量从温度高的部分传到温度低的部分D.金属的导电性随温度的升高而降低
16.关于铜晶体的堆积方式说法正确的是( )
A.按ABABAB…方式堆积,配位数为12 B.按ABABAB…方式堆积,配位数为8 C.简单立方堆积,配位数为6 D.按ABCABC……方式堆积,配位数为12 17.下列叙述中正确的是( )
A.有阳离子的晶体一定有阴离子 B.有阳离子的晶体一定是化合物
C.由单质组成的晶体如果固态时能导电也不一定是金属晶体
D.金属晶体都具有较高的熔点和银白色的金属光泽
18.在金属晶体中,金属原子的价电子数越多,原子半径越小,则自由电子与金属阳离子间的作用力越大,金属的熔、沸点越高。
由此判断下列各组金属熔、沸点高低顺序,其中正确的是( )
A.Mg>Al>Ca B.Al>Na>Li C.Al>Mg>Ca D.Mg>Ba>Al
19.关于下图不.正确的说法是( )
A.此种最密堆积为面心立方最密堆积 B.该种堆积方式称为铜
型
C.该种堆积方式可用符号……ABCABC……表示
D.该种堆积方式称为镁型
20.金属晶体中金属原子主要有三种
常见的堆积方式:体心立方堆积、面心立
方堆积和六方堆积,其结构单元分别如图
中甲、乙、丙所示,则甲、乙、丙三种结
构单元中,金属原子个数比为_______。
21.晶胞即晶体中最小的重复单元。
已知金晶体的晶胞是面
心立方体,即在立方体的8个顶点各有一个金原子,各个面的中
心有一个金原子,每个金原子被相邻的晶胞所共用(如图)。
金原
子的半径为d cm,用N A表示阿伏加德罗常数,M表示金的摩尔质
量。
(1)金晶体每个晶胞中含有________个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定________
_______________________________________________。
(3)一个晶胞的体积为______。
金晶体的密度为
____。
22.在1~18号元素中,部分连号元素单质的熔点
情况如图所示,试回答:
(1)c点代表的单质是__________,其熔点高的主要
原因是_________________________________。
(2)d所属的晶体类型是_____,粒子间的作用力为_______________________。
(3)上述元素形成的氢化物中能形成氢键的是____________。
(4)图中的a所代表的元素符号是________,它的氢氧化物与h点元素氢氧化物溶液反应的离子方程式是____________________________________ 22.(1)金属导电是靠________,该粒子在外加电场作用下发生定向移动形成电流,金属导电能力随温度升高而________;电解质溶液导电是靠________,电解质溶液导电能力随温度升高而________。
(2)金属晶体中金属原子的价电子数越________,原子半径越________,金属阳离子与自由电子之间的静电作用就越强,金属键就越________,因此,金属晶体的熔、沸点就越________,硬度就越________。
如Na、Mg、Al的熔点由高到低的顺序为____________________,硬度由大到小的顺序为________________。
23.(1)如图所示为二维平面晶体示意图,所表示的化学式为AX
的是________。
3
(2)已知铝为面心立方晶体,其结构如上图甲所示,面心立方的结构特征如上图乙所示。
若铝原子的半径为×10-10 m,试求铝金属晶体中的
晶胞长度,即上图丙中AB的长度为________m。
24.下图为一个金属铜的晶胞,请完成以下各题。
(1)该晶胞“实际”拥有的铜原子数是________个。
(2)该晶胞称为________。
(填序号)
A.六方晶胞B.体心立方晶胞C.面心立方晶胞
(3)此晶胞立方体的边长为a cm,Cu的相对原子质量为64,金属铜的密度为ρg/cm3,则阿伏加德罗常数为________(用a、ρ表示)。
25.现有四种金属晶体:Na、
Zn、Po、Au,下图所示为金属原子
的四种基本堆积模型。
请回答以下
问题:
(1)堆积方式的空间利用率最低的基本堆积模型是______(填编号),符合该堆积模型的金属晶体是________(填化学符号)。
(2)金属原子在二维平面里放置得到密置层和非密置层,其中非密置层的配位数是________,由非密置层互相错位堆积而成的基本堆积模型是________(填编号),符合该堆积模型的金属晶体是________(填化学符号)。
(3)按ABCABCABC……方式堆积的基本堆积模型是________(填编号),符合该堆积模型的金属晶体是________(填化学符号)。
