上海大学2018年硕士《冶金物理化学》考试大纲
上海大学2018年学术型硕士研究生初试科目及参考书目
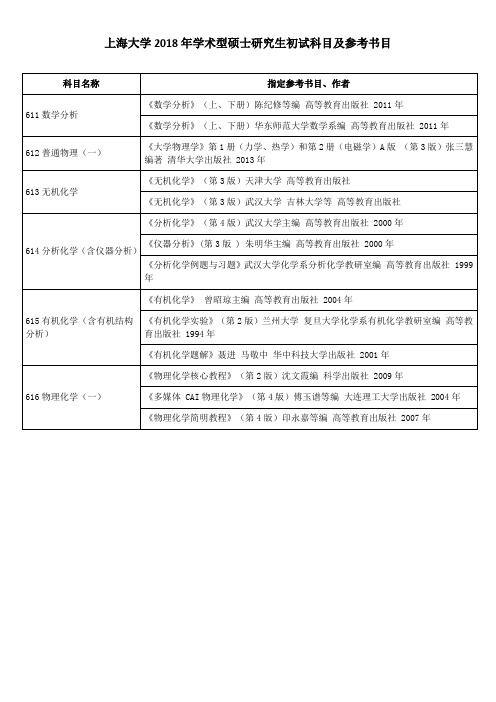
科目名称 611 数学分析 《数学分析》(上、下册)华东师范大学数学系编 高等教育出版社 2011 年 612 普通物理(一) 《大学物理学》第 1 册(力学、热学)和第 2 册(电磁学)A 版 (第 3 版)张三慧 编著 清华大学出版社 2013 年 《无机化学》(第 3 版)天津大学 高等教育出版社 613 无机化学 《无机化学》(第 3 版)武汉大学 吉林大学等 高等教育出版社 《分析化学》(第 4 版)武汉大学主编 高等教育出版社 2000 年 614 分析化学(含仪器分析) 《仪器分析》(第 3 版 ) 朱明华主编 高等教育出版社 2000 年 《分析化学例题与习题》武汉大学化学系分析化学教研室编 高等教育出版社 1999 年 《有机化学》 曾昭琼主编 高等教育出版社 2004 年 615 有机化学(含有机结构 分析) 《有机化学实验》(第 2 版)兰州大学 复旦大学化学系有机化学教研室编 高等教 育出版社 1994 年 《有机化学题解》聂进 马敬中 华中科技大学出版社 2001 年 《物理化学核心教程》(第 2 版)沈文霞编 科学出版社 2009 年 616 物理化学(一) 《多媒体 CAI 物理化学》(第 4 版)傅玉谱等编 大连理工大学出版社 2004 年 《物理化学简明教程》(第 4 版)印永嘉等编 高等教育出版社 2007 年 指定参考书目、作者 《数学分析》(上、下册)陈纪修等编 高等教育出版社 2011 年
《表征》霍尔编 徐亮 陆兴华译 商务印书馆 2003 年 《文化理论与大众文化导论》(第 5 版)斯道雷著 常江译 北京大学出版社 2010 年 《文化理论关键词》卡瓦拉罗 张卫东等译 江苏人民出版社 2006 年 《西方都市文化研究读本》薛毅(主编) 广西师范大学出版社 2008 年 《漫长的革命》雷蒙德 威廉斯 倪伟译 上海人民出版社 2012 年 618 文化研究 《知识分子论》萨义德著 单德兴译 三联书店 2005 年 《中文世界的文化研究》王晓明(编)上海书店 2012 年 《社会学的想象力》米尔斯著 李康译 北京师范大学出版社 2017 年 《关键概念:传播与文化研究辞典》费斯克著 许静译 新华出版社 2004 年 《媒体文化》凯尔纳著 丁宁译 商务印书馆 2004 年 《末日船票:日常生活中的文化分析》罗小茗 上海人民出版社 2015 年 《中国古代史》 朱绍侯等主编 福建人民出版社 《中国近代史》(第 4 版)李侃等著 中华书局 619 中国史综合 《中国现代史》王桧林主编 北京师范大学出版社 《国史纲要》 陈勇主编 上海大学出版社 620 世界史综合 《世界史》(六卷本)吴于廑 齐世荣主编 高等教育出版社 《全球化:全球治理》俞可平 社科文献出版社 2003 年 《全球化:文化冲突与共生》苏国勋等 社科文献出版社 2006 年 《全球化:西方理论前沿》杨雪冬 社科文献出版社 2002 年 《全球问题与新兴政治》 蔡拓 天津人民出版社 2011 年 《全球化背景下的宗教与政治》刘义 上海大学出版社 2011 年 621 全球学与全球化理论 《全球主义批评与当代中国意识形态建设》申小翠 光明日报出版社 2011 年 《全球学评论》(第一卷)郭长刚 商务印书馆 2012 年 《全球史评论》(第 1-6 卷)刘新成 《环境生态学导论》(第 2 版) 盛连喜主编 北京:高等教育出版社 2006 年 6 月 《总体设计》(第 1 版)【美】凯文·林奇 中国建筑工业
2018年硕士研究生招生考试大纲 .doc

2018年硕士研究生招生考试大纲009 工程学院目录初试考试大纲 1841热工学(工程热力学与传热学) 1842自动控制理论 5845水力学 8848运筹学 8915机械设计(含机械原理)10959 结构力学A 16960 结构力学B 17复试考试大纲18机械工程综合18动力工程专业综合20电子技术综合25土木工程综合考试28管理信息系统31工程水文学33理论力学34船舶结构力学35初试考试大纲841热工学(工程热力学与传热学)一、考试性质热工学(工程热力学与传热学)是动力工程专业硕士研究生入学考试的专业理论课程。
作为选拔性考试,具有较高的信度、效度、必要的区分度和适当的难度。
二、考察目标重点考核学生对工程热力学和传热学基本定律和基本原理的掌握,常用工质的热物理性质的了解,有关图表及计算公式的综合运用。
对典型热力工程和热力循环的计算和分析能力,对热量传递的工程问题的分析能力和热量传递工程计算方法。
能源合理利用及其高效转换的基本观念的掌握。
三、考试形式本考试为闭卷考试,满分为150分,考试时间为180分钟。
试卷结构:选择20%,计算题80%四、考试内容(一)基本概念1、主要内容:(1)热力系。
(2)热力状态和平衡状态。
(3)工质的状态参数。
状态方程。
热力参数坐标图。
(4)功和热量。
热力过程,可逆过程和不可逆过程。
热力循环。
2、具体要求:理解热力系、理想气体、平衡状态和可逆过程的基本概念。
掌握工质基本状态参数和热效率的计算、理想气体状态方程的应用。
了解热力系的分类和特点、工质状态参数性质。
(二)热力学第一定律1、主要内容:(1)热力学第一定律的实质。
(2)内能。
(3)热力学第一定律表达式。
(4)焓和稳定流动能量方程。
2、具体要求:了解热力学第一定律的来源和本质。
掌握热力学第一定律在不同热力系的表达方程、应用特点和工程计算方法、热与功的计算。
理解内能、焓、比热的定义和含义。
(三)气体的热力性质和热力过程1、主要内容:(1)实际气体和理想气体。
华东理工大学2018年硕士《物理化学》考试大纲_华东理工大学考研论坛

华东理工大学2018年硕士《物理化学》考试大纲1、物质的pVT关系和热性质理解pVT关系和热性质是物质的两类基本的宏观平衡性质。
掌握系统、环境、状态、平衡态、状态函数、强度性质、广延性质等基本概念,以及反映物质pVT关系的状态方程。
掌握流体的pVT状态图、pV图和压缩因子图的特点,气液相变和气液临界现象的特征,以及饱和蒸气压、沸点和临界参数的物理意义。
理解包括气液固三相的pVT状态图,掌握pT相图的特点以及三相点的意义,理解稳定平衡和亚稳平衡的区别和联系。
理解范德华方程及其对气液相变的应用。
了解什么是双节线,什么是旋节线。
理解普遍化范德华方程。
掌握pVT关系的普遍化计算方法。
理解对应状态原理。
掌握热力学第一定律。
掌握功、热、热力学能、焓等的定义和相互关系,理解<!--[if!vml]-->/_upload/article/images/88/f5/c3e126fd4b038f21d71f 6f31f991/179418c9-6a80-47a0-a968-febc43faaee1.gif<!--[endif]-->、<!--[if!vml]-->/_upload/article/images/88/f5/c3e126fd4b038f21d71f 6f31f991/4950fc51-342e-4a4a-bc92-3eecbb608fb2.gif<!--[endif]-->的适用条件和应用,及热力学标准状态的概念和意义。
掌握标准摩尔定容热容、标准摩尔定压热容、标准摩尔相变焓、标准摩尔生成焓、标准摩尔燃烧焓和标准熵的定义和应用。
了解热性质的实验测定原理和方法以及一些半经验方法。
2、热力学定律和热力学基本方程理解热力学第二定律的建立过程。
理解由热力学第二定律演绎得出的三个结论,即热力学温标、存在一个状态函数熵、以及熵增原理。
理解引入亥姆霍兹函数和吉布斯函数的意义。
2002-2015年上海大学冶金工程研究生入学考试试题845冶金物理化学

2009年攻读硕士学位研究生冶金物理化学入学考试试题答案前言:首先声明答案是我自己总结的(便于你参考),也是这份资料的核心关键,学长就是靠自己的总结的这份答案专业课考了132分(13年最后一题没做的情况下,最后一题15分),所以其重要性不言而喻,13年的试卷和09年的试卷内容基本雷同(修改了大题目的参数、增加了一个物理化学题),所以,掌握这份试卷是专业课考研的重中之重!一.名词解释(30)1.正规溶液:混合焓不为零,混合熵与理想溶液混合熵相同的溶液。
2.温度界面层:贴近相界面处,有温度梯度出现的流体薄层称之为温度界面层。
3.速度界面层:贴近相界面处,有速度梯度出现的流体薄层称之为速度界面层。
4.浓度界面层:贴近相界面处,有浓度梯度出现的流体薄层称之为浓度界面层注:界面层就是边界层5.炉渣的酸度:炉渣的酸碱度取决于炉渣组成中SiO 2与CaO 的比值,当R=W (SiO 2)%/W (CaO )%>1时,炉渣称之为酸性渣。
6.炉渣碱度:炉渣中主要碱性氧化物的溶度对主要酸性氧化物的浓度之比R=W (CaO )%/W(SiO 2)%>1时,炉渣为碱性渣。
二.简答题(50)1.理想溶液的物理意义是什么?(10)答:理想溶液是指组分i 在全部溶度范围内都服从拉乌尔定律的溶液;从分子模型上讲,组成理想溶液的组分分子的大小及作用力彼此相近,即当各组分混合成溶液时,没有热效应和体积的变化:ΔH=0,ΔV=0;而实际溶液一定的浓度区间常符合理想溶液的性质,所以引入理想溶液的概念从而对一些公式进行修正,使之应用于实际溶液。
2.正规溶液的性质有哪些?(10)答:正规溶液的性质主要有五点:(1)混合吉布斯自由能:Δmix G =X 1RTLnα1+X 2RTLnα2(2)混合熵:Δmix S =-X 1RTLnX 1-X 2RTLnX 2(3)混合焓:Δmix H =Δmix G +Δmix S=X 1RTLnα1+X 2RTLnα2-X 1RTLnX 1-X 2RTLnX 2=X 1RTLnγ1+X 2RTLnγ2(4)过剩函数:Δmix G E =Δmix Gre-Δmix Gid=X 1Δmix G 1E +X 2Δmix G 2E(5)α函数:α=Lnγ1/(X 1-X 2)23.选择作为金属热还原用的还原剂,要满足哪些要求?(10)答:(1)还原剂与被还原金属声称化合物的ΔG Θ与生成热之间要有足够大的差值,一边尽可能不由外部给热并使反应完全进行。
2018年化学考试大纲

2018年化学考试大纲D①②③④了解能源是人类生存和社会发展的重要基础。
了解化学在解决能源危机中的重要作用。
⑤了解焓变(A^O与反应热的含义。
⑥理解盖斯定律,并能运用盖斯定律进行有关反应焓变的计算。
⑦理解原电池和电解池的构成、工作原理及应用,能书写电极反应和总反应方程式。
了解常见化学电源的种类及其工作原理。
⑧了解金属发生电化学腐蚀的原因、金属腐蚀的危害以及防止金属腐蚀的措施。
(1)化学反应速率和化学平衡①了解化学反应速率的概念和定量表示方法。
能正确计算化学反应的转化率(《)。
②了解反应活化能的概念,了解催化剂的重要作用。
③了解化学反应的可逆性及化学平衡的建立。
④掌握化学平衡的特征。
了解化学平衡常数(K)的含义,能利用化学平衡常数进行相关计算。
⑤理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,能用相关理论解释其一般规律。
⑥了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。
(2)电解质溶液①了解电解质的概念。
了解强电解质和弱电解质的概念。
②理解电解质在水中的电离以及电解质溶液的导电性。
③了解水的电离、离子积常数。
④了解溶液pH的含义及其测定方法,能进行pH的简单计算。
⑤理解弱电解质在水中的电离平衡,能利用电离平衡常数进行相关计算。
⑥了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用。
⑦了解离子反应的概念、离子反应发生的条件。
掌握常见离子的检验方法。
⑧了解难溶电解质的沉淀溶解平衡。
理解溶度积(^p)的含义,能进行相关的计算。
(3)以上各部分知识的综合应用。
1.常见无机物及其应用(1)常见金属元素(如Na、Mg、Al、Fe、Cu等)①了解常见金属的活动顺序。
②了解常见金属及其重要化合物的制备方法,掌握其主要性质及其应用。
③了解合金的概念及其重要应用。
(2)常见非金属元素(如H、C、N、0、Si、S、Cl等)①了解常见非金属元素单质及其重要化合物的制备方法,掌握其主要性质及其应用。
2018年硕士研究生招生考试科目《 物理化学 》考试大纲 .doc

物理化学本科大纲要求的内容,包括热力学第一定律、热力学第二定律、相平衡、多组分系统热力学及其在溶液中的应用、化学平衡、统计热力学、电解质溶液、可逆电池的电动势及其应用、电解与极化、化学动力学、表面物理化学、胶体分散系统。
评分标准和要求
试卷有评分标准
备注
一级学科硕士点召集人签名:(学院盖章)学院分管院长签名:
试卷内容结构
基础知识内容约占50%;理解知识内容约占30%;综合知识内容约占20%
试卷难易结构
测试考生掌握物理化学的基础理论、基本知识的水平,考察考生运用基础理论和有关公式计算和解决物理化学问题的能力;试卷难易适中。
试卷题型结构
选择题,计算题,证明题及问答题。
试卷分值结构
选择题(20%),计算题(70%)及问答题(10%)。
上海大学847物理化学(二)2018年考研专业课大纲

2019年上海大学考研专业课初试大纲考试科目:847物理化学(二)一、复习要求:要求学生在掌握物理化学基本概念、知识和理论的基础上,能够运用所学公式、定律、定理、方程式求解物理化学中的若干问题。
二、主要复习内容:1.掌握热力学的基本概念,如:系统和环境、状态和状态函数、过程和途径,热力学可逆过程等;掌握热力学第一、第二和第三定律及其数学表达式;掌握系统状态变化过程中焓、熵、Gibbs自由能变化的计算和应用;熟悉热力学状态函数以及基本关系式的推导、适用条件和应用。
重点:化学反应、相变过程中焓变、熵变、Gibbs自由能变化的计算;热力学函数之间关系式的推导与证明。
2.掌握偏摩尔量和化学势的概念;掌握理想溶液和非理想溶液的概念;掌握活度及相关计算。
重点:气体、稀溶液、理想溶液、非理想溶液化学势的表示式;气体逸度、稀溶液和非理想溶液组分活度的计算。
3.熟悉相律、相平衡、自由能和相图之间的关系;了解相变的分类;掌握单元系Clausius-Clayperon方程以及二元系相图的基本类型;能够准确进行二元系相图的分析;熟悉三元系相图。
重点:单元系相图以及二元系相图的解析;简单三元系相图解析。
4.从热力学角度理解表面能、表面张力的基本概念;熟悉界面的特性和界面现象;了解物理吸附和化学吸附的特征;掌握Langmiur单分子层吸附等温式和BET多分子层吸附等温式;了解溶胶的光学、力学、热力学性质;掌握溶胶电动电势的计算。
重点:吸附等温线的工程应用;利用BET方程测定固体比表面积的原理;溶胶结构表示式;溶胶的电学性质、热力学稳定性和聚沉作用。
5.熟悉化学统计热力学中的Boltzmann假定和分布;了解统计热力学的基本概念和熵的统计概念及表达式;熟悉热力学函数与分子配分函数之间关系式的推导以及应用。
重点:热力学函数与配分函数关系式的推导。
6.掌握化学反应方向和限度的判断,以及反应的标准吉布斯自由能变化的计算;了解反应平衡常数的各种表示法;了解平衡常数的实验测定方法,以及温度、组份浓度(或其分压)对平衡常数的影响;掌握平衡混合物组成和其它因素对化学平衡影响的计算。
上海大学851金属学2018年考研专业课大纲

2019年上海大学考研专业课初试大纲考试科目:851金属学一、复习要求:要求考生熟悉金属学相关的基本概念和基本理论,并能运用这些理论来分析和阐释实际中和金属材料相关的现象。
二、主要复习内容:1.金属的微观结构:(1)金属的晶体结构:包括晶体中原子的相互作用结合方式,原子的聚集状态和排列方式,以及用极射投影分析晶体结构中晶面和晶向的相对位置。
(2)合金相结构:决定形成何种合金相的因素,固溶体的概念和分类,中间相的分类和决定因素。
重点:金属晶体的原子排列方式、晶胞原子数、配位数、致密度、间隙,固溶体和中间相的特点。
2、缺陷缺陷的形成与分类;点缺陷的平衡浓度;线缺陷位错的基本概念(类型与表征),位错的滑移与攀移、交割、增殖,位错的弹性性质,实际晶体中的位错;面缺陷(表面、晶界、相界、层错)。
重点:点缺陷的平衡浓度与温度、激活能的关系;位错的滑移与攀移运动;界面偏析与晶界的迁移。
3、固体中原子和分子的运动描述扩散现象的宏观规律(扩散第一方程、第二方程);扩散的微观理论,扩散机制,扩散系数与激活能、温度的关系;扩散驱动力的热力学分析;影响扩散的因素;反应扩散。
重点:扩散第一、第二方程及求解与应用;扩散系数与扩散激活能和温度间的关系表达式;扩散驱动力的热力学分析;影响扩散的因素。
4 材料的形变与回复、再结晶(1)金属变形的基本方式;弹性变形的特点;单晶塑性变形的进行方式(滑移、孪生、扭折)及应力与应变曲线;多晶塑性变形的主要特点、应力-应变曲线、组织和形貌。
(2)回复过程中对应的应力、组织结构的变化及其动力学过程;再结晶过程对应的形核和长大及其动力学过程;控制再结晶晶粒大小的方法。
重点:弹性变形的主要特点;多晶塑性变形发生的条件与其应力应变曲线特点;回复时间和再结晶进行的程度与激活能和温度的关系表达式;控制再结晶晶粒大小的方法。
5 单组元和二元、三元合金相图有关相图的基本知识(相、相律、相图的建立方法);使用相图的基本方法(确定相变点、杠杆法则);相平衡的热力学条件;匀晶相图、共晶相图和包晶相图的特点;三元相图的表达方式和使用方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
上海大学2018年硕士《冶金物理化学》考试大纲复习要求:
掌握冶金物理化学基本概念、基本理论及计算方法和分析问题方法,正确运用于分析和解决具体问题。
基本理论(包括溶液热力学理论,Gibbs自由能变化的计算、应用原则及活度数据的获得原理、方法,相图基本原理及典型二、三元相图基础知识,表面和界面基本理论,冶金动力学基本理论等)、冶金基本熔体(熔渣的基本物理化学性质及在冶金中的作用)、解决冶金实际问题常用的几种基本手段和方法(包括化学反应等温方程式和平衡移动原理的灵活运用;优势区图、位势图等几种热力学状态图的构成原理及使用方法等)。
二、主要复习内容:
冶金热力学基础
化学反应的标准吉布斯自由能变化及平衡常数,溶液的热力学性质-活度及活度系数,溶液的热力学关系式,活度的测定及计算方法,标准溶解吉布斯自由能及溶液中反应的吉布斯自由能计算。
重点:溶液相关基本概念及其物理意义,化学反应的吉布斯自由能计算(过剩全摩尔混合吉布斯自由能)及由此判断化学反应进行的方向,活度相关计算,金属原电池电动势与△H、△G和△S关系。
冶金动力学基础
化学反应的速率,分子扩散及对流传质,吸附化学反应的速率,反应过程动力学方程的建立,新相形成的动力学。
重点:一、二级化学反应相关计算及一级可逆化学反应速率方程推导,菲克第一、第二定律,朗格缪尔吸附等温式,双膜理论,未反应核模型。
金属熔体
熔铁及其合金的结构,铁液中组分活度的相互作用,铁液中元素的溶解及存在形式,熔铁及其合金的物理性质。
重点:合金密度等相关物性计算,活度相互作用系数及其转换关系。
冶金炉渣
二元系、三元系相图的基本知识及基本类型,三元渣系的相图,熔渣的结构理论,金属液与熔渣的电化学反应原理,熔渣的离子溶液结构模型,熔渣的活度曲线图,熔渣的化学性质,熔渣的物理性质。
重点:二、三元相图的基本性质及表示法,二、三元系平衡相的定量法则(直线法则和杠杆定律,重心法则),分析等温截面图和投影图。
炉渣酸度、碱度概念,熔渣的结构理论,金属液与熔渣的电化学反应
原理。
化合物的形成-分解、氢的燃烧反应
化合物的形成-分解反应的热力学原理,碳酸盐的分解反应,氧化物的形成-分解反应,金属(铁)氧化的动力学,可燃气体的燃烧反应,固体碳的燃烧反应,燃烧反应体系气相平衡成分的计算。
重点:平衡组成计算及判断过程进行的方向。
氧化物还原熔铁反应
氧化物还原的热力学条件,氧化物的间接还原反应,氧化物的直接还原反应,金属热还原反应,铁的渗碳及含碳量,熔渣中氧化物的还原反应,高炉冶炼的脱硫反应,铁浴熔融还原反应。
重点:氧化物还原的热力学条件,氧化物的间接还原反应,金属热还原用的还原剂,氧化物的直接还原反应,金属热还原反应,高炉冶炼的脱硫反应热力学及动力学。
氧化熔铁反应,造锍熔炼
氧化熔铁反应的物理化学原理,锰、硅、铬、钒、铌、钨的氧化反应,脱碳反应,脱磷反应,脱硫反应,吸气及脱气反应,脱氧反应,造锍熔炼。
重点:选择性氧化原理,铜的造锍熔炼,元素在渣金间的平衡分配常数,元素氧化的热力学及动力学(碳、磷、硫等元素),脱气反应热力学及动力学。
文章来源:文彦考研。
