pH(水的电离和溶液的pH)
水的电离与溶液pH关系

学生专用7月25日高二化学一、水的电离1、H2O + H2O H3O+ + OH- 简写: H2O H++ OH-2、 H2O的电离常数K电离==O)C(H)C(OH)C(H2-•+3、水的离子积25℃K W= c(H+)· c(OH-)= = 1.0×10-14。
4、影响因素:温度越高,Kw越大,水的电离度越大。
对于中性水,尽管温度升高Kw,增大,但仍是中性水,5、KW不仅适用于纯水,还适用于酸性或碱性的稀溶液,不管是哪种溶液均有:C(H+)H2O == C(OH―)H2OKW== C(H+)溶液·C(OH―)溶液6. K w揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K w不变,H+和OH-浓度大小是一种“此消彼涨”的动态关系。
二、影响水的电离平衡的因素条件K w平衡移动水的电离程度c(H+)c(OH-)c(H+)c(OH-)相对大小溶液的酸碱性升温↑→↗↗↗相等中性通HCl(g)—←↘↗↘c(H+)较大酸性加NaOH(s)—←↘↘↗c(OH-)较大碱性加NaCl(s)—————相等中性(1) K w不仅适用于水,还适用于酸性或碱性的稀溶液。
不管哪种溶液均有c(H+)H2O=c(OH-)H2O。
(2) 水溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
练习1 纯水在10℃和50℃的H+浓度,前者与后者的关系是()A.前者大B.后者C.相等大D.不能确定练习2 .水的电离过程为H2O H+ + OH-,在不同温度下其离子积为KW25℃=1×10-14, KW35℃ =2.1 ×10-14。
则下列叙述正确的是:()A、c(H+)随着温度的升高而降低B、在35℃时,纯水中 c(H+) >c(OH-)C、水的电离常数K25 ℃>K35 ℃D、水的电离是一个吸热过程练习3 0.01mol/L盐酸溶液中,c(H+)、 c(OH-)分别为多少?由水电离出的 c(H+) H2O 、c(OH-) H2O分别是多少?练习4 0.01mol/L NaOH溶液中, c(H+) 、 c(OH-)分别为多少?由水电离出的c(H+) H2O、c(OH-) H2O分别是多少?练习5、判断正误:1)任何水溶液中都存在水的电离平衡。
水的电离和溶液的酸碱性

水的电离和溶液的酸碱性◎重难点1.pH的计算2.酸碱稀释的pH的计算3.酸碱混合的pH计算4.酸碱中和滴定实验◎本节知识网络知识点1水的电离平衡水是一种极弱的电解质,它能微弱地电离,生成H3O+和OH-:H2O+H23O++OH-通常简写为:H2++OH-,水总是电离出等量的H+和OH-,从实验可知,在25℃时,1 L 纯水中只有1×10-7 mol H2O电离,即纯水中 [H+ ]=[OH-]=1×10-7mol. L-1在酸碱溶液中,+-知识点2水的电离平衡影响因素1、温度对水电离的影响水的电离是个吸热过程,故温度升高,水的离子积增大。
25℃时,K W= 1×10-14 ;100℃时,K W= 1×10-12。
(水的离子积只随温度的改变而改变)2、外加试剂对水电离的影响水的离子积是水电离平衡时的性质,它不仅适用于纯水,也适用于任何酸、碱、盐稀溶液。
即任何物质的水溶液中,25℃时,K W= c(H+)·c(OH-) =1×10-143、直接增大[H+]在H2 O ++OH-平衡中,加入(酸或强酸的酸式盐或中强酸的酸式盐),增大[H+],则平衡向左移动,α水减小,水的电离被抑制,由于水的电离平衡仍然存在,K w不变,则[OH-]必然会减小。
4、直接增大[OH-]在H2 O H+ +OH-平衡中,加入碱,增大[OH-] ,则平衡向左移动,α水减小,水的电离被抑制,由于水的电离平衡仍然存在,K w1×10-14,则[H+]必然会减小。
总结:(1)在纯水中分别加入等量的H+和OH-时,能同等程度地抑制水的电离,并使水电离出的[H+ ]和[OH-]均小于10-7mol .L-1。
(2)如果一个溶液中水的电离度小于纯水,即水的电离被抑制,表明既可以是加入酸或某些酸式盐,也可以是加入碱,则该溶液既可以显酸性也可以显碱性。
〖例1〗常温的某无色溶液中,由水的电离产生的C(H+)=1×10-12mol/l,则下列各组离子肯定能共存的是()A、Cu2+NO3-SO42-Fe3+B、Cl- S2- Na+K+C、SO32-NH4+ K+ Mg2+D、Cl- Na+ NO3- SO42-〖变式训练1〗下列说法正确的是( )A 酸溶于水后能促进水的电离,碱溶于水后能抑制水的电离。
第八章 第2讲 水的电离溶液的ph值

逆 正
正 正 逆 正
不变 不变
不变 增大 减小 不变
减小 增大
增大 增大 减小 增大
增大 增大
减小 增大 减小 增大
减小 减小
增大 增大 减小 减小
温度
其他:如加入Na
【问题引导下的再学习】
思考2:水的离子积常数Kw=c(H+)· c(OH-)中H+和 OH-一定是水电离出来的吗?
水的离子积常数Kw=c(H+)· c(OH-),其实质是水溶液中的 H+和OH-浓度的乘积,不一定是水电离出的H+和OH-浓度的 乘积,所以与其说Kw是水的离子积常数,不如说是水溶液中的 H+和OH-的离子积常数。即Kw不仅适用于水,还适用于酸性 或碱性的稀溶液。
知识梳理·题型构建
【问题引导下的再学习】
思考4:pH<7的溶液一定是酸性溶液吗?pH>7的溶 液一定是碱性溶液吗?pH=7的溶液一定是中性吗?
答案 不一定。上述说法只有在常温下才能满足。如在某温 度下,水的离子积常数为1×10-12,此时pH=6的溶液为中 性溶液,pH>6时为碱性溶液,pH<6时为酸性溶液。
思考3:在pH=2的盐酸溶液中由水电离出来的c(H+) 与c(OH-)之间的关系是什么?
【当堂检测】
求算下列溶液中H2O电离的c(H+)和c(OH-)。 (1)pH=2的H2SO4溶液 c(H+)=_____________,c(OH-)=____________。 10-2 mol· -1 L 10-12 mol· -1 L 10-12 mol· -1 L c(H+)水=c(OH-)水=______________。 (2)pH=10的NaOH溶液 10-10 mol· -1 L c(H+)=_____________,c(OH-)=_____________。 10-4 mol· -1 L c(H+)水=c(OH-)水=________________。 10-10 mol· -1 L (3)pH=2的NH4Cl溶液c(H+)=_________________。 10-2 mol· -1 L c(H+)水=__________________。 10-2 mol· -1 L (4)pH=10的Na2CO3溶液c(OH-)=______________。 10-4 mol· -1 L c(OH-)水=__________________。 10-4 mol· -1 L
化学课件《水的电离和溶液pH值》优秀ppt 人教课标版

(2)找准条件对水的电离平衡的影 响及H+和OH-的来源
(3)以水的电离生成的 C(H+)=C(OH-)为辅
内容提要
例题
总结
习题
解题思路
知识归纳
知识归纳:
1.常温时,某溶液中由水电离产生的C(H+) >1×10-7 mol/l 时,溶液是 能水解的盐(可能是强酸弱碱盐或 强碱弱酸盐等)
2.常温时,某溶液中由水电离产生C(H+)<1×10-7 mol/l 时,溶液是 能抑制水的电离的物质(可能是 酸或碱或其他特殊的物质,如NaHSO4等)
强酸强碱盐
4、温度
内容提要
内容提要
例题
总结
习题
二、影响水的电离平衡的因素
1、酸 2、碱
抑制水的电离,KW保持不变
3、盐
强酸弱碱盐 强碱弱酸盐 促进水的电离,KW保持不变
强酸强碱盐 不影响水的电离,KW保持不变 4、温度 升高温度促进水的电离,KW增大
注意:KW是一个温度函数,只随温度的升高而增大
酸 碱 强酸弱碱盐 强碱弱酸盐 强酸强碱盐 温度
(3)所以答案选D
返回
内容提要
例题
总结
习题
习 题1
习 题2
习 题3
习 题4
习 题5
2、常温时,在PH=8的CH3COONa 和NaOH两种溶液中,设由水电离产生的
C(OH-)分别为Amol/l与Bmol/l,则A和
B的关系为( C)
A、A< B
B、A=10-2B
C、B=10-2A D、A=B
返回
内容提要
94.对一个适度工作的人而言,快乐来自于工作,有如花朵结果前拥有彩色的花瓣。――[约翰·拉斯金] 95.没有比时间更容易浪费的,同时没有比时间更珍贵的了,因为没有时间我们几乎无法做任何事。――[威廉·班] 96.人生真正的欢欣,就是在于你自认正在为一个伟大目标运用自己;而不是源于独自发光.自私渺小的忧烦躯壳,只知抱怨世界无法带给你快乐。――[萧伯纳]
水的电离平衡与PH计算
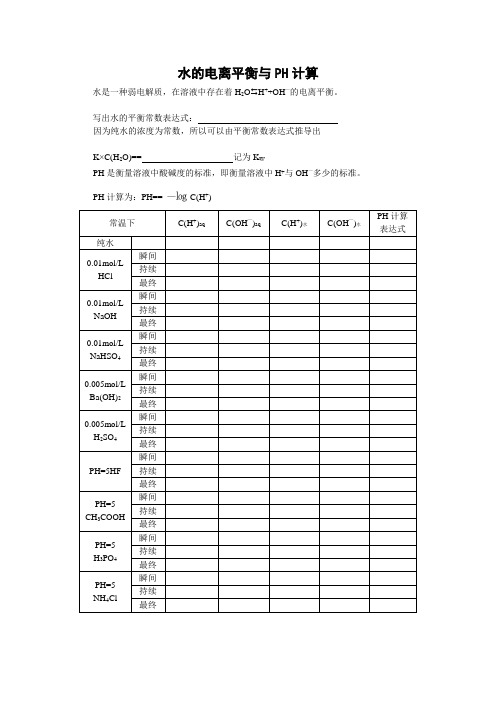
1:9混合
0.1mol/LHCl与0.01mol/LHCl
9:1混合
0.1mol/LNaOH与0.01mol/LNaOH等体积混合
0.1mol/LNaOH与0.01mol/LNaOH
1:9混合
0.1mol/LNaOH与0.01mol/LNaOH
9:1混合
C(OH—)aq
C(H+)水
C(OH—)水
PH计算表达式
纯水
0.01mol/L
HCl
瞬间
持续
最终
0.01mol/L
NaOH
瞬间
持续
最终
0.01mol/L
NaHSO4
瞬间
持续
最终
0.005mol/L
Ba(OH)2
瞬间
持续
最终
0.005mol/L
H2SO4
瞬间
持续
最终
PH=5HF
瞬间
持续
最终
PH=5
CH3COOH
瞬间
持续
最终
PH=9
NaHS
瞬间
持续
最终
PH=5
NaHSO3
瞬间
持续
最终
PH=9
Na2HPO4
瞬间
持续
最终
PH=5
NaH2PO4
瞬间
持续
最终
由上表可以得出的结论:
①;
②;
③;
混合溶液PH计算
常温
C(H+)aq
C(OH—)aq
C(H+)水
C(OH—)水
PH计算表达式
0.1mol/LHCl与0.01mol/LHCl等体积混合
水的电离及溶液的pH
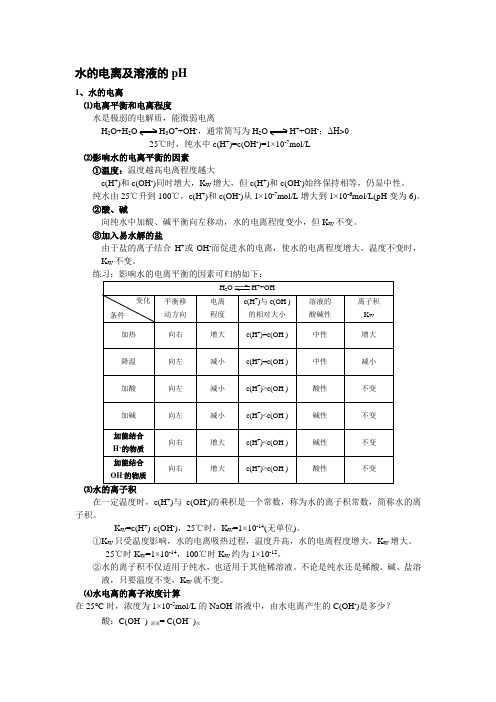
水的电离及溶液的pH1、水的电离⑴电离平衡和电离程度 水是极弱的电解质,能微弱电离H 2O+H 2O H 3O ++OH -,通常简写为H 2O H ++OH -;ΔH >025℃时,纯水中c(H +)=c(OH -)=1×10-7mol/L⑵影响水的电离平衡的因素①温度:温度越高电离程度越大c(H +)和c(OH -)同时增大,K W 增大,但c(H +)和c(OH -)始终保持相等,仍显中性。
纯水由25℃升到100℃,c(H +)和c(OH -)从1×10-7mol/L 增大到1×10-6mol/L(pH 变为6)。
②酸、碱向纯水中加酸、碱平衡向左移动,水的电离程度变小,但K W 不变。
③加入易水解的盐由于盐的离子结合H +或OH -而促进水的电离,使水的电离程度增大。
温度不变时,K W 不变。
练习:影响水的电离平衡的因素可归纳如下:H 2O H ++OH -平衡移 动方向 电离 程度 c(H +)与c(OH -)的相对大小 溶液的 酸碱性 离子积 K W 加热向右增大c(H +)=c(OH -) 中性 增大 降温 向左 减小c(H +)=c(OH -) 中性 减小 加酸 向左 减小c(H +)>c(OH -) 酸性不变加碱 向左 减小 c(H +)<c(OH -) 碱性 不变 加能结合 H +的物质 向右 增大c(H +)<c(OH -) 碱性 不变 加能结合 OH -的物质向右 增大c(H +)>c(OH -)酸性不变⑶水的离子积在一定温度时,c(H +)与c(OH -)的乘积是一个常数,称为水的离子积常数,简称水的离子积。
K W =c(H +)·c(OH -),25℃时,K W =1×10-14(无单位)。
①K W 只受温度影响,水的电离吸热过程,温度升高,水的电离程度增大,K W 增大。
25℃时K W =1×10-14,100℃时K W 约为1×10-12。
第6讲 水的电离和溶液pH计算
第6讲 水的电离和溶液pH 计算一、水的电离与水的离子积1.水的电离与水的离子积在纯水或水溶液中 H2O H ++OH — △H>02H2O H 3O ++OH — △H>025℃ c(H +)=c(OH -) =1×10-7mol/L c(H +)∙c(OH -)=1×10-14=Kw100℃ c(H +)=c(OH -) =1×10-6mol/L c(H +)∙c(OH -)=1×10-12=Kw说明:(1)Kw 只与温度有关,温度越高Kw 越大。
因水的电离是吸热过程,升高温度Kw 将增大,100℃时,c(H +)=c(OH -)=1×10-6mol/L ,Kw=c(H +)∙c(OH -)=1×10-12。
(2)Kw 不仅适用于纯水,也适用于酸,碱,盐的稀溶液。
酸性溶液: [H +]H2O +[H +]酸 OH —[]H2O =Kw碱性溶液:H2O =Kw [OH —]H2O +[OH —]碱 H +[](3)纯水中水的电离度αH2O %=181000107-×100%=1.8×10-7%。
(4)任何水溶液中,水所电离而生成的c(H +)H2O =c(OH —)H2O2.影响水的电离平衡的因素(1)温度:温度升高,水的电离度增大,水的电离平衡向电离方向移动,离子浓度增大。
(2)酸、碱:在纯水中加入酸或碱,抑制H 2O 的电离,均使水的电离平衡左移,此时若温度不变,Kw 不变,αH2O 变小;c(H +)发生改变,pH 也随之改变;若向水中加入酸,则c(H +)增大,c(OH —)变小,pH 变小(3)其他因素:Zn Na 2CO 3 NH 4Cl二、溶液的酸碱性和pH 值1.溶液的酸碱性(1)中性溶液: c(H +)=c(OH -)(2)酸性溶液:c(H +)溶液>c(OH -)溶液以0.1mol/L HCl 为例,由于酸电离出H +能使H2O H ++OH -平衡向左移动,即抑制了水的电离,溶液中H +由两部分组成,一部分为酸提供,另一部分为H 2O 提供,水电离提供的c(H +)远小于酸提供的c(H +),故可忽略,溶液中H +全部看作酸提供,故c(H +)溶液=0.1mol/L ,但溶液中OH -全部为H 2O 电离产生,c(OH -)溶液=c(OH -)O H 2,水电离产生 c(H +)和c(OH -)始终相等,因此有c(OH -)溶液 = c(OH -)O H 2 =c(H +)O H 2=L mol /1.010114-⨯=1×10-13,H 2O 的电离度αO H 2%=18100010113-⨯×100%=1.8×10-13%,酸溶液中水的电离度比纯水中水的电离度小。
有关水的电离及溶液的pH计算专题讲析
的 混合
数 很大 时 , 要 考虑水 电离 出的c ( H ) 或c ( O H 一 ) , 1 .若 两 者 p H< 7 , 两 强 酸 溶 液 混合 , 应 以 但 所得 溶液 的p H 总是 趋 近于7 ( 即强 碱稍 大于 溶液中主要存在的离子H + 为标准计算。 7 , 强 酸稍小 于7 ) 。 2 . 若两者p H > 7 , 两强碱溶液混合 , 应以 例3 p H= 1 2 的N a O H溶 液 加 水稀 溶 液 中主要存 在 的离子 O H 一 为标 准计算 。 3 .若 一 者p H < 7 , 另 一者 p H> 7 , 应 考 虑 酸 释到 原 来的 1 0 倍, 求稀释 后溶 液 的p H。 簿 碱 之 间的反应 。 r 。 解 析 N a O H 溶 液 中主 要存 在 O H一 , 荸 举 例1 p H= 1 0 与p H= 1 2 的 两种 强 碱 应 以主要存 在 的离子 O H 一 为 标准计 算 。 由于溶
化学 解题方略i
有 水 的 电离 溶液 的 p H计 算专 题 讲 析
口 付 小勤
水 的电离及 溶液 的p H 计算 ,是 历年 来各 省 市 高考 的热 点 和重 点 , 也 是 考 生在 高考 中 的容 易失 分 点 。笔 者根据 二十 多 年来 的高 三 教 学实践 和 探索 ,对 这类 知识 和题 型 的解 法
—
;
r 一
黼 ∞ 参 蓦
i
化学 ・ 奄 } 题方略
因为 n ( n ) 增大, n ( C H , C 0 0 H) 减小 , 则 c ( H + l ) c ( } r ) n ( } r ) 1 .稀 释促 进 弱 酸 或弱 碱 的电离 , 电 离 出 C ( C H3 C O O H )C ( C H 3 C 0 0 H ) V n ( C H 3 C 0 0 H) 的离 子 的物 质 的量增 大 ,分 子 的物质 的量减 专题三 : 弱酸溶 液或 弱碱溶液 的稀释
水的电离与溶液的酸碱性
水的电离与溶液的酸碱性水是生命之源,无论是在地球上还是在人体内,水都扮演着至关重要的角色。
然而,水并不是一个单纯的物质,它具有一定的电离性,从而使得水成为了一种溶剂,能够溶解许多物质。
同时,水的电离也与溶液的酸碱性息息相关。
水的电离是指水分子在一定条件下发生自身分解的过程,产生氢离子(H+)和氢氧根离子(OH-)。
这个过程可以用化学方程式表示为:H2O ⇌ H+ + OH-。
在纯净水中,水的电离程度非常低,只有极少数的水分子发生电离。
这是因为水分子是由一个氧原子和两个氢原子组成的,氧原子带有负电荷,而氢原子带有正电荷,因此水分子是一个极性分子。
这种极性使得水分子能够相互吸引,并形成氢键,从而稳定了水分子的结构。
当溶质溶解到水中时,它们与水分子发生相互作用,导致水的电离程度发生改变。
溶质可以是酸、碱或其他化合物。
酸是一种能够释放氢离子的物质,而碱是一种能够释放氢氧根离子的物质。
当酸溶解到水中时,它会释放出氢离子,增加了水中的H+浓度,使得水的电离程度增加。
相反,当碱溶解到水中时,它会释放出氢氧根离子,增加了水中的OH-浓度,同样也使得水的电离程度增加。
这种改变水的电离程度的能力被称为酸碱性。
溶液的酸碱性可以通过pH值来描述。
pH值是一个反映溶液酸碱性强弱的指标,其数值范围从0到14。
pH值小于7的溶液被称为酸性溶液,pH值大于7的溶液被称为碱性溶液,而pH值等于7的溶液被称为中性溶液。
pH值的计算公式为:pH= -log[H+],其中[H+]表示溶液中的氢离子浓度。
由于pH值是对数尺度,所以每个单位的pH值之间相差10倍。
溶液的酸碱性不仅仅与溶质的性质有关,还与溶液中的浓度有关。
当酸或碱的浓度增加时,溶液的酸碱性也会增强。
这是因为溶液中的酸碱物质的数量增加,增加了水的电离程度。
同样地,当酸或碱的浓度减少时,溶液的酸碱性也会减弱。
溶液的酸碱性对生命体系有着重要的影响。
在人体内,许多生物过程都需要在特定的酸碱环境下进行。
水的电离与溶液的pH 同步习题 高二上学期化学人教版(2019)选择性必修1
水的电离与溶液的pH一、水的电离1.关于水的电离平衡:H2O⇌H++OH﹣,下列说法正确的是()A.通入HCl,溶液的pH增大B.加入少量NaOH固体,将促进水的电离C.温度升高,c(OH﹣)增大D.加入少量FeCl3固体,将抑制水的电离2.某温度时,水的离子积常数为1.0×10-12,则纯水中的c(H+)为()A. 1.0×10–12mol•L–1B. 5.0×10–6 mol•L–1C. 1.0×10–6 mol•L–1D. 无法确定3.常温下,0.1mol·L-1的NaOH溶液中由水电离出的OH-的物质的量浓度为()A.0.1mol·L-1B.1.0×10-13mol·L-1C.1.0×10 -7mol·L-1D.无法确定4.下列关于水的离子积常数的叙述中,正确的是()A.因为水的离子积常数的表达式是K w=c(H+)•c(OH﹣),所以K w随溶液中c(H+)和c(OH﹣)的变化而变化B.纯水的K w=1×10﹣14C.水的离子积常数仅仅是温度的函数,随着温度的变化而变化D.100℃时c(H+)•c(OH+)=1×10﹣145.下列说法错误的是()A.水的离子积常数K w不仅适用于纯水,也适用于稀的酸、碱、盐溶液B.强酸与强碱形成的盐,其水溶液不一定呈中性C.电离常数大的酸溶液中c(H+)一定比电离常数小的酸溶液中的c(H+)大D.多元弱酸的各级电离常数逐级减小6.40℃时水的离子积K w=2.9×10﹣14,则在40℃时,c(H+)=1.0×10﹣6mol/L的溶液()A.呈中性B.呈碱性C.呈酸性D.无法判断7.已知水的电离方程式:H2O H++OH-,下列叙述正确的是()A.将水加热,水的电离平衡向右移动,c ( H + )增大B.向水中加入少量氢氧化钠,水的电离平衡向左移动,溶液中c(H +) 减小C.向水中加入少量硫酸,溶液中c(H +)增大,Kw增大D.向水中加入少量金属钠,溶液中c (OH-)降低8.已知水的电离达到平衡:H 2O H++ OH-,下列叙述正确的是()A. 25℃和100℃时,由水电离的c ( H+ )相等B. 向水中通入少量HCl,水的电离平衡向左移动,c (OH-)增大C. 向水中加入少量Ba(OH)2固体,水的电离平衡向右移动,c (H + )增大D. 向水中加入少量硫酸氢钠固体,溶液中的c (OH-) < c ( H + )9.下列离子:①Ba2+②F﹣③Al3+④S2﹣⑤K+⑥OH﹣⑦CH3COO﹣⑧SO42﹣,对水的电离平衡不产生影响的是()A.①③④B.②④⑦C.②⑥⑦D.①⑤⑧10.常温下,下列四种溶液中,由水电离产生的氢离子浓度之比(①:②:③:④)是()①1mol/L的盐酸②pH=1的醋酸溶液③pH=4的NH4Cl溶液④pH=10的Na2CO3溶液A.1:1:1010:1010B.1:10:1010:1010C.1:10:104:104D.14:13:1:111.某温度下,纯水中的c(H +)=5.0×10﹣7mol/L,则此时c(OH ﹣)=mol/L.相同条件下,测得①NaHCO3(aq)②CH3COONa(aq)③NaClO(aq)三种稀溶液的pH值相同.它们的物质的量浓度由大到小的顺序是.二、溶液的pH12.如表是人体内一些体液的正常pH值范围,下列有关说法正确的是()体液尿液胃液血浆胰液pH 4.7~8.40.9~1.57.35~7.457.5~8.0 A.人体的尿液一定呈酸性B.人体的胰液一定呈碱性C.人体的胃液能使紫色石蕊溶液变蓝色D.pH试纸可精确测得以上体液的pH13.物质的量浓度相同的下列溶液,pH由大到小排列正确的是()A.Ba(OH)2、Na2CO3、FeCl3、KClB.NaOH、Na2CO3、KNO3、NH4ClC.NH3•H2O、HCl、Na2SO4、H2SO4D.NaHCO3、醋酸、NaCl、HCl14.下列有关实验说法正确的是()A.利用精密pH试纸可较准确地测量饱和氯水的pHB.氧化还原滴定中用到高锰酸钾标准溶液,应盛装于酸式滴定管中C.润洗滴定管的方法是加入3~5mL溶液,倾斜转动润湿内壁后,从滴定管上口倒出溶液D.配制Fe(NO3)2溶液时,为抑制Fe2+的水解,应将Fe(NO3)2固体溶于浓HNO3,再稀释至所需浓度15.用pH试纸测定某无色溶液的pH,正确的是()A.用广泛pH试纸测得该溶液的pH为3.2B.用pH试纸蘸取溶液,观察其颜色变化并与标准比色卡对照C.用干燥、洁净的玻璃棒蘸取溶液,滴在pH试纸上,观察其颜色变化并与标准比色卡对照D.用干燥、洁净的玻璃棒蘸取溶液,滴在湿润的pH试纸上,所测得的pH一定偏小15.在常温下,取浓度相同的NaOH和HCl溶液,以3:2的体积比相混合(体积变化忽略不计),所得溶液的pH等于13,则原溶液的浓度为()A.0.01mol•L﹣1B.0.05mol•L﹣1C.0.017mol•L﹣1D.0.50mol•L﹣116.25℃时,下列说法中错误的是()A.pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=12.7(已知lg2=0.3)B.pH=3的HCl与pH=11的氨水等体积混合,溶液中的c(OH﹣)>c(H+)C.0.1mol/L的HCl与0.2mol/L的NH3•H2O等体积混合,溶液中2c(H+)+c(NH3•H2O)=c(NH4+)+2c(OH﹣)D.将10mL pH=a盐酸与100mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=1317.室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是()A.0.1mol•L﹣1的盐酸和0.1mol•L﹣1的氢氧化钠溶液B.0.1mol•L﹣1的盐酸和0.05mol•L﹣1的氢氧化钡溶液C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液D.pH=4的盐酸和pH=10的氨水18.下列选项中的数值前者一定小于后者的是()A.常温下向两份10mL 0.1mol/L的盐酸中分别加入10mL水和10mL 0.1mol/L的NaOH溶液所得混合液pHB.常温下,pH=2的醋酸和pH=12的Ba(OH)2溶液中水的离子积K wC.相同温度下,等浓度的NH4Cl溶液和氨水的导电能力D.相同条件下,等质量的固态硫与气态硫完全燃烧的焓变(△H)19.表示溶液酸碱性的方法,除常用的pH外,还有pOH和AG(酸度)等。
