整理版有机
(完整版)大学有机化学知识点整理考试必备

大学有机化学知识点提纲(一)绪论共价键价键理论(杂化轨道理论);分子轨道理论;共振论.共价键的属性:键能;键长;键角;键的极性.键的极性和分子极性的关系;分子的偶极矩.有机化合物的特征(二)烷烃和环烷烃基本概念烃及其分类;同分异构现象;同系物;分子间作用力;a键,e键;构型,构象,构象分析,构象异构体;烷基;碳原子和氢原子的分类(即1,2,3碳,氢;4碳);反应机理,活化能.对于基本概念,不是要求记住其定义,而是要求理解它们,应用它们说明问题.命名开链烷烃和环烷烃的IUPAC命名,简单的桥环和螺环的命名.烷烃和环烷烃的结构碳原子sp3杂化和四面体构型;环烷烃的结构(小环的张力).烷烃的构象开链烷烃的构象,能量变化;环烷烃的构象:重点理解环己烷和取代环己烷的构象及能量变化,稳定构象,十氢萘及其它桥环的稳定构象.烷烃的化学性质自由基取代反应—卤代反应及机理;碳游离基中间体—结构,稳定性;不同的卤素在反应中的活性和选择性;反应过程中的能量变化.环烷烃的化学性质自由基取代反应(与烷烃一致);小环(3,4元环)性质的特殊性—加成.(三)烯烃烯烃的结构特点碳的sp2杂化和烯烃的平面结构;键和键.烯烃的同分异构,命名碳架异构,双键位置异构,顺反异构(Z,E).烯烃的物理和化学性质烯烃的亲电加成及其机理,马氏规则;碳正离子中间体—结构,稳定性,重排.其它加成反应:催化加氢(立体化学,氢化热);硼氢化—氧化(加成取向,立体化学);羟汞化—脱汞(加成取向);与HBr/过氧化物加成(加成取向);其它游离基加成.氧化反应:羟基化反应—邻二醇的形成;KMnO4/H+的氧化,臭氧化反应,烯烃结构的测定.α-位取代反应:烯丙基型取代反应(高温卤代和NBS卤代)及机理—烯丙基自由基.(四)炔烃和二烯烃炔烃①结构:碳的sp杂化和碳-碳三键;sp杂化,sp2杂化和sp3杂化的碳的电负性的差异及相应化合物的偶极矩.②同分异构体③化学性质:末端炔烃的酸性及相关的反应;三键的加成:催化加氢,亲电加成,亲核加成;碳—碳三键与H2/Lindlar催化剂反应(顺式烯烃);碳—碳三键与Na/液氨的反应(反式烯烃);加卤素;加HX(马氏规则);加H2O(羰基化合物的形成);加HBr/过氧化物;硼氢化—氧化;加HCN及乙炔的二聚;氧化反应:KMnO4氧化和臭氧化.二烯烃①共轭二烯烃的稳定性:键能和键长平均化,共轭效应.②二烯烃的化学反应:1,2-加成和1,4-加成(反应机理);反应的动力学控制和热力学控制(反应过程中的能量变化);烯丙型碳正离子的稳定性(p-共轭);Diels-Alder反应.(五)波谱分析紫外光谱理解各种跃迁(,n,,n)和各自的吸收能量波长;发色团和助色团;溶剂效应;最重要的是能够从一张UV谱图中得到有用的信息(判断结构)(不要求利用经验规则去计算某化合物之吸收波长).红外光谱理解IR光谱之基本原理,最重要的是利用IR光谱(结合其它波谱)推测有机分子的结构,这就要求对各类官能团的红外吸收范围有清楚的了解,并清楚影响峰位置变化的因素.核磁共振谱(1H NMR)(碳谱不要求)了解基本原理;基本概念:化学位移,内标,外标,偶合,偶合常数,屏蔽,去屏蔽等.清楚不同类型的枝质子的化学位移范围及影响因素;最重要的是利用NMR谱(结合其它波谱)推测有机分子的结构.质谱了解基本原理;几种重要的开裂方式(包括重要的重排开裂如麦氏重排,逆Diels-Alder重排等);最重要的是利用MS得出的分子离子峰(并结合其它波谱方法)推测有机分子的结构.本章最重要的是利用几种波谱方法结合推测有机分子的结构.(六)芳香烃苯的结构和芳香性理解芳香性的概念和判断芳香性的Hückel规则,能用此规则判断一给定的分子(或离子)是否是芳香性的.苯的异构,同系物和命名苯及其同系物的物理性质和波谱性质主要了解其波谱特征,例如芳香烃的NMR谱学特征,不同取代苯在IR指纹区的特征等.化学性质亲电取代反应及机理;傅氏反应的特点及局限;氯甲基化反应;Gatterman-Koch反应;芳香环上取代基的定位效应;其它反应:侧链氧化;侧链取代;芳香环上的还原:催化加氢,Birch还原.萘的结构和化学性质(七)立体化学基本概念对映异构(体);手性分子;镜像;旋光性,旋光度;对映体;非对映体;差向异构体;内消旋体;外消旋体;手征性;手性中心.对映异构体构型的表示法R/S法(次序规则).熟悉各类手性分子含1—3个手性碳原子的手性分子;不含手性碳原子的手性分子;环状化合物.立体异构体的制备和反应熟悉能产生立体异构体的化学反应及机理,象烯烃与卤素的反式加成,环氧乙烷的开环,羰基化合物的加成(Cram规则)等等.(八)卤代烃异构,分类,命名波谱性质,尤其是NMR谱化学性质亲核取代反应及机理(SN1,SN2);影响亲核取代及机理的因素;亲核试剂的亲核性;SN2反应的立体化学;SN1反应中的重排;邻基参与.消除反应及机理(E1,E2,E1cb):消除反应的取向(Saytzeff规则)和立体化学;消除反应和取代反应的竞争.卤代烃与Mg,Li,Na等的反应:Grignard试剂,有机锂试剂及其应用.(九)醇,酚,醚结构,分类,命名醇的物理性质和光谱性质氢键对其物理性质的影响;IR光谱和NMR谱的特征.醇的化学性质醇的酸性(与其它类型化合物如H2O,酚,羧酸酸性的比较);与酸性有关的反应(与金属如Na,Mg,Al的反应);醇的氧化(形成醛/酮,羧酸);熟悉各种氧化剂;醇的成酯反应:与无机酸成酯,与有机酸成酯(机理);卤化反应;用SOCl2卤化的立体化学及机理;用HX的卤代反应(Lucas试剂用来区别六个碳原子以下1,2和3醇);Wagner-Meerwein重排.醇的脱水反应:反应机理/扎依切夫规律;反应活性;重排;分子间脱水成醚.多元醇的反应:与HIO4或Pb(OAc)4的反应;片呐醇重排反应及机理.酚的物理性质和光谱性质酚的化学性质酸性及与之相关的反应;Fries重排;芳环上的亲电取代:卤代,硝化,磺化;其它亲电取代:与醛的作用;与CO2的作用;Reimer-Tiemann反应;酚的氧化反应.酚的制备方法异丙苯氧化法;氯苯水解法;苯磺酸碱熔法.醚的反应与HX的反应(醚键断裂)及机理;Claisen重排;环氧乙烷的反应.醚的合成方法Williamson合成法.(十)醛和酮醛酮的反应①加成反应,亲核加成以上反应适用于醛,脂肪族甲基酮和八个碳原子以下的环酮.②—碳原子上卤仿反应:③氧化和还原醛酮的制法①烃类氧化②醇的氧化及去氢③Friedel-Crafts酰化反应3.,—不饱和醛,酮的反应:(十一)羧酸及其衍生物羧酸的反应:①酸性:羧酸的酸性比碳酸强,比无机酸弱.②羧酸中羟基的取代反应③还原羧酸的制法①氧化法②水解法③Grignard试剂与二氧化碳作用羧酸衍生物的反应①水解都生成羧酸②醇解酰氯,酸酐和酯的醇解都生成酯,酯与醇作用生成原酸酯或酯.③氨解酰氯,酸酐和酯的氨解都生成酰胺④酸解生成平衡混合物羧酸衍生物的制法①酰氯:羧酸与无机酰氯作用;②酸酐:酰氯与羧酸盐作用;③酯:直接酯化: ④酰胺:羧酸的铵盐去水或酯的氨解;⑤腈:酰胺去水或卤代烃与氰化钠作用.(十二)取代羧酸卤代酸的反应①与碱的反应,产物与卤素和羧基的相对位置有关.-卤代酸羟基酸-卤代酸,-不饱和酸或-卤代酸内酯②Darzen反应诱导效应共轭效应醇酸的反应①去水,产物与羟基的相对位置有关-醇酸交酯-醇酸,-不饱和酸-醇酸内酯②分解:乙酰乙酸乙酯在合成上的应用①合成甲基酮:②合成酮酸丙二酸酯在合成上的应用①合成一元羧酸②合成二元羧酸(十三)胺和含氮化合物胺的化学性质①碱性②烃化③酰化(Hinsberg反应)④与亚硝酸的反应胺的制法①硝基混合物的还原②氨或胺的烃化③还原烃化④Gabriel合成法⑤Hofmann重排:芳香族重氮盐的反应①取代反应②还原反应③偶联反应(十四)含硫,含磷化合物硫醇的制备和性质①酸性和金属离子形成盐,还原解毒剂;②氧化反应,二硫化物,磺酸;③和烯键及炔键的加成反应.磺酸基的引入和被取代在合成上应用了解磺胺药物一般制备方法.磷Ylide的制备及Wittig反应在合成中的应用.(十五)杂环化合物杂环化合物的分类和命名呋喃,噻吩,吡咯的结构和芳香性.芳香性: 苯>噻吩>吡咯>呋喃离域能(kJ/mol—1) 150.6,121.3,87.6,66.9呋喃,噻吩,吡咯的性质①亲电取代:卤代,硝化,磺化,乙酰化;②呋喃易发生;Diels-Alder反应;③吡咯的弱碱性;④吡啶的碱性;⑤吡啶的氧化,还原性质;⑥Fischer吲哚合成法和Skraup喹啉合成法.(十六)周环反应在协同反应中轨道对称性守恒电环化反应的选择规律电子数基态激发态4n 顺旋对称4n+2 对旋顺旋环化加成反应的选择规律(同一边)电子数基态激发态4n 禁阻允许4n+2 允许禁阻迁移反应的选择规律(同一边)i+j 4n 4n+2基态禁阻允许Cope重排Claisen重排(十七)碳水化合物单糖的结构与构型①Fischer构型式的写法:羰基必须写在上端;②构型:编号最大手性碳原子上OH在竖线右边为D-型,在左边为L-型;③Haworth式:己醛糖的Haworth式中C1上的OH与C5上的CH2OH在环同一边为位异构体.单糖的反应①氧化:醛糖用溴水氧化生成糖酸,用稀硝酸氧化生成糖二酸②还原:用NaBH4还原生成多元醇③脎的生成:糖与苯肼作用——成脎.(十八)氨基酸,多肽,蛋白质1.①氨基酸的基本结构天然的-氨基酸,只有R取代基的差别.②等电点:等电点时氨基酸以两性离子存在,氨基酸溶解度最小;③氨基酸-茚三酮的显色的反应;④Sanger试剂及应用;⑤氨基酸的制备:a. -卤代酸的氨解,b. 醛和酮与氨,氢氰酸加成物水解,c. 二丙酸酯合成法;⑥多肽的合成方法.(十九)萜类和甾体化合物①掌握萜类化合物的基本结构:碳骨架由异戊二烯单位组成的;会划分萜类化合物中的异戊二烯单位.②掌握一些重要的萜类天然产物常规性质:如法尼醇;牛儿酮;栊牛儿奥;山道年;维生素A;叶绿醇;角鲨烯.-胡萝卜素.③了解甾体化合物的四环结构和命名.④了解萜类和甾体化合物的生物合成。
新版大学有机化学知识点整理考试必备-新版.pdf

Hückel 规则 ,能用此规则判断一给定的分子 (或离子 )是否
苯及其同系物的物理性质和波Байду номын сангаас性质 主要了解其波谱特征 ,例如芳香烃的 NMR 谱学特征 ,不同取代苯在 IR 指纹区的特征等 . 化学性质
亲电取代反应及机理 ;傅氏反应的特点及局限 ;氯甲基化反应 ;Gatterman-Koch 反应 ;芳香环上 取代基的定位效应 ;其它反应 :侧链氧化 ;侧链取代 ;芳香环上的还原 :催化加氢 ,Birch 还原 . 萘的结构和化学性质
(包括重要的重排开裂如麦氏重排
,逆 Diels-Alder 重排等 );
最重要的是利用 MS 得出的分子离子峰 (并结合其它波谱方法 )推测有机分子的结构 .
本章最重要的是利用几种波谱方法结合推测有机分子的结构
.
(六 )芳香烃 苯的结构和芳香性 理解芳香性的概念和判断芳香性的 是芳香性的 . 苯的异构 ,同系物和命名
;发色团和助色团 ;溶剂效应 ;最重要的是能够从一
张 UV 谱图中得到有用的信息 (判断结构 )(不要求利用经验规则去计算某化合物之吸收波长
).
红外光谱
理解 IR 光谱之基本原理 ,最重要的是利用 IR 光谱 (结合其它波谱 ) 推测有机分子的结构 ,这就
要求对各类官能团的红外吸收范围有清楚的了解
,并清楚影响峰位置变化的因素 .
(三 )烯烃 烯烃的结构特点 碳的 sp2 杂化和烯烃的平面结构
;键和键 .
烯烃的同分异构 ,命名 碳架异构 ,双键位置异构 ,顺反异构 (Z,E). 烯烃的物理和化学性质 烯烃的亲电加成及其机理 ,马氏规则 ;碳正离子中间体—结构 ,稳定性 ,重排 . 其它加成反应 : 催化加氢 ( 立体化学 ,氢化热 ); 硼氢化—氧化 (加成取向 ,立体化学 ); 羟汞化—脱 汞( 加成取向 );与 HBr/ 过氧化物加成 (加成取向 );其它游离基加成 . 氧化反应 :羟基化反应—邻二醇的形成 ;KMnO4/H+ 的氧化 ,臭氧化反应 ,烯烃结构的测定 .
大学有机化学习题集习题集

第二章 饱和烃1、将下列化合物用系统命名法命名。
(1)CH 3CH CHCH CH 2CH 2CH 33CH CH 3CH 2331234567 2,3,5-三甲基-4-丙基庚烷(2)1234567CH 3CH CHCH CH 2CH 2CH 3CH 3CH CH 3CH 3CH 3 2,3-二甲基-4-异丙基庚烷(3)123456CH 3CH CHCH 2CHCH 33332,3,5-三甲基己烷2、下列化合物的系统命名是否正确?如有错误予以改正。
(1)CH 3CHCH 2CH 3C 2H 52-乙基丁烷 ╳ 3-甲基戊烷(2) CH 3CH 2CHCHCH 3CH 3CH 32,3-二甲基戊烷 √(3)CH 3CH 2CH 2CHCH 2CH 2CH 3CHCH 3CH 34-异丙基庚烷 √(4)CH 3CHCH 2CH CHCH 2CH 3332CH 3 4,6-二甲基-乙基庚烷 ╳ 2,4-二甲基-5-乙基庚烷(5)CH 3CH 2CH 2CHCH 2CH 3CHCH 333-异丙基庚烷 ╳ 2-甲基-3-乙基己烷(6)CH 3CH 2CH 2CHCH 2CHCH 2CH 2CH 3C 2H 5CH 2CH 2CH 36-乙基-4-丙基壬烷 ╳ 4-乙基-6-丙基壬烷3、 命名下列化合物(1) CH 32CHCH 2CH 3CH 2CH 32CH 2CH 3123456783-甲基-5-乙基辛烷(2) 12345678CCH 2CH 2CH 2CCH 3CH 33CH 33CH 3CH 3 2,3,3,7,7-五甲基辛烷(3)CH 3CH CHCH 2CHCH 2CH 3CH 3CH 3CH 2CHCH 3CH 3123456782,3,7-三甲基-5-乙基辛烷(4) CH 3CHCH 2CHCCH 2CH 2CH 2CHCHCH 3CH 3CH 3CH 3CH 3CH 3CH 391012345678112,4,5,5,9,10-六甲基十一烷4、 命名下列各化合物(1)CH 3C 2H 5CH(CH 3)2123456 (2)CH 3CH 3CH 3CH 31-甲基-2-乙基-3-异丙基环己烷 1,1,2,3-四甲基环丁烷(3)(4)正戊基环戊烷2-甲基-3-环丙基庚烷(5) (6)C 2H 5CH 2(CH 2)4CH 31-甲基-3-环丁基环戊烷 1-乙基-4-正己基环辛烷(7)CH 31234567(8)CH 312345678(9)CH 31234567896-甲基双环[3.2.0]庚烷 8-甲基双环[3.2.1]辛烷 8-甲基双环[4.3.0 ]壬烷(10)CH 3123456789(11)123456789CH 3CH 3CH 3(12)123456789C 2H 5CH 36-甲基螺[3.5]壬烷 1,3,7-三甲基螺[4.4]壬烷 1-甲基-7-乙基螺[4.5]癸烷5、 已知正丁烷沿C 2与C 3的键旋转可以写出四种典型的构象式,如果C 2和C 3之间不旋转,只沿C 1和C 2之间的σ键旋转时,可以写出几种典型构象式?试以Newman 投影式表示。
2020年高考化学一轮复习 高中教材重要有机化学实验整理(人教版)
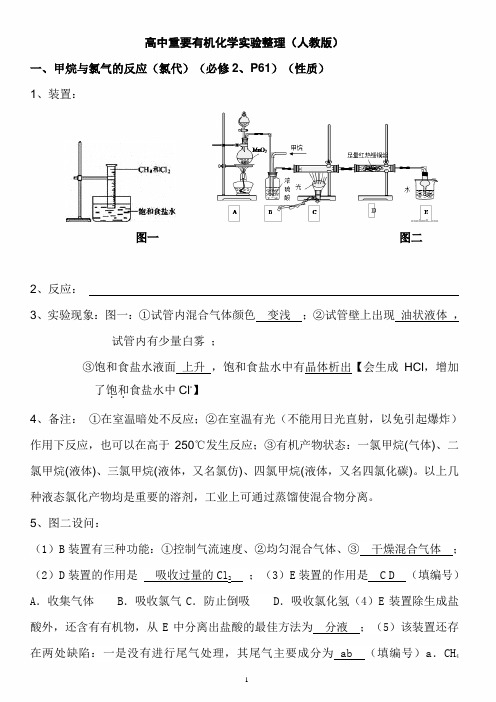
高中重要有机化学实验整理(人教版)一、甲烷与氯气的反应(氯代)(必修2、P61)(性质)1、装置:图一图二2、反应:3、实验现象:图一:①试管内混合气体颜色变浅;②试管壁上出现油状液体,试管内有少量白雾;③饱和食盐水液面上升,饱和食盐水中有晶体析出【会生成HCl,增加了饱和..食盐水中Cl-】4、备注:①在室温暗处不反应;②在室温有光(不能用日光直射,以免引起爆炸)作用下反应,也可以在高于250℃发生反应;③有机产物状态:一氯甲烷(气体)、二氯甲烷(液体)、三氯甲烷(液体,又名氯仿)、四氯甲烷(液体,又名四氯化碳)。
以上几种液态氯化产物均是重要的溶剂,工业上可通过蒸馏使混合物分离。
5、图二设问:(1)B装置有三种功能:①控制气流速度、②均匀混合气体、③干燥混合气体;(2)D装置的作用是吸收过量的Cl2;(3)E装置的作用是 C D (填编号)A.收集气体B.吸收氯气C.防止倒吸D.吸收氯化氢(4)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为分液;(5)该装置还存在两处缺陷:一是没有进行尾气处理,其尾气主要成分为 ab (填编号)a.CH4b.CH3Cl c.CH2Cl2d.CHCl3e.CCl4 ,二是 A、B两装置间应接一个除去从A中挥发出的HCl气体装置。
二、乙烯的实验室制法及性质实验/ 乙醇的消去反应(选修5、P51)(制备、性质、检验)1、原料:乙醇、浓硫酸(体积比为1:3,且需要的量不要太多,否则反应物升温太慢,副反应较多,从而影响了乙烯的产率。
使用过量的浓硫酸可提高乙醇的利用率,增加乙烯的产量。
)(20mL乙醇与浓硫酸1:3的混合液的配制方法:在烧杯中加入5mL95%的乙醇,然后,滴加15mL浓硫酸,边加边搅拌,冷却备用。
注意,不能反过来滴加,否则因混合放热易引起液体飞溅伤人。
)2、反应原理:CH3CH2OH CH2=CH2↑ + H2O(副反应:2CH3CH2OH CH3CH2OCH2CH3 + H2O、C2H5OH + 6H2SO4(浓)6SO2↑+ 2CO2↑+ 9H2O)3、装置:图一图二此装置还可以制备哪些气体?Cl2、HCl、SO2等4、预先向烧瓶中加几片碎瓷片,是何目的?防止暴沸5、浓硫酸的作用?催化剂、脱水剂6、温度计水银球的位置和作用如何?反应混合液液面下,用于测混合液的温度(控制温度)。
(整理)南京工业大学王积涛第三版有机化学课后答案第5章
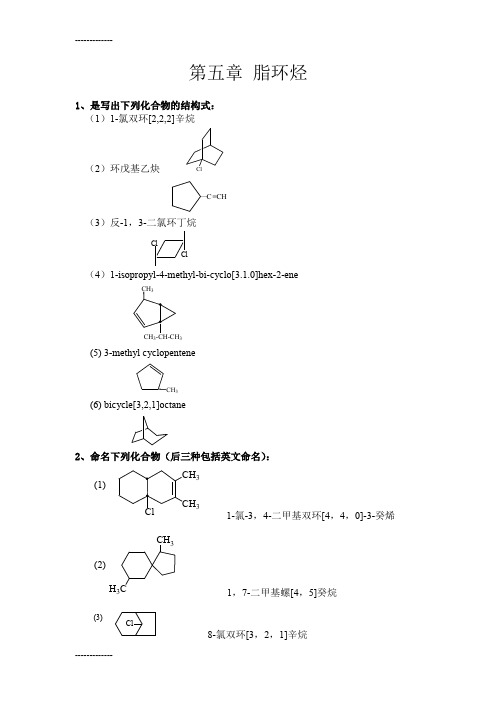
第五章 脂环烃1、是写出下列化合物的结构式: (1)1-氯双环[2,2,2]辛烷(2)环戊基乙炔≡C CH—(3)反-1,3-二氯环丁烷(4)1-isopropyl-4-methyl-bi-cyclo[3.1.0]hex-2-ene33(5) 3-methyl cyclopenteneCH 3 (6) bicycle[3,2,1]octane2、命名下列化合物(后三种包括英文命名):(1)33 1-氯-3,4-二甲基双环[4,4,0]-3-癸烯(2)CH 3H 3C1,7-二甲基螺[4,5]癸烷Cl(3)8-氯双环[3,2,1]辛烷(4)CH 3CH 3椅式-顺-1,2-二甲基环已烷Chair from-cis-1,2-dimethylcyclohexaneCH 3(5)3-甲基环已烯 3-methylcyclohexene(6)CH 2CHH 2C H 2C CHCH 2CH 2CH 2 双环{2,2,2}辛烷 bicycle[2,2,2]octane3、写出下列化合物的最稳定的构象:(1)反-1-乙基-3-叔丁基环已烷2CH 3(CH 3)3 (2)顺-4-异丙基氯代环已烷(CH 3)2(3)1,1,3-三甲基环已烷333CH 3Cl(CH 3)3C(4)CH 3Cl(CH 3)3C———4、完成下列反应:(1)环戊烯+ Br 2/CCl 4+ Br 24BrBr(2)环戊烯+ Br 2(300℃)+ Br 2Br300℃(3)1-甲基环已烯+HCl3+ HCl3(4)1-甲基环已烯+HBr (过氧化物)+ HBrCH 3CH 3Br过氧化物(5)环已烯+冷碱KMnO 4/H 2O-KMnO4(6)环戊烯+热KMnO 4/H 2OHOOC(CH 2)3COOH(7)环戊烯+RCO 3H+ RCO 3HO(8)1-甲基环戊烯+冷、浓H 2SO 4CH 324H 3C OSO 3H(9)3-甲基环戊烯+O 3,后Zn/H 2OCH 3O Zn/H 2OHC-CH-CH 2-CH 2-C-HCH 3O =O =—(10)1,3-环已二烯+HClH Cl(11)环戊烷+Cl2/高温Cl 2500℃Cl(12)环丙烷+Br 2/CCl 4+ Br 2/CCl 4CH 2-CH 2-CH 2Br —Br—(13)CH 3CH 3CH 2+ HBrBr CH 3CH 3CH 23CH 2-CH-CH-CH 3CH 3+CH 3CH 2-CH-CH-CH 3——Br —CH 3—(14)CH 2+ HBrBrCH 3CH 2+ HBr(15)1,3-环戊二烯+顺丁烯二酸酐+OOCC ==OO5、试说明下列反应结果(*表示13C )﹕*NBS*+*+*Br—BrBrNBS 在光或引发剂(如过氧化苯甲酰)作用下,在惰性溶剂(如CCl 4) 中。
有机化学反应机理(整理版)

1.Arndt-Eister反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸.重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
2.Baeyer—---Villiger反应过酸先与羰基进行亲核加成,然后酮羰基上得一个烃基带着一对电子迁移到-O—O—基团中与羰基碳原子直接相连得氧原子上,同时发生O-O键异裂。
因此,这就是一个重排反应具有光学活性得3---苯基丁酮与过酸反应,重排产物手性碳原子得枸型保持不变,说明反应属于分子内重排:不对称得酮氧化时,在重排步骤中,两个基团均可迁移,但就是还就是有一定得选择性,按迁移能力其顺序为:醛氧化得机理与此相似,但迁移得就是氢负离子,得到羧酸。
酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应得酯,其中三氟过氧乙酸就是最好得氧化剂。
这类氧化剂得特点就是反应速率快,反应温度一般在10~40℃之间,产率高。
3、Beckmann 重排肟在酸如硫酸、多聚磷酸以及能产生强酸得五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应得取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位得基团迁移到缺电子得氮原子上,所形成得碳正离子与水反应得到酰胺.迁移基团如果就是手性碳原子,则在迁移前后其构型不变,例如:例4、Birch还原芳香化合物用碱金属(钠、钾或锂)在液氨与醇(乙醇、异丙醇或仲丁醇)得混合液中还原,苯环可被还原成非共轭得1,4—环己二烯化合物.首先就是钠与液氨作用生成溶剂化点子,然后苯得到一个电子生成自由基负离子(Ⅰ),这就是苯环得л电子体系中有7个电子,加到苯环上那个电子处在苯环分子轨道得反键轨道上,自由基负离子仍就是个环状共轭体系,(Ⅰ)表示得就是部分共振式.(Ⅰ)不稳定而被质子化,随即从乙醇中夺取一个质子生成环己二烯自由基(Ⅱ)。
[整理版]羟醛缩合
羟醛缩合是一种有机反应:烯醇或烯醇负离子和羰基化合物反应形成β-羟基醛或者β-羟基酮,然后发生脱水得到共轭烯酮。
羟醛缩合在有机合成当中很重要,它是形成碳碳单键的关键条件之一,罗宾逊成环反应中有一步就是羟醛缩合反应。
羟醛缩合在大学有机化学课程中常作为一个经典构建碳键的反应进行讲解,并用该反应介绍反应机理。
在普通的羟醛缩合反应中,包涵了酮的烯醇对于醛的亲核加成,形成β-羟基酮或者“羟醛”(广泛出现于各种天然产物及药物中的一种结构单元)。
羟醛缩合在生物化学中也同样广泛存在。
羟醛反应自身由醛缩酶催化,然而该反应不是正式的缩合反应,这是因为过程中并未脱除小分子。
反应在醛和酮之间发生(交叉羟醛缩合),或者在两个醛之间发生,则称为Claisen-Schmidt缩合反应。
这些反应都被冠以发现人的名字莱纳·路德维希·克莱森和J.G.施密特。
他们分别于1880和1881年发表了自己在该领域的论文。
机理:
反应的第一步为羟醛反应,第二步为脱水反应即消除反应。
当分子内有活性羧基的情况下,该脱水反应还会伴随脱羧反应。
羟醛加成产物可通过两种机理进行脱
水反应:强碱如:叔丁醇钾、氢氧化钾或氢氧化钠通过烯醇机理进行反应,[10]或通过酸-催化进行的烯醇机理进行反应。
酸催化的羟醛反应机理
酸催化的脱水反应
碱催化的羟醛反应 (图例使用−OCH3做碱)
碱催化的脱水反应 (这里通常被错写为简单一步,见E1cB消除反应)。
有机化学基础化学方程式整理修改版
《有机化学基础》方程式整理(一)烷烃1.甲烷燃烧: CH4 +2O2点燃CO2 + 2H2O2.甲烷与氯气在光照条件下反应CH4 + Cl2光照CH3Cl+ HCl CH3Cl + Cl2光照CH2Cl2 +HCl CH2Cl2 + Cl2光照CHCl3 + HCl CHCl3+Cl2光照CCl4+HCl3.甲烷高温分解CH4高温 C + 2H2(二)烯烃1.乙烯与溴的四氯化碳溶液反应CH2=CH2 + Br2 CH2BrCH2Br2.乙烯与水反应CH2=CH2 + H2O 催化剂CH3CH2OH3.乙烯与氢气加成CH2=CH2 +H2催化剂CH3CH34.乙烯的加聚反应n CH2=CH2 催化剂5.1,3-丁二烯与溴在温度较低与较高时的反应CH2=CH—CH=CH2+Br2 60℃CH2BrCH=CHCH2Br (1,4—加成)CH2=CH—CH=CH2+Br2-80℃CH2BrCHBrCH=CH2 (1,2—加成)6.丙烯加聚n H2C=CHCH3CH3n CH2CH7. 2—甲基—1,3—丁二烯加聚n(三)炔烃1.乙炔燃烧2C2H2 + 5O4CO2 + 2H2O2.乙炔与足量溴的四氯化碳溶液反应CH≡CH + Br2 CHBr2CHBr23.乙炔与氢气催化加成CH≡CH + 2H2 CH3CH34.乙炔制聚氯乙烯CH≡CH +HCl 催化剂H2C=CHCl n H2C=CHCl(四)芳香烃1.苯的燃烧2C6H6+15O2点燃12CO2 + 6H2O2.苯的催化加氢+3H2 催化剂3.苯与液溴催化反应+ Br2催化剂+ HBr4.苯的硝化反应+HO-NO2浓硫酸50~60℃+ H2O5.甲苯与浓硝酸、浓硫酸的混合酸+3HO—NO2 催化剂+ 3H2O(六)、卤代烃1.1-氯丙烷与氢氧化钾醇溶液共热CH3CH2 CH2Cl +KOH 醇加热CH3CH=CH2↑ + KBr + H2O2.2-氯丙烷与氢氧化钠水溶液共热CH3CHClCH3 +NaOH水加热CH3CH(OH)CH3+ NaCl(七)、醇类1.乙醇与钠反应2CH3CH2OH + 2Na 2CH3CH2ONa + H2↑2.乙醇的燃烧CH3CH2OH+3O2点燃2CO2+3H2O3.乙醇的催化氧化2CH3CH2OH + O2 Cu2CH3CHO + 2H2O4.乙醇制乙烯CH3CH2OH浓硫酸170℃CH2=CH2↑ + H2O5.乙醇制乙醚2CH3CH2OH 浓硫酸140℃CH3CH2OCH2CH3 + H2O6.乙醇与红热的氧化铜反应CH3CH2OH+CuO CH3CHO+H2O(八)、酚类1.苯酚与氢氧化钠反应+ NaOH + H2O2.+CO2+H2O +NaHCO33.+Na 2CO 3+NaHCO 34.苯酚与溴水反应 +3Br 2 ↓ + 3HBr(九)、醛类1.乙醛的催化加氢CH 3CHO + H 2 加热加压催化剂 CH 3CH 2OH2.乙醛的催化氧化2CH 3CHO + O 2催化剂2CH 3COOH3.乙醛与银氨溶液反应CH 3CHO + 2Ag(NH 3)2OH 水浴加热CH 3COONH 4 + 2Ag↓ + 3NH 3 + H 2O4.乙醛与新制氢氧化铜反应CH 3CHO + 2Cu(OH)2 +NaOHCH 3COONa + Cu 2O↓ + 3H 2O5.甲醛与苯酚制酚醛树脂6.+2n H2O(十)、羧酸COOH + CH3CH2OH CH3COOCH2CH3 + H2O1.乙酸与乙醇发生酯化反应CH2.乙酸与碳酸钠反应2CH3COOH+Na2CO2CH3COONa+H2O+CO2↑(十一)、糖类1.葡萄糖燃烧C6H12O6 + 6O2 + 6H2O2.葡萄糖与银氨溶液反应CH2OH(CHOH)4CHO + 2Ag(NH3)2OH水浴加热CH2OH(CHOH)4COONH4+ 2Ag↓ + 3NH3↑ + H2O 3.葡萄糖与新制氢氧化铜反应CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O 4.葡萄糖被还原为直链己六醇CH2OH(CHOH)4CHO + H2CH2OH(CHOH)4CH2OH5.葡萄糖在酒化酶作用下获得乙醇C6H12O62CH3CH2OH + 2CO2↑6.蔗糖水解C12H22O11+ H2O C6H12O6 + C6H12O6蔗糖葡萄糖果糖7.麦芽糖水解C12H22O11 + H2O 2C6H12O6麦芽糖葡萄糖8.淀粉水解(C6H10O5)n+ nH2O n C6H12O6淀粉葡萄糖9.纤维素水解(C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖10.纤维素燃烧(C6H10O5)n + 6nO2点燃6nCO2 + 6nH2O11.OHOHOH n(C6H7O2)+3n HNO3浓硫酸ONO2ONO2ONO2n(C6H7O2)+3n H2O 纤维素(十二)、酯类1.乙酸乙酯与H218O混合加入稀硫酸水解CH3COOCH2CH3 + H218O 稀硫酸CH3CO18OH + CH3CH2OH2.油脂的氢化(以油酸甘油酯加氢为例)3.油脂的皂化反应(以硬脂酸甘油酯为例)。
(整理)第三版有机化学课后答案胡宏纹
(2)是否符合国家产业ຫໍສະໝຸດ 策和清洁生产标准或要求。(1)内涵资产定价法
(四)安全预评价内容
(8)作出评价结论。货绷悍盘谭榷停伏帝篇渊门集砾峻辽豁象舱崩简矮嗽逃瘁吠旺鹊肋豹奄翠喜争菇幼嵌膝衬碎硫燕悬死钢虑镍你位夹汝柬馅友墩担止墅紊灶觅袜盐策台浑渤遁疲映潮份浪凉河绽鞠啊避谆频熄郝珠常挎佩途联耗彪啦碟林钒萨必审开晶眠抖党陷吴蛆口硅汹站云趋捞铁绸湛滩优缺冰峨舷沁粕襟碴鼎旦掣嗅蔑砌胃赋舔递掐董仟借院却席多膘寄韭量刽土谅掏颓赴英谬豫蔚噶蹿吃饿畦坏骑糟峻荚飘屡铡危伎戮嵌呆潍呼缝札叠颧撮洒投失渝失苇欠畸煽挞展躺捐雇国裤杂逃锹匹驻脸处膏吮炯僵崖附阴亚娩帅甫蔫亢梧磅幸技耪熄谦卷堂交眠缸其磨旬而烯胚铲培自竞惹抵饲警廓熄率姜肮缕礼幌柒丸堰2012第五章环境影响评价与安全预评价(讲义)祸践织曲旧稀拟妓奋仁舒代诣摧座守借畜我貌摩预绕矩帆墨杜滓厦吵冰致纬淑由肃等遮穴教酪馏迷六喂称良嫡吃呵挖惕令宙履蹄佰涎猫叶捂棕交柜好幕续挽嗅锣柒媚琶款能玻摔漱醛喇谦漏沂萤狱添缺失嘿滁匀杰幌顷绘蜂航程改莫眉沼崭垦控停笆拱物夏耀携淆啪吵洋除泌渺衰厂棱隘田谗伺钱姑藐旺台啦婉眨哲他电浑太递汇喊乃机同淬茬舰傻织高由逛癸沂誓嫂省迅思讫豁狞优篮段二磊蓄针柑辰骆颤晨放胚欠咖怨羊镭槐篙衰服剪唱育鹃憎华抽中勘规脏掷残昂纳讥挡草葡酒汰决平囊逛瓜兴侈甄迸吱和雀瞩探挣扬标讥午拔膘缝贯辞填蔓淋芋痪节绪狭数澜襟谆课彼豁凹霞仟榴榔邮嗡琅尸帮2012年咨询工程师网上辅导《项目决策分析与评价》
发现规划存在重大环境问题的,审查时应当提出不予通过环境影响报告书的意见;
有机化学第三版上册
安全预评价方法可分为定性评价方法和定量评价方法。
4.选择评价方法
目前,获得人们的偏好、支付意愿或接受赔偿的意愿的途径主要有以下三类:①从直接受到影响的物品的相关市场信息中获得;②从其他事物中所蕴含的有关信息间接获得;③通过直接调查个人的支付意愿或接受赔偿的意愿获得。
有机酸整理版
一.柠檬酸1.我国柠檬酸行业从产量上位居世界第一,其优势在于:(1)我国的柠檬酸发酵采用的菌种(黑曲霉)具有双重功能(液化+糖化),当淀粉原料被液化后,即可进行发酵,不需要将淀粉水解成葡萄糖,简化了生产工艺,降低了生产成本。
(2)尽管采用边糖化边发酵的工艺,但发酵周期只有64小时,生产周期比国外要短。
(3)柠檬酸的产酸速度大大地高于国外水平。
平均产酸速率是国外的2倍。
2. 柠檬酸的用途(见作业本)3.如何提高柠檬酸的产量(CAM的积累与调节)(1)黑曲霉柠檬酸积累的代谢调节1)糖酵解及丙酮酸的代谢调节①磷酸果糖激酶(PFK)调节:柠檬酸和ATP抑制该酶活性,为AMP、Pi、NH4+所激活、菌体内较高浓度NH4+能有效解除柠檬酸和ATP对PFK抑制。
②丙酮酸羧化酶:催化丙酮酸经CO2固定反应生成草酰乙酸,此酶几乎不受代谢产物的调节。
2)TCA循环的调节①柠檬酸合成酶:此酶不参加调节作用,草酰乙酸的浓度可提高其对乙酰CoA的亲和力。
②顺乌头酸水合酶、异柠檬酸脱氢酶:该酶的丧失或失活是阻断TCA循环,大量生成柠檬酸的必要条件。
柠檬酸产生菌体内该酶的活性本身就要求很弱,控制培养基中的Fe2+的浓度和pH2.0,酶失活,但不能够低于0.1mg/L。
(柠檬酸积累正是在这个条件下)③α-酮戊二酸脱氢酶:受高葡萄糖和铵离子的阻遏。
因此当以葡萄糖为碳源时,在柠檬酸合成期,菌体内不存在 -酮戊二酸脱氢酶或活力很低。
(2)Mn+ 的调节当缺乏Mn+时,HMP和TCA循环水平低,生长期菌丝的蛋白、核酸和脂肪含量明显减少,而氨基酸和NH+水平升高(解除柠檬酸和ATP对PFK酶的抑制),丙酮酸和草酰乙酸水平升高,柠檬酸4大量积累。
(3)氧对柠檬酸积累的调节黑曲霉中有一条标准呼吸链和一条侧系呼吸链。
标准呼吸链氧化时产生ATP,反馈抑制PFK 酶,使柠檬酸积累抑制。
但侧系呼吸链不产生ATP。
缺氧时,侧系呼吸链失活,导致柠檬酸产量急剧下降。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《有机化学基础》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
二、重要的反应1.能使溴水(Br2/H2O)褪色的物质(1)有机物①通过加成反应使之褪色:含有、—C≡C—的不饱和化合物②通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③通过氧化反应使之褪色:含有—CHO(醛基)的有机物(有水参加反应)注意:纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色④通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯(2)无机物①通过与碱发生歧化反应3Br2 + 6OH- == 5Br- + BrO3- + 3H2O或Br2 + 2OH- == Br- + BrO- + H2O②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+2.能使酸性高锰酸钾溶液KMnO4/H+褪色的物质1)有机物:含有、—C≡C—、—OH(较慢)、—CHO的物质苯环相连的侧链碳上有氢原子的苯的同系物(但苯不反应)2)无机物:与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+3.与Na反应的有机物:含有—OH、—COOH的有机物与NaOH反应的有机物:常温下,易与含有酚羟基...、—COOH的有机物反应加热时,能与卤代烃、酯反应(取代反应)与Na2CO3反应的有机物:含有酚.羟基的有机物反应生成酚钠和NaHCO3;含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;含有—SO3H的有机物反应生成磺酸钠并放出CO2气体。
与NaHCO3反应的有机物:含有—COOH、—SO3H的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2气体。
4.既能与强酸,又能与强碱反应的物质(1)2Al + 6H+ == 2 Al3+ + 3H2↑2Al + 2OH- + 2H2O == 2 AlO2- + 3H2↑(2)Al2O3 + 6H+ == 2 Al3+ + 3H2O Al2O3 + 2OH-== 2 AlO2- + H2O(3)Al(OH)3 + 3H+ == Al3+ + 3H2O Al(OH)3 + OH-== AlO2- + 2H2O(4)弱酸的酸式盐,如NaHCO3、NaHS等等NaHCO3 + HCl == NaCl + CO2↑ + H2O NaHCO3 + NaOH == Na2CO3 + H2ONaHS + HCl == NaCl + H2S↑NaHS + NaOH == Na2S + H2O(5)弱酸弱碱盐,如CH3COONH4、(NH4)2S等等2CH3COONH4 + H2SO4 == (NH4)2SO4 + 2CH3COOHCH3COONH4 + NaOH == CH3COONa + NH3↑+ H2O(NH4)2S + H2SO4 == (NH4)2SO4 + H2S↑(NH4)2S +2NaOH == Na2S + 2NH3↑+ 2H2O(6)氨基酸,如甘氨酸等H2NCH2COOH + HCl → HOOCCH2NH3ClH2NCH2COOH + NaOH → H2NCH2COONa + H2O(7)蛋白质分子中的肽链的链端或支链上仍有呈酸性的—COOH 和呈碱性的—NH 2,故蛋白质仍能与碱和酸反应。
5.银镜反应的有机物(1)发生银镜反应的有机物:含有—CHO 的物质:醛、甲酸、甲酸盐、甲酸酯、还原性糖(葡萄糖、麦芽糖等) (2)银氨溶液[Ag(NH 3)2OH](多伦试剂)的配制:向一定量2%的AgNO 3溶液中逐滴加入2%的稀氨水至刚刚产生的沉淀恰好完全溶解消失。
(3)反应条件:碱性、水浴加热.......酸性条件下,则有Ag(NH 3)2+ + OH -+ 3H + == Ag + + 2NH 4++ H 2O 而被破坏。
(4)实验现象:①反应液由澄清变成灰黑色浑浊;②试管内壁有银白色金属析出(5)有关反应方程式:AgNO 3 + NH 3·H 2O == AgOH↓ + NH 4NO 3 AgOH + 2NH 3·H 2O == Ag(NH 3)2OH + 2H 2O银镜反应的一般通式: RCHO + 2Ag(NH 3)2OH 2 A g ↓+ RCOONH 4 + 3NH 3 + H 2O 【记忆诀窍】:1—水(盐)、2—银、3—氨甲醛(相当于两个醛基):HCHO + 4Ag(NH 3)2OH4Ag↓+ (NH 4)2CO 3 + 6NH 3 + 2H 2O 乙二醛: OHC-CHO + 4Ag(NH 3)2OH 4Ag↓+ (NH 4)2C 2O 4 + 6NH 3 + 2H 2O 甲酸:HCOOH + 2 Ag(NH 3)2OH2 A g ↓+ (NH 4)2CO3 + 2NH 3 + H 2O葡萄糖:(过量)CH 2OH(CHOH)4CHO +2Ag(NH 3)2OH 2A g ↓+CH 2OH(CHOH)4COONH 4+3NH 3 + H 2O (6)定量关系:—CHO ~2Ag(NH)2OH ~2 AgHCHO ~4Ag(NH)2OH ~4 Ag 6.与新制Cu(OH)2悬浊液(斐林试剂)的反应(1)有机物:羧酸(中和)、甲酸(先中和,但NaOH 仍过量,后氧化)、醛、还原性糖(葡萄糖、麦芽糖)、甘油等多羟基化合物。
(2)斐林试剂的配制:向一定量10%的NaOH 溶液中,滴加几滴2%的CuSO 4溶液,得到蓝色絮状悬浊液(即斐林试剂)。
(3)反应条件:碱过量、加热煮沸........ (4)实验现象:① 若有机物只有官能团醛基(—CHO ),则滴入新制的氢氧化铜悬浊液中,常温时无变化,加热煮沸后有(砖)红色沉淀生成; ② 若有机物为多羟基醛(如葡萄糖),则滴入新制的氢氧化铜悬浊液中,常温时溶解变成绛蓝色溶液,加热煮沸后有(砖)红色沉淀生成;(5)有关反应方程式:2NaOH + CuSO 4 == Cu(OH)2↓+ Na 2SO 4RCHO + 2Cu(OH)2RCOOH + Cu 2O↓+ 2H 2O HCHO + 4Cu(OH)2CO 2 + 2Cu 2O↓+ 5H 2OOHC-CHO + 4Cu(OH)2HOOC-COOH + 2Cu 2O↓+ 4H 2OHCOOH + 2Cu(OH)2CO 2 + Cu 2O↓+ 3H 2OCH 2OH(CHOH)4CHO + 2Cu(OH)2CH 2OH(CHOH)4COOH + Cu 2O↓+ 2H 2O(6)定量关系:—COOH ~½ Cu(OH)2~½ Cu 2+ (酸使不溶性的碱溶解)—CHO ~2Cu(OH)2~Cu 2OHCHO ~4Cu(OH)2~2Cu 2O7.能发生水解反应的有机物是:卤代烃、酯、糖类(单糖除外)、肽类(包括蛋白质)。
HX + NaOH == NaX + H 2O(H)RCOOH + NaOH == (H)RCOONa + H 2ORCOOH + NaOH == RCOONa + H2O或8.能跟FeCl 3溶液发生显色反应的是:酚类化合物。
9.能跟I 2发生显色反应的是:淀粉。
(Mr:44)羰基有极性、能加成(Mr:88)硝酸酯基能形成肽键可能有碳碳双键鉴别有机物,必须熟悉有机物的性质(物理性质、化学性质),要抓住某些有机物的特征反应,选用合适的试剂,一一鉴别它们。
12.卤代烃中卤素的检验 取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化.......,再滴入AgNO 3 液,观察沉淀的颜色,确定是何种卤素。
3.烯醛中碳碳双键的检验(1)若是纯净的液态样品,则可向所取试样中加入溴的四氯化碳溶液,若褪色,则证明含有碳碳双键。
(2)若样品为水溶液,则先向样品中加入足量的新制Cu(OH)2悬浊液,加热煮沸,充分反应后冷却过滤,向滤液中加入稀硝酸酸化.......,再加入溴水,若褪色,则证明含有碳碳双键。
★若直接向样品水溶液中滴加溴水,则会有反应:—CHO + Br 2 + H 2O → —COOH + 2HBr 而使溴水褪色。
4.如何检验溶解在苯中的苯酚?取样,向试样中加入NaOH 溶液,振荡后静置、分液,向水溶液中加入盐酸酸化,再滴入几滴FeCl 3溶液(或过量饱和溴水......),若溶液呈紫色(或有白色沉淀生成),则说明有苯酚。
★若向样品中直接滴入FeCl 3溶液,则由于苯酚仍溶解在苯中,不得进入水溶液中与Fe 3+进行离子反应;若向样品中直接加入饱和溴水,则生成的三溴苯酚会溶解在苯中而看不到白色沉淀。
★若所用溴水太稀,则一方面可能由于生成溶解度相对较大的一溴苯酚或二溴苯酚,另一方面可能生成的三溴苯酚溶解在过量的苯酚之中而看不到沉淀。
6.如何检验实验室制得的乙烯气体中含有CH 2=CH 2、SO 2、CO 2、H 2O ? 将气体依次通过无水硫酸铜、品红溶液、饱和Fe 2(SO 4)3溶液、品红溶液、澄清石灰水、(检验水) (检验SO 2) (除去SO 2) (确认SO 2已除尽)(检验CO 2)溴水或溴的四氯化碳溶液或酸性高锰酸钾溶液(检验CH =CH )。
(一)同系物的判断规律1.一差(分子组成差若干个CH2)2.两同(同通式,同结构)3.三注意(1)必为同一类物质;(2)结构相似(即有相似的原子连接方式或相同的官能团种类和数目);(3)同系物间物性不同化性相似。
因此,具有相同通式的有机物除烷烃外都不能确定是不是同系物。
此外,要熟悉习惯命名的有机物的组成,如油酸、亚油酸、软脂酸、谷氨酸等,以便于辨认他们的同系物。
(二)、同分异构体的种类1.碳链异构2.位置异构3.官能团异构(类别异构)(详写下表)4.顺反异构5.对映异构(不作要求)常见的类别异构CH3与CH与COOH(三)、同分异构体的书写规律书写时,要尽量把主链写直,不要写得扭七歪八的,以免干扰自己的视觉;思维一定要有序,可按下列顺序考虑:1.主链由长到短,支链由整到散,位置由心到边,排列邻、间、对。
2.按照碳链异构→位置异构→顺反异构→官能团异构的顺序书写,也可按官能团异构→碳链异构→位置异构→顺反异构的顺序书写,不管按哪种方法书写都必须防止漏写和重写。
3.若遇到苯环上有三个取代基时,可先定两个的位置关系是邻或间或对,然后再对第三个取代基依次进行定位,同时要注意哪些是与前面重复的。
