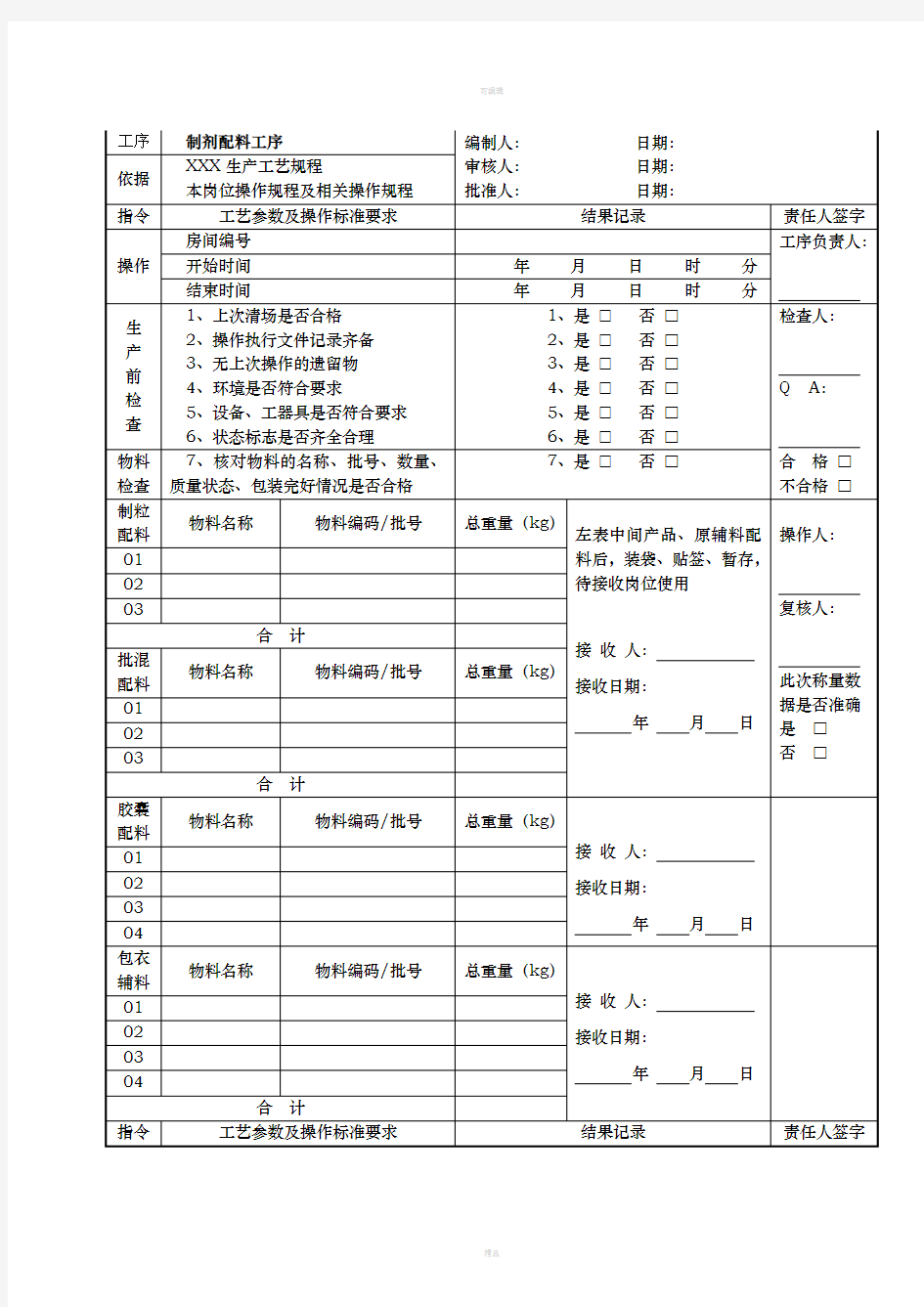
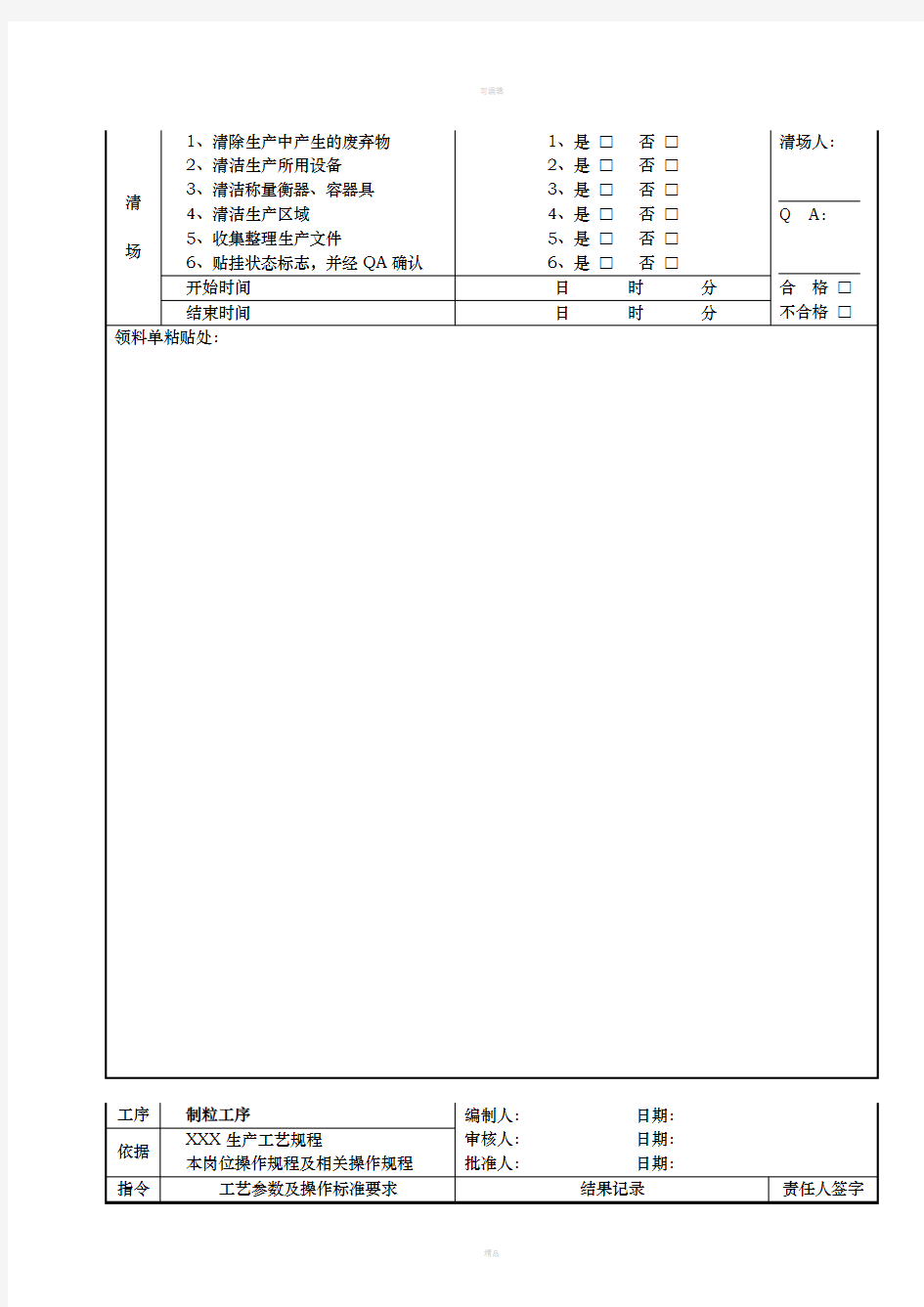
中药制剂固体制剂车间批生产记录模版
固体制剂车间工艺设计毕业论文
固体制剂车间工艺设计毕业论文 1设计依据及设计围 1.1设计依据 1.1.1设计任务 课题名称:布洛芬剂车间工艺设计 生产规模:年产片剂(奥美沙坦酯)6.5亿片 1.1.2设计规和标准 1.药品生产质量管理规(2010年修订,国家食品药品监督管理局颁发) 2.药品生产质量管理规实施指南(2010年版,中国化学制药工业协会) 3.医药工业厂房洁净设计规,GB50457-2008 4.洁净厂房设计规,GB 50073-2001 5.建筑设计防火规,GB/T50016-2006(2006年版) 6.设计规和标准建筑设计防火规,GB/T50016-2006(2006年版) 7.爆炸和火灾危险环境电力装置设计规,GB50058-1992 8.工业企业设计卫生标准,GBZ 1-2010 1.2设计围 本设计参照《医药建筑项目初步设计容及深度的规定》、《车间装置设计》;及校本科生毕业小设计总体要求。 此次设计的围限于片剂车间围的工艺设计及对辅助设施、公用工程等提出设计条件,包括相关的生产设备、车间布置设计、带控制点的工艺流程设计,同时对空调通风、
照明、洁净设施、生产制度、生产方式、土建、环保等在的一些非工艺工程提出要求。
2设计原则及指导思想 2.1设计原则 2.1.1医药工业洁净厂房设计规 1.工艺布局应按生产流程的要求,做到布置合理,紧凑,有利生产操作,并能保证对生产过程进行有效的管理。 2.工艺布局要防止人流、物流之间的混杂和交叉污染,并符合下列基本要求: a分别设置人员和物料进出生产区的通道,极易造成污染的物料(如部分原辅料,生产中废弃物等),必要时可设置专用入口,洁净厂房的物料传递路线尽量要短。 b人员和物料进入洁净生产区应有各自的净化用室和设施。净化用室的设置要求与生产区的空气洁净度级别相适应。 c生产操作区应只设置必要的工艺设备和设施。用于生产、贮存的区域不得用作非本区域工作人员的通道。 3.在满足工艺条件的前提下,为了提高净化效果,节约能源,有空气洁净度要求按下列要求布置: a空气洁净度高的房间或区域宜布置在人员最少达到的地方,并宜靠近空调机房。 b不同空气洁净度级别的房间或区域宜按空气洁净度级别高低有及外布置。 c空气洁净度相同的房间或区域宜相对集中。 d不同空气洁净度房间之间相互联系应有防止污染措施,如气闸室或传递窗(柜)等。 4.洁净厂房应设置与生产规模相适应的原辅材料、半成品、成品存放区域,且尽可能靠近与其相联系的生产区域,减少运输过程中的混杂与污染。存放区域应安排试验区,
磷酸肌酸钠原料药批生产记录知识讲解
磷酸肌酸钠原料药批 生产记录
兔肉处理岗位生产指令单 格式号:YL·G02-07-006-01-LJ-01 生产指令指令日期指令号 生产日期生产批号 投料量兔肉 kg 指令者复核者接受者 本岗位本批生产小结兔肉收率>25% 兔肉合格品 kg ×100%= % 领用兔肉 kg 岗位负责人: 年月日 工艺员评价1.本批生产过程无偏离规程作业。□ 2.本批生产过程中工艺卫生符合要求。□ 3.本批清场符合要求。□ 4.本批生产记录清晰、完整。□ 工艺员: 年月日
兔肉处理岗位操作记录 格式号:YL·Z02-02-107-01 生产批号 生产日期年月日时分—时分 操作指令及工艺参数实际操作记录 按《兔肉处理岗位标准操作规程》[YL·Z02-02-107]进行操 作。 1生产前检查 上批清场合格证 清洁状态标识 设备运行状态标识 公用系统 2挂状态标识 3根据生产指令领取所需原辅料 4操作过程 4.1将领用兔肉用纯化水洗两遍,洗净血垢后,再用注射用水冲洗一遍,将水控干,用手术刀片将兔肉剔下,再用不锈钢菜刀切成1cm左右的小块,装入保鲜袋中冻存,标明品名、批号、数量和生产日期。 4.2及时填写操作记录及物料结存台帐。 4.3操作前用纯化水清洗工具和双手。 5清场 5.1本批生产文件及状态标识及时清除。 5.2容器具已清洁。 5.3清洁墙面、门窗、地面。 5.4清除废弃物。 5.5清洁废物桶。有□无□ 已清洁□待清洁□ 备用□其它□ 正常□异常□ 已挂状态标识□ 领用兔肉 kg 非用肉组织 kg 不合格 kg 兔肉合格品 kg 兔肉收率 % 时间:时分至时分 已清除□未清除□ 已清洁□未清洁□ 已清洁□未清洁□ 已清除□未清除□ 已清洁□未清洁□ 检查情况:合格□不合格□检查人: 操作者:复核者:
固体制剂综合车间GMP设计
广西科技大学 生物与化学工程学院 “固体制剂综合车间GMP设计” 课程设计说明书 题目:固体制剂综合车间GMP设计指导教师:廖兰 组别:第三组 小组成员及学号:韦炳生(2) 徐孔兰(2) 吴俊良(2) 覃桂芳(2) 梁翠娟(2) 梁晓斌(2) 日期:2016年11月22日
制药工艺学课程设计任务书(第三组) 设计题目固体制剂综合车间GMP设计(片剂5亿片/年,胶囊剂5 亿粒/年) 一、设计内容和要求 1.确定工艺流程及净化区域划分。 2. 每位组员详细叙述一个固体制剂工艺设备的工作原理、结构组成及关于此设备国内外的现状、研究前沿。 3. 物料衡算、设备选型。 计算基础数据。 年工作日:250天。生产班别:2班生产,每班8h,班有效工作时间6~7h。 生产方式:间歇生产。 假设片剂平均片重为0.3g/片,胶囊平均粒重为0.3g/粒;要求生产工艺流程中有两种或三种制粒方式,包装方式有铝塑包装和瓶装两种方式。(其它未给出的工艺参数,请参考文献自定) 4. 紧扣GMP规范要求设计车间工艺平面布置图。 5. 编写设计说明书。 二、设计成果 1.设计说明书一份,包括工艺概述、工艺流程示意图、物料衡算、工艺设备选型说明、主要设备一览表、车间工艺平面布置说明、车间技术要求、工艺流程及净化区域划分说明;每位学生的设备详细综述。 2.车间平面布置图一张(1:100)(A1,CAD制图)。 (注:加粗部分每位学生单独完成上交,其余部分以小组为单位上交)
目录 目录 (3) 1.布洛芬简介 (5) 2.性质与产品概况 (6) 2.1布洛芬胶囊的作用与特点 (6) 2.1.1胶囊剂的作用 (6) 2.1.2胶囊剂的特点 (6) 2.1.3胶囊剂产品概况 (6) 2.2布洛芬片剂 (7) 3.原辅料及质量要求 (9) 3.1 制备 (9) 3.1.1处方 (9) 3.1.2制法 (9) 3.3.3处方分析 (10) 3.2辅料的选用原则 (10) 3.3产品的质量标准 (10) 3.4工艺路线流程 (12) 3.4.1胶囊工艺路线流程 (13) 3.4.2片剂工艺路线流程 (14) 4.工艺路线的设计 (15) 4.1制备流程 (15) 4.1.1粉碎 (15) 4.1.2筛分 (15) 4.1.3混合 (15) 4.1.4制粒 (16) 4.1.5干燥 (16) 4.1.6整粒,总混 (16) 4.1.7填充、压片 (16) 4.1.8包装 (16) 5.物料衡算 (18) 5.1物料衡算基础 (18) 5.2物料衡算条件 (18) 5.3原辅料物料衡算 (18) 6.工艺的设备选型及说明 (23) 6.1工艺设备设计与选型的步骤 (23) 6.1.1工艺设备设计与选型概述 (23) 6.1.2工艺设备设计与选型的任务 (23) 6.1.3工艺设备设计与选型的原则 (23) 6.1.4主要设备选型与计算 (24)
固体制剂综合车间GMP设计
XX科技大学 生物与化学工程学院 “固体制剂综合车间GMP设计” 课程设计说明书 题目:固体制剂综合车间GMP设计 指导教师:廖兰 组别:第三组 小组成员及学号:韦炳生(5) 徐孔兰(6) 吴俊良(7) 覃桂芳(8) 梁翠娟(9) 梁晓斌(0) 日期:2016年11月22日 制药工艺学课程设计任务书(第三组) 设计题目固体制剂综合车间GMP设计(片剂5亿片/年,胶囊剂5
亿粒/年) 一、设计内容和要求 1.确定工艺流程及净化区域划分。 2. 每位组员详细叙述一个固体制剂工艺设备的工作原理、结构组成及关于此设备国内外的现状、研究前沿。 3. 物料衡算、设备选型。 计算基础数据。 年工作日:250天。生产班别:2班生产,每班8h,班有效工作时间6~7h。 生产方式:间歇生产。 假设片剂平均片重为0.3g/片,胶囊平均粒重为0.3g/粒;要求生产工艺流程中有两种或三种制粒方式,包装方式有铝塑包装和瓶装两种方式。(其它未给出的工艺参数,请参考文献自定) 4. 紧扣GMP规X要求设计车间工艺平面布置图。 5. 编写设计说明书。 二、设计成果 1.设计说明书一份,包括工艺概述、工艺流程示意图、物料衡算、工艺设备选型说明、主要设备一览表、车间工艺平面布置说明、车间技术要求、工艺流程及净化区域划分说明;每位学生的设备详细综述。 2.车间平面布置图一X(1:100)(A1,CAD制图)。 (注:加粗部分每位学生单独完成上交,其余部分以小组为单位上交) 目录 目录2 1.布洛芬简介4 2.性质与产品概况5 2.1布洛芬胶囊的作用与特点5 2.1.1胶囊剂的作用5 2.1.2胶囊剂的特点5 2.1.3胶囊剂产品概况5 2.2布洛芬片剂6 3.原辅料及质量要求8 3.1 制备8 3.1.1处方8
药品制剂取样管理规定
药品制剂取样管理规定 1 主题内容与适用范围 本文件规定了公司制剂的取样、方法、数量和取样程序的要求 本文件适用于公司制剂产品的取样。 2 引用标准 ICH Q7a 2000年11月 《药品生产质量管理规范》 2010年修订 《兽药生产质量管理规范》 2002年6月 3 职责 3.1 各制剂生产单位负责本单位产品的请验,负责协助取样员取样后包装的恢复。 3.2 质量保证部负责请验单的审核确认。 3.3 质监中心负责抽取公司制剂产品的检验用样和产品留样。 4 管理规定 4.1 取样程序 4.1.1注射剂 由生产车间填写请验单,经质量保证部驻车间质量员审核确认后送至质监中心取样组,取样员凭请验单到生产车间或仓库取样。请验单属于重要记录,由请验单位自行印刷,编号下发。编号原则为车间代码+序列号。 4.1.2 口服制剂 由生产车间根据生产进度填写相应请验单,各步中间体按各品种工艺规程要求
请验。片剂、胶囊剂铝塑后,请验微生物限度检查。颗粒剂、干混悬剂分装后,按全检请验。请验单经质量保证部驻车间质量员审核确认后,送至质监中心取样组,取样员凭请验单到现场抽取各中间体及产品。各步中间体检验完后,岗位出具《检验结果通知单》给车间。 4.1.3 取样后在取样容器上贴好标签。标签格式见附录。 4.1.4 取样后需填写取样记录,内容包括:取样日期、产品名称、产品规格、产品批号、件数、取样件数、取样数量、来源、取样人等,并及时输入微机台帐。取样记录格式见质监中心《产品分样操作规程》取样、分样记录。 4.1.5 取样员将抽取样品送各相应岗位,做好交接记录;留样交留样室,并做好交接记录。 4.2 取样工具的准备所有取样工具均要求洁净,并保证对检品和产品不会造成污染。 4.2.1 塑料袋取样用塑料袋应清洁、无污染,不得重复使用。 4.2.2 取样勺由生产车间生产岗位负责提供。 4.3 取样数量注射剂每个批号随机开5箱;每箱开2中盒;口服固体制剂桶装、袋装中间体每件抽取,请验微生物限度检查用样品抽取不少于10筐,每筐不少于2个包装。复试样品抽取量执行《化验室OOS/OOT调查管理规程》。 4.4 取样方法 4.4.1注射剂 4.4.1.1 按规定随机选择抽样件数,然后打开包装箱背面,抽取所需样品。整批产品取样完毕,由车间负责补齐数量并恢复原包装,并在背面开口处盖上“检”字章后用胶带封箱。取样员将所取检品混匀,送检。 4.4.1.2 复试时,按4.4.1.1到物资管理部仓库取样。
片剂批生产记录.doc
批生产记录 产品名称: 规格: 批号: 包装规格: 理论产量: 实际产量: 成品率: 质量结论: 生产车间审核人:年月日生产部审核人:年月日质量部审核人:年月日
片剂批生产记录目录 □1、批生产指令单 □2、原辅料领料单、退料单 制粒岗位 □3、上批称量、配料岗位清场合格证(副本)□4、称量、配料岗位生产记录 □5、称量、配料岗位清场记录 □6、本批称量、配料岗位清场合格证(正本)□7、上批物料混合岗位清场合格证(副本)□8、物料混合岗位生产记录 □9、物料混合岗位清场记录 □10、本批物料混合岗位清场合格证(正本)□11、上批制料岗位清场合格证(副本) □12、制粒岗位生产记录 □13、制料岗位清场记录 □14、本批制粒岗位清场合格证(正本) □15、配料制粒岗位质量监控记录 □16、干燥质量监控记录 □17、上批整粒总混岗位清场合格证(副本)□18、整粒总混岗位生产记录 □19、整粒总混岗位清场记录 □20、本批整粒总混岗位清场合格证(正本)□21、整粒总混质量监控记录 □22、半成品检验报告单 压片岗位 □23、上批压片岗位清场合格证(副本) □24、压片岗位生产记录 □25、压片岗位清场记录 □26、本批压片岗位清场合格证(正本) □27、压片岗位质量监控记录包衣岗位 □28、包衣材料领料单、退料单 □29、上批包衣岗位清场合格证(副本)□30、包衣岗位生产记录 □31、包衣岗位清场记录 □32、本批包衣岗位清场合格证(正本)□33、包衣岗位质量监控记录 内包装岗位 □34、批内包装指令单 □35、内包材领料单、退料单 □36、上批内包装岗位清场合格证(副本)□37、内包装岗位生产记录 □38、内包装岗位清场记录 □39、本批内包装岗位清场合格证(正本)□40、内包装岗位质量监控记录 外包岗位 □41、批外包装指令单 □42、外包材领料单、退料单 □43、上批外包装岗位清场合格证(副本)□44、打码岗位生产记录 □45、外包装岗位生产记录 □46、本批次包装盒、标签、说明书样稿□47、外包装岗位清场记录 □48、本批外包装岗位清场合格证(正本)□49、外包装质量监控记录 □50、成品检验报告书 □51、成品验收入库单 □52、成品审核放行单
中药制剂生产
中药制剂生产基础知识 第一章片剂 第一节概述 一、中药片剂的含义 中药片剂系指药材提取物、药材提取物加药材细粉或药材细粉与适宜辅料混合匀压制 而成的圆片状或异型片状的制剂。主要供内服,亦有外用。 片剂问世于 10 世纪后叶,而中药片剂创用于 20 世纪 50 年代。近些年来,由于新技术、新工艺、新设备、新辅料的应用,中药片剂的剂型理论、生产技术日臻完善,中药片剂的品种不断增加,质量迅速提高,已发展成为目前临床应用最广泛的广泛的剂型之一。 二、中药片剂的特点 主要优点:①剂量准确,因病人近片服用,而片内药物均匀、含量差异小;②质量稳定,因系固体剂型,且某些易氧化变质或潮解的药物,可借助包衣或包合作用加以保护,水分、光线、空气对其影响较小;③生产机械化、自动化程度高、产量大、成本低,药剂卫生易达标;④服用、携带、贮藏等较文便;⑤品种丰富能满足医疗、预防用药的不同需求。 缺点在于:①制备或贮藏不当会影响片剂崩解、吸收;②某些中药片剂易引湿受潮;含挥发性成分的片剂,久贮时其成分含量下降;③片剂中药物的溶出度和生物利用度较胶囊剂、散剂稍差;④儿童和昏迷病人不易吞服。 三、片剂的分类按给药途径结合制法与作用,片剂可分为以下几类: (一)内服片 系供口服,在胃肠道崩解、吸收而发挥局部或全身疗效的片剂。 1.普通压制片(素片)系指药物与辅料混合后,经加工压制而成的片剂。一般不包衣的片剂多属此类,如安胃片、葛根芩连片。 2.包衣片系指在压片(常称片心)外包衣膜的片剂。如三七伤药片、盐酸黄连素片。 3.咀嚼片指在口中嚼碎后咽下的片剂,多用于维生素类及治疗胃部疾患的药物。如酵母片、乐得胃片。 4.分散片系指遇水能迅速崩解形成具较大粘性的均匀的混悬性水分散体的片剂。这种片剂一般由药物和崩解剂及溶胀辅料组成。可吞服,也可放入水中迅速分散后口服,还可咀嚼或含吮。如复方阿司区林分散片。
新版GMP问题解答(二)
新版GMP问题解答(二) 来源:安徽省药监局网站 洁净区的消毒一直是困扰使用方的难题,采用何种消毒剂比较合适? 答:在选择一种消毒剂时,首先要了解消毒剂的性质,但同时也应该认识到没有一种消毒剂是完全理想的。目前大多数企业采用甲醛熏蒸的方式,缺点是对人员的毒性大,残留量比较难测试。 越来越多的企业采用过氧化氢和过氧乙酸的喷雾方式(VHP),干雾或者蒸汽。灭菌效果可以验证,残留量容易测试。 是不是意味着一定要清洗完毕就马上烘干?采用空调加大通风干燥方式是否符合此条? 答:物品应该在清洗后干燥,干燥后再存放。干燥可采用压缩空气吹干、烘干、通风等方式,不推荐采取空调加大通风干燥方式,空调加大通风干燥方式耗时长,干燥效果不理想。 清洗完毕的设备应及时干燥,以防止微生物滋生以及水或溶剂、清洁剂对设备的腐蚀、氧化,干燥一般采用烘干、压缩空气吹干的方式。通过通风的方式干燥,应考虑干燥的时间较长造成的不良影响。 化验室的仪器维修后是否要进行重新验证?如HPLC(高效液相色谱)更换氘灯或电路板、修理进样器。 答:需要重新确认。 维修、更换关键部件需要针对影响部分重新确认。更换氘灯需要校验;换电路板视其功能而定,如果是主板需要确认;修理进样器需进行功能测试和校验。 称量间是否可放置多个物料? 答:原则是只可以放置一种物料。未开始称量的物料可以在称量间外指定区域短暂放置。称量时应逐个物料分别称量,称量完成后应按产品将不同物料集中存放。 持续稳定性考察的时间应当涵盖药品有效期,考察方案应当至少包括以下内容 答:A.每种规格、每个生产批量药品的考察批次数。 B .相关的物理、化学、微生物和生物学检验方法,可考虑采用稳定性考察专属的检验方法。 C.容器密封系统的描述。 D.检验项目,如检验项目少于成品质量标准所包含的项目,应当说明理由。 E.检验方法依据。 有下列情况之一的,由药品监督管理部门收回《药品GMP证书》 答:A.企业(车间)不符合药品GMP要求的。 B.企业因违反药品管理法规被责令停产整顿的。 C.其他需要收回的。
口服固体制剂车间设计Word
口服固体制剂车间设计 口服固体制剂车间GMP设计原则 固体制剂车间GMP设计原则及技术要求工艺设计在固体制剂车间设计中起到核心作用,直接关系到药品生产企业的GMP验证和认证。 应遵循以下设计原则和技术要求。 1、根据GMP及其《洁净厂房设计规范》 (GB 50073—2001)和国家关于建筑、消防、环保、能源等方面的规范设计。 2、固体制剂车间在厂区中布置应合理,应使车间人流、物流出人口尽量与厂区人流、物流道路相吻合,交通运输方便。由于固体制剂发尘量较大其总图位置应不影响洁净级别较高的生产车间如大输液车间等。在生产过程中产生的容易污染环境的废弃物的专用出口,避免对原辅料和内包材造成污染。 3、若无特殊要求,生产内别为丙类,耐火等级二级。洁净度300000级、温度18℃~26℃、相对湿度45℅~65℅。 4、充分利用建设单位现有的技术、装备、场地、设施。要根据生产和投资规模合理选用生产工艺设备,提高产品质量和生产效率。设备布置便于操作,辅助区布置适宜。为避免外来因素对药品产生污染,洁净生产区只设置与生产有关的设备、设施和物料存放间。空压站、除尘间、空调系统、配电等公用辅助设施,均应布置在一般生产区。 5、粉碎机、旋振筛、整粒机、压片机、混合制粒机需设置除尘装置。热风循环烘箱、高效包衣机的配液需排热排湿。各工具清洗间墙壁、地面、吊顶要求防霉且耐清洗。 相关工序的特殊要求(见图 A B)
备料室的设置 综合固体制剂车间原辅料的处理量大,应设置备料室,并布置在仓库附近,便于实现定额定量、加工和称量的集中管理。生产区用料时由专人登记发放,司确保原辅料领用。车间 与仓库在一起,可减少或避免人员的误操作所 造成的损失。仓库布置了备料中心,原辅料在 此备料,直接供车间使用。车间内不必再考虑 备料工序,可减少生产中的交叉污染。 固体制剂车间产尘的处理 固体制剂车间特点是产尘的工序多,班次 不一。发尘量大的粉碎、过筛、制粒、干燥、 整粒、总混、压片、充填等岗位,需设计必要 的捕尘、除尘装置(见左图) 产尘室内同时设置回风及排风,排风系统 均与相应的送风系统连锁,即排风系统只有在迭风系统运行后才能开启,避免不正确的操作,以保证洁净区相对室外正压(见图)。
板蓝根颗粒提取批生产记录
板蓝根颗粒 提取批生产记录 、 指令单号: 产品批号: 药材用量:共 1 味,总计 252 Kg 浸膏数量: Kg 操作日期:年月日至月日 汇总人: 审核人:
**********
提取批生产指令 指令依据板蓝根颗粒浸膏工艺规程 标准依据中国药典(2015年版一部) 产品代码产品名称药材总量制剂总量浸膏数量产品批号TQ001板蓝根颗粒浸膏252 kg万袋 药材用量 名称物料代码批生产处方量名称物料代码批生产处方量板蓝根YJ004252kg 备注:生产处方量为饮片或净料量,领料量按药材领用量=处方投料量÷炮制得率计。 设备多功能提取罐、提取液储罐、双效节能浓缩器、浓缩液储罐、醇沉罐、球形真空减压浓缩器 提取方法 将称量好的板蓝根净药材投入到多功能提取罐中,要求每罐煎煮两次,第一次加入8倍量水,浸泡30分钟,煎煮2小时(药液沸腾开始计时),煎液滤过注入储罐,再加入6倍量水,煎煮1小时,煎液滤过注入提取液储罐。 操作要求1.生产过程符合“板蓝根颗粒浸膏工艺规程”要求; 2.按各岗位标准操作规程进行操作; 3.按上述设备的标准操作规程进行操作; 4.收膏在D级洁净区进行。 5.各区按相应生产区的清洁规程进行清洁。 6.按上述各设备的清洁标准操作规程对设备进行清洁或消毒。 7.所有工序的物料交接必须进行复核复秤。 8.各工序按“交接班管理规程”进行交接班。 9.按“清场管理规程”要求进行转换品种或批号的清场。
提取工艺参数1、提取:将称量好的板蓝根净药材投入到多功能提取罐中,要求每罐煎煮两次,第一次加入8倍量水,浸泡30分钟,煎煮2小时(药液沸腾开始计时),煎液滤过注入储罐,再加入6倍量水,煎煮1小时,煎液滤过注入提取液储罐。 2、浓缩:煎液全部浓缩至相对密度为(50℃测),注入浓缩液储罐中。 3、醇沉:加入乙醇,使含醇量达到60%,搅拌30分钟,室温静置48小时使沉淀。 4、收膏:将药液浓缩至相对密度为(50℃测)的浸膏。 下达人下达时间年月日QA复核人批准人接收人
固体制剂车间设计要点79
固体制剂车间设计要点 摘要:本文根据固体制剂产品生产特点,结合工程实践,通过分析其生产工艺 特点及工艺流程,总结出一些在工程设计中需要注意的设计要点。 关键词:固体制剂;工程设计,设计要点 1固体制剂简述 固体制剂是我们日常生活中接触最多的一种口服制剂产品。常见的固体剂型有颗粒剂、 片剂、胶囊剂、散剂、滴丸剂和膜剂。根据用途,片剂可细分为:口服用片剂、口腔用片剂、皮下给药片剂、外用片剂;根据剂型,片剂又可细分为:普通片、包衣片、泡腾片、咀嚼片、分散片、缓释片、多层片。 2 固体制剂的特点 固体制剂在药物制剂中约占70%。由于剂型品种最为丰富、临床用药最为方便,固体制 剂长期以来在国内外占据着用药主流剂型地位。在我国5000多家医药制剂生产企业中,有 固体制剂药物生产的厂家占到一半以上,可以说固体制剂是我国制药生产中的普遍剂型。 尽管固体制剂种类繁多但它们的共同点及特点表现为: (1)与液体制剂相比,物理、化学稳定性好,生产制造成本较低,服用与携带比较方便; (2)制备过程的前处理经历相同的单元操作,以保证药物的均匀混合与准确剂量,而且 剂型之间有着密切的联系; (3)药物在体内首先溶解后才能透过生理膜,被吸收进入血液循环中。 现阶段,受制于固体制剂生产工艺工序多、过程复杂等因素,国内外固体制剂生产很难 实现全过程自动化、在线连续化生产模式。各工艺生产工序自成单元。 3固体制剂生产的工艺流程 固体制剂剂型主要是片剂、胶囊剂和颗粒剂三种,它们生产前段工序相似:均需要经过 粉碎过筛称量、制粒、总混等工序,这些工序在各种固体制剂生产过程中均是属于必不可缺 的工序。固体制剂工艺流程的不同,在于制剂种类的不同和包装种类的不同。制剂种类的不 同体现在压片、胶囊填充及包衣工序上。包装种类的不同一方面体现在外包装选用的是铝塑、铝铝还是瓶包装。 固体制剂车间设计要点 (1)工艺布局理念 1)“U”型工艺布局 考虑到固体制剂车间的物料运输量较大,车间内物流宜按工艺流程顺序进行布置,以缩 短运输路线,避免物料在车间内部折返,避免前后工序物料的交叉污染。在车间布置中应使 得整个车间呈U字型布局,所有工序按照主工艺流程围绕着中间站进行布置,把制粒、总混、压片、包衣等不同工艺房间区分,各工序集中设置,形成工序单元。各集中工序单元围绕中 间站、按照工艺流程设置,人流从一侧进出,物流由另一侧进入车间。车间内物料单相运输,有效降低了交叉污染的风险。这种模块化的固体制剂工艺布局模式,可灵活的将多个工艺模 块有机的组合在一起,形成整体车间。此种工艺布局方式更适合多品种小产能的固体制剂车 间生产 2)垂直流工艺布局 与平面流对应的垂直流、多层布局模式等,物料利用重力传送,可有效节约人力和能耗;管道输送实现连续化生产,整个物流简捷,按照工艺流程单向流动,整个车间分设在一至三层,其中三层为称配投料区,二层为固体制剂生产的包装前工序,一层为集中包装区。物料 粉碎、过筛后,直接利用管道输送至二层固体制剂车间;固体制剂的包装前工序与包装工序 分别布置于二层和一层,半成品利用层间提升机转运;各层均采用直线型布局,使物料路径 最短。降低了固体制剂生产中大宗物料的运输路径。此种工艺布局方式更适合单品种大产能 的固体制剂车间生产。 3)结合仓储物流 为了缩短运输路线,可将固体制剂车间与仓库组合成一幢厂房设计,按不同防火分区考虑;并应根据全厂区人物流的方向,将车间与仓库南北方向或东西方向布置,车间通过货运
关于加强固体制剂车间生产现场管理的规定
关于加强固体制剂车间生产现场管理的规定 一、劳动纪律管理 1、员工如需请假、调休(意指周一至周五08:30---17:00)需提前一天请假,并办好手续(程序如下:生产内勤处取单—请假人签字(写明事由)—车间主任助理签字—车间主任签字—生产部经理签字(5日内)—总经理签字(超出5日)—单子交回内勤处),方可离开,否则按旷工论处;若是当天请下午假者,需上午12:30之前办完手续,逾时不给批准,情节严重者或延误生产造成不能及时交货的按自动离职论处。(以上两点特殊情况除外)。 2、上班期间不得迟到、早退,违者按公司规定处理;用餐时间不得超过公司规定,违者按迟到、早退处理;加班时间提前离开车间者,扣除加班工资。 3、所有进/出车间人员都必须把鞋子(拖鞋和洁净鞋)放入更鞋柜内,放不下也应摆好。按规定洗手、消毒、更衣,必须随手关门。 4、非生产用品及个人杂物不得带入生产区内,不得玩手机、听音乐;不得从事与生产无关的活动。 5、每周三下午2点开班组长会,地点是配料前室,相关人员务必参加。主要内容是总结上周本班组遇到的问题,要求提出解决的办法或可操作性建议(强调:此项必须做到),以防下次不出现或少出现类似问题。 二、生产质量管理 1、各岗位操作人员不得串岗,具体由各班组长督促。遇到一切异常情况(尤其是设备出现问题)必须及时上报、不得不报、瞒报。 2、安排好的事情及时去做、保质、保量完成。做完后及时汇报生产质量情况(尤其是在双休日及其他加班时间更要特别注意),违者按后果的严重程度,予以相应的处罚。 3、在生产前必须在生产的操作间及设备填写状态标识牌(包括产品名称、批号、操作人、生产日期),各岗位由各班组长督促。 4、岗位所出物料标签内容填写完整(特别强调压板出来的框子、桶必须注明品名、批号、净重等),容器内外壁保持清洁。违者按造成后果的严重程度予以相应处罚。
生产指令管理规程
标题生产指令、包装指令管理规程 文件编码SMP-PMP-003.B 起草人起草日期年月日 审核人审核日期年月日 批准人批准日期年月日 颁发部门质量保障部生效日期年月日 分发部门生产技术部、质量保障部、固体制剂车间 目的:规范生产指令的管理,保证生产有序和可控。 范围:适用于批生产指令、批包装指令及岗位操作指令的管理。 职责:1. 车间主任负责指令的下达与过程检查。 2. QA人员负责本规程的复核与监督。 3. 生产操作人员负责指令的执行。 内容: 1 生产过程指令包括:批生产指令、批包装指令、岗位操作指令,其分别以批生产指令、批包装指令、各工序批生产记录的形式体现。 2 批生产指令、批包装指令 2.1 批生产指令、批包装指令一式两份。 2.2 批生产指令的内容包括: 2.2.1 产品名称、批号、规格、批量、生产开始日期,生产品种所执行的工艺规程编号。 2.2.2 批处方组成:原辅料的名称、规格、单位、用量。 2.2.3 指令编制人、审核人、签发人的姓名及日期等。 2.3 批包装指令的内容包括: 2.3.1 产品名称、批号、包装规格、批量、包装日期、生产日期、有效期至; 2.3.2 包材及标签的名称、规格、单位、数量; 2.3.3 指令编制人、审核人、签发人的姓名及日期; 2.4 批生产指令、批包装指令的使用 2.4.1 批生产指令、批包装指令由固体制剂车间根据生产技术部下达的生产计划及生产进度进行编制,车间主任签发,QA审核。 2.4.2 说明:批包装批量=批待包产品的总重量/单位待包品平均重量(片剂为平均片重、胶囊剂为平均粒重、颗粒剂为每袋标示量)。 2.4.3 批生产指令第一联做为生产配料的依据;批包装指令第一联作为包装生产的依据。 2.5 批生产指令、批包装指令的归档管理
最新固体制剂设计实例
固体制剂设计实例
固体制剂设计实例 片剂车间设计举例 片剂车间工艺布置图(见图)所示 该车间生产类别为丙类,耐火等级为二级构形式为单层框架,层高为5, 10m;洁净控制区设吊顶;吊顶高度为2.70m;车间内的人员和物料通过各自的专用通道进入洁净区,人流和物流无交叉。整个车间主要出入口分三处,一处是人流出人口,即人员由门厅经过更衣进入车间,再经过洗手、更洁净衣进入洁净生产区、手消毒;一处是原辅料人口,即原辅料经过脱外包由传递窗送入;另一处为成品出口。车间内部布置主要有湿法混合制粒、烘箱烘干、压片、高效包衣、铝塑内包等工序。 胶囊车间设计举例
胶囊车间工艺布置图(见图)所示。 胶囊车间工艺布置图,该车间生产类别为丙类,耐火等级为二级。层高为 5.10m;洁净控制区设吊顶,吊顶高度为2.70m;一步制粒间局部抬高至 3.5m。洁净级别为30万级。车间内人流和物流分开,人员和物料通过各自的专用通道并经过一定的净化措施进入洁净区。进出车间主要分三处,一处是人流出入口,即人员更衣、洗手、更洁净衣、手消毒进入洁净生产区;一处是原辅料人口,即原辅料经过脱外包外清由传递窗送人;另一处为成品出口。车间内部布置主要设置集混合制粒干燥为一体的一步制粒机、全自动胶囊充填机、铝塑内包等工序。 制剂综合车间设计 1、综合车间图(见图)
2、 由于片剂、胶囊剂、颗粒剂的生产前段工序一样,如混合、制粒、于燥和整粒等,因此将片剂、胶囊剂、颗粒剂生产线布置在同一洁净区内,这样可提高设备的使用率,减少洁净区面积,从而节约建设资金。在同一洁净区内布置片剂、胶囊剂、颗粒剂三条生产线,在平面布置时尽可能按生产工段分块布置,如将造粒工段(混合制粒、干燥和整粒总混)、胶囊工段(胶囊充填、抛光选囊)、片剂工段(压片、包衣)和内包装等各自相对集中布置,这样可减少各工段的相互干扰,同时也有利于空调净化系统合理布置。 中间站的布置
生产记录
中间产品交接标准操 1 目的 建立中间产品交接的标准操作程序,防止错收、错发。 2 范围 固体制剂车间中间产品的交接。 3 责任 3.1 中间站管理人员及各工序操作人员对本标准操作程序负责。 3.2 车间工艺员、质监员负责监督与检查。 4 内容 4.1 中间产品进出中间站必须有递交单,并且填写中间产品进出站台帐,执行严格的交接程序。 4.2 中间产品进站。 4.2.1 工序操作人员要将进站的物料填写中间产品递交单(一式二份),写明品名、规格、批号、重量、工序名称、加工状态、递交人、接收人、日期,随同中间产品递交中间站。 4.2.2 中间站管理员按递交单逐项核对无误,检查外包装清洁后,在递交单上签字,并填写进出站台帐,双方签字后,由工序操作人员将中间产品码放到指定位置。 4.2.3 递交单由工序操作人员留一份贴于本工序批生产记录背面,中间站管理员留存一份备查。 4.3 中间产品出站。 4.3.1 中间产品必须有质监科发放的中间产品检验合格报告单,并有质监员在中间产品出站记录台帐上签字放行,方可办理出站手续。 4.3.2发出中间站的中间产品,需由中间站管理员填写递交单,会同中间产品检验合格报告单一同按程序4.2项下递交出站。 5 记录 记录名称保存部门保存期限 中间产品递交单固体制剂车间三年 中间站物料进站记录台帐 中间站物料出站记录台帐 6 培训 6.1 培训对象:车间工艺员、中间站管理员、工序操作人员。 6.2 培训时间:一小时。
返工通知单
返工记录表
交接班记录 一.交接班的规定 1. 为明确职责,交接班时,双方应履行交接手续,在按规定的项目逐项交接清楚后,交接人员先在交接班记录薄上签名,然后接班人依次签名,从此时起,岗位的全部工作,由接班人员负责。交班负责人才能离开岗位。 2. 交班工作由当班人员,事先做好交班准备工作,检查应交的有关事项,整理各种资料、记录薄,检查应交的物件是否齐全,室内的整洁工作,以及为下一班做好准备,接班后立即要执行的准备工作。填写交接班记录薄等待交接。 3. 接班人员应提前10分钟到达,由负责人查阅交接班记录薄,了解有关工作的注意事项,然后准时开始正式进行交接班工作。如果遇有特殊情况,可以延迟时间进行交接班。 4. 值班人员必须遵照规定的轮值表值班,未经带班员和主管同意不得私自调班。当值人员因故提前离开或迟到虽有他人代替,亦应办理交接手续,绝对不允许不办理交接手续而离开岗位。交接禁止使用电话等通讯方式或口头交接班。接班人员未到岗位,交班人员不得离开值班岗位。 5. 交接班手续未结束前,一切工作应由交班人员负责。如在交接班时发生事故,应由交班人员负责处理,交班人员可要求及指挥接班人员协助处理。 6.在下列情况下,不得进行交接班: (1)在交班人处理事物未结束时不得交班; (2)在处理事故时(但可在告一段落时,得到带班员或主管同意后,方可进行交接班); (3)接班人员有喝酒情况或精神不正常时;或接班人突发疾病等特殊情况; (4)交班人员未正式办理交接班手续,就擅自离开工作岗位。 二. 交接班准备工作 交班准备工作,应由当班人员事先做好交班准备工作。 1.检查本班人员的精神状态,仪容、仪表; 2.对本班次需要注意的事项进行安排指导; 3. 检查各种记录是否齐全、正确; 4. 检查岗位使用物品功能是否正常;
中药制剂生产厂房设施规范
中药制剂生产厂房设施规范 第八条中药材和中药饮片的取样、筛选、称重、粉碎、混合等操作易产生粉尘的,应当采取有效措施,以控制粉尘扩散,避免污染和交叉污染,如安装捕尘设备、排风设施或设置专用厂房(操作间)等。 ?检查时需注意: —是否采取有效措施控制处理过程粉尘扩散;排风设施是否经过适当过滤后排放。 —是否采取有效措施对筛选后药材进行区分。—检查捕尘设备是否经过必要的清洁,避免交叉污染。 第九条中药材前处理的厂房内应当设拣选工作台,工作台表面应当平整、易清洁,不产生脱落物。 ?检查时需注意: —拣选工作台面积是否与生产规模相适应;避免不同品种、批号药材同时进行拣选。 第十条中药提取、浓缩等厂房应当与其生产工艺要求相适应,有良好的排风、水蒸汽控制及防止污染和交叉污染
等设施。 ?检查时需注意: —涉及有机溶媒提取的,提取、浓缩厂房设计及内部照明设施 是否符合防爆要求。 —提取、浓缩是否设置有效的排风、水蒸汽控制措施,避免操作间墙面发生霉变污染产品。 第十一条中药提取、浓缩、收膏工序宜采用密闭系统进行操作,并在线进行清洁,以防止污染和交叉污染。采用密闭系统生产的,其操作环境可在非洁净区;采用敞口方式生产的,其操作环境应当与其制剂配制操作区的洁净度级别相适应。 ?检查时需注意:—采用密闭系统操作的,应有验证数据证明收膏及储存过程可有效避免外界环境对浸膏的污染; —密闭系统的呼吸器是否经过完整性检测; 是否对密闭系统进行密闭性的验证,是否对密闭系统进行清洁验证,并依照验证结果制 定清洁规程,并遵照执行; 采用敞口方式收膏的,收膏操作间洁净级别是否与制 剂要求的洁净级别一致;如口服类为D级。 第十二条中药提取后的废渣如需暂存、处理时,应当有专用区
固体制剂GMP综合车间设计实例探讨
固体制剂GMP综合车间设计实例探讨 硬件建设如厂房、设施等的改造或建设是药品生产企业实施GMP的基础。一般由企业根据具体品种的生产工艺提出要求,由设计单位设计图纸,并征求企业意见,进行论证后交由企业实施。而由于设计单位对企业生产工艺和GMP领悟不深刻,药品生产企业对设计过程不了解,很多设计方案虽然好像满足了GMP,但很多情况和实际生产过程或现场发生矛盾。不少设计方案,以已有的车间模式为样本,进行套用修改,不能很好地与具体品种或企业现场实际相结合,在实际运行过程中,根本不能达到GMP,给企业GMP改造或建设留下硬伤,这不得不引起人们的高度注意。本文以某一厂家为例,来探讨固体制剂综合车间的GMP设计。 1 问题的导入 该企业车间为固体制剂综合车间,主要生产片剂、胶囊和颗粒3种剂型的产品,且3种剂型为不同成分的产品。由于全为固体制剂,该企业希望可以通过合并相同工段等方式,降低建设成本。根据我国1998版GMP,由于该3种剂型所要求的生产洁净级别相同,都是30万级,且其前段制颗粒工序即粉碎、过筛、造粒、干燥、总混工序相同,故可集中共用。而后段工序压片、包衣、胶囊填充不同,需分块布置。最后包装工序也有部分相同,也可集中设置。由此可知在同一车间生产3种剂型具有可行性,并且可以通过整合共用工序设备从而提高设备使用率,减少洁净区面积,从而节约建设资金。但主要问题在于如何合理设计,使其在节约资金的同时,也能够符合GMP,以保证药品质量。本文通过分析该固体车间的特点和车间GMP设计的要求,得出设计草案。 2 固体制剂综合车间的特征分析 2.1前段工序相同 该车间主要生产片剂、胶囊和颗粒3种剂型的产品,这3种属于最常见的固体剂型,生产使用量大。不论采用何种生产工艺,片剂、胶囊剂、颗粒剂的生产前段制粒工序都大体相同,如混合、制粒、干燥和整粒等,因此将片剂、胶囊剂、颗粒剂生产线布置在同一洁净区内,这样可提高设备使用率,减少洁净区面积,从而节约建设资金。 2.2涉及物料种类多 由于该车间主要生产片剂、胶囊和颗粒3种剂型的产品,且3种剂型为不同成分的产品,可知,该车间涉及物料种类多,可以通过设置物料暂存和中转站,明确人物流分离,加强人员的管理等措施来避免物料混淆。 2.3产尘的工序多 固体制剂生产过程中易产生大量的粉尘,如果处理不当会对药品质量产生很大的影响。发尘量大的粉碎、过筛、制粒、干燥、整粒、总混、压片、充填等工段,都需设计必要的捕尘、除尘装置。并且应该把产生大量粉尘的的前工序区域联立在一起,组成前工序区域,从而有利于粉尘处理。 2.4小批量、多品种
英文 原料药批生产记录 模板
BATCH PRODUCTION RECORD The following code has been given to the finished product. Revision level: Reasons for Revision:
INPUT DETAILS
Product Name: Flunixin meglumine Doc No: Batch No: Stage: Ⅰ PRODUCT OUTPUT DETAILS Out put weight/ Output Molecule mass Actual yield ratio calculation: Yield ratio = -------------------------------------------------- Input weight / Input Molecule mass Calculated by Verified by
Product Name: Flunixin meglumine Doc No: Batch No: Stage: Ⅰ Op. No Operation Date Time (hrs) Remarks Done by Checked by From To Duration 01 Make sure that R2201 is clean and dry 02 Charge 98kg of purified water , 53kg of MA , 38.7kg of CA , and 3.67kg of TS into R2201 03 Start agitation and keep for 15~20minutes 04 Heat to reflux and maintain the reflux for 2 hours at 10±5℃ 05 Prepare 36% potassium hydroxide solution by adding 25.2kg of potassium hydroxide and 44.8kg of purified water 06 Add 30.5kg of hydrochloric acid and 9.5kg of purified water to prepare another 23% hydrochloric acid solution 07 Then charge excess 4 kg of purified water to R2201 08 Adjust the reaction mass at pH=9 by dropping 36% potassium hydroxide solution 09 Cool the temperature below 10℃ and recheck whether pH is still at 9~10, if not , add 36% potassium hydroxide further to correct it 10 Make sure that ST2202 is dry and clean 11 Centrifuge the mass from R2201 and wash the wet cake and R2201 with 100kg of purified water (clean the R2201 as per procedure specified in Page No of) 12 Spin dry for 40~50minutes and introduce mother liquid back R2201 Note: Shift in–charge should cross check the S. No:and shall sign in ‘checked by’ column.
