包装灭菌验证-纸塑包装检验报告
产品包装规范范本
产品包装规范 编号: 1、目的 为了规范公司产品包装作业的运作,保证产品能满足环境试验的要求,保护产品在运输中不受破坏,特制定本规范。 2、适用范围 本规范适用于公司所有产品的包装作业之运作,主要是针对纸箱包装件的质量标准给予合理规范。 3、内容 3.1包装准备 3.1.1 产品准备 产品应是经检验合格可以出货的产品。 3.1.2 材料准备 以本规范之要求准备相应的包装材料 3.2 包装基本要求 3.2.1 为了保护产品之塑料、金属等基本面免受破坏、划伤,产品外层应使用热缩膜或包装塑胶袋进行单独包装 3.2.2 为了缓冲产品在运输中产生的冲力,要对产品进行加强保护,填塞产品与产品之间的缝隙、产品与内(外)包装之间的缝隙、内包装盒与外包装箱之间的缝隙。对于一些运输较远的产品,应在外包装箱与内包装盒之间铺垫防震材料。 3.2.3 在满足3.2.1要求与3.2.2要求后可按照客户包装要求进行包装 4、包装材料 4.1热缩膜 4.1.1 热缩膜的宽度为130mm和160mm两种规格,单层厚度要求0.025mm,材质为PVC 4.2 纸箱、纸盒 4.2.1 纸箱采用外购件,检查纸箱时应注意各面均应使用厚度大于6mm的双层瓦楞加强牛皮纸,外观尺寸应符合要求。 4.2.2 纸盒采用外购件,检查纸盒时应注意各面均应使用厚度大于2mm的细瓦楞
复350克灰底白板纸,外观尺寸应符合要求。 4.3 透明胶带 4.3.1 透明胶带的规格为50mm±2mm,厚度为0.03mm~0.04mm。 4.3.2 透明胶带的材料为OPP。 4.4 塑料打包带 4.4.1 打包带的材质为PP,颜色为白色。 4.4.2 打包带的规格为宽11mm~13mm,厚度0.8mm~1.0mm。 4.4.3 打包带的抗拉力至少达到130KG。 4.5 泡沫纸 4.5.1 泡沫纸单层厚度要达到5mm 5、包装流程 5.1 封塑、装盒 5.1.1 对于电源类的模块产品以及信号类产品,对每个产品使用热缩膜进行包装,防止运输过程中由于摩擦而损坏产品的塑料、金属表面。对于防雷箱产品应首先使用泡沫纸将其内部空间进行填塞,以防止运输途中的震动对其内部防雷器所造成的损伤。再将防雷箱放入塑胶袋中封装,封装时各面应平整。 5.1.2 将塑封好的电源类模块产品及信号类产品装入相应的产品包装盒中,可一只盒子装入多个产品,若产品装入后于包装盒之间有较大缝隙(缝隙超过5mm)的地方,应使用泡沫纸进行填塞。 5.2 装箱、封箱 5.2.1用透明胶带将纸箱箱底的中缝处封牢,表面平整,再将包装盒依次正确放入包装纸箱内,然后将箱盖中缝用透明胶带封牢,封箱胶带切口要平整,封箱胶带要完全与纸箱粘在一起,若有不平之处要用手将其抹平。纸箱超高允许公差为+5mm/-5mm,超高多余5mm则应将多余产品重新装入新箱,如超高多余-5mm 则内包装盒与外包装箱之间缝隙应用泡沫纸填塞紧密(塑封好的防雷箱装入外包装箱时,四周应使用泡沫纸填塞)。 5.2.2 对于需远距离运输的产品,应在包装外箱内部四周使用泡沫纸进行铺垫后再放入产品包装盒,以减少剧烈震动对产品所产生的影响。 5.3 贴纸
包装材料检验记录
包装材料检验记录 编号:RD-5007 [性状]本品为。 一.标准依据: 1.内包装膜、袋:依据YBB00072005《药用低密度聚乙烯膜、袋》及参照《中国药典》2010年版微生物限度检查法 2.瓦楞纸箱:依据中华人民共和国国家标准GB6453-86《瓦楞纸箱》标准。 3.复合塑编袋(三合一):依据GB/T8947-1998《复合塑料编织袋》检查。 二.内包装膜、袋的检查: 1.外观: 取本品适量,在自然光线明亮处,正视目测;表面应光洁、平整、色泽均匀,不得有穿孔、异物、异味、粘连。袋的热封部位应平整、无虚封。 2.接头数(膜):随机记录,实用时复核,每卷不得多于3个,并在接头处加一标记。3.卷面和端面:目测,应缠紧、缠齐,端面应平整,不允许有错层、塔层、松层或管芯自由脱落现象,不允许有严重碰伤、压陷。 4.印刷质量: 4.1印刷图案、文字:与标准样张核对,文字应无错漏,文字内容应有批准文号、品名、规格、适应症、用法用量等内容,文字清晰。手拭,文字应不脱落、不掉色。4.2印刷错位:与标准样张核对,以分度尺为0.5mm的直尺测量,应在指定位置±2mm 内。 4.3印刷色泽:色泽均匀,与标准样张核对,同批与不同批之间不允许有明显色差。5.微生物限度检查:取试样,用开孔面积为25cm2的消毒过的金属模板压在内层面上,将湿润的无菌棉签在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次,共擦抹4个位置100cm2。每支棉签抹完后立即剪断,投入盛有50ml无菌生理水的锥形瓶中,全部擦抹棉签投入瓶中后,将瓶迅速摇晃1分钟,即得供试液,取供试液参照中国药典2005年版附录微生物限度检查法项下规定,按《微生物限度检验操作规程》检验。 细菌:≤800个/g;霉菌(酵母菌):≤80个/g;大肠埃希菌不得检出。
验证报告(包装)
包装验证 版本/修改状态:A/0生效日期: 文件编号:发放号:控制状态: 拟制:审核:批准:
目录 第一部分总则 (3) 一、适用范围 (3) 二、过程要求(本包装需满足特性): (3) 三、验证方案 (3) 四、验证小组人员职责权限 (4) 第二部分试验和过程验证 (5) 一、封口验证: (5) 二、包装完好性试验 (7) 三、阻菌性试验(琼脂接触攻击试验) (17) 四、灭菌适应性试验 (14) 五、贮存试验 (14) 第三部分结论 (26)
第一部分总则 本包装是用于最终灭菌医疗器械包装的,在规定的生产、灭菌、运输、贮存过程中,能够保持产品无菌性、完整性、无相互兼容性、强度等理化特性的一次性使用包装材料。 一、适用范围 适用于我公司生产的一次性使用医疗器具的包装。 二、过程要求(本包装需满足特性): 1、微生物屏障 2、无毒性 3、物理和化学特性的符合性 4、与材料所用的灭菌过程的适应性 5、与成型和密封过程的适应性 6、包装材料灭菌前后的贮存寿命 7、变更时的再确认 三、验证方案 1、目的:通过各种试验和过程验证来证明此包装材料能够满足预期用途。 2、适用范围:适用于本公司一次性无菌医疗器械的纸塑、复合(透析 式)单包装。
3?试验和验证方法及预计完成时间: a) 封口验证;2008年3月完成。 b) 包装完好性试验;2008年3月完成。 c) 阻菌性试验(微生物屏障)2008年3月完成。 d) 毒性试验(生物兼容性测试);2008年3月完成 e) 化学特性测试;2008年3月完成。 f) 灭菌适应性试验;2008年3月完成。 g) 贮存试验;2008年3月完成。 四、验证小组人员职责权限
包装车间工作规范及要求
包装车间工作规范及要求 目录 第一部分----岗位分析: (一)、包装车间的组织工作、人员配备及工作介绍 一、组织工作: 二、人员配备: 三、主要工作介绍: 四、存在的几个问题及部分解决方法: (二)、相关部门、信息接口及信息表单: 第二部分----操作程序: 一、总流程 二、成品入库程序----检验程序----返修/退货程序 三、包装材料/内配件的准备流程----再制品加工流程 第三部分---岗位职责: 一、包装主任职责 二、检验组长职责 三、成品仓管职责 四、包装组长职责
包装车间工作规范及要求(讨论) 第一部分----岗位分析: (一)、包装车间的组织工作、人员配备及工作介绍: 2、说明: a、车间仓库职能主要体现在成品与包材两方面,其中包材主要有包装箱、包装袋等几类材料,有负责操作(有专职收发管理员,也有操作工兼任)。 b、打包组负责打包、打托、铆铆钉等工作(由专职打包员或操作工兼任)。 C、检验组的人员管理归质检部门,日常生产服从包装车间按排。 二、人员配备:
2、说明: a、质检组设置了2个小组,配置1小组长,有2名检验员,有2名质保资料管理员,小计5人; b、包装组设置了5个小组,每组设有名包装工,暂无小组长,小计人; c、综合生产保障下设:打包组有人,装卸组有人。打单组人:合计人。 三、包装车间主要工作阐述: 1、根据业务部门下达的出货周计划保质、保量、按交期完成生产任务; 2、根据客户需求,完成临时性增加的订单; 3、积极的反馈前工序或者外协采购件的质量问题,并参与问题分析,根据实际提出相应 的改善措施。 4、生产余料的清退工作(生产完的订单不常用的产品及时的退回仓库) 5、现场环境的清扫、物品的整理工作(5S) 6、协调相关部门的工作、反馈并处理异常; 7、车间内部的日常工作与管理,制度的建设及实施。 四、目前存在的几个问题及部分解决办法(由于本人任职时间不长,看到的问题也不深,暂写以下几点): 问题1:目前车间实际的产能、发货情况不能满足客户需求,经常的出现加班加点,还是不能按计划完成任务。 原因:1、包装车间一线操作人员不能满足日常实际生产;2、下达的出货计划时间比较紧,往往都是当需要发的订单当天陆续发到车间,不能给车间生产和检验相应的准备和突发异常处理的时间,一天的工作当中,大家上午都比较空闲,等10点以后当天的出货计划下达后,才开始真正的忙碌起来 建议:1、公司根据实际产能招收相应的包装生产人员;2、业务根据客户需求制定祥细的出货计划提前把计划告知车间,车间根据出货计划细分到各组提前准备生产物料、检验等辅助工作。 1、车间生产、检验人员对于当天具体工作按排缺乏针对性。 原因:个人觉得对于车间的计划应该是祥细的,具体到产品的规格/型号、数量、交期等而不是对员工下达物流方向,如果笼统的需求会让生产人员的对于需要出货的具体产品,前期的相应准备会有“盲区” 建议:1、此项工作具体还是需要业务和车间主要负责人进行统筹、业务所下达的出货计
包装材料实验报告
西南林业大学材料工程学院包装工程专业实验报告 课程:包装材料学 姓名:李天卓 学号:20131052046 班级:包装工程2013级 任课教师: 解林坤 时间:2015.11.06
一厚度的测定 一、实验原理 厚度是指纸和纸板等材料在两侧压板间规定压力下直接测量的结果,单位是mm或μm。厚度是影响纸和纸板技术性能的一项关键指标,要求一批产品各张纸或纸板之间的厚度应趋于一致,同一张纸或纸板不同部位之间厚度也应一致。对于具有特殊用途要求的产品如标准纸板还应进行更为严格的全幅校验。在测量时可根据纸的厚薄采用多层测量或单层测量,最后以单层测量的结果表示纸的厚度。 二、测试仪器: 测定纸和纸板厚度的主要仪器是厚度测定仪,有手动、电动之分,以手动为例,其基本结构如图1所示,测定时将纸或纸板放在两受压面之间进行测量。测量过程中受压面间的压力为100 kPa±10 kPa,测厚时,受压测量面积为200 mm2。 图1 厚度测定仪 1—拨杆;2一指针;3一重锤;4一测量杆; 5一测量头;6一量砧;7一底座 三、试验步骤 (1)把测微计放置在无震动的水平面上,调好零点,按标准规定采取试样,以每张纸样上切取100 mm×100 mm的试样至少5张。 (2)按下拨杆,抬起测量头至足以放人纸样的高度(若为电动仪器,则由仪器自动控制高度),置纸样于测量头与测量砧之间。
(3)缓慢放松拨杆,使测量头以低于3 mm/S的速度将测量面轻轻压到试样上(若为电动测厚仪,则自动下降接触纸样),注意避免产生任何冲击作用,待指示值稳定后2~5 s内读数,避免人为对测微计施加任何压力。 (4)对每个试样进行一次测定,测定点离任何一端不小于20 mm或在试样的中心点。宽度在100 mm以下的盘纸,应按全宽切取5条长300 mm的纸条,在每条不同位置测量其厚度,至少两处。 四、结果表示: 以所有测定值的算术平均值表示结果,并报出最大值和最小值。 厚度小于0.05mm的纸,准确至0.001 mm; 厚度小于0.2 mm的纸,准确至0.005mm; 厚度大于0.2mm的纸,准确至0.01 mm。 实验结果:0.33×0.01mm=0.0033mm 二纸和纸板耐折度的测定 一、实验原理 耐折度是指试样在一定张力下,抗往复折叠的能力,以折叠次数表示。耐折度受纤维的长度、纤维本身的强度和纤维间的结合状况影响。凡纤维长度大纤维的强度高和纤维结合力大者,其耐折度就高。耐折度也受纸张水分含量的影响,水分含量低纸张发脆,耐折度低,适当增加含水量,纸张的柔性提高,耐折度随之增大,但水分含量超过一定限度耐折度开始下降。另外,耐折度受打浆程度的影响,在一定程度内,耐折度随打浆度的增加而增加,继续提高打浆度到一定程度,由于纤维的平均长度下降,纤维交织紧密,纸质变脆,则使耐折度下降。因此,在实际生产上控制好影响因素,对保证纸张有较好的耐折强度甚为重要。 许多纸和纸板如白纸板和箱纸板等在加工和使用过程中要经受多次折叠,而耐折度则能较好地反映出纸张抗反复折叠的能力,因此,耐折度的检测被广泛采用。 常用的耐折度仪有两种,一种为卧式的,称作肖伯尔(Schopper)式和立式,称作MIT式,二者的主要区别在于对试样的折叠角度不同,肖伯尔式的折叠角度为180°,MIT式的折叠角度为135°。
产品包装规范范本
********** * 有限公司 包装作业指导书(通用)
、目的 为了规范公司产品包装作业,保护产品在存储、运输中不受破坏,特制定本规范。 二、适用范围 适本规范适用于公司所有消防类产品的包装作业,主要是针对纸、木箱包装件的质量标准给予合理规范。 三、职责 生产部:严格遵守包装需求。 质量部:负责包装质量监控。 采购部:推动包装标准在供应商端的执行。 四、定义 1、小型产品 直径或长宽尺寸小于50mm的产品,如:螺母,螺杆,接头等; 2、中型产品 直径或长宽尺寸在50~300mm勺产品,如:超细干粉灭火装置,气溶 胶灭火装置等; 3、大型产品直径或长宽尺寸在300mm以上的产品,如:消防控制柜、 火灾报警控制器等; 4、不规则产品产品形状不规则,且不能使用通用包材进行包装的产品;
5、内包装与产品直接接触,最小包装的包装形式,主要是保护产品质量,多用软包装材料,如PE袋、气泡袋、编织袋等; 6外包装是集中产品包装于一体的容器,主要用来保障产品在流通中 的安全,便于装卸、运输等。其包装兼顾防震功能和美观,如纸箱,木箱等;五、包装材料 1包装纸箱 1.1瓦楞纸箱应符合GBT6543-2008的相应要求。 1.2纸箱所用纸板应符合GB/T 6544-2008的相应要求。 1.3瓦楞纸箱的设计长、宽之比一般不大于 2.5 : 1;高、宽之比一般不大于2:1,一般不小于0.15 : 1。 1.4在无特殊要求条件下,一般选用单瓦楞纸箱,纸箱的层数不少于3层, 纸箱所用纸板边压强度不小于3500N/m(按20KG堆叠5层,面积40*30CM 计算,需要3588N/M)。
验证报告(包装)
包装验证 版本/修改状态:A/0 生效日期:文件编号:发放号:控制状态:拟制:审核:批准:
目录 第一部分总则 (3) 一、适用范围 (3) 二、过程要求(本包装需满足特性): (3) 三、验证方案 (3) 四、验证小组人员职责权限 (4) 第二部分试验和过程验证 (5) 一、封口验证: (5) 二、包装完好性试验 (7) 三、阻菌性试验(琼脂接触攻击试验) (17) 四、灭菌适应性试验 (14) 五、贮存试验 (14) 第三部分结论 (26)
第一部分总则 本包装是用于最终灭菌医疗器械包装的,在规定的生产、灭菌、运输、贮存过程中,能够保持产品无菌性、完整性、无相互兼容性、强度等理化特性的一次性使用包装材料。 一、适用范围 适用于我公司生产的一次性使用医疗器具的包装。 二、过程要求(本包装需满足特性): 1、微生物屏障 2、无毒性 3、物理和化学特性的符合性 4、与材料所用的灭菌过程的适应性 5、与成型和密封过程的适应性 6、包装材料灭菌前后的贮存寿命 7、变更时的再确认 三、验证方案 1、目的:通过各种试验和过程验证来证明此包装材料能够满足预期用途。 2、适用范围:适用于本公司一次性无菌医疗器械的纸塑、复合(透析式) 单包装。 3.试验和验证方法及预计完成时间:
a﹚封口验证;2008年3月完成。 b﹚包装完好性试验;2008年3月完成。 c﹚阻菌性试验(微生物屏障)2008年3月完成。 d﹚毒性试验(生物兼容性测试);2008年3月完成。 e﹚化学特性测试;2008年3月完成。 f﹚灭菌适应性试验;2008年3月完成。 g﹚贮存试验;2008年3月完成。 四、验证小组人员职责权限
BOPP薄膜进料检验标准
适用范围: 本标准适用于印刷、复合(含淋膜复合)用普通塑料薄膜入仓前的检验。铝箔AL 和聚酰胺薄膜(BOPA)参照规定的内容。 标准内容: 1.抽样标准及方法: 以该进货批次同种规格,同种材质的材料总数的10%抽验。 拆开包装后,抽去膜卷表面1-2圈后取约1米长作为待测样品。 2.检验项目及方法: 印刷、贴合用普通塑料薄膜(PET、BOPP、CPP、LDPE)入仓前检验项目及方法 铝箔AL和BOPA薄膜因其特殊性,进料检验时不得开启原包装。这两种材料进料验证时主要检查供方产品标识、合格证和供方检验报告的正确性和完整性。AL和BOPA 的厚度、宽度、电晕处理值在原料上机使用拆除包装时由品管取样测试验证并做相应
判定和记录。 3.批次检验结果与判定: 上述检验指标全部合格才判定该抽样批次合格。若有一项不合格则判为不合格。但是某些不致影响材料本身应该具有的性能或不致影响最终产品的性能的缺陷,可以报上级视情形考虑降级使用。 4.记录与区分: 所有检验数据及判定结果,填入《进料检验记录》并交品管部主管确认。 检验合格的材料作合格标识,交仓库于备料区区分摆放。 遇有不合格物料,贴不合格标识,填写《不合格原料报告处理单》交相关部门领导确认后与供应商联络处理。 检验员及时对检验合格和不合格的物料作出明确、固定的标识,并通知仓库按区域摆放。
附表1 普通型双向拉伸聚丙烯薄膜1.外观应符合表1规定 表1 2.尺寸偏差 薄膜宽度允差±2mm 厚度偏差、厚度平均偏差应符合表2规定 表2 每卷薄膜接头及每段长度应符合表3规定 表3
3.物理机械性能应符合表4规定 表4 4.卫生性能 符合GB9688之规定,嗅觉应无异味。 附件2 热封型双向拉伸聚丙烯薄膜 2.尺寸偏差
产品包装、包装标志、装车发货规范
包装、包装标志、装箱发货管理规范 一、适用范围 本规范适用于本厂环保设备产品包装、包装储运标志、收发货标志、装车发货流程的要求。 二、引用标准 1、GB/T 13384—92 机电产品包装通用技术 2、GB191—2008 包装储运图示标志 3、GB6388—86 运输包装收发货标志 4、GB/T 6543-2008 瓦楞纸箱标准 5、GB/T 6544-1999 瓦楞纸板标准 6、GB/T 5033-85 出口产品包装用瓦楞纸箱 7、GB/T 5034-85 出口产品用瓦楞纸板标准 8、AS2008 包装箱验收标准 三、包装的要求 包装的方法有箱装、敞装、局部包装、捆装、裸装、袋装和托盘装等。 产品的包装应符合科学、牢固、美观和适销的要求,在正常的储运、装卸条件下,应保证产品制造厂发货之日起,至少一年(出口产品至少二年)内不因包装不善而产生锈蚀、长霉、降低精度、残损或散失等现象,特殊要求按双方协议执行。 (一)包装箱的一般要求 包装箱含木箱、瓦楞纸箱、胶合板箱、纤维板箱、钙镁砼箱、竹胶板箱、塑料箱、金属箱等。
根据我厂的情况,对如下常用的包装箱作以下要求: 1、木质包装箱的要求。见《AS2008 包装箱验收标准》 2、瓦楞纸箱 1)、内销瓦楞纸箱应符合《GB/T 6543-2008瓦楞纸箱》规定。出口产品用瓦楞纸箱应符合《GB/ 5033-85出品产品包装用瓦楞箱》板规定。 2)、内销纸箱用瓦楞纸板应符合《GB/T 6544-1999瓦楞纸板》规定。出口产品瓦楞纸箱用瓦楞纸板应符合《GB/ 5034-88 出品产品用瓦楞纸板》规定。 3)、瓦楞纸箱的验收要求 ⑴、包装纸箱应符合科学、牢固、美观和适销的要求,在正常的储运、装卸条件下,应保证产品不因包装不善而产生锈蚀、长霉、降低精度、残损或散失等现象,特殊要求按双方协议执行。 ⑵、纸箱的接合可用钉线或粘合剂等方式。不得有粘合及钉合不良、不规则、脏污、伤痕等使用的缺陷。金属钉线的宽度不小于1.5mm,钉线不得有锈斑、剥层、龟裂、或其他使用上的缺陷。 ⑶、瓦楞纸箱接合搭接搭边的宽度单边瓦楞纸箱为30mm以上,双瓦楞纸箱为35mm以上。钉线的间隙为单钉不大于80mm,双钉不大于110mm。搭接部分中线钉合,采用斜钉(与纸箱直边约成45°)或横钉。箱钉应排列整齐、均匀。头尾钉距底面压痕中线的距离为13+ 7mm。钉合应钉牢、钉透。不得有叠钉、翘钉,不转角等缺陷。 - ⑷、瓦楞纸箱接头粘合搭接搭边宽度不小于30mm。粘合剂涂布均匀充分,不得有多余的粘合剂溢出现象。粘合应牢固,剥离时至少有70%的粘合面。
验证报告记录(包装)
验证报告记录(包装)
————————————————————————————————作者:————————————————————————————————日期:
包装验证 版本/修改状态:A/0 生效日期:文件编号:发放号:控制状态:拟制:审核:批准:
目录 第一部分总则 (5) 一、适用范围 (5) 二、过程要求(本包装需满足特性): (5) 三、验证方案 (5) 四、验证小组人员职责权限 (6) 第二部分试验和过程验证 (7) 一、封口验证: (7) 二、包装完好性试验 (9) 三、阻菌性试验(琼脂接触攻击试验) (17) 四、灭菌适应性试验 (16) 五、贮存试验 (16) 第三部分结论 (26)
第一部分总则 本包装是用于最终灭菌医疗器械包装的,在规定的生产、灭菌、运输、贮存过程中,能够保持产品无菌性、完整性、无相互兼容性、强度等理化特性的一次性使用包装材料。 一、适用范围 适用于我公司生产的一次性使用医疗器具的包装。 二、过程要求(本包装需满足特性): 1、微生物屏障 2、无毒性 3、物理和化学特性的符合性 4、与材料所用的灭菌过程的适应性 5、与成型和密封过程的适应性 6、包装材料灭菌前后的贮存寿命 7、变更时的再确认 三、验证方案 1、目的:通过各种试验和过程验证来证明此包装材料能够满足预期用途。 2、适用范围:适用于本公司一次性无菌医疗器械的纸塑、复合(透析 式)单包装。 3.试验和验证方法及预计完成时间:
a﹚封口验证;2008年3月完成。 b﹚包装完好性试验;2008年3月完成。 c﹚阻菌性试验(微生物屏障)2008年3月完成。 d﹚毒性试验(生物兼容性测试);2008年3月完成。 e﹚化学特性测试;2008年3月完成。 f﹚灭菌适应性试验;2008年3月完成。 g﹚贮存试验;2008年3月完成。 四、验证小组人员职责权限 姓名部门职位责任/权限
范例4:纸塑包装(初包装)过程确认
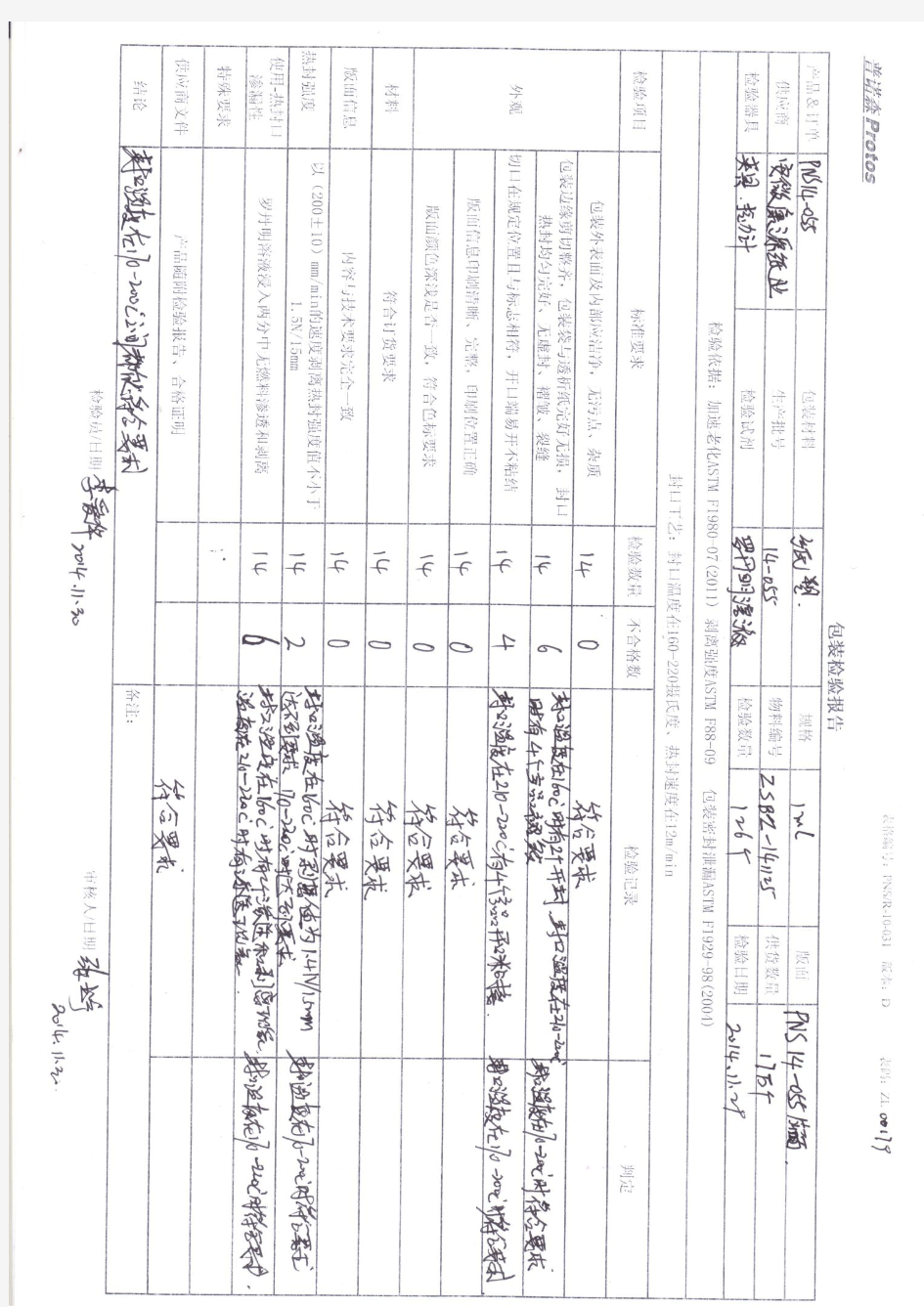
范例4纸塑包装(初包装)过程确认 纸塑包装(初包装)过程确认方案 1 目的 本方案的目的在于对本公司无菌XXXX产品的初包装设备、包装封口机进行热合包装过程确认,以确保能提供安全有效的包装工艺。 2 范围 2.1 设备:本次验证确认的设备为XXXX包装封口机,内部设备编号为XXX。 2.2 材料:本次确认使用的材料为PE复合薄膜和55g/m2医用涂胶透析纸。材料的体技术参数见供应商提供的资料。 2.3本次OQ过程由两部门组成: 2.3.1确认设备的功能操作; 2.3.2 确认当设备运行于常规条件、上限条件、下限条件时的封合过程,OQ过程需要对产品的时 机封合过程和/或样品的封合过程进行评估,OQ的评估应包括产品在灭菌前和灭菌后性能的比较结果。 2.4 封口过程: 预热设备后,将XXXX的包装纸袋,放上输送带入口,在相应参数条件下进行热封口操作,形成单个产品。本次确认过程将通过调整温度工艺参数的范围设定,进行比较包装效果,寻找最合适的参数范围。根据厂家的指导文件,我们采用热封温度200℃作为温度范围的中间值;为了生产效率,速度选择较快速度12m/min。由于封合压力等的变化对过程的输出性能影响不明显, 编者说明:如采用非包装袋形式的,而采用纸塑在线自动热合成型的包装形式的可采用本方案,但是要调整相关内容。 3 依据文件 . ISO11607-1:2009《最终灭菌医疗器械的包装第1部分:材料、无菌屏障系统、包装系统的要求》 . ISO11607-2:2006《最终灭菌医疗器械的包装第2部分:成形、密封和组装过程的确认要求》. GB/T2828.1-2008 . 包装确认控制程序 . 热封包装操作规程
产品包装规范(一)
产品包装规范要求 1.目的 为了规范公司产品包装作业的运作,保证产品能满足环境试验的要求,保护产品在运输中不受破坏,方便客户验收,保证现场方便安装,特制定本规范。 2.范围 本规范适用于公司所有产品的包装作业之运作,主要是针对整套设备包装及运输的质量标准给予合理规范。 3.内容 a.包装前准备 1)产品准备: 产品应经检验部门检验合格,并做好防护和有关内包装后方可进行外包装,并贴有合格标识; 2)材料准备:根据产品的特点和储运条件,选择适当的内外包装材料保证产品完整不受损坏; 3)技术文件准备:产品使用说明书,产品合格检验报告,电气图纸与装配图纸等; b.基本要求 1>为了保护产品之塑料,金属等基本面免受破坏,对产品加保护膜 或其它保护性物质进行包装; 2>为了缓冲产品在运输过程中产生的冲力,要对产品进行加强保 护,在产品与包装箱之间用钢丝或加紧螺栓加紧; 3>包装后的产品要方便装车与卸货,且起吊时要保证箱体受力,
安全可靠; 4>包装箱的外形尺寸和包装件的重量应符合运输部门超限,超长 的有关规定; 5>客户有要求的,按照客户要求进行包装。 c. 装箱、封箱、贴纸 装箱 装箱前——产品装箱前确保内外表面干净,无污痕,无锈迹,符合食品机械要求,装箱前、用塑料薄膜或纸胶带密封,尽量保证无空气进入产品内部,防止生锈; 箱体结构——包装箱的结构应按产品(被包装物)的特点,包装重量,运输要求和包装方式设计。以下框架供参考: 图一 封箱:各面之间相互连接紧密,要达到棱角分明,整齐美观的效果. 贴纸: 正面:包装标识;背面:装箱清单,公司标识;侧面为装箱
号。如图: 其中包装标识是用模板喷漆。 d.产品固定要求: 产品应垫稳,卡牢,固定在包装箱内。 产品固定方法: 1.通过产品底座上的螺栓孔,和箱子底座固定在滑木板或枕木上; 2.当产品不能直接固定在箱子底座上时,应用木方支撑,然后用木条,螺栓固定在箱子底座上;
封口验证报告
XXXXXX公司封口机验证报告
一、设备简介 兄弟牌SF-150型封口机是一款适用于我司医疗器械包装的封口机。该封口机适用于我公司一次性使用非织布手术巾包与一次性非织布手术衣的包装工艺。 二、验证目的 对兄弟牌SF-150型封口机的制造,安装,运行性能各个环节进行确认,以证实机器符合设计要求,符合我公司产品包装工艺对设备的要求。 三、验证范围 本验证方案适用于我公司兄弟牌SF-150型封口机的安装、运行及性能的验证,以确保此封口机安装正确,运行稳定,符合我公司产品包装工艺对设备的要求。 五、验证依据及采用文件 4.1医疗器械生产质量管理规范的程序文件 4.2设备管理程序 4.3无菌包装验证方案——兄弟牌封口机验证 六、验证小组的人员及职责 5.1 5.2、验证项目小组责任 验证项目小组组长:负责组织起草验证方案,组织实施验证方案和完成验证报告。
验证项目小组组员:分别负责起草验证方案、负责实施方案中安装确认、运行确认和性能确认的具体工作。 七、验证内容 6.1、预确认 查设备图纸、结构、技术参数、设备的备用品等。 6.2、安装确认 查设备安装电源接地保护、主要技术参数的确认、文件(如使用说明书、设备出厂合格证)等。 6.3、运行确认 主要开机、停机、平稳性检查(主要检查开机,关机的指示灯情况),空运转情况检查(主要查设备安装稳固性、电源连接、各运转部件及调节按钮的灵活性、速度和频率等)、仪表工作状态检查、记录检查等。 6.4、性能确认 性能确认是对预确认的再确认,也就是机器在用户处,正式摸拟实际生产状态来检查机器的使用性能。 根据需要验证设备的参数,选择适当的纸塑包装袋等进行模拟生产,验证需要连续运转一定时间进行。 八、结果评价与建议 验证小组负责对验证结果进行综合评价,做出验证结论,确认验证设备的检测程序及验证管袋封口确认记录表。 九、备注 1、设备应在当前条件下使用,使用条件发生变更应报验证工作领导小组审核,必要时重新验证。 2、设备应按批准的标准操作、维护、保养规程进行操作和保养。 十、附件 附件一验证方案会签单表 附件二验证报告证书 附件三安装环境、位置检查纪录 附件四安装确认检查纪录 附件五公用介质连接检查纪录 附件六设备主要技术参数检查纪录 附件七开机、停机平稳性检查纪录 附件八空运转检查纪录 附件九仪表工作情况检查纪录
PE袋初包装封口验证报告
PE袋初包装封口验证报告 文件编号:YWY/G-01-2015 C/0 编制:日期: 审核:日期: 批准:日期: 验证时间: 第一章总则 1.1.验证目的 根据ISO13458-2003(YY/T0287-2003)标准中“当生产和服务提供过的输出不能由后续的监视或测量加以验证时,组织应对任何这样的过程实施确认”。为此针对本公司生产的无菌医疗器械产品的初包装的工艺过程进行验证,使产品的单只包装符合GB/T19633-2005(ISO11607)《最终灭菌医疗器械的包装》标准的相关要求,同时对包装所用的材料和设备仪器进行验证。 1.2范围 1.2.1本验证适用于本公司生产的一次使用无菌医疗器械产品的PE成型 袋的 包装验证。所涉及的产品有: (1)、一次性使用无菌吸痰管; (2)、一次性使用无菌导尿管; (3)、一次性使用无菌胃管;
(4)、一次性使用无菌喂食管; (5)、一次性使用无菌肛门管; (6)、一次性使用无菌婴儿尿袋; (7)、一次性使用无菌引流袋; 1.2.2本次验证用的设备为自动热合封口机,设备的编号为:YS—29,安 装在净化车间内。 1.2.3初包装材料 本次确认使用的材料为PE复合膜,单层厚度为0.05mm,材料的技术参数由供应商提供。 由于初包装材料及热合封口的工艺及设备已被生产实践所确定,所以本次 的验证采用回顾性验证,在热合封口统计分析的基础上,证实初包装热合封口的生产工艺条件适用性的验证 1.3验证 1.3.1验证方案:由本公司技术部制定,报管理者代表审批后方可实施。 1.3.2验证实施:由相关职能部门的人员组成验证小组,管理者代表负责 按验证 方案组织实施。 1.3.3验证资料:所有有关验证的资料、所取得的数据、记录和验证报告 由技术 部汇编并存档。 1.3.4依据文件:
包装材料完整性试验报告
包装材料完整性试验报告
1 包装材料的要求 据EN868-1、YY/T0313-1998标准。 1.1 用作制造一次性使用输液器和一次性使用无菌注射器的包装材料原料可以是原始材料或再生材料,但应有原料特别是回收材料的来源,明确其历史和可追溯性,并受到控制,以确保成品始终能满足要求。 1.2 包装材料的设计必须在满足原定用途的条件下,把对使用者或患者的安全造成危害的可能性降低到最小程度。 1.2.1 包装材料与灭菌过程相容性:包装材料与产品按一定方式组合装入灭菌器后,具有足够的透气性和灭菌剂渗透性,以能达到灭菌所要求的条件和灭菌后除去灭菌剂。 1.2.2 包装材料与一次性使用输液器和一次性使用注射器的相容性(即包装与医疗器材相互无不良影响):主要考虑的有:拟包装的医疗器械的大小和形状,有几何锐边凸出部分,对物理和其它防护的要求,医疗器械对特殊危险例如辐射、湿气、机械性撞击,静电放射的敏感性。 1.2.3 包装材料与标识方式的相容性:标识方法必须对包装材料与采用的灭菌过程的相容性无不良影响,印刷或书写所采用的油墨不会转移到一次性使用输液器、一次性使用注射器等医疗器械上,也不会和包装材料起反应而影响包装材料的效用,也不会变色而使标识变的模糊不清,对固定在包装材料表面的标识,其附着方式必须能耐受灭菌过程的使用及制造厂规定的贮存和运输条件。 1.2.4 包装材料能够提供对物理、化学和微生物的防护。 1.2.5 包装材料在使用场所与使用者撕开包装取出使用时的要求相容性(例如无菌的开封)。 1.3 在使用条件下,在灭菌前、中、后,包装材料不可释放已知是有毒的,其数量足以对健康危害的物质。 1.4 生物相容性:按一次性使用输液器和一次性使用注射器的预期用途,对包装材料的生物相容性进行评价(见ENISO10993-1)。
产品包装纸箱设计规范
1. 目的 规范产品包装纸箱设计要求,以确保产品在搬运,储存及运输过程中之品质保证。 2. 範圍 本规范规定了本公司纸箱结构的一般性设计要求,规定,适用于本公司产品包装纸箱设计的相 关部门 3. 瓦楞纸箱设计步骤内容: 3.1. 纸箱的结构选型(本公司包装箱一般采用GB/T6543-2008 0201型结构) 3.2. 纸箱单箱重量(毛重)规定 根据国家标准,对人工搬运的单件包装箱最大重量规定为18kg,考虑到公司产品的特殊性 及人员搬运操作方便性,公司规定产品包装单件重量不得大于15kg 3.3.
纸箱最外面的那层称为面纸,最里内的纸称为里纸,中间凹凸不平的纸为坑纸,两坑纸中间纸称为隔纸,其材质表达方式为: ◇前面的字母(如K,A,B)表示为面纸纸质 ◇中间符号(如=)表示瓦楞层数,9表示E坑幼坑纸,3表示B坑单瓦楞 ◇后面表示字母(如K,A,B)表示为里纸纸质 ◇如K=K,表示为面纸和里纸都是K纸材质,双层瓦楞纸(默认BC组合瓦楞) 3.4. 依照集装箱配合最优尺寸及堆码方式进行外箱尺寸设计 3.4.1.栈板规格规定1100×1100mm(单面木质栈板) 3.4.2.外箱标准堆码方式为重叠反交错和旋转交错两种 ◆重叠式和正反交错堆码方式 外箱标准设计内尺寸 B: 330mm 依产品重量及纸质 长宽比:1.5 ◆旋转交错方式 外箱标准设计内尺寸 L:370mm B:330mm H:依产品重量及纸质 长宽比:1.12
3.5.尺寸设计要求 3.5.1.公司外箱公用尺寸为L500mm*B330mm和L370mm*330mm两种,高度依产品包装方式数量及重 量决定 3.5.2.其他外箱尺寸管制 3.5.2.1.瓦楞纸箱的尺寸以内尺寸为标准,如需标注外尺寸应在尺寸前加“外”字,单位为 毫米(mm),内尺寸就是纸箱内净空尺寸,以长、宽、高顺序表示,字母代号以L、B、 H表示。 3.5.2.2.一般公差:单瓦楞纸箱±3mm,双瓦楞纸箱±5mm 3.5.2.3.外尺寸应符合GB/T4892标准规定: ◆长、宽之比不大于2.5:1(RL=1~1.5内最佳) ◆宽、高之比不大于2:1,不小于0.15:1 3.5.2. 4.纸箱尺寸展开图 ◆纸箱接头G的制造尺寸:单瓦楞纸板为30mm,双瓦楞纸板为40mm ◆外尺寸在内尺寸基础上+纸板厚度 3.6.瓦楞纸箱强度设计 瓦楞纸箱的强度是评价瓦楞纸箱的重要指标,同时也是设计瓦楞纸箱的重要条件。根据瓦楞纸箱的实际应用情况,瓦楞纸箱的强度设计主要包括空箱抗压强度和堆码强度两方面。 瓦楞纸箱的堆码强度是用于评估在包装件静态仓储情况下,瓦楞纸箱至堆垛坍塌时所能承
验证方案(纸塑包装单包装)
纸塑包装单包装确认方案 版次:A/0版 受控状态:
目录 目录 (2) 1目的 (3) 2范围 (3) 3依据文件 (3) 4确认小组成员 (4) 5IQ(Installation Qualification) (5) 6OQ(Operational Qualification) (6) 7PQ(Performance Qualification) (10) 注: 1、依据标准ISO11607-1.-2:2006 参考GB/T19633-2005; 2、本方案包含了IQ/OQ/PQ; 3、依据文件部分务必形成文件,请确认,若没有,请完成。
1目的 本方案的目的在于对注射器的初包装设备吸塑包装机进行安装确认和操作确认,以确保能提供合适的包装设备和操作方法。 该设备放置于………。 2范围 2.1设备:本次验证确认的设备为吸塑包装机,**内部编号为*********。 2.2材料:本次确认使用的材料为PET/PE复合薄膜和60g/m2医用涂胶透析纸。材料的具 体参数见供应商提供资料。 2.3重新确认条件 2.3.1 设备相关变动,与吸塑、热封部位的维护、改动。 2.3.2产品包装材料的变更。 2.3.3吸塑、热合模具的修理。 2.3.4使用新的模具。 2.3.5有严重产品相关质量事故的发生。 2.4OQ包括两部分组成:1、确认设备的功能操作;2、确认当设备运行于常规条件、上 限条件、下限条件时的封合过程,OQ过程需要对产品的实际封合过程和/或样品的封合过程进行评估,OQ的评估应包括产品在灭菌前和灭菌后性能的比较结果。 2.5封口过程 注射器公司将生产不同型号的注射器。公司外购的PET/PE薄膜和医用透析纸,薄膜经吸塑包装机吸塑成型,放入产品,然后与透析纸进行热封。然后由切断刀将已经热合的包装切割,形成单个产品。 3依据文件 3.1包装验证控制程序 3.2吸塑包装工艺守则 3.3设备维修保养管理制度 3.4医用透析纸质量标准 3.5产品初始污染菌监督管理办法
IQC进料检验规范
深圳科士达科技股份有限公司 Shenzhen Kstar Science And Technology Co.,Ltd. IQC进料检验规范 文件编号:SZK-OA-WI-019 版本:D 制定部门:品保部 总页数:9页
提供IQC进料检验工作指引,明确各种原材料检验项目及接收标准,确保进料能满足及适合公司生产需要,以求产品品质最终能满足客户需求。 范围: 此检验标准适用于本公司产品所需的原材料及其包装材料的检验(已通过认证
的合格供应商及其所供的原材料)。 权责: 资材单位:物料的核对、点收与材料送检、合格品入库、不良品退货,物料定购及供应商联络。 品保部(IQC):负责物料的具体检验、物料检验结果的判定和不合格品的审核及判退、以及物料信息的收集及供应商品质异常信息的联络。 品保部经理:异常物料的判定处理及采用方式的最终核准。 定义: 缺陷定义 4.1.1致命缺陷、严重缺陷、轻缺陷 4.1.1.1致命缺陷(CRI):凡会对使用者生命及财产安全造成危险性之妨害或导 致产品完全失去功能之缺陷。 4.1.1.2严重缺陷(MAJ):凡导致产品失去部分功能,从而无法达到预期使用的 目的,或严重影响产品的外观, 导致客户不接收的缺陷。 4.1.1.3轻微缺陷(MIN):除去致使缺陷和严重缺陷以外的缺陷(如:不会造成产品或客户的影响)。 进料:指用于产品上的原材料及外加工之半成品物料的进收统称为进料。 抽样检验:是指依材料检验作业指导书从一批物料中随机抽取一定数量之样品进行检验的一种方式,并根据 随机取样检验的结果来判定整批物料是否合格。 选别:是指对抽样不合格批物料,按照规格标准要求,剔除不良品的一种方式。 (生产选别、供应商选别) 特采:是指送检的产品不符合规格要求,与规格标准差异轻微不影响装配或不影响产品使用功能,对产品进 行的让步接收的一种方式。 紧急放行:(在通常情况不准使用未经检验合格的物料)在生产急需上线来不及等待检验结果,而一旦不符 合规格要求,又能及时追回和更换的条件允许放行的一种方式。 免检:对于长期进料品质稳定的物料免于进料检验。 管制物料:采购首次进料、进料检验异常、在制程中发生不良而导致停线及报废清仓之严重物料、客户抱怨 材料。 去除管制材料原则:除首次进料外,连续3批进料检验合格,由QE或品保经理判定品质稳定。 加严检验:当物料出现重大品质问题或持续得不到改善时,需执行的一种抽检方式(依据)如: 同一供应商所供同一款物料连续三批出现进检不合格;制程中发生严重不良导致返工停线之物料;客户强 烈投诉造成公司损失之物料均需执行加严检验。 内容: 进料检验作业流程图(见附件二) 进料的送检: 5.2.1仓管员根据“送货单”进行核对收料,针对“ROHS”物料,须依据“ROHS
产品包装规范
产品包装规范 1目的: 为了规范公司产品包装作业的运作,保证产品能满足环境试验的要求,保持产品在搬运、储存、开包过程中避免意外损伤,保持包装箱内产品的完整性, 保证产品性能和特性符合顾客要求。特制定本规范。 2范围: 本规范规定了本公司机械、电工、仪器仪表、等产品包装的基本要求、包装方式与包装方法、技术要求、实验方法、包装标志与随机文件等内容。适用于本厂产品包装的操作、验收及包装后的仓储管理和运输质量控制。 3规范性引用文件: GB /T 191 包装储运图示标志 GB/T 4768 防霉包装 GB/T 4879 防锈包装 GB/T 5048 防潮包装 GB/T 6543 瓦楞纸箱 GB/T 6544 瓦楞纸板 GB/T 7284 框架木箱
GB/T 10819 木质底盘 GB/T 12464 普通木箱 GB/T 12464 普通木箱 GB/T 6546 瓦楞纸板边压强度的测定法 GB/T 6545 瓦楞纸板耐破强度的测定法 GB/T 4857.1 试验时部位标示方法 GB/T 4857.3 运输包装件静载荷堆码试验方法 GB/T 4857.5 跌落试验方法 GB/T 4857.10 运输包装件正弦振动试验方法 4 内容 4.1包装准备 4.1.1产品准备 所有待包装的产品必须是经过质量部检验合格确认可以出货的产品。 4.1.2材料准备 以本规范之要求准备与待包装产品相适应的包装材料。 4.2基本要求 4.2.1包装应符合科学、经济、牢固、美观和适销的要求。在流通环境下,应保证产品在供需双方协议期内不因包装不善而产生锈蚀、霉变、降低精度,残损或散
失等现象。 4.2.2包装设计应根据产品特点、流通环境条件和客户要求进行,做到包装紧凑、防护合理、安全可靠。 4.2.3产品需经检验合格,做好防护处理,方可进行内外包装。随机文件应齐全。 4.2.4包装件外形尺寸和质量应符合国内外运输方面有关超限、超重的概念。 4.2.5产品包装环境应保持清洁、干燥、无有害介质。 4.3包装方式与防护包装方法 4.3.1包装方式主要有箱装(普通木箱、滑木箱、框架木箱、瓦楞纸箱、胶合木箱、纤维板箱、钙塑箱、塑料箱、金属箱、钙塑瓦楞箱、蜂窝纸板箱等)、敞开包装、局部包装、捆扎包装、裸装、袋装和托盘包装等。 4.3.2防护包装方法主要有:防水包装、防潮包装、防霉包装、防锈包装、缓冲包装、防尘包装和防静电包装等。应根据产品特点和储运、装卸条件,选用适当的防护包装方法。 5技术要求 5.1包装材料 选用的包装材料不应引起产品的表面色泽改变或锈蚀,也不应由于包装材料的变形而引起产品损坏。 5.1.1 木材
产品包装材料验证报告模板
文件编号:产品包装材料验证报告 拟制日期年月日 审核日期年月日 批准日期年月日 版号生效日期年月日 有限公司
产品包装材料验证报告 一、总则 1 包装材料的要求 依据:YY/T0681.1、YY/T0313 、YZB/国《体》产品注册标准。 用作制造XXXX的包装材料原料是原始材料,应有原料的来源,明确其历史和可追溯性,并受到控制,以确保成品始终能满足要求。 2 包装材料的设计必须在满足原定用途的条件下,既能够确保内包装材料的符合性,又把对使用者或患者的安全造成危害的可能性降低到最小程度。 2.1 包装材料与XXXX的相容性(即包装与医疗器材相互无不良影响):主要考虑的有:包装材料的安全性毒性的要求,拟包装的医疗器械的大小和形状,对物理和其它防护的要求,医疗器械对特殊危险例如辐射、湿气、机械性撞击,静电放射的敏感性。 2.2 包装材料与标识方式的相容性:标识方法必须对包装材料与采用的灭菌过程的相容性无不良影响,印刷或书写所采用的油墨不会转移到XXXX产品上,也不会和包装材料起反应而影响包装材料的效用,也不会变色而使标识变的模糊不清,对固定在包装材料表面的标识,其附着方式必须能耐受灭菌过程的使用及制造厂规定的贮存和运输条件。 3 包装材料能够提供对物理、化学和微生物的防护。 3.1包装材料在使用场所与使用者撕开包装取出使用时的要求相容性(例如无菌的开封)。
3.2 在使用条件下,在灭菌前、中、后,包装材料不可释放已知是有毒的,其数量足以对健康危害的物质。 3.3无菌状态的保持:(即从其产品灭菌后,成为无菌之时起,直至规定的失效日期或使用时止),包装完整性及包装材料的微生物阻隔特性。 3.4 材料的毒性检测。
