第一章 四谱解析-红外
第一章_有机化合物的波谱综合解析-3

红外光谱(i nfra r ed spectroscopy 缩写为IR )由于分子吸收了红外线的能量并导致分子内振动能级的跃迁而产生的记录信号。
IR 谱主要提供分子中官能团的结构信息。
横坐标:波数(σ)400~4000cm -1;表示吸收峰的位臵。
纵坐标:透过率(T %),表示吸收强度。
T ↓,表明吸收的越好,故曲线低谷表示是一个好的吸收带。
%100%0⨯=I IT I :表示透过光的强度;I 0:表示入射光的强度。
红外光谱官能团区(4000-1500 cm -1)由分子的伸缩振动导致,用于鉴定各种不同官能团产生红外光谱的必要条件:1.红外辐射光的频率与分子振动的频率相当,才能满足分子振动能级跃迁所需的能量,而产生吸收光谱。
2.只有能引起分子偶极矩的变化的振动才能产生IR 光谱。
完全对称的分子H 2、O 2、N 2不会产生红外吸收光谱。
H―C≡C―H 、R―C ≡C―R ,其C≡C (三键)振动也不能引起红外吸收。
指纹区(1500-650 cm-1)分子弯曲及伸缩振动吸收峰,多用于鉴定基团的结合方式官能团区(高频区)1500-4000 cm-1Y -H 伸缩振动区2500~3700 cm-1,Y= O、N、C。
Y≡Z 三键和累积双键伸缩振动区2100~2400 cm-1,主要是:C≡C、C≡N 三键和C=C=C、C=N=O 等累积双键的伸缩振动吸收峰。
Y=Z双键伸缩振动区1600~1800 cm-1,主要是:C=O、C=N、C=C等双键。
指纹区(低频区)650-1500 cm-1主要是:C-C、C-N、C-O等单键和各种弯曲振动的吸收峰,其特点是谱带密集、难以辨认。
红外谱图各主要官能团红外光谱的特征吸收峰频率3600-3200NH, OH d, br, s3300C CHstrong3100-3010 =C-H middle2960-2850 -C-H strong2260-21002700-CHO doubleC Cvariable1850-1690 C=OAcids, esters Ketones Aldehydes very strong1680-1620 or 1600-1500 C=C variable 1470-1350 bend C-H1000-700 bend alkenes benzene substituted type4000cm-1650cm-11300-1030 bend C-O C-N几个明显的红外特征峰-OH(醇和酚):-OH吸收处于3200~3650cm-1,由于-OH可形成分子间或分子内氢键,而氢键所引起的缔合对红外吸收峰的位臵、形状和强度都有重要影响。
有机物分子结构分析四谱原理

有机物分子结构分析四谱原理学过有机化学的同学都知道,我们在确定有机物名称的时候,需要注意元素组成、分子式的确定、化学键的判断、官能团类别等。
而在化学结构分析中最主要的四种分析仪器红外图谱、质谱、核磁图谱和紫外图谱,再有机分析上也很通用。
本文通过简单的动图解析红外图谱、质谱、核磁图谱和紫外图谱工作机理,给大家一个一目了然的机会。
紫外可见吸收光谱(UV-vis)物质分子吸收一定的波长的紫外或可见光时,分子中的价电子会从低能级跃迁到高能级而产生的吸收光谱。
利用物质的紫外可见光谱及吸收程度可以对物质的组成、含量和结构进行分析、测定、推断。
紫外光谱样品要求:1)、样品溶液的浓度必须适当,且必须清澈透明,不能有气泡或悬浮物质存在;2)、固体样品量>0.2g,液体样品量>2mL。
红外光谱(IR)一定频率的红外线经过分子时,被分子中相同振动频率的键振动吸收,记录所得透过率的曲线即为红外光谱。
只有引起分子偶极矩变化的振动才能产生红外吸收。
红外吸收光谱主要用于结构分析、定性鉴别及定量分析。
分子振动分为两种形式:伸缩振动和弯曲振动,其中伸缩振动又包含对称和非对称两种模式。
1)、样品必须预先纯化,以保证有足够的纯度;2)、样品须预先除水干燥,避免损坏仪器,同时避免水峰对样品谱图的干扰;3)、易潮解的样品,请用户自备干燥器放置;4)、对易挥发、升华、对热不稳定的样品,请用带密封盖或塞子的容器盛装并盖紧,同时必须在样品分析任务单上注明;5)、对于有毒性和腐蚀性的样品,用户必须用密封容器装好。
送样时必须分别在样品瓶标签的明显位置和分析任务单上注明。
红外测试样品制备方法:1、固体样品:压片法、粉末法、薄膜法、糊剂法;2、液体样品:液体试样、液膜法。
我们可以通过红外光谱的特征吸收峰,判断分子的结构式。
以下面甲醇红外光谱分析过程为例:NMR是研究原子核对射频辐射的吸收,在外加磁场的作用下,自旋核吸收电磁波的能量后从低自旋能级跃迁到高自旋能级,所得到的的吸收图谱为核磁共振谱。
红外光谱分析.

红外光谱分析序言二十世纪初叶,Coblentz发表了一百多个有机化合物的红外光谱图,给有机化学家提供了鉴别未知化合物的有力手段。
到四十年代红外光谱技术得到了广泛的研究和应用。
当今红外光谱仪的分辨率越来越高,检测范围扩展到10000-200cm-1,样品量少至微克级。
红外光谱提供的某些信息简捷可靠,检测样品中有无羰基及属于哪一类(酸酐、酯、酮或醛)是其他光谱技术难以替代的。
因此,对从事有机化合物为研究对象的化学工作者来说,红外光谱学是必需熟悉和掌握的一门重要光谱知识。
一、基本原理1、基本知识光是一种电磁波。
可根据电磁波的波长范围分成不同类型的光谱,它们各自反映出物质的不同类型的运动形式。
表1列出这些电磁波的波长,其所在区域的光谱名称,以及对应的运动形式。
红外光谱研究的内容涉及的是分子运动,因此称之为分子光谱。
通常红外光谱系指2-25μ之间的吸收光谱,常用的为中红外区4000-650cm-1(2.5-15.4μ)或4000-400cm-1。
这段波长范围反映出分子中原子间的振动和变角振动,分子在振动运动的同时还存在转动运动。
在红外光谱区实际所测得的图谱是分子的振动与转动运动的加合表现,即所谓振转光谱。
每一化合物都有其特有的光谱,因此使我们有可能通过红外光谱对化合物作出鉴别。
红外光谱所用的单位波长μ,波数cm-1。
光学中的一个基本公式是λυ= C,式中λ为波长,υ为频率,C为光速(3×1010cm/s)。
设υ为波数,其含义是单位长度(1cm)中所含的波的个数,并应具有以下关系:波数(cm-1)=104/波长(μ)波长和波数都被用于表示红外光谱的吸收位置,即红外光谱图的横坐标。
目前倾向于普遍采用波数为单位,而在图谱上方标以对应的波长值。
红外光谱图的纵坐标反映的是吸收强度,一般以透过率(T%)表示。
2、红外光谱的几种振动形式主要的基本可以分为两大类:伸缩振动和弯曲振动。
(1)伸缩振动(υ)沿着键轴方向伸或缩的振动,存在对称与非对称两种类型。
有机化学《红外光谱解析》简述
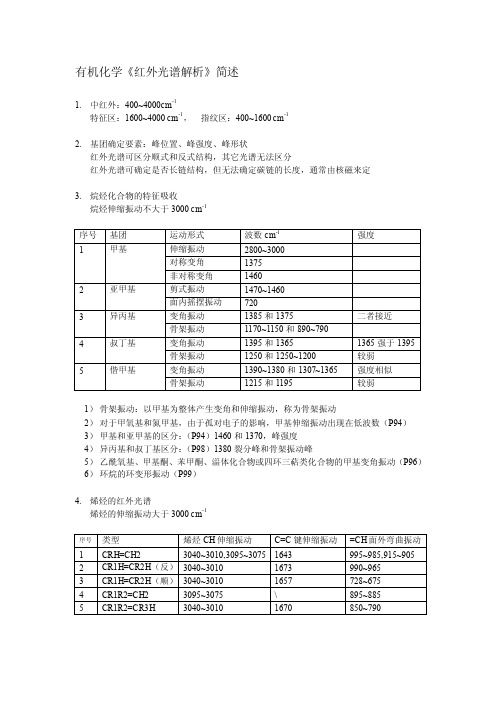
有机化学《红外光谱解析》简述1.中红外:400~4000cm-1特征区:1600~4000 cm-1,指纹区:400~1600 cm-12.基团确定要素:峰位置、峰强度、峰形状红外光谱可区分顺式和反式结构,其它光谱无法区分红外光谱可确定是否长链结构,但无法确定碳链的长度,通常由核磁来定3.烷烃化合物的特征吸收烷烃伸缩振动不大于3000 cm-11)骨架振动:以甲基为整体产生变角和伸缩振动,称为骨架振动2)对于甲氧基和氮甲基,由于孤对电子的影响,甲基伸缩振动出现在低波数(P94)3)甲基和亚甲基的区分:(P94)1460和1370,峰强度4)异丙基和叔丁基区分:(P98)1380裂分峰和骨架振动峰5)乙酰氧基、甲基酮、苯甲酮、淄体化合物或四环三萜类化合物的甲基变角振动(P96)6)环烷的环变形振动(P99)4.烯烃的红外光谱烯烃的伸缩振动大于3000 cm-11)烯烃化合物的特征吸收主要表现在三个区域:A:双键碳原子上的CH伸缩振动:》3000B:C=C键的伸缩振动:1600~1680 cm-1C:双键碳原子上的CH的面外变角振动此外,对于乙烯端基=CH2还存在1400 cm-1处的剪式振动和1800 cm-1处的泛音吸收2) 端位烯基=CH2的变角振动呈剪式振动,具有一定的参考价值,其波数较为固定,在1420 cm-1附近(P103)3)环烯(P103)环比较大没有环张力时,可按顺式烯烃处理。
4)连烯的特征吸收:C=C=C在1950~1940 cm-1处存在特征吸收5)炔类化合物的特征吸收A:——C≡C-H中C-H伸缩振动2262~2100 cm-1B:≡C-H的伸缩振动位于3300 cm-1处该处只有N-H 和O-H存在氢键型的干扰吸收,但后者的峰形较宽,且随浓度变化而移动,二者之间还是易于区别的。
C:除上述二个特征吸收外,≡C-H的面外振动在700~610 cm-1处呈一宽峰,其倍频位于1370~1225 cm-1,宽而弱6) 化合物的不饱和度计算:F=1+n4+1/2(n3-n1)n1: H原子n3:N原子n4:C原子O原子通常不计入例如:分子式为C13H24的化合物,其不饱和度F=1+13+1/2(-24)=2环单键为1,苯环通常》45.芳烃化合物红外光谱可以检定苯环的存在与否,亦可分析取代基的情况苯环的存在与否首先通过3100~3000 cm-1及1650~1450 cm-1(苯环骨架振动)两个区域的吸收形态的检查而确定。
有机化合物的四谱解析

例: 计算C3H4Cl2的 M:M+2:M+4 的相对强度 解:氯的同位素比值为3:1,则用二项式计算: (3+1)2 = 9 + 6 + 1
所以 C3H4Cl2 中氯元素在质谱中峰的强度比是: 9:6:1
9:6:1
23
3. 官能团和化合物类型
质谱中各种碎片离子峰可以提供一些重要的官能团信息。 a) 重要的低质量端离子。如m/z29可能是C2H5或CHO。 b) 高质量离子的研究。通常研究分子离子与高质量碎片离子
M+
解:最大荷质比m/z为102,下一个荷质比的峰m/z为87,相差 15 , 对 应 一 个 -CH3 , 中 性 碎 片 丢 失 合 理 , 所 以 可 以 确 定 m/z(102)为分子离子峰,分子量为102。
17
2. 化学式
同位素离子峰可以帮助确定分子组成。对于有机分子,总 有一些M+1、M+2、M+3等峰伴随着分子离子峰M出现,即 以同位素峰簇存在。
化合物: C10H11BrO2
21
含Cl, Br原子的分子,其强度比符合二项式(a + b)n的展开 式, 其中:a – 常见元素的丰度;b – 同位素的丰度; n - 该元 素的个数。 如: CHCl3: (3 + 1)3 = 27 + 27 + 9 + 1
∴ 同位素丰度为 M:(M+2):(M+4):(M+6) =27:27:9:1
的质量差,由此得到有明确解释的结构信息。如[M-1]+表 示分子离子失去一个H,一个强的[M-1]+暗示存在一个活泼 H和缺乏其它活泼基团,又如[M-15]+, [M-18]+, [M-20]+等总 是表示分子离子失去CH3, H2O, HF。 c) 特征离子。少数特征基团在质谱上对应某些特征峰。如苯 基 的 m/z77 , 苄 基 的 m/z91 , 苯 酰 基 的 m/z105 , 伯 胺 基 的 m/z30,伯醇的m/z31等。
第一章红外物理基础解读

1.太阳
T≈ 5600K
2897 P 0.5 m T
太阳辐射的光谱分布可以用5600 K的黑体的辐射来近似表示
• 曲线1: 温度为6000K的黑体; • 曲线2:太阳在大气层外的辐出度光谱分布 • 曲线3:太阳在海平面上的辐出度光谱分布
太阳辐射很接近于黑体辐射
2.月亮
Reflected Sunlight(太阳反射) Thermal Emission(自身辐射)
2004年
陈永甫编著,《红外辐射、红外器件与典型应用》,电子 工业出版社,2004年
张敬贤等,《微光与红外成像技术》,北京理工大学出版
社,1995年 A.R.杰哈著,《红外技术应用》,化工出版社,2004年
其他:
– 《红外探测器》 – 《红外电子学》 – 《红外光学系统》 – 《红外光谱》 – 《红外技术实验与方法》 – 《红外系统》
• Comman sense approach to thermal imaging, Gerald C. Holst, JCD, SPIE, 2000.
• Maldague, Xavier P. V., Theory and practice of infrared technology for nondestructive testing, John Wliley & Sons, 2001
学习本课程的意义
拓宽知识面
将理论知识用于实践,融会贯通,提高解决实际
问题的能力
了解红外与微光技术实际应用水平和最新发展动
态
为以后的工作和科研提供参考
主要参考书目
吴宗凡等,《红外与微光技术》,国防工业出版社, 1998年 张建奇等,《红外物理》,西安电子科技大学出版社,
有机化学的四谱综合解析

说明 K 带的存在,即存在共轭的两个不饱和键 (共轭二烯或-、不饱和醛酮);
3、在 250-300 nm 有中等强度吸收,且常有 不同程度的精细结构:
苯环或某些杂芳环的存在
4、在 250-350 nm 有中、低强度吸收: 羰基或共轭羰基的存在 5、在 300 nm 以上有强吸收: 化合物中含有大量共轭体系,多为稠 环芳烃及其衍生物
解析红外谱图“三要素”
峰形
强度
位置
峰形
强度
摩尔消光系数
>200
强度
很强
符号
vs s m w
75~200 25~75
5~25 0~5
强 中等
弱 很弱
vw
位置
吸收峰的位置与分子结构有关
有机化合物是多原子分子,分子振动情况复杂 不可能把所有峰都归属于分子内的某种振动 一定的官能团总是有一定的特征吸收
常见基团按六个区进行分析:
1. 4000~2500cm-1:
这是X-H(X=C、N、O、S)伸缩振动区。
醇、酚
游离O-H伸缩振动,3600cm-1 氢键缔合的O-H的伸缩振动, 3300cm-1 C-O伸缩振动,1250~1000cm-1,在 谱图中一般为最强峰
苯乙醇
当分子间 –OH 有缔合时,红外吸收向较低波数 移动(3300 cm-1)附近, 峰形宽而钝。
倍频峰
苯环还有2000~1667cm-1 谱带,是 C-H 面外弯曲振动引起, 对苯环的取代位置判别有一定帮助。
4. 1500~1300cm-1:
苯环(~1450、~1500cm-1的红外吸收进入此区),杂 芳环、硝基的吸收可能进入此区。
此区域主要提供 C-H 弯曲振动的信息。CH3 在~1380、 ~1460cm-1处同时有吸收,而前一吸收峰发生分叉时表示偕 二甲基(两甲基连在同一碳原子上)。
红外光谱

13
水分子——非线性分子
f 3 3 6 3
1 as 3756 cm OH 1 s 3652 cm OH
OH 1595cm 1
14
CO2分子 ——线性分子
f 3 3 5 4
S CO 1388 as CO 2349 CO 667 CO 667
三、红外光谱的吸收强度
四、红外吸收强度及其表示符号
摩尔消光系数(ε)
>200 75~200 25~75 5~25
强度
很强 强 中等 弱
符号
VS S M W
0~5
很弱
VW
分子振动
一、红外光谱产生的第一个条件
•
当一束具有连续波长的红外光通过物质,物质分 子中某个基团的振动频率或转动频率和红外光的 频率一样时,分子就吸收能量由原来的基态振(转 动能级跃迁到能量较高的振(转)动能级,分子吸收 红外辐射后发生振动和转动能级的跃迁,该处波 长的光就被物质吸收。所以,红外光谱法实质上 是一种根据分子内部原子间的相对振动和分子转 动等信息来确定物质分子结构和鉴别化合物的分 析方法。将分子吸收红外光的情况用仪器记录下 来,就得到红外光谱图。红外光谱图通常用波长 (λ)或波数(σ)为横坐标,表示吸收峰的位置,用透 光率(T%)或者吸光度(A)为纵坐标,表示吸收强度
23
第三节
红外分光光谱仪与制样
一、 傅立叶变换红外吸收光谱仪(FT-IR)
光源
迈克尔逊干涉仪
吸收池
干涉图 检测器
傅里叶变换
红外吸收光谱 图
数据处理 仪器控制
二、制样方法
(1) 气体样品: 气态样品 可在玻璃气槽内进行测定, 它的两端粘有红外透光的NaCl或KBr窗片。先将气槽抽 真空,再将试样注入。 (2) 液体和溶液样品(液体池):液体样品可滴在可
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
不饱和度 = 1 + 12 +
1 ×(0 - 24) = 1 2
华东理工大学——王朝霞课件
15
例:某化合物分子式为C6H8N2,推测结构。
华东理工大学——王朝霞课件
16
解:不饱和度为4,推知可能含苯环; 从3030 cm-1、 1593 cm-1、 1502 cm-1有吸收峰可以证实这 点; 从 750 cm-1吸收说明该化合物有三个相邻氢,说明是有间 位取代; 3285 cm-1、 3193 cm-1的吸收是很特征的伯胺吸收(属于对 称伸缩振动和反对称伸缩振动); 另外可以指认的有:3387 cm-1、3366 cm-1( -NH2-伸缩振 动)、1634 cm-1( -NH2弯曲振动)、1274-1( C-N)伸缩振 动等; NH2 所以结果是该化合物是间苯二胺。
-OH吸收处于 3200~3650cm-1 ,由于 -OH 可形成分子间或 分子内氢键,而氢键所引起的缔合对红外吸收峰的位置、形 状和强度都有重要影响。 • 游离 –OH 吸收在较高波数 3610~3640 cm-1,峰形尖锐。 • 分子间 –OH缔合时,红外吸收向较低波数移动( 3300 cm-1 )附近,峰形宽而钝。 • 分子内 –OH缔合时,红外吸收移向更低波数,例如羧酸内 由于强烈缔合,吸收峰的底部可延续到~2500cm-1 ,形成很宽 的吸收带。
NH2
华东理工大学——王朝霞课件 17
1000-700 bend alkenes benzene substituted type 1470-1350 bend C-H 1300-1030 bend C-O C-N
strong 3100-3010 =C-H middle
华东理工大学——王朝霞课件
4
几个明显的红外特征峰
-OH(醇和酚):
华东理工大学——王朝霞课件
6
C-H (烃基):
C-H 键伸缩振动的分界线是 3000 cm-1:
不饱和碳(双键及苯环)> 3000 cm-1; 饱和碳(除三元环外) < 3000 cm-1。 不饱和碳的 C-H 伸缩振动吸收峰强度较低,往往在 > 3000 cm-1处以饱和碳的 C-H 吸收峰的小肩峰的形式出现。
华东理工大学——王朝霞课件 1
产生红外光谱的必要条件: 1. 红外辐射光的频率与分子振动的频率相当,才能满足分子振 动能级跃迁所需的能量,而产生吸收光谱。 2. 只有能引起分子偶极矩的变化的振动才能产生 IR光谱。 完 全 对 称 的 分 子 H2 、 O2 、 N2 不 会 产 生 红 外 吸 收 光 谱 。 H―C≡C―H 、 R―C≡C―R , 其 C≡C ( 三键 )振 动 也不 能 引起红外吸收。 红外光谱 官能团区 ( 4000-1500 cm -1) 由分子的伸缩振动导致 , 用于鉴定各种不同官能团 指纹区 ( 1500-650 cm-1) 分子弯曲及伸缩振动吸收峰 , 多用于鉴定基团的结合方式
红外光谱( infrared spectroscopy
缩写为IR)
由于分子吸收了红外线的能量并导致分子内振动能级的跃 迁而产生的记录信号。 IR谱主要提供分子中官能团的结构信息 。
I T度。
横坐标:波数(σ) 400~4000 cm-1;表示吸收峰的位置。 纵坐标:透过率( T %),表示吸收强度。 T↓,表明吸收的越好,故曲线低谷表示是一个好的吸收带。
华东理工大学——王朝霞课件
5
-NH2:
与 –OH 相似,游离的 –NH2 在 3300~3500 cm-1,缔合 后吸收峰的位置会降低 100 cm-1,这里要区别几种不同的胺 :
①伯胺有两个吸收峰,原因在 –NH2 有两个 N-H键,振动有 对称和非对称两种伸缩振动,所以与 –OH区别较大,吸收 强度比–OH弱; ②仲胺只有一种振动,吸收峰比 –OH 要尖锐; ③叔胺因 N 上无 H ,所以在此区域无吸收。
华东理工大学——王朝霞课件
9
苯环取代的判断
770~730cm-1 710~690cm-1
尖、强
一取代 二取代(邻位) 二取代(间位) 二取代(对位)
770~735cm -1
810~750cm-1 710~690cm -1 833~810cm-1
强
强 中 强
华东理工大学——王朝霞课件
10
红外谱图解析
2
华东理工大学——王朝霞课件
Y- H 伸缩振动区 2500~3700 cm-1, Y = O、 N、 C。 Y≡Z 三键和累积双键伸缩振动区 2100~2400 cm-1,主要是:C≡C、C≡N 三键和C=C=C、C=N=O 等累积双 键的伸缩振动吸收峰。 Y= Z双键伸缩振动区 1600~1800 cm-1,主要是:C=O、 C= N、C=C等双键。
甲基或亚甲基如果与氧原子相连,吸收峰的位置会向 较低波数移动。
华东理工大学——王朝霞课件
8
芳烃:
在3110~3010 cm-1有 C=C-H伸缩振动产生的中强吸收峰, 在1600~1450 cm-1处有苯环 C=C伸缩振动产生的4个吸收峰, 其中 1600 cm-1和 1500 cm-1较强。
C≡C-H 在 ~3300 cm-1 有很尖锐的吸收峰,不易和其他不 饱和 C-H 吸收峰混淆。
华东理工大学——王朝霞课件
7
饱和碳的 C-H 伸缩振动一般可见四个吸收峰,其中 CH3两个: ~2960cm-1、 ~2870cm-1; -CH2- 两个: ~2925cm-1 、 ~2850cm-1。由此两组峰的强度可大致判断甲基和亚甲基 的比例。 CH3 在 ~1380、 CH2在 ~1460cm-1 处同时有吸收,而前一 吸收峰发生分叉时表示偕二甲基(两甲基连在同一碳原子 上)。
官能团区(高频区) 1500-4000 cm -1
红 外 谱 图
指纹区(低频区) 650-1500 cm -1
主要是:C-C、C-N、C-O等单 键和各种弯曲振动的吸收峰,其特 点是谱带密集、难以辨认。
3
华东理工大学——王朝霞课件
各主要官能团红外光谱的特征吸收峰频率
4000cm
-1
650cm-1
3600-3200 NH, OH d, br, s 3300
1. 观察特征频率区,找出特征吸收峰,判断苯环、双 键、羰基、三键、羟基、胺基等官能团,以确定所 属化合物的类型。
2. 观察指纹区,进一步确定基团的结合方式。指纹区 对用已知物鉴别未知物十分有用。
华东理工大学——王朝霞课件
11
例:
1. 3030cm-1 =C—H伸缩振动; 2. C—H 伸缩振动; 3. 1625cm-1 C= C伸缩振动; 4. C—H( —CH3、 —CH2)面内 弯曲振动;
华东理工大学——王朝霞课件 12
三者的异同点: 1. 缔 合 O—H 的 伸缩 振 动 吸收峰:均出现在 3350 cm-1处左右,差距不大 。 2. C—O 键 的 伸 缩 振 动 吸 收峰有明显的差异: 伯醇: 1050~ 1085 cm-1; 仲醇: 1100~ 1125 cm-1; 叔醇: 1150~ 1120cm-1。
C C H
2700 -CHO double
2960-2850 -C-H strong
2260-2100
C C
variable
1680-1620 or 1600-1500 C=C variable 1850-1690 C=O Acids, esters Ketones Aldehydes very strong
华东理工大学——王朝霞课件
13
例:某化合物分子式为C12H24O2,推测结构。
华东理工大学——王朝霞课件
14
解 : 由最强的吸收峰 1703 cm-1 知此化合物含羰基,与不饱 和度为1吻合; 2920 cm-1 、 2851cm-1 处吸收很强,而 2956 cm-1 、 2866 cm-1处吸收较弱,说明-CH2-的数目多于-CH3的数目; 在723cm-1处(相当于720cm-1处)有吸收峰,证明有长 链的 -CH2-; 2956~2851cm-1的吸收是叠加在另一个宽峰之上,从分 子式中含2个氧原子,分析此宽峰来自-OH; 所以此化合物应该是一个含长碳链的羧酸: CH3-(CH2)10-COOH
