备战高考化学压轴题专题化学反应的速率与限度的经典推断题综合题含答案解析
备战高考化学化学反应的速率与限度推断题综合题含详细答案

备战高考化学化学反应的速率与限度推断题综合题含详细答案一、化学反应的速率与限度练习题(含详细答案解析)1.某反应在体积为5L 的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A 、B 、C 均为气体)。
(1)该反应的化学方程式为_______________。
(2)反应开始至2分钟时,B 的平均反应速率为_______________。
(3)能说明该反应已达到平衡状态的是_______________。
A .v(A)=2v(B) B .容器内气体密度不变 C .v 逆(A)=v 正(C)D .各组分的物质的量相等E. 混合气体的平均相对分子质量不再改变的状态 (4)由图求得平衡时A 的转化率为_______________。
(5)下表是该小组研究影响过氧化氢H 2O 2分解速率的因素时采集的一组数据:用2210mL?H O 制取2150mLO 所需的时间(秒)30%H 2O 2 15%H 2O 2 10%H 2O 2 5%H 2O 2无催化剂、不加热 几乎不反应 几乎不反应 几乎不反应 几乎不反应 无催化剂、加热360s480s 540s 720s MnO 2催化剂、加热 10s25s60s120s①该研究小组在设计方案时。
考虑了浓度、_______________、_______________等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_______________。
(6)将质量相同但聚集状态不同的2MnO 分别加入到5mL5%的双氧水中,并用带火星的木条测试。
测定结果如下: 催化剂()2MnO操作情况观察结果反应完成所需的时间①写出22H O 发生分解的化学反应方程式_______________。
②实验结果说明催化剂作用的大小与_______________有关。
【答案】2A(g)+B(g)⇌2C (g) 0.1 mol/(L∙min) C E 40% 温度 催化剂 增大反应物浓度越大,可以加快反应速率;升高温度,可以加快化学反应速率;使用合适的催化剂,可以加快化学反应速率;(答其中一条即可) 2H 2O 22MnO ==2H 2O+ O 2↑ 固体的接触面积【解析】 【分析】通过各物质的物质的量变化与计量系数呈正比,可得反应式为2A(g)+B(g)⇌2C (g),同时通过变化量可以就算化学反应速率以及反应物的转化率;平衡状态的判定:A.v(A)=2v(B) ,没有体现正逆方向,不能判定是否达到平衡,错误;B.容器内气体密度不变,该体系从开始反应到平衡,密度是定值没有变化,不能判定是否达到平衡状态,错误;C.v 逆(A)=v 正(C),不同物质正逆反应速率呈计量系数比,可以判定达到平衡,正确;D.各组分的物质的量相等,不能作判定,错误,可以改成各物质的量保持不变,可判定平衡;E.混合气体的平均相对分子质量在数值上等于摩尔质量M ,由于前后气体粒子数目可变,则混合气体的相对分子质量和M 是变量可以作平衡的判定依据,正确;根据表格,探究双氧水的浓度、反应的温度、催化剂对过氧化氢H 2O 2分解速率的影响,在探究不同的因素时才用控制变量法来探究可得结果。
备战高考化学压轴题之化学反应的速率与限度(备战高考题型整理,突破提升)附答案解析

备战高考化学压轴题之化学反应的速率与限度(备战高考题型整理,突破提升)附答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH 2COONH4(s)2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___(填选项);A.2v生(NH3)=v耗(CO2)B.密闭容器中氨气的物质的量不变C.容器中CO2与NH3的物质的量之比保持不变D.密闭容器中总压强保持不变E.形成6个N-H键的同时有2个C=O键断裂(2)能使该反应的反应速率增大的是___(填选项);A.及时分离出CO2气体B.适当升高温度C.加入少量NH2COONH4(s)D.选择高效催化剂(3)如图所示,上述反应中断开反应物中化学键吸收的能量___形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。
【答案】AC BD 大于【解析】【分析】(1)根据化学平衡状态的特征解答;(2)增大浓度或升高温度或加催化剂可加快反应速率来解答;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,结合化学键分析解答。
【详解】(1)A.平衡时应有v生(NH3)=2v耗(CO2),所以2v生(NH3)=v耗(CO2)时,反应没有达到平衡状态,故A错误;B.密闭容器中氨气的物质的量不变,说明正、逆反应速率相等,可以判定反应达到平衡状态,故B正确;C.只要反应发生,容器中CO2与NH3的物质的量之比就是2:1,始终保持不变,不能判定反应是否达平衡状态,故C错误;D.密闭容器中总压强保持不变,说明气体的总物质的量不变,反应达平衡状态,故D正确;E.形成6个N-H键等效于2个C=O键形成的同时有2个C=O键断裂,正、逆反应速率相等,达平衡状态,故E正确;故答案为AC;(2)A.及时分离出CO2气体,生成物浓度减小,反应速率减小,故A错误;B.适当升高温度,反应速率加快,故B正确;C.加入少量NH2COONH4(s),固体物质量变但浓度不变,故C错误;D.选择高效催化剂,反应速率加快,故D正确;故答案为:BD;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,即反应中断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量。
高考化学——化学反应的速率与限度的推断题综合压轴题专题复习及答案解析

高考化学——化学反应的速率与限度的推断题综合压轴题专题复习及答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.某温度下在2L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。
(1)该反应的化学方程式是________________________(2)若A、B、C均为气体,10min后反应达到平衡,①此时体系的压强是开始时的________倍。
②在该条件达到平衡时反应物的转化率为________%(计算结果保留1位小数)(3)关于该反应的说法正确的是_________。
a.到达10min时停止反应b.在到达10min之前C气体的消耗速率大于它的生成速率c.在10min时B气体的正反应速率等于逆反应速率【答案】2C A+3B 97或1.29或1.3 66.7% b、c【解析】【分析】(1)由图可知,C是反应物,物质的量分别减少2mol,A、B生成物,物质的量增加1mol、3mol,物质的量变化比等于系数比;(2)①体系的压强比等于物质的量比;②转化率=变化量÷初始量×100%;(3)根据化学平衡的定义判断;【详解】(1)由图可知,C是反应物,物质的量减少2mol,A、B生成物,物质的量分别增加1mol 、3mol,物质的量变化比等于系数比,所以该反应的化学方程式为:2C A+3B;(2)①体系的压强比等于物质的量比,反应前气体总物质的量是7mol、反应后气体总物质的量是9mol,所以此时体系的压强是开始时的97倍;②转化率=变化量÷初始量×100%=2÷3×100%=66.7%;(3)a.根据图象,到达10min时反应达到平衡状态,正逆反应速率相等但不为0,反应没有停止,故a错误;b.在到达10min之前,C的物质的量减少,所以 C气体的消耗速率大于它的生成速率,故b 正确;c.在10min时反应达到平衡状态,所以B气体的正反应速率等于逆反应速率,故c正确;选bc。
高考化学压轴题专题化学反应的速率与限度的经典推断题综合题及答案解析

高考化学压轴题专题化学反应的速率与限度的经典推断题综合题及答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH 2COONH4(s)2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___(填选项);A.2v生(NH3)=v耗(CO2)B.密闭容器中氨气的物质的量不变C.容器中CO2与NH3的物质的量之比保持不变D.密闭容器中总压强保持不变E.形成6个N-H键的同时有2个C=O键断裂(2)能使该反应的反应速率增大的是___(填选项);A.及时分离出CO2气体B.适当升高温度C.加入少量NH2COONH4(s)D.选择高效催化剂(3)如图所示,上述反应中断开反应物中化学键吸收的能量___形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。
【答案】AC BD 大于【解析】【分析】(1)根据化学平衡状态的特征解答;(2)增大浓度或升高温度或加催化剂可加快反应速率来解答;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,结合化学键分析解答。
【详解】(1)A.平衡时应有v生(NH3)=2v耗(CO2),所以2v生(NH3)=v耗(CO2)时,反应没有达到平衡状态,故A错误;B.密闭容器中氨气的物质的量不变,说明正、逆反应速率相等,可以判定反应达到平衡状态,故B正确;C.只要反应发生,容器中CO2与NH3的物质的量之比就是2:1,始终保持不变,不能判定反应是否达平衡状态,故C错误;D.密闭容器中总压强保持不变,说明气体的总物质的量不变,反应达平衡状态,故D正确;E.形成6个N-H键等效于2个C=O键形成的同时有2个C=O键断裂,正、逆反应速率相等,达平衡状态,故E正确;故答案为AC;(2)A.及时分离出CO2气体,生成物浓度减小,反应速率减小,故A错误;B.适当升高温度,反应速率加快,故B正确;C.加入少量NH2COONH4(s),固体物质量变但浓度不变,故C错误;D.选择高效催化剂,反应速率加快,故D正确;故答案为:BD;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,即反应中断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量。
高考化学压轴题专题化学反应的速率与限度的经典推断题综合题含答案解析
高考化学压轴题专题化学反应的速率与限度的经典推断题综合题含答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.新型材料 AIN 应用前景广泛,对其制备过程的研究成为热点。
(1)将物质的量均为a mol 的 Al2O3与N2充入恒温恒容密闭容器中,控制温度发生反应:2Al2O3(s)+2N2(g) 4AlN(s) +3O2(g) △H>0。
①下列可作为反应达到平衡的判据是_________(填序号)。
A.固体的质量不再改变B.2v正(N2)=3v逆(O 2)C.△H不变D.容器内气体的压强不变E.N2分子数与 O2分子数比为 2:3②在起始压强为p的反应体系中,平衡时 N2的转化率为α,则上述反应的平衡常数K p__________(对于气相反应,用某组分 B 的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作K p,如p(B) =p总·x(B) ,p总为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
③为促进反应的进行,实际生产中需加入焦炭,其原因是____________。
(2)铝粉与 N2在一定温度下可直接生成 AlN,加入少量 NH4Cl 固体可促进反应。
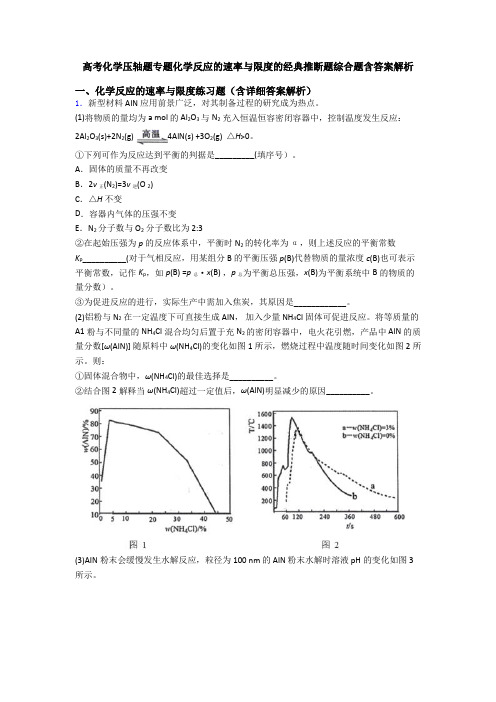
将等质量的A1粉与不同量的 NH4Cl混合均匀后置于充 N2的密闭容器中,电火花引燃,产品中 AlN的质量分数[ω(AlN)] 随原料中ω(NH4Cl)的变化如图1所示,燃烧过程中温度随时间变化如图2所示。
则:①固体混合物中,ω(NH4Cl)的最佳选择是__________。
②结合图2解释当ω(NH4Cl)超过一定值后,ω(AlN)明显减少的原因__________。
(3)AIN粉末会缓慢发生水解反应,粒径为100 nm 的 AlN 粉末水解时溶液 pH的变化如图3 所示。
①AlN 粉末水解的化学方程式是______________。
②相同条件下,请在图3中画出粒径为40 nm 的AlN粉末水解的变化曲线____________。
备战高考化学—化学反应的速率与限度的推断题综合压轴题专题复习附答案解析

备战高考化学—化学反应的速率与限度的推断题综合压轴题专题复习附答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.(1)已知3H 2(g)+N 2(g)2NH 3(g),某温度下,在容积恒定为2.0L 的密闭容器中充入2.0molN 2和2.0molH 2,一段时间后反应达平衡状态,实验数据如下表所示: t/s50 150 250 350 n(NH 3)/mol 00.240.360.400.400~50s 内的平均反应速率v(N 2)=__。
(2)已知:键能指在标准状况下,将1mol 气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E 表示,单位为kJ/mol 。
N ≡N 的键能为946kJ/mol ,H-H 的键能为436kJ/mol ,N-H 的键能为391kJ/mol ,则生成1molNH 3过程中__(填“吸收”或“放出”)的能量为__。
(3)为加快反应速率,可以采取的措施是__。
a.降低温度b.增大压强c.恒容时充入He 气d.恒压时充入He 气e.及时分离NH 3 (4)CO 2的回收与利用是科学家研究的热点课题,可利用CH 4与CO 2制备“合成气”(CO 、H 2)。
科学家提出制备“合成气”反应历程分两步: 反应①:CH 4(g)C(ads)+2H 2(g)(慢反应)反应②:C(ads)+CO 2(g)2CO(g)(快反应)上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:CH 4与CO 2制备“合成气”的热化学方程式为___。
能量变化图中:E 5+E 1___E 4+E 2(填“>”、“<”或“=”)。
【答案】3111.210mol L s ---⨯⋅⋅ 放出 46kJ b()()()()()42231CH g +CO g 2CO g +2H g Δ=+E -E kJ/mol H ƒ <【解析】 【分析】 【详解】(1)根据化学反应速率之比等于物质对应计量数之比可知,0~50s 内的平均反应速率()()311230.24mol112L N NH 1.210mol L s 2250sv v ---==⨯=⨯⋅⋅;(2)该反应中反应物总键能为(3×436+946)kJ/mol=2254 kJ/mol ,生成物的总键能为6×391 kJ/mol=2346 kJ/mol ,反应物总键能小于生成物总键能,由此可知,生成2molNH 3时,放出(2346-2254) kJ=92 kJ 能量,则生成1molNH 3过程中放出能量为92kJ=46kJ 2; (3)a .降低温度会使化学反应速率降低,故a 不符合题意; b .增大压强能够增大化学反应速率,故b 符合题意;c .恒容时充入He 气,各组分的浓度未发生改变,化学反应速率不变,故c 不符合题意;d .恒压时充入He 气,容器体积将增大,各组分浓度将减小,化学反应速率将减小,故d 不符合题意;e .及时分离NH 3,将使体系内压强降低,化学反应速率将减小,故e 不符合题意; 故答案为:b ;(4)由图可知,1molCH 4(g)与1molCO 2(g)的总能量为E 1kJ ,2molCO(g)与2molH 2(g)的总能量为E 3kJ ,生成物总能量高于反应物总能量,该反应为吸热反应,则由CH 4与CO 2制备“合成气”的热化学方程式为:()()()()()42231CH g +CO g 2CO g +2H g Δ=+E -E kJ/mol H ƒ;反应①为慢反应,反应②为快反应,由此可知反应①的活化能大于反应②的活化能,即E 4-E 1>E 5-E 2,故E 5+E 1<E 4+E 2。
备战高考化学专题训练---化学反应的速率与限度的推断题综合题分类附答案解析

备战高考化学专题训练---化学反应的速率与限度的推断题综合题分类附答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.能源与材料、信息一起被称为现代社会发展的三大支柱。
面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。
某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):时间/min12345氢气体积/mL(标况)100240464576620①哪一段时间内反应速率最大:__________min(填“0~1”“1~2”“2~3”“3~4”或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。
他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。
你认为可行的是____________(填字母序号)。
A.KCl溶液 B.浓盐酸 C.蒸馏水 D.CuSO4溶液(2)如图为原电池装置示意图:①将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是_______(填字母)。
A.铝片、铜片 B.铜片、铝片C.铝片、铝片 D.铜片、铜片写出插入浓硝酸溶液中形成的原电池的负极反应式:_______________。
②若A为Cu,B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2。
写出B电极反应式:________;该电池在工作时,A电极的质量将_____(填“增加”“减小”或“不变”)。
若该电池反应消耗了0.1mol FeCl3,则转移电子的数目为_______。
【答案】2~3 AC B Cu-2e−=Cu2+ Fe3++e−=Fe2+减小 0.1N A【解析】【分析】(1)①先分析各个时间段生成氢气的体积,然后确定反应速率最大的时间段。
高考化学压轴题专题化学反应的速率与限度的经典推断题综合题附答案

高考化学压轴题专题化学反应的速率与限度的经典推断题综合题附答案一、化学反应的速率与限度练习题(含详细答案解析)1.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH 2COONH4(s)2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___(填选项);A.2v生(NH3)=v耗(CO2)B.密闭容器中氨气的物质的量不变C.容器中CO2与NH3的物质的量之比保持不变D.密闭容器中总压强保持不变E.形成6个N-H键的同时有2个C=O键断裂(2)能使该反应的反应速率增大的是___(填选项);A.及时分离出CO2气体B.适当升高温度C.加入少量NH2COONH4(s)D.选择高效催化剂(3)如图所示,上述反应中断开反应物中化学键吸收的能量___形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。
【答案】AC BD 大于【解析】【分析】(1)根据化学平衡状态的特征解答;(2)增大浓度或升高温度或加催化剂可加快反应速率来解答;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,结合化学键分析解答。
【详解】(1)A.平衡时应有v生(NH3)=2v耗(CO2),所以2v生(NH3)=v耗(CO2)时,反应没有达到平衡状态,故A错误;B.密闭容器中氨气的物质的量不变,说明正、逆反应速率相等,可以判定反应达到平衡状态,故B正确;C.只要反应发生,容器中CO2与NH3的物质的量之比就是2:1,始终保持不变,不能判定反应是否达平衡状态,故C错误;D.密闭容器中总压强保持不变,说明气体的总物质的量不变,反应达平衡状态,故D正确;E.形成6个N-H键等效于2个C=O键形成的同时有2个C=O键断裂,正、逆反应速率相等,达平衡状态,故E正确;故答案为AC;(2)A.及时分离出CO2气体,生成物浓度减小,反应速率减小,故A错误;B.适当升高温度,反应速率加快,故B正确;C.加入少量NH2COONH4(s),固体物质量变但浓度不变,故C错误;D.选择高效催化剂,反应速率加快,故D正确;故答案为:BD;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,即反应中断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
备战高考化学压轴题专题化学反应的速率与限度的经典推断题综合题含答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。
科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式:2NO+2CO 催化剂2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO 浓度如表:请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):(1)若1molNO和1molCO的总能量比1molCO2和0.5molN2的总能量大,则上述反应的H___0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)计算4s时NO的转化率为____________。
(4)下列措施能提高NO和CO转变成CO2和N2的反应速率的是______(填序号)。
A.选用更有效的催化剂B.升高反应体系的温度C.降低反应体系的温度D.缩小容器的体积(5)由上表数据可知,该反应在第______s达到化学平衡状态。
假如上述反应在密闭恒容容器中进行,判断该反应是否达到平衡的依据为________(填序号)。
A.压强不随时间改变B.气体的密度不随时间改变C.c(NO)不随时间改变D.单位时间里消耗NO和CO的物质的量相等(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。
为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
①请在上表格中填入剩余的实验条件数据_____、_____、______、______、______。
②请在给出的坐标图中,画出上表中的Ⅰ、Ⅱ两个实验条件下混合气体中NO 浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________。
【答案】< 1.875⨯10-4mol ·L -1·s -1 90% ABD 4 AC 5.80⨯10-3 280 1.20⨯10-31.20⨯10-3 5.80⨯10-3【解析】 【分析】反应热的正负可根据反应物和生成物的总能量的大小比较;能提高反应速率的因素主要有增大浓度、使用催化剂、升高温度、增大表面积、构成原电池等,压强能否改变反应速率要看是否改变了浓度;反应是否达到平衡可以从速率(正逆反应速率是否相等)、量(是否保持不变)、压强、气体平均密度,气体平均摩尔质量、颜色等方面判断;验证多个因素对化学反应速率的影响规律,要控制变量做对比实验,每组对比实验只能有一个变量。
【详解】(1)反应物比生成物的总能量大,说明是放热反应,H ∆<0;(2)V(N 2)=0.5V(NO)= 341.0010mol / 2.5010mol /0.52L Ls--⨯-⨯⨯=1.875⨯10-4mol · L -1· s -1。
(3)NO 的转化率等于反应掉的NO 除以原有总的NO ,可列式3431.0010 1.00101.0010---⨯-⨯⨯=90% 。
(4)催化剂可以加快反应速率,A 正确;温度越高,反应速率越快,B 正确,C 错误;缩小容器体积,会增大各组分的浓度,浓度越高,反应速率越快,D 正确。
故答案选ABD ;(5)由表中数据可知,第4s 后,反应物的浓度不再变化,达到平衡;A .恒温恒压下,压强不变意味着气体的总物质的量不变,而该反应两边的气体计量数之和不同,气体的总物质的量不变说明达到平衡,A正确;B.气体的密度等于气体的质量除以体积,因为所有组分都是气体,气体的质量不变,因为恒容容器,所以气体不变,所以气体的密度永远不变,与平衡没有关系,B错误;C.c(NO)不变,意味着达到平衡,C正确;D.因为NO和CO的化学计量数之比为1:1,且都是反应物,所以单位时间里消耗NO和CO的物质的量一定相等,不能说明达到平衡,D错误;故答案:4;AC;(6)①验证多个因素对化学反应速率的影响规律,要控制变量做对比实验。
I和II因为催化剂的比表面积不同,所以其他条件应该是一样的,研究的是催化剂比表面积对化学反应速率的影响规律;II和III因为温度不一样,所以其他条件应该是一样的,研究的是温度对化学反应速率的影响规律;故答案是:5.80⨯10-3,280,1.20⨯10-3,1.20⨯10-3 ,5.80⨯10-3 ;②I和II的区别是催化剂的比表面积,催化剂加快反应速率,所以II更快的达到平衡,但催化剂不影响平衡,所以I和II平衡时NO的浓度一样,c(NO)变化曲线如图:。
【点睛】验证多个因素对某物质或某性质的影响规律,要控制变量做对比实验,每组对比实验只能有一个变量。
2.化学反应速率和限度与生产、生活密切相关。
(1)某同学为了探究锌与硫酸反应过程中的速率变化,在 400mL 稀硫酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):①哪一时间段反应速率最大_______min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”),原因是________。
②求 3~4 分钟时间段以盐酸的浓度变化来表示的该反应速率________设溶液体积不变)。
(2)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
请回答下列问题:①硫酸铜溶液可以加快氢气生成速率的原因是_______。
②实验室中现有 Na2SO4、MgSO4、Ag2SO4、K2SO4等 4 种溶液,可与实验中 CuSO4溶液起相似作用的是_______。
③要减慢上述实验中气体产生速率,可采取的合力措施有_______、_______(答两种)。
(3)某温度下在 4 L 密闭容器中,X、Y、Z 三种气态物质的物质的量随时间变化曲线如图。
①该反应的化学方程式是_______。
②该反应达到平衡状态的标志是_______(填字母)A.Y 的体积分数在混合气体中保持不变 B.X、Y 的反应速率比为 3:1C.容器内气体压强保持不变 D.容器内气体的总质量保持不变E.生成 1 mol Y 的同时消耗 2 mol Z③2 min 内 Y 的转化率为_______。
【答案】2~3 因该反应是放热反应,此时温度高且盐酸浓度较大,所以反应速率较快.0.025 mol·L-1·min-1 CuSO4与 Zn 反应生成的 Cu 附着在 Zn 表面形成铜锌原电池加快了化学反应速率; Ag2SO4适当增加硫酸的浓度增加锌粒的表面积;升高温度等(答两种即可)3X(g)+Y(g)⇌2Z(g) AC 10%【解析】【分析】(1)①相同时间内收集的气体体积越多,该反应速率越快;温度越高化学反应速率越快;②先计算生成氢气物质的量,再根据关系式计算消耗n(HCl),利用v=nV tVV计算盐酸反应速率;(2) Zn和硫酸的反应中加入少量的CuSO4溶液,能置换出一定量Cu,在溶液中形成Cu/Zn 原电池,原电池反应比化学反应速率快;②所给四种溶液中只Zn只能置换出Ag;③从影响反应速率的因素分析;(3)①根据图知,随着反应进行,X、Y的物质的量减少而Z的物质的量增加,则X和Y是反应物而Z是生成物,反应达到平衡时,△n(X)=(1.0-0.4)mol=0.6mol、△n(Y)=(1.0-0.8)mol=0.2mol、△n(Z)=(0.5-0.1)mol=0.4mol,同一可逆反应中同一段时间内参加反应的各物质的物质的量变化量之比等于其计算之比,据此确定化学方程式;②可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变;③Y的转化率=()()n Yn Y反应的反应初始×100%;【详解】(1)①相同通条件下,反应速率越大,相同时间内收集的气体越多;由表中数据可知,反应速率最大的时间段是2∼3min,原因是:该反应是放热反应,温度越高,反应速率越大;②3∼4分钟时间段,收集的氢气体积=(576−464)mL=112mL,n(H2)=0.11222.4/LL mol=0.005mol,根据氢气和HCl关系式得消耗的n(HCl)=2n(H2)=2×0.005mol=0.01mol,则v(HCl)=0.01mol0.4L1min⨯=0.025 mol/(L⋅min);(2)Zn和硫酸的反应中加入少量的CuSO4溶液,能置换出一定量Cu,在溶液中形成Cu/Zn原电池,而加快化学反应速率;②所给四种溶液中只Zn只能置换出Ag,即Ag2SO4与CuSO4溶液具有相似的作用;③为加快Zn和硫酸的反应速率可从升温、适当增大硫酸的浓度、增大锌的比表面积等角度考虑,可采取的合力措施有:增加锌的表面积;升高温度或适当增大硫酸的浓度等;(3)①根据图知,随着反应进行,X、Y的物质的量减少而Z的物质的量增加,则X和Y是反应物而Z是生成物,反应达到平衡时,△n(X)=(1.0−0.4)mol=0.6mol、△n(Y)=(1.0−0.8)mol=0.2mol、△n(Z)=(0.5−0.1)mol=0.4mol,同一可逆反应中同一段时间内参加反应的各物质的物质的量变化量之比等于其计算之比,X、Y、Z的计量数之比=0.6mol:0.2mol:0.4mol=3:1:2,则该反应方程式为3X(g)+Y(g)⇌2Z(g);②A.Y的体积分数在混合气体中保持不变,说明各物质的量不变,反应达到平衡状态,故A正确;B.X、Y的反应速率比为3:1时,如果反应速率都是指同一方向的反应速率,则该反应不一定达到平衡状态,故B错误;C.反应前后气体压强减小,当容器内气体压强保持不变时,各物质的物质的量不变,反应达到平衡状态,故C正确;D.容器内气体的总质量一直保持不变,故D错误;E.生成1mol Y的同时消耗2molZ,所描述的为同向反应过程,不能判断反应达到平衡状态,故E错误;答案选AC;③Y的转化率=()()n Yn Y反应的反应初始×100% =10.91-×100%=10%。
3.某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
根据图中数据,完成下列问题:(1)该反应的化学方程____;(2)反应开始至2min,气体Z的平均反应速率为_____;(3)达到平衡后,下列说法不正确的是_____。
A.X、Y、Z的浓度之比是1:2:3B.X的消耗速率和Y的生成速率相等C.Z的浓度保持不变【答案】3X+2Y3Z 0.125mol/ ( L n min) B【解析】【分析】【详解】(1)根据图知,随着反应的进行X、Y的物质的量减少,而Z的物质的量增大,所以X和Y 是反应物、Z是生成物,10min时反应达到平衡状态,则参加反应的△n (X) = (1.00-0.25)mol=0.75mol、△n(Y)=(1.00-0.50) mol=0.50mol、△n ( Z)=(0.75-0) mol=0.75mol,同一可逆反应中同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.75mol: 050mol:0.75mol=3:2:3所以该反应方程式:3X+2Y3Z;(2) 0-2min内Z的平均反应速率v=ctVn=0.50mol2L2min=0.125mol/ ( L n min),故答案为:0.125mol/ ( L n min);(3) A.相同容器中,X、Y、Z的浓度之比等于其物质的量之比=0.25mol:0.50mol:0.75mol=1:2:3,故A正确;B.该反应中X、Y的计量数之比为3:2,当X的消耗速率与Y的生成速率之比为3:2时该反应达到平衡状态,所以当X的消耗速率和Y的生成速率相等时该反应没有达到平衡状态,故B错误;C.当Z的浓度保持不变时,正逆反应速率相等,可逆反应达到平衡状态,故C正确;故选B。
