第十三章 醛和酮(一)醛和酮的命名
醛、酮的结构、命名

2,3-二甲基-4-戊烯醛
CH3—CH=CH—CH—C—CH3 CH3
3-甲基-4-己烯-2-酮
(3)含醛基、酮基的碳链上的氢被芳环或环烷基 取代,就把芳环或环烷基当作主链上的取代基看待:
H3C CH CHO O C CH2CH3
2-苯丙醛
1-环己基-1-丙酮
醛基与芳环、脂环或杂环上的碳原子直接相连 时,它们的命名可在相应的环系名称之后加上“醛” 字。 CHO
CHO
1
2
CHO
环己醛
1,2-萘二醛
(4)多元醛、酮命名
含有两个以上羰基的化合物,可用二醛、 二酮等,醛作取代基时,可用词头“甲酰基”或 “氧代”表示;酮作取代时,用词头“氧代”表 示。
O 4 CH3CCH2CCH3 2 3
δ γ β α CH3CH=CHCH 2CHO β —戊烯醛 丁烯醛
O C C C C C H
OH CH3—CH—CH2CHO β-羟基丁醛
O CH3CH—C—CHCH3 Br Br α,α'-二溴-3-戊酮
(2)不饱和醛、酮的命名
从靠近羰基一端给主链编号。命名 称为“某烯醛(酮)”或“某炔醛 (酮)”。
3-甲基丁醛
H5C6
CH CHO
CH3
2-苯基丙醛
O
O
O
H3C
3-甲基环戊酮
CH3CH2-C-CH2CH3
3-戊酮
CH3-C-CH2-C-CH3
2,4-戊二酮
O
醛、酮碳原子的位次,除用1,2,3,4,…表示 外,也可用α,β,γ…希腊字母表示。α是指官能 团羰基旁第一个位置,β是指第二个位置…。酮中一 边用α,β,γ…,另一边用α’ β’ γ’…。
醛和酮的英文命名

醛的命名 醛基的命名 酮的命名 酮基的命名
本节内容
醛的命名
IUPAC命名法:将相应烃IUPAC名词尾e改成al表 示一元醛;直接在烃名后加dial表示二元醛。
普通命名法:将相应羧酸普通名词尾ic acid改为 aldehyde。
HCHO
methanal 甲醛 (formaldehyde) 蚁醛
普通命名法:用词头for2CH2 C OH
4-methanoylbutanoic acid 4-甲酰基丁酸 (4-formylbutyric acid) 4-甲酰基丁酸
5-oxopentanoic acid 5-氧代戊酸
酮的命名
IUPAC命名法:将相应烃IUPAC名词尾e改成one 表示一元酮;直接在烃名后加dione表示二元酮。
普通命名法:ketone作为母体,其前隔开,写酮 基所连的两个烃基。
CH3COCH3
propanone 丙酮 (acetone) 丙酮
CH3COCH2CH3 2-butanone 2-丁酮 (ethyl methyl ketone) 甲乙酮
酮的命名
CH3COCH2CH2Cl 4-chloro-2-butanone 4-氯-2-丁酮
CH3CH2COCH2OH 1-hydroxy-2-butanone 1-羟基-2-丁酮
CH3COCOCH3
2,3-butanedione 2,3-丁二酮
(CH3)2C CHCOCH C(CH3)2
2,6-dimethyl-2,5-heptadien-4-one 2,6-二甲基-2,5-庚二烯-4-酮
酮基的命名
IUPAC命名法:用词头oxo,意为氧代。 普通命名法:用词头keto,意为氧代。
醛、酮

(2)负氢还原法 ①LiAlH4及NaBH4
氢化铝锂(LiAlH4)是强还原剂,它 对羰基、硝基、氰基、羧基、酯、酰胺、 卤烃等都进行还原。氢化铝锂非常活泼, 遇到含有活泼氢的化合物迅速分解,所 以使用LiAlH4为还原剂时,反应是在醚 溶液中进行的。由于LiAlH4分子中的四 个氢都是负性的,所以它可还原四个分 子醛、酮。LiAlH4对C=C,C≡C键不起 作用,可用于 α,β-不饱和醛、酮的选择 性还原。
R + + C O + H CN (R')H R C (R')H CN OH
醛、甲基脂肪酮和C8以下环酮都能反应。
反应机理:
HCN
R
C R' O + CN
-
OHH+
H
+
+ CN
慢
-
R C R'
R C R'
OCN
OH CN
HCN 快
CN+
加成速率:
H H C O> H3C H C O> H3C H3C C O> H3C R R C O> R' C O
O CH3CH2CH2CCH3 O CH3CH2CCH2CH3 O (CH3)2CHCCH3
四、醛、酮的结构
醛酮的官能团是羰基。
O
C O
π键 σ键
SP2杂化
O
电负性 C < O
O
π电子云偏向氧原子
极性双键
五、醛、酮的物理性质
1.甲醛为气体,其40%的水溶液称为福尔马 林, C12以下的醛、酮是液体,其余为固体; 低碳醛有强烈刺激气味,C6~C14的醛、酮有 花果香味。 C=O 与H2O形成氢键,增加在水中的 2. 溶解度。 H3C H HC
有机化学基础知识点整理醛与酮的命名与性质

有机化学基础知识点整理醛与酮的命名与性质【正文开始】有机化学基础知识点整理——醛与酮的命名与性质一、醛的命名与性质醛是一类含有醛基(—CHO)的有机化合物,常见的代表性醛有甲醛、乙醛、丙醛等。
醛的命名遵循一定的规则,主要根据它所附加的碳链的长度来确定前缀和后缀,具体如下:1. 将碳链数目大于三的醛分子命名为“醛”。
例如:乙醛(CH3CHO),己醛(C5H11CHO)。
2. 当醛基所在的碳为主链的一部分时,醛的命名按照碳链命名规则确定。
例如:丁醛(C3H7CHO),己醛(C5H11CHO)。
3. 当醛基不是主链的一部分时,用羟基所在的碳数作为前缀,并在前面加上碳链信息。
例如:羟基在第二个碳上的正丁醇(CH3CH(OH)CH2CHO)。
通过命名规则,我们可以准确命名各种结构的醛化合物,从而更好地了解醛的性质。
醛具有以下几个主要特点:1. 醛具有较高的融点和沸点。
2. 醛具有一定的水溶性,在溶液中可以形成醛醇互变体。
3. 醛具有还原性,可以和氧化剂发生反应。
4. 醛具有与胺和水合物等发生加成反应。
二、酮的命名与性质酮是一类含有酮基(—CO—)的有机化合物,常见的代表性酮有丙酮、己酮等。
酮的命名也遵循一定的规则,与醛的命名规则类似,具体如下:1. 将碳链数目大于三的酮分子命名为“酮”。
例如:丙酮(C3H6O),己酮(C5H10O)。
2. 当酮基所在的碳为主链的一部分时,酮的命名按照碳链命名规则确定。
例如:丁酮(C4H8O),己酮(C5H10O)。
3. 当酮基不是主链的一部分时,用羰基所在的碳数作为前缀,并在前面加上碳链信息。
例如:羰基在第三个碳上的2-丁酮(CH3CH2COCH2CH3)。
酮具有以下几个主要特点:1. 酮具有较低的融点和沸点。
2. 酮在水中基本不溶,但可以溶于有机溶剂。
3. 酮不具有亲核性,不易被亲核试剂攻击。
4. 酮具有与杂环化合物和烷基锂等发生加成反应。
总结:本文对醛和酮的命名和性质进行了整理和总结。
醛和酮的命名和反应特点

醛和酮的命名和反应特点醛和酮是有机化合物中常见的两类功能团,它们在有机合成和生物化学等领域具有重要的地位。
本文将介绍醛和酮的命名规则以及它们的主要反应特点。
一、醛的命名和反应特点醛是含有羰基(C=O)的有机化合物,它们的命名通常根据其碳链长度和取代基来进行。
以下是几个常见的醛的命名示例:1. 甲醛(HCHO)是最简单的醛,也称为福尔马林。
它的命名来自于甲基(CH3)和醛(al)这两个单词的组合。
2. 乙醛(CH3CHO)是一种含有两个碳原子的醛,它的命名来自于乙烯(C2H4)和醛(al)这两个单词的组合。
3. 丁醛(CH3CH2CH2CHO)是一种含有四个碳原子的醛,它的命名来自于丁烯(C4H8)和醛(al)这两个单词的组合。
醛通常具有以下几个反应特点:1. 氧化反应:醛可以被氧化为相应的羧酸。
常见的氧化剂有酸性高锰酸钾(KMnO4)和酸性过氧化氢(H2O2)。
2. 加成反应:醛具有与亲核试剂发生加成反应的能力。
其中最常见的是醛和水(H2O)发生加成反应生成醇。
3. 缩合反应:醛可以与胺或另一个醛发生缩合反应,生成相应的亚胺或醇醛。
这种反应被广泛应用于化学合成中。
二、酮的命名和反应特点酮是由两个碳原子上分别连接有两个烷基或芳基的羰基化合物。
与醛类似,酮的命名也根据碳链长度和取代基来进行。
以下是几个常见的酮的命名示例:1. 丙酮(CH3COCH3)是最简单的酮,它也是只含有三个碳原子的酮。
其命名来自于丙烯(C3H6)和酮(one)这两个单词的组合。
2. 甲基乙基酮(CH3COCH2CH3)是一种含有四个碳原子的酮,它的命名来自于甲基(CH3)、乙基(C2H5)和酮(one)这三个单词的组合。
3. 邻二甲苯酮(C6H4(COCH3)2)是一种含有苯环的酮,它的命名体现了对位取代基的位置关系。
酮的反应特点与醛类似,但也存在一些差异:1. 氧化反应:酮相较醛来说较不容易被氧化,但依然可以通过特定条件下的氧化反应将酮转化为相应的酸。
醛和酮的结构、分类和命名.
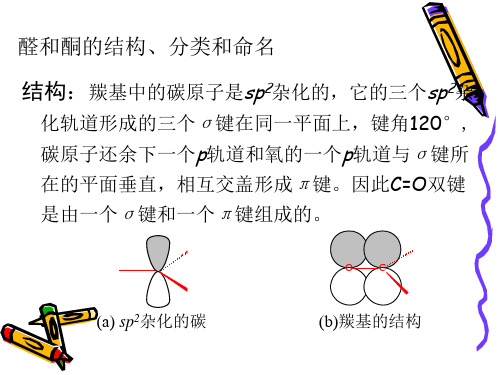
结构:羰基中的碳原子是sp2杂化的,它的三个sp2杂
化轨道形成的三个σ 键在同一平面上,键角120°,
碳原子还余下一个p轨道和氧的一个p轨道与σ 键所
在的平面垂直,相互交盖形成π 键。因此C=O双键
是由一个σ 键和一个π 键组成的。
O C
(a) sp2杂化的碳
(b)羰基的结构
二苯酮 甲基乙基酮
♪根据烃基的饱和或不饱和:分为饱和醛、酮和不饱和醛、酮
♪根据分子中羰基的数目:分为一元、二元或多元醛、酮 ♪脂环酮:脂环的一个或多个CH2被C=O所置换,如环己酮
命名
1、习惯命名法:醛类按分子中碳原子数称某醛(与 醇相似)。包含支链的醛,支链的位次用希腊字母α,
β,γ……表明。紧接着醛基的碳原子为α 碳原子,
其次的为β 碳原子……,依此类推。例如:
乙醛
丙烯醛
α -氯丙醛
酮类按羰基所连的两个烃基来命名(与醚相似)。 例如:
甲基乙基酮
甲基乙烯基酮
甲基-α -氯乙基酮
2、IUPAC命名法:
选含羰基的最长碳链为主链,从靠近羰基一端给主链
编号。醛基因处在链端,因此编号总为1。酮羰基的
位置要标出(个别例外)。
2-甲基丙醛
丁酮
2-甲基-3-戊酮
不饱和醛酮的命名是从靠近羰基一端给主链编号:
3-甲基-4己烯-2-酮
羰基在环内的脂环酮,称为环某酮;若羰基在环外,则
将环作为取代基。
4-甲基环己酮
2-甲基环己基甲醛
命名含有芳基的醛、酮,总是把芳基看成 取代基:
O C H
O C
CH2CH3
苯甲醛
Hale Waihona Puke 1-苯基-1-丙酮酮还有一种衍生物命名法,把酮看成是“甲酮”的衍 生 物,在“甲酮”前边加上两个取代基的名称,“甲” 字可 省略:
《有机化合物的分类和命名》醛酮命名基础

《有机化合物的分类和命名》醛酮命名基础在有机化学的广袤世界中,有机化合物的分类和命名就如同给每一个独特的分子赋予一个专属的身份标识。
而醛和酮作为其中重要的两类化合物,其命名规则具有一定的规律性和系统性。
首先,让我们来了解一下醛和酮的基本结构特征。
醛的官能团是醛基(CHO),醛基中的碳原子与氢原子相连,另一端与烃基相连。
而酮的官能团是羰基(C=O),羰基的碳原子两侧都连接着烃基。
醛的命名相对较为直接。
对于简单的醛,通常以相应的烃基名称加上“醛”字来命名。
比如,含有一个碳原子的醛称为甲醛,含有两个碳原子的醛称为乙醛。
当醛基连接的烃基较为复杂时,就需要将烃基的名称作为母体,醛基作为取代基来命名。
再来看酮的命名。
酮的命名通常是选取含有羰基的最长碳链作为主链,称为“某酮”。
羰基的位置用数字标明,数字从靠近羰基的一端开始计数。
如果分子中存在多个羰基,就需要用“二酮”“三酮”等表示羰基的个数。
为了更清晰地理解醛酮的命名,我们通过一些具体的例子来加以说明。
例如,CH₃CH₂CH₂CHO 这个化合物,我们可以根据其结构,判断出这是一个含有四个碳原子的醛,按照简单醛的命名规则,它被命名为丁醛。
再看一个复杂一点的例子,。
在这个化合物中,醛基连接在苯环上。
此时,我们将苯环作为母体,醛基作为取代基,按照“取代基位置取代基名称母体名称”的顺序,这个化合物被命名为 3-硝基苯甲醛。
对于酮的命名,比如 CH₃COCH₂CH₃,含有四个碳原子,羰基位于第二个碳原子上,所以它被命名为 2-丁酮。
,这个化合物含有两个羰基,且分别位于 2 号和 4 号碳原子上,主链有六个碳原子,因此被命名为 2,4-己二酮。
在实际的命名过程中,还需要注意一些特殊情况。
比如,如果分子中同时存在醛基和其他官能团,醛基的优先级通常较高,优先以醛来命名。
另外,对于一些常见的取代基,我们需要熟悉它们的名称和缩写。
例如,甲基(CH₃)、乙基(CH₃CH₂)、苯基(C₆H₅)等。
醛和酮的分类、结构和命名

01
02
03
酮基
酮的官能团是酮基,其结 构为C=C=O,其中2个C 原子之间形成双键,并与 氧原子形成双键。
酮基的电子分布
酮基中的碳原子为sp杂化, 与氧原子形成双键,同时 与另一个碳原子形成单键。
酮的稳定性
酮的稳定性与其取代基的 性质有关,如甲基、乙基 等烷基可以稳定酮的结构。
醛和酮的反应活性
亲核加成反应
醛和酮可以与亲核试剂发生加成反应,如醇、 胺等。
氧化反应
醛容易被氧化,如被氧化成羧酸;而酮则相 对稳定,不易被氧化。
亲电加成反应
在一定条件下,醛和酮可以发生亲电加成反 应,如与氢氰酸、格氏试剂等反应。
还原反应
醛和酮都可以被还原成醇,如用氢化铝锂还 原。
05 醛和酮的应用
醛在工业上的应用
合成香料
醛是许多香料的主要组成 部分,如香草醛和香豆素 等,用于制造香水和食品 添加剂。
醛和酮在生物体内的生理作用 和代谢机制也是未来研究的重 点,有助于发现新的药物靶点 和生物活性分子。
THANKS FOR WATCHING
感谢您的观看
对未来研究的展望
随着有机化学的发展,醛和酮 的研究将不断深入,有望发现 更多具有重要应用价值的醛和
酮化合物。
对于醛和酮的反应机制和反应 条件的研究,将有助于更好地 理解和控制化学反应,提高化
合物的合成效率。
随着计算化学的发展,计算机 模拟和理论计算在醛和酮的研 究中将发挥越来越重要的作用 ,有助于深入理解其结构和反 应性质。
脂肪族醛是指碳原子之间通过单键连接的醛类化 合物,其通式为R-CHO。
命名规则
脂肪族醛的命名通常采用系统命名法,将醛基作 为取代基,以烃基名称作为母体,在烃基名称后 加上“醛”字。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十三章醛和酮(一) 醛和酮的命名(二) 醛和酮的结构(三) 醛和酮的制法(四) 醛和酮的物理性质(五) 醛和酮的化学性质(六) α,β-不饱和醛、酮的特性(七) 乙烯酮卡宾第十三章醛和酮分类:①根据烃基的不同,可将醛、酮分为:脂肪族醛、酮,芳香族醛、酮;饱和醛、酮,不饱和醛、酮;②根据醛、酮分子中羰基的个数,可分为:一元醛、酮,二元醛、酮等;③根据酮羰基所连的两个烃基是否相同,分为:单酮,混酮。
官能团:醛 R -C -H O酮 (-CHO 为醛基)(两个R 可以相同,也可不同)C O(羰 基)R -C -R°O'(一) 醛和酮的命名(1)普通命名法(2) 系统命名法(一) 醛和酮的命名醛、酮的命名与醇相似。
(1) 普通命名法酮的普通命名法是按照羰基所连接的两个烃基命名。
甲乙酮CH 3CCH 2CH 3OCH 3CH 2CH 2CHO CH 3CHCH 2CHO CH 3CH 3-C-CH=CH 2O 正丁醛异戊醛甲基乙烯基酮CHO 苯甲醛C-CH 3O 苯乙酮C-O二苯甲酮(2) 系统命名法CH 3CHCH 2CHO CH 3CH 3CH 2-C-CH-CH 3O CH 343-甲基丁醛2-甲基-3-戊酮β−甲基丁醛12345苯基丙烯醛3-CH=CH-CHO (肉桂醛)321321CH 3CH=CHCHO CH-CHO CH 32-丁烯醛苯基丙醛2−CH 3C-CH 2-CCH 3O O β−戊二酮戊二酮 2,4-(巴豆醛)1234苯基丙醛α−(二) 醛和酮的结构羰基的结构:C O sp 杂化C O电子云分布: C Oδ−δ+C OCH 3CH 3C OH H2.27D2.85D极性分子 有偶极矩(三) 醛和酮的制法(1)醇的氧化或脱氢(2) 羰基合成(3) 同碳二卤化物水解(4) 羧酸衍生物的还原(5) 芳烃的氧化(6) 芳环上的酰基化(三) 醛和酮的制法(1) 醇的氧化或脱氢RCH 2OH RCHORCOOH及时蒸出1 醇醛酸。
[O]:KMnO 4K 2Cr 2O 7+H 2SO 4CrO 3+吡啶CrO 3+醋酐 丙酮-异丙醇铝等 、、、、。
2 醇酮R --R' OHR -C -R'O氧化到醛、酮,不破坏双键氧化到醛、酮通用,氧化性强,须将生成的醛及时蒸出CH 3(CH 2)5CHCH 3OHCH 3(CH 2)5CCH 3O22724 100 C 。
所以,生成的乙醛很容易脱离体系。
CH 3CH 2OHK 2Cr 2O 7+H 2SO 450 C。
CH 3CHOK Cr O +H SO CH 3COOHb.p 78 C。
b.p 21 C。
b.p 118 C。
例:H 2O 2-辛醇2-辛酮CH 3C-CH=CHCH=CCH=CH 2CH 3OCH 3CHCH=CHCH=CCH=CH 2OHCH 3丙酮,异丙醇铝苯,回流,80%Oppenauer 氧化CH 3-CH -CH 3OHCH 3-C -CH 3O(or ZnO,380 C 。
Cu,300 C 。
)脱氢:(2) 羰基合成由α-烯烃合成多一个碳的醛!CH 2=CH 2 + COCH 3CH 2CHO[Co(CO)],加压CH 2-CH 2C OH 2CH 3CH 2CH 2CHO +CH 3CHCHOCH 3正丁醛(多)异丁醛(少)2CH 3CH=CH 2+CO[Co(CO)4]2,加压CH 3CH-CH 2C O例1:例2:(3) 同碳二卤化物水解该法一般主要用于制备芳香族醛、酮。
例如:BrC-CH 3Cl ClBrCH 2CH 3BrC-CH 3O OH -H 2O2Cl 2间溴乙苯间溴苯乙酮间溴二氯乙苯−α,α−CHCl 2+ H 2O+CHO+ 2HCl苯二氯甲烷苯甲醛或Fe不用碱!因醛对碱敏感(4) 羧酸衍生物的还原(Rosenmond 还原)3OCH 3COCl3OCH 3CHO(1) LiAl(OBu-t)3H,乙醚,-78 C。
(2) H 2O , H + , 60%(2) H 2O , H + , 88%(1) Al(n-Bu)2H , 己烷,-78 C。
CH 3(CH 2)10OC 2H 5OCH 3(CH 2)10CHO三叔丁基氢化铝锂,空间障碍大,还原性不及LiAlH 4↙二丁基氢化铝R ClO + H 2R HO Pd/BaSO 4↙(5) 芳烃的氧化甲基直接与芳环相连时,可被氧化成醛基。
例如甲苯用铬酰氯、铬酐等氧化或催化氧化则生成苯甲醛:CH 3CHO + H 2O+ O 2V 2O 5CH 2CH 3COCH 3+ O 2硬脂酸钴120-130 C。
乙苯用空气氧化可得苯乙酮:CH 3CrO (CH 3CO)2O2CH(OCCH 3)2OCHO二乙酸酯不易被氧化易被氧化α−H,(6) 芳环上的酰基化+ HClCH 3C-ClO +AlCl 3H 3CC O CH 3C O +(90%)(9%)苯甲酰氯+ CH 3CH 2CH 2C-ClO3+ HCl CCH 2CH 2CH 3O(不重排!)AlCl3,Cu2Cl2+ CO + HCl CHO CH3+ CO + HCl AlCl3,Cu2Cl2CH3CHO(46-51%)该反应的本质是亲电取代反应,CO与HCl首先生成[HC+=O]AlCl4-。
加入Cu2Cl2的目的是使反应可在常压下进行,否则需要加压才能完成。
Gattermann-Koch 反应(由苯或烷基苯制芳醛):(四) 醛和酮的物理性质物态:CH 2O 为气体;C 2-C 12醛、酮为液体;C 13以上醛、酮为固体。
沸点:与分子量相近的醇、醚、烃相比,有b.p :醇>醛、酮>醚>烃。
原因:a. 醇分子间可形成氢键,而醛、酮分子间不能形成氢键;b. 醛、酮的偶极矩大于醚、烃的偶极矩:C=O OR R'µ=1.3Dµ=2.8D溶解度:与醇相似。
低级醛、酮可溶于水;高级醛、酮不溶于水。
因为醇、醛、酮都可与水形成氢键:H H C=OHR C=OR H H R'IR光谱:νC=O:1680-1850cm-1(很强峰);注意:丙酮的νC=O 为1715 cm-1,乙醛的νC=O为1730 cm-1。
νC-H(醛):∼2720cm-1(中等强度尖峰)。
讨论:①不同羰基的大致吸收位置:②-I效应、环张力等使νC=O 波数升高;共轭效应使νC=O波数波数降低例1:正辛醛的红外光谱例2:苯乙酮的红外光谱NMR 谱3-C-R-CH 2-C-R-C-H O O O δ=2.1δ=2.3δ=8−10例1:丁酮的核磁共振谱例2:苯甲醛的核磁共振谱(五) 醛和酮的化学性质(1) 羰基的亲核加成(甲) 与氢氰加成(乙) 与亚硫酸氢钠加成(丙) 与醇加成(丁) 与金属有机试剂加成(戊) 与氨的衍生物加成缩合(己) 与Wittig试剂加成(2) α-氢原子的反应(甲) 卤化反应(乙) 缩合反应(丙) Mannich反应(3) 氧化和还原(甲) 氧化反应(乙) 还原反应(丙) Cannizzaro反应(岐化反应)(五) 醛和酮的化学性质(1)羰基的亲核加成从的结构考虑:C=Oδ+δ−a.有双键,可以加成;b.稳定性C O C ONuE+->所以亲核试剂首先进攻!即发生亲核加成反应,其通式为:R (R')H+ Nu -R OH NuR NuO-2C=Oδ+δ−(甲) 与氢氰酸加成反应式:实验证明:①OH -加速反应,H +减慢反应。
②Why?+ NaCN R H C=O OH -x(CH 3)OH -δ+δ−+ H CN RH 羟基腈α−氰醇α−或R OH Nu(CH 3)HC=O δ+δ−(CH 3)HCN OH -H +-2O 比HCN 更强的Nu加OH -可使[CN -]C=OH +C=O H+H+(羰基碳更正)以上实验事实说明:HCN 与醛、酮的加成是分步进行的,首先由CN -(亲核试剂)首先进攻,也就是说HCN 与醛、酮的加成是亲核加成。
即:慢2R H+ CN-2HR CNO -C=Oδ+δ−(CH 3)ROHCNH(CH 3)(CH 3)①②反应活性:①HCHO>CH3CHO>ArCHO>CH3COCH3>CH3COR>RCOR>ArCOAr醛的活性大于酮;脂肪族醛、酮大于芳香族醛、酮。
②p-NO2-C6H4-CHO>ArCHO>p-CH3-C6H4-CHO③例外:C6H5COCH3>(CH3)3C-CO-C(CH3)3(后者的空间障碍特别大。
)反应范围:所有的醛、脂肪族甲基酮、八个碳以下的环酮。
例1:CH 3-C-H + HCNOCH 3-CH-CNOH OH-2+CH 3-CH-COOHOH乳酸羟基丙酸α−乙醛例2:-CH 3-C-CNOH OCH 3-C-CH 3 + HCNCH 3CH 2=C-COOCH 3CH 3CH 3OH,H 2SO 4α−甲基丙烯酸甲酯MMA丙酮丙酮氰醇水解、酯化、脱水同时进行用途、意义:制备α-羟基酸、多一个碳的羧酸。
(乙) 与亚硫酸氢钠加成饱和NaHSO 3易溶于水不溶于溶液(CH 3)HSO 3HONa R R OH SO 3Na(CH 3)H羟基磺酸钠α−( )饱和NaHSO 3分子内中和+ NaHSO 3R (CH 3)HC=O δ+δ−反应范围:所有的醛、脂肪族甲基酮、八个碳以下的环酮。
反应活性:似与HCN 的加成。
(醛>酮、脂肪族>芳香族)用途:A. 鉴别醛酮:C-CH3OCH2CHO 饱和NaHSO3白x例:B. 分离提纯醛酮:在酸或碱的浓度较大时,平衡反应朝着加成产物分解为原来的醛、酮的方向进行:orR OHSO3Na (CH3)HRHOSO3NaH(CH3)C3R(CH3)HC=Oδ+δ−遇酸或碱分解CH 2CHO饱和NaHSO 3白CH CHSO Na OHH +orOH -过滤CH 2CHO例1:C-CH 3O C-CH 3O 例2:饱和NaHSO 3CHOOHOHCHSO 3Na x白()过滤H +orOH -CHOC .制备α-羟基腈CHOCHOHSO 3Na CHOHCN CHOHCOOH 3NaCN 2苦杏仁酸(67%)此法的优点是可以避免使用有毒的氰化氢,而且产率也较高。
(丙) 与醇加成醛加醇容易,酮困难。
R-C-H + R'OHO干HCl亲核加成R-C-OR'OHHR-C-OR'HOR'半缩醛(不稳定)缩醛(稳定)干HClS 1N反应式:半缩醛C=OH R H+δ−δ+R-CH-O-R'OH +H-H +OH快H+慢R'OH 更有利于Nu 进攻C=O R H反应机理:R-CH-O-R'OH快H +R-C R'OH R-CH-OR'OH 2+-H 2O 2R-CH-OR'H +OR'-H +R-CH-OR' OR'缩醛半缩醛缩醛具有双醚结构,对碱和氧化剂稳定,但遇酸迅速水解为原来的醛和醇R-CH-OR'OR'H 2O/H +O缩醛对碱和氧化剂稳定所以,制备缩醛时必须用干燥的HCl 气体,体系中不能含水。
