中考化学化学质量守恒定律(大题培优 易错 难题)含答案
2020-2021备战中考化学培优 易错 难题(含解析)之气体和固体分离和提纯附答案

一、中考初中化学气体和固体的除杂分离和提纯1.下列有关图像中不正确的是( )A.镁在装有空气的密闭容器内燃烧B.质量相同的粉末状碳酸钙和块状碳酸钙与足量稀盐酸反应C.两份完全相同的双氧水在有无MnO2的情况下产生O2 (其中a无MnO2, b有MnO2)D.电解水生成气体的体积【答案】B【解析】【分析】【详解】A、镁可与空气中的氧气、氮气、二氧化碳等反应,但是反应后所有物质都在密闭容器内,根据镁元素质量守恒,反应前后镁元素质量不变,所以镁元素质量随着反应进行,质量不变,选项A正确;B、质量相同的粉末状碳酸钙和块状碳酸钙所含有的碳元素质量相等,其中的碳元素全部转化为二氧化碳中碳元素,所以最终两者生成的二氧化碳质量相等,粉末状碳酸钙与盐酸接触更充分,所以反应速率快,当碳酸钙被全部消耗完毕前,相同时间内,粉末状碳酸钙生成二氧化碳多,但是最终两者生成二氧化碳质量相等,选项B 错误;C 、二氧化锰作为催化剂,加速过氧化氢的分解,因此相同时间内,加入二氧化锰的过氧化氢生成的氧气多,但是过氧化氢总量相同,最终生成氧气的质量相等,所以斜率大的为加入二氧化锰的过氧化氢,即为b ,a 则为未加二氧化锰的,选项C 正确;D 、水电解方程式为2222H O 2H +O ↑↑通电,从化学方程式可以看出,相同时间内生成氢气与氧气的体积比为2:1,选项D 正确。
故选B 。
2.下列图像能正确反映其对应关系的是A .表示向一定量的稀硫酸中加入足量的铜粉B .表示向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液C .表示向一定量的氢氧化钠溶液中滴加稀硫酸D .表示将等质量的大理石分别与等量且足量的稀盐酸反应【答案】C【解析】【分析】【详解】A 、铜与稀硫酸不能反应,不能生成氢气,该选项对应关系不正确;B 、向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液时,氯化银沉淀不溶于盐酸,立即产生白色沉淀,该选项对应关系不正确;C 、向一定量的氢氧化钠溶液中滴加稀硫酸时,氢氧化钠和稀硫酸反应生成硫酸钠和水,随着反应进行,pH 不断减小,恰好完全反应时pH=7,继续加入稀硫酸时pH 小于7,该选项对应关系正确;D 、将等质量的大理石分别与足量的等体积等溶质质量分数的稀盐酸反应时,最终生成二氧化碳质量相等,该选项对应关系不正确。
2023年中考化学专题训练——有关质量守恒定律的计算
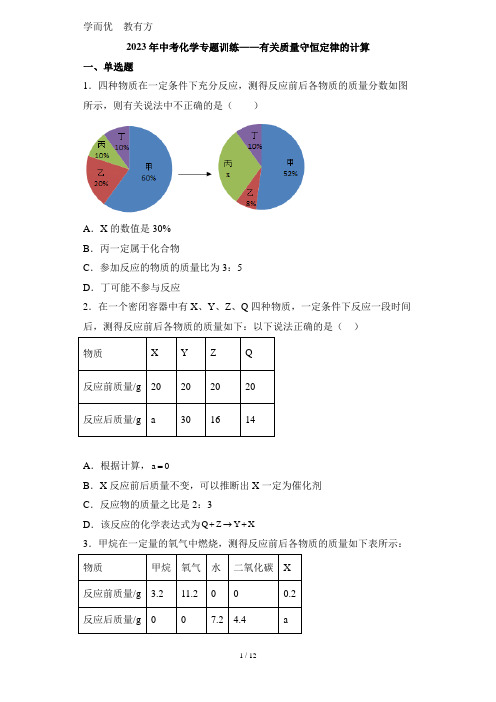
2023年中考化学专题训练——有关质量守恒定律的计算一、单选题1.四种物质在一定条件下充分反应,测得反应前后各物质的质量分数如图所示,则有关说法中不正确的是()A.X的数值是30%B.丙一定属于化合物C.参加反应的物质的质量比为3:5D.丁可能不参与反应2.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下反应一段时间后,测得反应前后各物质的质量如下:以下说法正确的是()A.根据计算,a0=B.X反应前后质量不变,可以推断出X一定为催化剂C.反应物的质量之比是2:3+→+D.该反应的化学表达式为Q Z Y X3.甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:下列判断正确的是()A.表中a的值为2.8 B.X一定是该反应的催化剂C.X可能含有氢元素D.X一定含有氧元素4.有一包铜和碳组成的固体混合物,在一定条件下与氧气完全反应,生成固体氧化铜和气体二氧化碳,并测得在反应前后固体的质量不变,则原固体混合物中碳的质量分数是()A.15% B.20% C.32% D.80%5.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中正确的是()物质 a b c d反应前的质量(g) 64 32 28 40反应后的质量(g) 52 X 28 76A.a和d是反应物B.c一定是催化剂C.X=24g D.该反应是化合反应6.一定条件下,M、N、P、Q四种物质在一密闭容器内充分反应,测得反应前后各物质的质量如表,下列描述中不正确的是()物质M N P Q反应前质量/g 3.4 0.8 64.6 0反应后质量/g 0 X 66.4 1.6A.N物质可能为该反应的催化剂B.该反应为分解反应C.该反应中,P、Q两种物质变化的质量比为9:8D.该反应中,一定有元素化合价改变7.密闭容器中,下列各组物质在一定条件下充分反应后,冷却至室温,密闭容器中的气态物质为纯净物的是()A.分子数比为1:1的CO和2O B.物质的量比为4:3的C和2OC .质量比为1:5的4CH 和2OD .质量比为3:8的C 和2O8.科学兴趣小组同学对一个化学反应前后各物质的质量进行了测定(见下表),据表分析下列结论中正确的是( )A .该反应是一个化合反应B .该反应中生成乙物质14.9克C .丙物质反应后的总质量是9.6克D .丁物质一定是该反应的催化剂9.80gFe 2O 3和CuO 的固体混合物,在高温条件下与足量的CO 充分反应后,得到金属的质量可能是( ) A .50gB .60gC .70gD .80g10.如图是某化学反应中各物质质量与时间的变化关系。
专题08 质量守恒定律和化学方程式-2021年中考化学真题分类训练(第01期)(教师版含解析)
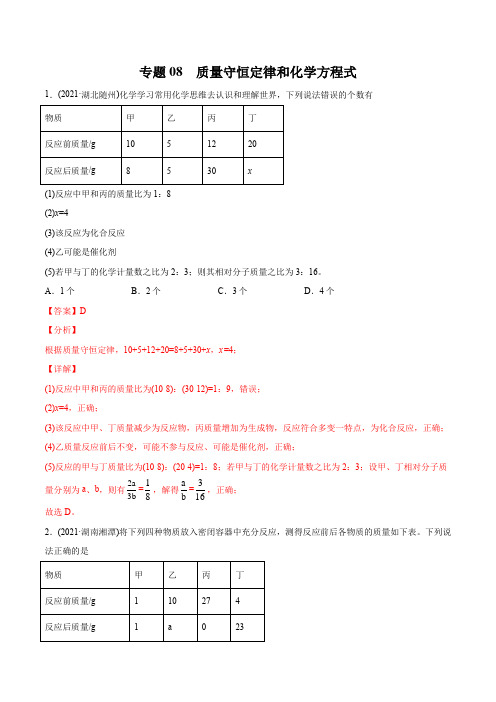
专题08 质量守恒定律和化学方程式1.(2021·湖北随州)化学学习常用化学思维去认识和理解世界,下列说法错误的个数有(1)反应中甲和丙的质量比为1:8(2)x=4(3)该反应为化合反应(4)乙可能是催化剂(5)若甲与丁的化学计量数之比为2:3;则其相对分子质量之比为3:16。
A.1个B.2个C.3个D.4个【答案】D【分析】根据质量守恒定律,10+5+12+20=8+5+30+x,x=4;【详解】(1)反应中甲和丙的质量比为(10-8):(30-12)=1:9,错误;(2)x=4,正确;(3)该反应中甲、丁质量减少为反应物,丙质量增加为生成物,反应符合多变一特点,为化合反应,正确;(4)乙质量反应前后不变,可能不参与反应、可能是催化剂,正确;(5)反应的甲与丁质量比为(10-8):(20-4)=1:8;若甲与丁的化学计量数之比为2:3;设甲、丁相对分子质量分别为a、b,则有2a3b=18,解得ab=316,正确;故选D。
2.(2021·湖南湘潭)将下列四种物质放入密闭容器中充分反应,测得反应前后各物质的质量如下表。
下列说法正确的是A .a 的值是8B .甲物质一定是该反应的催化剂C .该反应属于分解反应D .反应过程中乙、丁的质量比是5:2 【答案】C 【分析】 本题考查计算。
【详解】根据表格信息可知,丙从27g 变成0g ,是反应物,丁从4g 增加到23g ,是生成物,由于反应前后物质的质量是守恒的,所以推算出乙的质量应该是27g -19g=8g ,写出该反应的方程式为:+ 丙丁乙。
A 、因为生成乙的质量为8g ,所以a 应该是8+10=18,故A 不符合题意;B 、甲反应前后质量不变,可能是催化剂,也可能是不参与反应的杂质,故B 不符合题意;C 、该反应由一种物质生成两种物质,是分解反应,故C 符合题意;D 、反应中乙生成了8g ,丁生成了19g ,所以质量比为8:19,故D 不符合题意; 故选C 。
中考化学培优冲刺课程第9讲、运用元素质量守恒解题(学生版)

中考化学冲刺第9讲、运用元素质量守恒解题“质量守恒定律”即参加反应前各物质的质量总和等于反应后生成各物质的质量总和,利用质量守恒法的主要依据是反应前后质量总和不变,这种解题技巧的优点是基于宏观的统揽全局的方式列式,可以避开繁杂的运算,不去追究细枝末节,因而能使复杂的计算化繁为简,化难为易,是我们化学计算中必须掌握的方法之一。
由质量守恒法推知,在化学反应前后,一定不变的是:1、反应前后物质的总质量2、元素的种类3、元素的质量4、原子的种类5、原子的数目6、原子的质量一定改变的是:物质的种类及物质的粒子构成方式;可能改变的是:元素的化合价或分子总数。
下面我们来探讨质量守恒法在化学计算中的应用:例1:化学反应中,肯定有变化的是()A.原子的数目B.分子的种类C.分子的数目D.总质量例2:某物质在空气中燃烧后生成二氧化碳和水,该物质()A.只含碳元素B.只含碳、氢元素C.一定含碳、氧、氢元素D.一定含碳、氢元素,可能含氧元素例3:物质X是一种重要的阻燃剂,工业上用三氧化二锑[Sb2O3]生产X的化学方程式为:Sb2O3+2H2O2=X+2H2O.根据质量守恒定律,推断X的化学式为()A.SbO2B.H3SbO4C.HSbO3D.Sb2O5例4:将铁片分别放入下列溶液中,充分反应后溶液的质量(不包括固体)比反应前减轻的是()A.硫酸铜溶液B.稀硫酸C.氢氧化钠溶液D.氯化氢溶液例5:将A、B、C三种物质各10g加热进行化合反应,(其中B是催化剂)生成D,当A己全部反应后,测得生成的D为16g,反应后的混合物中B和C的质量之比为()A.5:1 B.5:3 C.5:2 D.4:1例6:在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得部分数据如表:物质甲乙丙丁反应前质量/ g 18 1 2 32反应后质量/ g X 26 2 12下列说法中,不正确的是()A.反应后物质甲的质量为13g B.乙是反应物C.参加反应的甲和丁的质量为1:4 D.物质丙可能是该反应的催化剂例7:密闭容器中有甲、乙两种物质各10g,加热一段时间后测得容器中各物质的质量如表所示物质甲乙丙丁反应后质量/ g 1.6 X 0.9 2.2下列选项正确的是()A.该反应为化合反应B.X=5.3C.该反应中甲和乙的质量比为84:53 D.丙、丁一定是单质例8:A、B、C三种物质各15g,在一定的条件下充分反应只生成30gD;若再增加10gC,A与C恰好完全反应.则参加反应的A与B的质量比为()A.3:2 B.2:3 C.5:2 D.5:3例9:一定量的乙醇在氧气不足的条件下燃烧,得到CO、CO2和水的总质量为27.6 g,其中水的质量为10.8 g,则参加反应的乙醇的质量是多少?生成一氧化碳的质量是多少?例10:有一种含CaCO3与CaO的混合物,测得其中钙元素的质量分数为50%,取该混合物16 g,经高温煅烧后,将剩余固体投入足量的水中,固体全部溶解生成Ca(OH)2,则生成Ca (OH)2的质量为( )A、3.7 gB、7.4 gC、14.8 gD、22.2 g例11:锌粉、铝粉、铁粉、镁粉的混合物3.8g与一定质量的溶质质量分数为25%的稀硫酸(H2SO4)恰好完全反应,将反应后的混合物蒸发水分得固体(不含结晶水)11 g,则反应中生成氢气的质量为( )A、0.15 gB、0.20 gC、0.30 gD、0.45 g例12:某二价金属M的氧化物10 g与90 g稀硫酸恰好完全反应后,形成无色透明溶液,测得反应后溶液中溶质的质量分数为30% 。
中考化学热点微专题2 质量守恒定律的应用之定量计算

好题精选
8. (2019德阳)如图是某化学反应中各物质的质量与时间的变化关系。下列叙述中正 确的是( B ) A. a时刻时,各物质的质量关系一定是甲=乙+丙+ 丁 B. 该反应在b时刻时结束 C. 相对分子质量甲>乙>丙>丁 D. 该反应所属的基本反应类型为分解反应
9. (2020郑州一检)3 g某物质完全燃烧后生成4.4 g二氧化碳和1.8 g水。则下列相关说 法正确的是( D ) A. 无法计算出该物质完全燃烧消耗氧气的质量 B. 该物质一定含有碳、氢元素,可能含有氧元素 C. 该物质分子中碳原子和氢原子的个数比为2∶1 D. 3 g该物质含碳元素的质量为4.4 g× 12
河南真题、备用卷
1. (2012河南10题1分)一定条件下,下列物质在密闭容器内充分反应,测得反应前后
各物质的质量如下:
纯净物
乙醇 氧气 二氧化碳 水
X
反应前质量/g
2.3
4
0
0
0
反应后质量/g
0
0
2.2
2.7 待测
下列说法正确的是( B )
A. 反应后X的质量为1.5 g
B. X中一定含有碳元素和氧元素
2H2O
通电
=====
2H2↑+O2↑
2×18
2×2 1×32
36
4 32
2(水的化学计量数)=
36(水的质量) 18(水的相对分子质量)
(2020万唯河南大模考)4.4 g某有机物在氧气中燃烧,经测定生成物有7.2 g水、10 g二
氧化碳和一氧化碳且其中碳元素的质量分数是36%。则该有机物中所含碳元素的质
_3_C__2H__4_+__8_O_2_=__=点_=燃_=_=__4_C_O__2_+__6_H_2_O_+__2_C__O___。
无锡中考化学计算题(大题培优易错试卷)

一、中考初中化学计算题1.小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。
操作过程如下:请计算:(1)20g样品中碳酸钠的质量为__________g;(2)反应后所得滤液中氢氧化钠的质量分数为多少?__________(写出计算过程)(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水__________g.【答案】10.6 4% 120【解析】【分析】【详解】(1)20g样品中碳酸钠的质量为20g×53%=10.6 g(2)解:设反应生成氢氧化钠的质量为x;Na CO+Ca(OH)=CaCO+2NaOH23231068010.6g x106/10.6g=80/x 解得x=8 g氢氧化钠的质量分数=8g/200g×100%=4%答:反应后所得滤液中氢氧化钠的质量分数为4% 。
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水的质量为X根据溶液稀释前后溶质的质量不变有:200g ×4%=(200g-X) ×10%X=120g2.为测定石灰石样品中碳酸钙的含量,小明取25g石灰石样品与一定质量的14.6%的稀盐酸恰好完全反应,将反应所得混合物蒸干得到固体27.2 g(不含结晶水,假设样品中的杂质既不与稀盐酸反应)。
试计算:(1)参加反应的盐酸的质量______。
(2)石灰石样品中碳酸钙的含量______。
【答案】100g 80%【解析】【分析】【详解】设样品中杂质的质量为x ,反应消耗盐酸的为y3222CaCO +2HCl =CaCl +CO +H O1007311125g-x14.6%y 27.2g-x↑⨯ 10073111==25g-x 14.6%y 27.2g-x ⨯ x=5g y=100g石灰石样品中碳酸钙的质量分数为25g-5g100%=80%25g⨯ 答:样品中碳酸钙的含量为80%,反应消耗盐酸的为100g 考点:根据化学方程式的计算3.将Na 2CO 3和NaCl 固体混合物32.9g 放入烧杯中,此时总质量为202.9g ,加入326.9g 盐酸,恰好完全反应,待没有气泡逸出后再次称量,总质量为521.0g .计算所得溶液中溶质的质量分数______(CO 2的溶解忽略不计). 【答案】10 【解析】 【分析】首先根据质量守恒定律:化学反应前后,物质的质量不变,可先求出产生的气体二氧化碳的质量=202.9g+326.9g-521.0g=8.8g ,再根据化学反应方程式:Na 2CO 3+2HCl=2NaCl+H 2O+CO 2↑可知,反应后所得溶液中溶质是NaCl ,但NaCl 来自两部分,一是反应生成的,二是原固体混合物中含有的,生成的NaCl 可通过化学方程式来求解,原固体混合物中含有的NaCl 可通过混合物32.9g 减去Na 2CO 3的质量 【详解】解:根据质量守恒定律,反应生成的CO 2质量=202.9g+326.9g-521.0g=8.8g 设Na 2CO 3的质量为x ,生成的NaCl 的质量为y 。
【化学】化学流程图的专项培优 易错 难题练习题(含答案)含答案

一、中考初中化学流程图1.如图是常见物质的转化关系图(个别产物可能略去).其中A、B常温下均为液态,且组成元素相同;F是大理石的主要成分.请回答:(1)A的名称是_____,在反应①中,物质X起_____作用;(2)说出物质Z的一个用途_____;(3)反应②的化学方程式为_____;(4)反应⑥的化学方程式为_____;(5)反应①﹣⑥涉及的基本反应类型有_____种.【答案】双氧水或过氧化氢溶液催化做导线等 CaO+H2O = Ca(OH)2CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ 3种【解析】【分析】已知F是大理石的主要成分,则F是碳酸钙,最后得到了蓝色沉淀,由此可以推出D为氢氧化钙,则可想到是生石灰和水化合生成了氢氧化钙,又因为已知A、B常温下均为液态,且组成元素相同,可以推知B是水,A是双氧水,双氧水在二氧化锰的催化作用下可生成水和氧气,所以X是二氧化锰,C是氧气,最后生成的蓝色沉淀是氢氧化铜,则往前推一下可知H是硫酸铜,再往前推测可知E是氧化铜,则Z是铜。
【详解】(1)A的名称是过氧化氢溶液,在反应①中,二氧化锰是过氧化氢溶液分解的催化剂,物质X起催化作用;(2)物质Z是铜,它的一个用途是做电线;(3)反应②是氧化钙和水反应生成氢氧化钙,反应的化学方程式为CaO+H2O = Ca(OH)2;(4)反应⑥是氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;(5)反应①过氧化氢生成氧气和水是分解反应;反应②是氧化钙和水反应生成氢氧化钙、反应③是氧气和铜反应生成氧化铜都是化合反应,④⑤⑥都是复分解反应,涉及的基本反应类型有3种.2.实验室以一种工业废渣(主要成分为MgCO3、MgO和SiO2)为原料制备MgCO3•3H2O.其主要实验过程如图:已知:SiO 2不溶于水,常温下不与硫酸、碳酸钠反应。
(1)“酸溶”时发生反应的化学方程式为_____和_____。
中考化学利用化学方程式的简单计算(大题培优 易错 难题)含答案

中考化学利用化学方程式的简单计算(大题培优 易错 难题)含答案一、初中化学利用化学方程式的简单计算1.深圳进行机动车限牌,汽车尾气污染得到控制。
如图是汽车处理尾气反应的微观过程,有关说法正确的是( )A .反应前后分子的种类、数目都发生了变化B .反应的生成物质量之比是7:11C .反应的化学方程式为22 CO+NO N+CO 催化剂D .催化剂加快反应速率,增加了生成物的质量【答案】A 【解析】 【分析】结合图示,根据质量守恒定律及反应物生成物可知,反应的方程式为:222CO+2NON+2CO =催化剂,结合方程式进行分析即可。
【详解】A 、由微粒的变化可知,分子的种类及数目发生了变化,故A 正确;B 、由方程式可知,反应的生成物质量之比是28:(44×2)=7:22,故B 错误;C 、方程式未配平,故C 错误;D 、催化剂能加快反应的速率,但不会增加生成物的质量,故D 错误。
故选A 。
【点睛】此类题目重在从图中提炼信息,根据信息进行题目的解答和分析。
要注意排除干扰微粒以及补充缺少的微粒,让图恰好体现反应的本质关系。
2.现有下列四组物质:①乙炔(C 2H 2)和苯(C 6H 6);②乙烷(C 2H 6)和乙醇(C 2H 6O);③丁烷(C 4H 10)和乙醚(C 4H 10O);④甲苯(C 7H 8)和甘油(C 3H 8O 3)。
当总质量一定时,各组中的两种物质无论按何种质量比混合,完全燃烧生成水的质量均相同。
符合该条件的共有 A .1组 B .2组C .3组D .4组【答案】B 【解析】试题分析∶ 根据定组成定律和化学方程式可知(1)(4)组符合,(2)(3)组不符合。
考点∶ 考查根据定组成定律和化学方程式的应用。
3.质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反应aA+bB ═cC+dD 中,下列说法正确的是A.化学计量数a与b之和一定等于c与d之和B.若A和C都是盐,则该反应一定是复分解反应C.反应物A和B的质量比一定等于生成物C和D的质量比D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg【答案】D【解析】试题分析:A、化学方程式中化学式前面化学计量数实际就是物质的分子个数,而质量守恒定律告诉我们:分子个数在化学反应前后可能发变化,故化学计量数a与b之和不一定等于c与d之和,错误,B、若A和C都是盐,则该反应不一定是复分解反应,还可能是置换反应,错误,C、反应物A和B的质量比不一定等于生成物C和D的质量比,错误,D、若取xgA和xgB反应,由于可能有反应物过量,故生成C和D的质量总和不一定是2xg,正确,故选D考点:质量守恒定律,基本反应类型4.科学家最新发现,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如下。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
=
×100% =31.6%,错误。故选 B。
点睛:结合新信息,灵活运用化学式的意义是解题的关键。
6.软玉也称“中国玉”,以新疆“和田玉”为代表,生成“和田玉”矿床的反应方程式是
5CaMg(CO3)2+8SiO2+H2O=Ca2Mg5(Si4O11)2(OH)2+7CO2↑+3R,则 R 的化学式为( )
【答案】B
【解析】
【分析】
反应后质量减少的物质是反应物,减少的质量是参加反应的质量,反应后质量增多的物质
是生成物,增多的质量是生成的质量。X 反应后质量增多,是生成物,生成的质量是 18g-
2g=16g,Z 反应后质量减少,是反应物,参加反应的质量是 16g-6g=10g,W 反应后质量减
少,是反应物,参加反应的质量是 16g-11g=5g,5g+10g<16g,所以 Y 是反应物,参加反应
A.CaCO3
B.Ca(OH)2
C.Mg(OH)2
D.MgCO3
【答案】A
【解析】
【分析】
根据质量守恒定律,反应前后元素种类及原子个数均不变。
【详解】
由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式
5CaMg(CO3)2+8SiO2+H2O=Ca2Mg5(Si4O11)2(OH)2+7CO2↑+3R,反应前钙、镁、碳、氧、硅原子 个数分别为 5、5、10、47、8,反应后的生成物中钙、镁、碳、氧、硅原子个数分别为 2、
加上相应的数字,2N 表示 2 个氮原子,元素是一个宏观概念,无数量的意义,此选项错 误; D. 氯化钠溶液中含有 Na+和 Cl﹣,此选项正确。 故选 D。
11.如图为某反应的微观示意图,下列说法正确的是( )
A.该反应属于分解反应
B.反应前后分子种类没有改变
C.反应前后原子数目发生改变
D.参加反应的两种分子个数比为 1:1
【答案】D
【解析】
A、根据图可知:两种单质生成一种化合物,属于化合反应,不属于分解反应,故错误;
B、根据图可知:氢分子和氯分子变化成了氯化氢分子,反应前后分子种类发生了改变,故
错误;
C、由微粒的变化可知,反应前后原子数目没有发生改变,故错误;
D、由微粒的变化可知,参加反应的两种分子个数比为 1:1,故正确。
2.工业制钛反应为:TiF4+2H2SO4 Δ 4HF+2X+TiO2,X 的化学式为
A.H2S 【答案】D
B.P4
C.SO2
D.SO3
【解析】
【详解】
加热
由 TiF4+2H2SO4
4HF+2X+TiO2 可知,反应前后钛原子都是 1 个,氟原子都是 4 个,氢
原子都是 4 个,反应前硫原子是 2 个,反应后应该是 2 个,包含在 2X 中,反应前氧原子是 8 个,反应后应该是 8 个,其中 6 个包含在 2X 中,X 的化学式是 SO3。 故选:D。
5.过氧乙酸(C2H4O3)是常见的消毒剂。下列有关过氧乙酸的说法正确的是 A.分子中含 O3 分子 B.氢、氧原子的个数比为 4:3 C.分子中有 9 种元素 D.碳的质量分数为 24% 【答案】B 【解析】A.分子是由原子构成的,过氧乙酸分子中含有氧原子,不是 O3 分子,错误; B.由化学式可知,过氧乙酸(C2H4O3)中氢、氧原子的个数比为 4:3,正确;C.分子是 由原子构成的,不是由元素组成的,错误;D.过氧乙酸(C2H4O3)中碳元素的质量分数
1:12,故选项错误。故选 B。
10.学习化学需要使用化学符号。下列叙述正确的是 A.NH3 中的 3 表示 3 个氨气分子 B.铝片表面氧化物的化学式为 AlO C.2N 表示 2 个氮原子或 2 个氮元素 D.氯化钠溶液中含有 Na+和 Cl﹣ 【答案】D 【解析】 【详解】 A. NH3 中的 3 表示 1 个氨气分子中有 3 个氢原子,此选项错误; B. 铝片表面氧化物的化学式为 Al2O3,此选项错误; C. 由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前
4.托盘天平两边放两个等质量的烧杯、内装浓度和质量都相同的稀盐酸,若左杯中投入一 块生石灰,向右边杯中投入一块石灰石,且两块固体质量相等,则反应后天平的指针将 () A.偏向左边 B.偏向右边 C.仍指零处 D.无法确定 【答案】A 【解析】 【详解】 生石灰即氧化钙,虽与盐酸反应,但无气体生成;石灰石主要成分是碳酸钙,与盐酸反应 会产生二氧化碳气体,两固体质量相等,由于石灰石一侧产生气体,故质量减小,天平指 针偏向另一侧。选 A。
B.一个丙氨酸分子中含有 13 个原子
C.丙氨酸中氮、氢元素的质量比为 2:1 D.丙氨酸中氮元素的质量分数最小
【答案】D
【解析】 【详解】 A、丙氨酸是由碳、氢、氧、氮四种元素组成的,故选项说法正确; B、1 个丙氨酸分子是由 3 个碳原子、7 个氢原子、2 个氧原子和 1 个氮原子构成的,则一 个丙氨酸分子中含有 13 个原子,故选项说法正确; C、丙氨酸中氮元素与氢元素的质量比为 14:(1×7)=2:1,故选项说法正确; D、丙氨酸中各元素的质量比为 C:H:N:O=36:7:14:32,故氢元素的质量分数最小 ,故选项说法错误。 故选:D。
数目不变,则 2R 中含有 2 个铁原子和 4 个硫原子,则化学式为 FeS2 ,故选 D。
8.常温下,氯气与苛性钠溶液反应产物是氯化钠、次氯酸钠(NaClO)和水。次氯酸钠中氯 元素的化合价为 A.-1 B.+1 C.-2 D.+2 【答案】B 【解析】NaClO 中钠元素的化合价为+1 价,氧元素的化合价为-2 价,设氯元素的化合价为 x ,根据化合价的代数和为 0,+1+x+(-2)=0,得 x=+1,故选 B。
16.下图为某化学反应的微观模拟示意图,下列说法中,不正确的是
A.该反应不属于置换反应 B.图示中 x 的数值为 3
可。
7.质量守恒定律是帮助我们认识化学反应实质的重要理论.某物质与水和氧气反应的化学
方程式为 2R+2H2O+7O2 =2FeSO4 +2H2SO4 :则 R 的化学式应为
A.FeS
B.Fe2S3
C.FeO
D.FeS2
【答案】D
【解析】
【分析】
根据质量守恒定律,反应前后原子个数不变。
【详解】
根据质量守恒定律,反应前后原子个数不变,反应物中氢、氧原子个数分别为 4、16,反 应后的生成物中氢、硫、氧、铁原子个数分别为 4、4、16、2,根据反应前后原子种类、
催化剂
根据图中的微粒模拟图,可推测其反应的化学方程式为: CH2O+O2
ቤተ መጻሕፍቲ ባይዱ
CO2 +H2O
CH2O+O2CO2+H2O。 【详解】 A、置换反应是指由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反 应,该反应的生成物是两种化合物,错误; B、根据 O2、CO2、H2O 都无毒,可推测这种有毒气体的化学式为 HCHO,正确; C、四种物质中,只有 CO2、H2O 两种物质属于氧化物,其余物质不是氧化物,错误; D、根据化学方程式可知,该反应中 A 与 C 的质量比=30:44,错误。 故选 B。
中考化学化学质量守恒定律(大题培优 易错 难题)含答案
一、初中化学质量守恒定律
1.图反映了某个化学反应各物质质量与时间的关系。下列描述正确的是
A.该反应是化合反应 B.甲的相对分子质量大于乙 C.丙是反应物,甲和乙是生成物 D.t1 时,丙的质量一定等于甲、乙的质量之和 【答案】C 【解析】 【分析】 【详解】 A、由图知从 0 到 t1 时间内丙物质逐渐减少,甲乙两物质逐渐增加。所以,丙为反应物, 甲、乙为生成物,该反应分解反应,描述错误; B、甲的生成量比乙多,但分子个数不知,相对分子质量甲不一定比乙大,描述错误; C、 丙是反应物,甲和乙是生成物,描述正确; D、t1 时,参加反应的丙质量一定等于甲、乙的质量之和,描述错误。 故选 C。
15.下图为某反应的部分微观示意图,其中不同的球代表不同元素的原子。下列说法正确 的是( )
A.该反应属于置换反应 B.参加反应的两种分子个数比为 1:1 C.1 个 X 分子中含有 3 个原子 D.1 个 X 分子中含有 3 种不同的原子 【答案】C 【解析】 【分析】 由图可知,不同球代表不同元素的原子,两种化合物反应生成单质与化合物,由原子守恒 可知,X 中含 1 个大黑球和 2 个小白球,以此来解答。 【详解】 A.反应物无单质,不属于置换反应,故 A 错误; B.由图可知,参加反应的两种分子个数比为 1:2,故 B 错误; C.原子守恒可知,X 中含 1 个大黑球和 2 个小白球,即 1 个 X 分子中含有 3 个原子,故 C 正确; D.X 中含 1 个大黑球和 2 个小白球,有 2 种不同原子,故 D 错误; 故选:C。
B、过氧乙酸(C2H4O3)中碳元素的质量分数为:
12 2
×100%=31.6%,故
12 2 1 4 163
选项正确;
C、过氧乙酸的相对分子质量为122 14 163 =76,相对分子质量的单位为 1,常省
略,故选项错误;
D、过氧乙酸中,碳、氢、氧三种元素的质量比为(12×2):(1×4):(16×3)=6:
3.一定条件下,某装置中发生了化学反应,测得反应前后各物质的质量变化如下表所示。
下列说法中,正确的是( )
物质
甲
乙
丙
丁
反应前的质量/g
60
1.5
0
0
反应后的质量/g
33
x
24
3
A.x 的值等于 0.5 B.丙和丁的质量变化比为 8:1 C.乙一定是催化剂 D.该反应是化合反应 【答案】B 【解析】 【分析】 由表中数据分析可知,反应前后甲的质量减少了 60g﹣33g=27g,故是反应物,参加反应 的质量为 27g;同理可以确定丙是生成物,生成的质量为 24g﹣0g=24g;丁是生成物,生 成的质量为 3g﹣0g=3g;由质量守恒定律,乙的质量不变,可能作该反应的催化剂,也可 能没有参加反应。 【详解】 A、乙的质量不变,x 的值等于 1.5,故选项说法错误; B、丙和丁的质量变化比为 24g:3g=8:1,故选项说法正确; C、乙的质量不变,可能作该反应的催化剂,也可能没有参加反,故选项说法错误; D、该反应的反应物为甲,生成物是丙和丁,符合“一变多”的形式,属于分解反应,故 选项说法错误。 故选 B。
