水分析化学第三版课后习题答案
水分析化学智慧树知到课后章节答案2023年下厦门理工学院

水分析化学智慧树知到课后章节答案2023年下厦门理工学院厦门理工学院第一章测试1.滴定分析法要求化学反应必须具有确定的化学计量关系,即反应按一定的反应方程式进行。
()答案:对2.水分析化学是以水为研究对象,综合应用分析化学的理论知识和方法,研究与分析水体系中物质的组成、性质、含量的科学。
()答案:对3.水质指标和水污染物是一样的含义()答案:错4.水体有自净功能,所以水不容易被污染()答案:错5.水质标准是表示生活饮用水、工农业用水及各种受污染水中污染物质的最高容许浓度或限量阈值的具体限制和要求。
()答案:对6.浊度、色度和电导率属于水体的化学指标。
()答案:错7.以化学反应为基础的分析方法称为化学分析方法。
()答案:对8.化学分析方法包括哪些方法?()答案:滴定分析法 ;重量分析法9.水分析化学的四大经典滴定是()答案:氧化还原滴定;络合滴定 ;沉淀滴定 ;酸碱滴定10.水的微生物指标包括哪几类?()答案:二氧化氯;细菌总数 ;游离性余氯 ;总大肠菌群第二章测试1.系统误差是可测误差,因此总能用一定的方法加以消除。
()答案:对2.精密度是指测定值与真实值之间的符合程度。
()答案:错3.0.06080有4位有效数字()答案:对4.滴定分析对化学反应的要求是反应必须有确定的化学计量关系,反应必须完全且速度要快。
()答案:对5.下面有关准确度与精密度的关系表述正确的是()答案:准确度高则要求精密度一定要高;6.在滴定分析测定中,属偶然误差的是()答案:滴定管最后一位估读不准确7.下列不属于典型的四大化学滴定分析法的是()答案:电位滴定法8.可用下法中哪种方法减小分析测定中的偶然误差?()答案:增加平行试验的次数。
9.已知标准溶液B与被测物质A之间的化学反应为:aA + bB = cC + dD,则滴定度TB/A与物质的量浓度CB之间的换算公式为:TB/A=()。
答案:VACB/VB10.在酸性溶液及标准状态下,以下各组离子可以共存的是()。
分析化学第三版习题答案

分析化学(化学分析部分)(第三版) 习题参考答案第1章 绪论1-1 简述分析化学的定义、任务和作用。
1-2 化学分析法有什么特点?1-3 仪器分析法有什么特点?1-4 如何选择分析方法?1-5 已知铅锌矿的K 值为0.1,若某矿石样品的最大颗粒直径为30 mm ,问最少应采集多少千克的样品才有代表性?解:当K = 0.1,d = 30 mm ,m = Kd 2 = 0.1 ⨯ 302 = 90 (kg)最少应采集90千克的样品才有代表性。
1-6 取锰矿试样15 kg ,已知K 值为0.3,当破碎至全部通过10号筛时,请问最少试样量为多少?用四分法可连续缩分几次?解:当K = 0.3,d = 2.00 mm ,m = Kd 2 = 0.3 ⨯ 22 = 1.2 (kg)即破碎至全部通过10号筛时,样品的最大颗粒直径为2 mm ,则最少试样量为1.2 kg 。
由15/2n = 1.2,有2n = 12.5,n = 3.6 ≈ 3 (次)用四分法连续缩分3次后,试样量为1.88 kg 。
1-7 一含Pb 试样0.5250 g 经过适当处理定量地生成PbSO 4沉淀0.4264 g 。
求算该样品中Pb 组分以PbSO 4、Pb 和PbO 等形式表示的质量分数。
解:4PbSO 0.4264 81.22%0.5250ω== Pb 40.4264M(Pb)0.4264207.21 = = 55.49%0.5250M(PbSO )0.5250303.26ω=⨯⨯ PbO 40.4264M(PbO)0.4264223.21 59.78%0.5250M(PbSO )0.5250303.26ω=⨯=⨯= 1-8 计算下列溶液的物质的量浓度:(1) 相对密度为1.057含HCl 12%(质量分数)的盐酸溶液;(2) 相对密度为0.954 含NH3 11.6%(质量分数)的氨水溶液。
解:(1)1.057100012%c 3.5 (mol/L)36.46⨯⨯==(2)0.954100011.6%c 6.50 (mol/L)17.03⨯⨯==第2章定量分析中的误差及分析数据的处理2-1 按照误差的分类,下列情况各引起什么误差?(1) 砝码腐蚀。
(完整版)《水分析化学》课后习题答案

第七章
1、参比电极和指示电极的种类和作用有哪些?
指示电极分为金属基电极和膜电极两大类。
金属基电极分为金属---金属离子电极、金属---金属微溶盐电极、均相氧化还原电极。
常用的参比电极有甘汞电极和银-氯化银电极。
2、玻璃电极使用前为何必须在蒸馏水中浸泡24h以上?
由于干玻璃电极对氢离子的传感不灵敏,即对pH值不响应,因此需要用蒸馏水浸泡:一方面,使玻璃电极的薄膜表面形成一层水合硅胶,水合硅胶层与水溶液之间的离子交换平衡是产生电极电位的根源,会恢复玻璃电极对pH值的响应。
另一方面,玻璃电极的薄膜内外表面的结构、性质常有差别或不对称,引起不对称电位,浸泡的目的是使其不对称电位减少并达到稳定。
3、电极使用前为何要用pH标准缓冲溶液标定pH计?
一般由于温度的影响、电子元件的老化、玻璃电极产家不一或浸泡时间不一等因素,常使pH计测量结果产生偏差,因此除了用仪器上的温度调节钮对温度进行补偿外,必须在测定之前用标准缓冲溶液进行校正。
分析化学第三版习题答案

分析化学第三版习题答案分析化学(化学分析部分)(第三版)习题参考答案第1章绪论1-1 简述分析化学的定义、任务和作用。
1-2 化学分析法有什么特点? 1-3 仪器分析法有什么特点? 1-4 如何选择分析方法?1-5 已知铅锌矿的K 值为0.1,若某矿石样品的最大颗粒直径为30 mm ,问最少应采集多少千克的样品才有代表性?解:当K = 0.1,d = 30 mm ,m = Kd 2 = 0.1 ? 302 = 90 (kg) 最少应采集90千克的样品才有代表性。
1-6 取锰矿试样15 kg ,已知K 值为0.3,当破碎至全部通过10号筛时,请问最少试样量为多少?用四分法可连续缩分几次?解:当K = 0.3,d = 2.00 mm ,m = Kd 2 = 0.3 ? 22 = 1.2 (kg)即破碎至全部通过10号筛时,样品的最大颗粒直径为2 mm ,则最少试样量为1.2 kg 。
由15/2n = 1.2,有2n = 12.5,n = 3.6 ≈ 3 (次) 用四分法连续缩分3次后,试样量为1.88 kg 。
1-7 一含Pb 试样0.5250 g 经过适当处理定量地生成PbSO 4沉淀0.4264 g 。
求算该样品中Pb 组分以PbSO 4、Pb 和PbO 等形式表示的质量分数。
解:4PbSO 0.426481.22%0.5250ω==Pb 40.4264M(Pb)0.4264207.21= = 55.49%0.5250M(PbSO )0.5250303.26ω=PbO 40.4264M(PbO)0.4264223.2159.78%0.5250M(PbSO )0.5250303.26ω==?=1-8 计算下列溶液的物质的量浓度:(1) 相对密度为1.057含HCl 12%(质量分数)的盐酸溶液;(2) 相对密度为0.954 含NH3 11.6%(质量分数)的氨水溶液。
解:(1)1.057100012%c 3.5 (mol/L)36.46==(2)0.954100011.6%c 6.50 (mol/L)17.03==第2章定量分析中的误差及分析数据的处理2-1 按照误差的分类,下列情况各引起什么误差?(1) 砝码腐蚀。
分析化学--第三版课后-习题答案

第三章 思考题与习题1.指出在下列情况下,各会引起哪种误差?如果是系统误差,应该采用什么方法减免? 答:(1)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(2)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(3)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(4)系统误差中的试剂误差。
减免的方法:做空白实验。
(5)随机误差。
(6)系统误差中的操作误差。
减免的方法:多读几次取平均值。
(7)过失误差。
(8)系统误差中的试剂误差。
减免的方法:做空白实验。
2解:因分析天平的称量误差为mg 2.0±。
故读数的绝对误差g a 0002.0±=E根据%100⨯T E =E ar 可得 %2.0%1001000.00002.01.0±=⨯±=E ggg r%02.0%1000000.10002.01±=⨯±=E ggg r这说明,两物体称量的绝对误差相等,但他们的相对误差并不相同。
也就是说,当被测定的量较大时,相对误差就比较小,测定的准确程度也就比较高。
3解:因滴定管的读数误差为mL 02.0±,故读数的绝对误差mL a 02.0±=E 根据%100⨯TE =E ar 可得 %1%100202.02±=⨯±=E mL mLmL r%1.0%1002002.020±=⨯±=E mLmL mLr这说明,量取两溶液的绝对误差相等,但他们的相对误差并不相同。
也就是说,当被测定的量较大时,测量的相对误差较小,测定的准确程度也就较高。
5答::0.36 应以两位有效数字报出。
6答::应以四位有效数字报出。
7答::应以四位有效数字报出。
8答::甲的报告合理。
因为在称样时取了两位有效数字,所以计算结果应和称样时相同,都取两位有效数字。
9解:根据方程2NaOH+H 2C 2O 4·H 2O==Na 2C 2O 4+4H 2O 可知,需H 2C 2O 4·H 2O 的质量m 1为:g m 13.007.1262020.01.01=⨯⨯= 相对误差为 %15.0%10013.00002.01=⨯=E ggr则相对误差大于0.1% ,不能用H 2C 2O 4·H 2O 标定0.1mol·L -1的NaOH ,可以选用相对分子质量大的作为基准物来标定。
水三课后作业解答与说明
(6)
dCC k 2C A0te kt dt
积分得
CC kC A0 (te
kt
e kt 1 ) C A0 1 1 kt e kt k
(7)
讨论如下:
dCC k 2C A0te kt dt dCB CA0 k 2te kt CA0 ke kt dt
2000
2500
lg
对 t 作图
Fig. 3 中直线斜率
0 0 (cNaOH cCH )k 3COOC2 H5
2.303
2.2650 104 ,k=0.1056 L/mol·s。
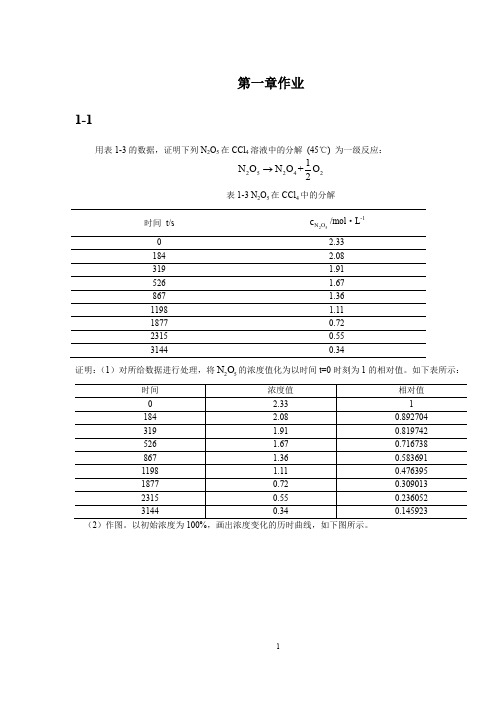
1-4
由表 1-5 数据确定反应的级数及每一温度的速率常数。反应物的初始浓度为 100 mg/L。 表 1-5 反应物的质量浓度 时间/d 0.1 0.5 1.0 1.5 2.0 3.0 4.0 解: 反应级数的确定如 1-1 及 1-2 所示:
t1 2 1200s; t1 4 2400s;
即存在关系: t1 2 : (t1 4 t1 2 ) =1:1 故根据基元反应中反应物级数与半衰期关系 t1 2 普遍存在的问题: 解:一级反应动力学的积分式为 ln c ln c0 kt , ln c 对 t 作图
1.0
1 可知,n=1 (C A0 ) n 1
对(1)积分:
6
CA CA0e kt
将(4)带入(2)有:
(4)
dCB kCB kCA0e kt dt
该方程两边同时乘以 e 得
kt
(5)
dCB kt e kCBekt kCA0 dt
积分,可得:
CB
0
分析化学第三版课后习题答案
第三章 思考题与习题1.指出在下列情况下,各会引起哪种误差?如果是系统误差,应该采用什么方法减免? 答:(1)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(2)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(3)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(4)系统误差中的试剂误差。
减免的方法:做空白实验。
(5)随机误差。
(6)系统误差中的操作误差。
减免的方法:多读几次取平均值。
(7)过失误差。
(8)系统误差中的试剂误差。
减免的方法:做空白实验。
2解:因分析天平的称量误差为mg 2.0±。
故读数的绝对误差g a 0002.0±=E根据%100⨯T E =E ar 可得 %2.0%1001000.00002.01.0±=⨯±=E ggg r%02.0%1000000.10002.01±=⨯±=E ggg r这说明,两物体称量的绝对误差相等,但他们的相对误差并不相同。
也就是说,当被测定的量较大时,相对误差就比较小,测定的准确程度也就比较高。
3解:因滴定管的读数误差为mL 02.0±,故读数的绝对误差mL a 02.0±=E 根据%100⨯TE =E ar 可得 %1%100202.02±=⨯±=E mL mLmL r%1.0%1002002.020±=⨯±=E mLmL mLr这说明,量取两溶液的绝对误差相等,但他们的相对误差并不相同。
也就是说,当被测定的量较大时,测量的相对误差较小,测定的准确程度也就较高。
5答::0.36 应以两位有效数字报出。
6答::应以四位有效数字报出。
7答::应以四位有效数字报出。
8答::甲的报告合理。
因为在称样时取了两位有效数字,所以计算结果应和称样时相同,都取两位有效数字。
9解:根据方程2NaOH+H 2C 2O 4·H 2O==Na 2C 2O 4+4H 2O 可知,需H 2C 2O 4·H 2O 的质量m 1为:g m 13.007.1262020.01.01=⨯⨯= 相对误差为 %15.0%10013.00002.01=⨯=E ggr则相对误差大于0.1% ,不能用H 2C 2O 4·H 2O 标定0.1mol·L -1的NaOH ,可以选用相对分子质量大的作为基准物来标定。
分析化学第三版课后习题答案问答题部分
第三章 思考题与习题10答:乙的准确度和精密度都高。
因为从两人的数据可知,他们是用分析天平取样。
所以有效数字应取四位,而甲只取了两位。
因此从表面上看甲的精密度高,但从分析结果的精密度考虑,应该是乙的实验结果的准确度和精密度都高。
14 解:(1)%83.243%69.24%93.24%87.24=++=-x(2)24.87%(3)%23.0%06.25%83.24-=-=-=E -T x a (4)%92.0%100-=⨯=TE E ar 15 解:(1)%43.675%407.67%43.67%47.67%37.67%48.67=++++=-x∑=+++==-%04.05%03.0%04.0%06.0%05.0||1i d n d (2)%06.0%100%43.67%04.0%100=⨯=⨯=--x d d r (3)%05.015%)03.0(%)04.0(%)06.0(%)05.0(122222=-+++=-=∑n dS i(4)%07.0%100%43.67%05.0%100=⨯=⨯=-xS S r(5)X m =X 大-X 小=67.48%-67.37%=0.11%21 解:(1)n=5%04.355%98.34%19.35%01.35%11.35%92.34=++++==∑-n x x %11.01506.015.003.007.012.01222222=-++++=-=∑n d s i经统计处理后的测定结果应表示为:n=5, %,04.35=-x s=0.11%(2)%04.35=-x , s=0.11% 查表t 0.95,4=2.78因此 %14.0%04.355%11.078.2%04.35,±=⨯±=±=-ns t x fp μ第四章 思考题与习题11解:已知 M CaO =56.08g/moL,HCl 与CaO 的反应:CaO+2H +=Ca 2++H 2O即:2=ab稀释后HCl 标准溶液的浓度为: 1331783.008.562005000.010000.1210-⋅=⨯⨯⨯=⨯⨯=L mol M T C CaOCaOHCl HCl设稀释时加入纯水为V ,依题意: 1.000×0.2000=0.1783×(1+10-3×V) ∴ V=121.7mL 12解:设应称取x gNa 2CO 3+2HCl==2NaCl+CO 2+H 2O 当V1=V=20mL ,时x=0.5×0.10×20×10-3×105.99=0.11g当V2=V=25mL ,时x=0.5×0.10×25×10-3×105.99=0.13g此时称量误差不能小于0.1% 16解: 根据公式:VM m c B B B ⨯=(1) 已知 g m O Cr K 709.14722=,mL V 500=和 moL g M O Cr K 2.294722= 代入上式得:111000.010005002.294709.14722--⋅=⋅⨯=L moL L mL mLmoL g gc O Cr K(2) C r 2O 72-+6Fe 2++14H +==2Cr 3++6Fe 3++7H 2O+-⨯=227261Fe O Cr n n 3227231O Fe O Cr n n ⨯=-∴Fe O Cr K Fe O Cr K M LmL c T ⨯⨯⋅⨯=-6100011722722 =111845.556100011000.0---⋅⨯⨯⋅⨯⋅moL g LmoL L moL =0.03351g ·mL -132722327223100011O Fe O Cr K O O Cr K M LmL c T ⨯⨯⋅⨯=- =0.1000mL ·L -1117.159310001--⋅⨯⨯⋅⨯moL g L mL=0.04791g ·mL -118解: HAc%=HAcHAc HAc NaOH NaOH V c M V c 310-⨯⨯=%10010055.105.601017.203024.03⨯⨯⨯⨯⨯- =3.47%21解: 2NaOH+H 2C 2O 4 ==Na 2C 2O 4+2H 2O设H 2C 2O 4的百分含量为x% ,得gx x x M x C S O C H NaOH 4583.0%5.004.90001.0%1018.0%5.0001.0%422=⨯⨯⨯⨯=⨯⨯⨯⨯=第五章 思考题与习题解答20解:(1) [H 1410]--+⋅=l mol13421073.35.01341000250][--⋅⨯=⨯=L mol O NaC根据多元酸(碱)各型体的分布分数可直接计算有: CK a1=5.9×10-2 , CK a2=6.4×10-5Na 2C 2O 4在酸性水溶液中以三种形式分布即:C 2O 42-、HC 2O 4-和H 2C 2O 4。
《水分析化学》课后习题答案
水分析化学平时作业整理第一章1.简述水分析化学课程的性质及任务。
性质:水分析化学是研究水及其杂质、污染物的组成、性质、含量和它们的分析方法的一门学科。
任务:通过水分析化学学习,掌握水分析化学的四大滴定方法(酸碱滴定法、络和滴定法、沉淀滴定法和氧化还原滴定法)和主要仪器分析法(如吸收光谱法、色谱法和原子光谱法等)的基本原理、基本理论、基本知识、基本概念和基本技能,掌握水质分析的基本操作,注重培养学生严谨的科学态度,培养独立分析问题和解决实际问题的能力。
2.介绍水质指标分几类,具体包括哪些指标?(1) 物理指标 1) 水温 2) 臭味和臭阈值 3) 颜色和色度 4)浊度 5)残渣 6)电导率 7)紫外吸光度值 8)氧化还原电位(2)微生物指标 1) 细菌总数 2) 总大肠菌群 3) 游离性余氯 4) 二氧化氯(3) 化学指标 1) pH 值 2) 酸度和碱度 3) 硬度4) 总含盐量 5) 有机污染物综合指标 6) 放射性指标第二章1.简述水样分析前保存的要点是什么?水样保存希望做到:减慢化学反应速度,防止组分的分解和沉淀产生;减慢化合物或络合物的水解和氧化还原作用;减少组分的挥发溶解和物理吸附;减慢生物化学作用。
水样的保存方法主要有加入保存试剂,抑制氧化还原反应和生化作用;控制pH 值和冷藏冷冻等方法,降低化学反应速度和细菌活性。
2.测定某废水中的COD ,十次测定结果分别为50.0,49.2,51.2,48.9,50.5,49.7,51.2,48.8,49.7和49.5 mgO 2/L ,问测量结果的相对平均偏差和相对标准偏差(以CV 表示)各多少?第三章1.已知下列各物质的Ka或Kb,比较它们的相对强弱,计算它们的Kb或Ka,并写出它们的共轭酸(或碱)的化学式。
(1)HCN NH4+ H2C2O44.93×10-10(Ka)5.6×10-10(Ka) 5.9×10-2(Ka1)6.4×10-5(Ka2)(2)NH2OH CH3NH2 AC-9.1×10-9(Kb) 4.2×10-4(Kb) 5.90×10-10(Kb)解:(1)酸性强弱:H2C2O4 > NH4+ >HCN(2)碱性强度:CH3NH2 > NH2OH >AC-2.简述酸碱滴定中指示剂的选用原则。
水三课后作业解答与说明
6
CA CA0e kt
将(4)带入(2)有:
(4)
dCB kCB kCA0e kt dt
该方程两边同时乘以 e 得
kt
(5)
dCB kt e kCBekt kCA0 dt
积分,可得:
CB
0
d (ekt CB ) kCA0 dt ,
0
t
CB CA0 kte kt
dcC k 2C A0te kt kt 1 1 k1 k2 时, 2 kt kt dcB C A0 k te C A0 ke kt 1 kt 1
t=0 时,
dcC =0 dcB dcC 1 dcB dcC dcB
t 时, lim
(t t ) t1 2 =1.12d, t1 4 =2.4d,则 1 4 1 2 1 ,故可确定该反应为一级反应。 t1 2
对上图中的曲线进行指数拟和,得到 y = 99.618e-0.6041t,则 k10 =0.6041 用同样方法求的 k 20 0.9831 , k 25 1.2941 , k 30 1.5498 , k 40 2.6197 如果能够证明在不同温度下的反应都属于一级反应也可以采用曲线拟合的方式来求解反应级数。
(
dcA 1 ) / (L h /106 mol) dt
1 / (L /106 mol) cA
Fig. 9 Lineweaver-Burk 作图 线性关系非常好,符合 Michaelis-Menten 方程 有 M-M 方程得, (
dcA 1 1 k2 k3 1 1 ) dt k3c0 k1 cA k3c0
2
ln 2 14.79 min 。 k
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章 思考题与习题1.指出在下列情况下,各会引起哪种误差?如果是系统误差,应该采用什么方法减免?答:(1)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(2)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(3)系统误差中的仪器误差。
减免的方法:校准仪器或更换仪器。
(4)系统误差中的试剂误差。
减免的方法:做空白实验。
(5)随机误差。
(6)系统误差中的操作误差。
减免的方法:多读几次取平均值。
(7)过失误差。
(8)系统误差中的试剂误差。
减免的方法:做空白实验。
2解:因分析天平的称量误差为mg 2.0±。
故读数的绝对误差g a 0002.0±=E 根据%100⨯TE =E ar 可得 %2.0%1001000.00002.01.0±=⨯±=E ggg r%02.0%1000000.10002.01±=⨯±=E ggg r这说明,两物体称量的绝对误差相等,但他们的相对误差并不相同。
也就是说,当被测定的量较大时,相对误差就比较小,测定的准确程度也就比较高。
3解:因滴定管的读数误差为mL 02.0±,故读数的绝对误差mL a 02.0±=E 根据%100⨯TE =E ar 可得 %1%100202.02±=⨯±=E mL mLmL r%1.0%1002002.020±=⨯±=E mLmLmL r这说明,量取两溶液的绝对误差相等,但他们的相对误差并不相同。
也就是说,当被测定的量较大时,测量的相对误差较小,测定的准确程度也就较高。
5答::0.36 应以两位有效数字报出。
6答::应以四位有效数字报出。
7答::应以四位有效数字报出。
8答::甲的报告合理。
因为在称样时取了两位有效数字,所以计算结果应和称样时相同,都取两位有效数字。
9解:根据方程2NaOH+H 2C 2O 4·H 2O==Na 2C 2O 4+4H 2O 可知,需H 2C 2O 4·H 2O 的质量m 1为:g m 13.007.1262020.01.01=⨯⨯=相对误差为 %15.0%10013.00002.01=⨯=E ggr则相对误差大于0.1% ,不能用H 2C 2O 4·H 2O 标定0.1mol·L -1的NaOH ,可以选用相对分子质量大的作为基准物来标定。
若改用KHC 8H 4O 4为基准物时,则有:KHC 8H 4O 4+ NaOH== KNaC 8H 4O 4+H 2O需KHC 8H 4O 4的质量为m 2 ,则 g m 41.022.2042020.01.02=⨯⨯=%049.0%10041.00002.02=⨯=E ggr相对误差小于0.1% ,可以用于标定NaOH 。
10答:乙的准确度和精密度都高。
因为从两人的数据可知,他们是用分析天平取样。
所以有效数字应取四位,而甲只取了两位。
因此从表面上看甲的精密度高,但从分析结果的精密度考虑,应该是乙的实验结果的准确度和精密度都高。
11.当置信度为0.95时,测得Al 2O 3的μ置信区间为(35.21±0.10)%,其意义是( D )12. 衡量样本平均值的离散程度时,应采用( D ) 13 解:根据%1001⨯=-xS S r得 %100%68.30%5.0⨯=S则S=0.1534%当正确结果为15.34%时, %0.1%100%34.15%1534.0%1002=⨯=⨯=-xS S r14 解:(1)%83.243%69.24%93.24%87.24=++=-x(2)24.87%(3)%23.0%06.25%83.24-=-=-=E -T x a(4)%92.0%100-=⨯=TE E ar 15 解:(1)%43.675%407.67%43.67%47.67%37.67%48.67=++++=-x∑=+++==-%04.05%03.0%04.0%06.0%05.0||1i d n d(2)%06.0%100%43.67%04.0%100=⨯=⨯=--x d d r (3)%05.015%)03.0(%)04.0(%)06.0(%)05.0(122222=-+++=-=∑n d S i(4)%07.0%100%43.67%05.0%100=⨯=⨯=-xS S r(5)X m =X 大-X 小=67.48%-67.37%=0.11%16解:甲:%15.393%18.39%15.39%12.391=++==∑-n x x%04.0%19.39%15.391-=-=-=E -T x a %03.013%)03.0(%)03.0(12221=-+=-=∑n dS i-=xS S r 11%08.0%100%15.39%03.0%100=⨯=⨯乙:%24.393%28.39%24.39%19.392=++=-x%05.0%19.39%24.392=-==E -x a %05.013%)04.0(%)05.0(12222=-+=-=∑n dS i%13.0%100%24.39%05.0%100222=⨯=⨯=-x S Sr由上面|Ea 1|<|Ea 2|可知甲的准确度比乙高。
S 1<S 2﹑Sr 1<Sr 2 可知甲的精密度比乙高。
综上所述,甲测定结果的准确度和精密度均比乙高。
17 解:(1)根据σμ-=x u 得u 1=5.204.040.2030.20-=- 5.104.040.2046.202=-u(2)u 1=-2.5 u 2=1.5 . 由表3—1查得相应的概率为0.4938,0.4332则 P(20.30≤x≤20.46)=0.4938+0.4332=0.927018 解: σμ-=x u =32.02.126.11-=- 查表3-1,P=0.4987 故,测定结果大于11.6g·t -1的概率为: 0.4987+0.5000=0.998719解: σμ-=x u =9.123.015.4359.43≈-查表3-1,P=0.4713 故在150次测定中大于43.59%出现的概率为: 0.5000-0.4713=0.0287 因此可能出现的次数为 150⨯0.0287(次)4≈ 20 解:(1) %01.05%022.0≈==-nxσσ(2)已知P=0.95时,96.1±=μ,根据 -±=-xu x σμ得%02.0%13.1%01.096.1%13.1±=⨯±=μ 钢中铬的质量分数的置信区间为%02.0%13.1± (3)根据ns t x s t x fp xf p ,,±=±=---μ得%01.0,±=±=--ns t x fp μ已知%022.0=s , 故 5.0%022.0%01.0==nt查表3-2得知,当201=-=n f 时,09.220,95.0=t 此时5.02109.2≈即至少应平行测定21次,才能满足题中的要求。
21 解:(1)n=5%04.355%98.34%19.35%01.35%11.35%92.34=++++==∑-n x x%11.01506.015.003.007.012.01222222=-++++=-=∑n d s i经统计处理后的测定结果应表示为:n=5, %,04.35=-x s=0.11%(2)%04.35=-x , s=0.11% 查表t 0.95,4=2.78因此 %14.0%04.355%11.078.2%04.35,±=⨯±=±=-ns t x fp μ22解:(1)%60.58=-x , s=0.70% 查表t 0.95,5=2.57因此 %73.0%60.586%70.057.2%60.58,±=⨯±=±=-ns t x fp μ(2)%60.58=-x , s=0.70% 查表t 0.95,2=4.30因此 %74.1%60.583%70.030.4%60.58,±=⨯±=±=-ns t x fp μ由上面两次计算结果可知:将置信度固定,当测定次数越多时,置信区间越小,表明-x 越接近真值。
即测定的准确度越高。
23 解:(1)8.053.183.159.183.111=--=--=-x x x x Q n n n查表3-3得Q 0.90,4=0.76,因Q>Q 0.90,4 , 故1.83这一数据应弃去。
(2)6.053.183.165.183.111=--=--=-x x x x Q n n n查表3-3得Q 0.90,5=0.64,因Q<Q 0.90,5, 故1.83这一数据不应弃去。
24 解:(1) 1038.041056.01034.01032.01029.0=+++=-x0011.0140018.00004.00006.00009.0122222=-+++=-=∑n d s i82.00011.01029.01038.011=-=-=-s x x G 64.10011.01038.01056.041=-=-=-s x x G 查表3-4得, G 0.95,4=1.46 , G 1<G 0.95,4 ,G 2>G 0.95,4故0.1056这一数据应舍去。
(2) 1032.031034.01032.01029.0=++=-x00025.0130002.00003.01222=-+=-=∑n d s i当 P=0.90时,92.22,90.0=t 因此 0004.01032.0300025.092.21032.0,1±=⨯±=±=-ns t x fp μ当 P=0.95时,30.42,90.0=t 因此0006.01032.0300025.030.41032.0,1±=⨯±=±=-ns t x fp μ由两次置信度高低可知,置信度越大,置信区间越大。
25解:根据4%05.0|%46.54%26.54|||=-=-=-s T x t 查表3-2得t 0.90,3=3.18 , 因t>t 0.95,3 ,说明平均值与标准值之间存在显著性差异。
26. 某药厂生产铁剂,要求每克药剂中含铁48.00mg.对一批药品测定5次,结果为(mg ·g -1):47.44,48.15,47.90,47.93和48.03。
问这批产品含铁量是否合格(P=0.95)?解: 89.47503.4893.4790.4715.4844.47=++++==∑-n x x27.015)14.0()04.0()01.0()26.0()45.0(22222=-++++=s41.027.0|00.4889.47|||=-=-=-s T x t 查表3-2, t 0.95,4 =2.78 , t<t 0.95,4说明这批产品含铁量合格。
