山东大学2017年无机化学专业硕博连读研究生培养方案
2017年硕博连读及申请审核制博士生拟录取名单
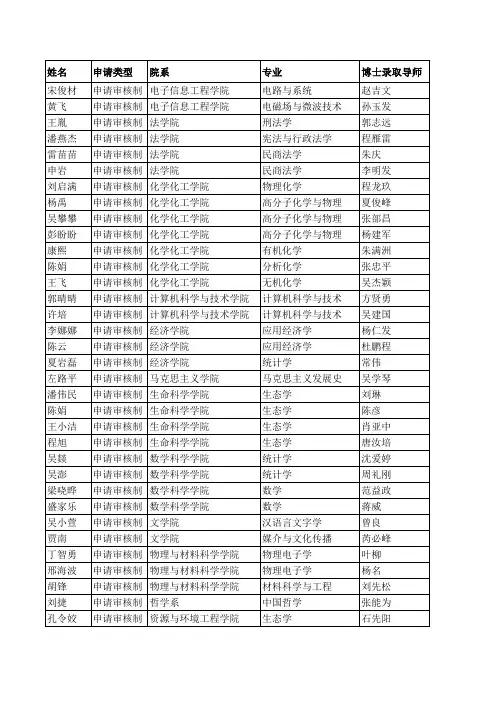
申请类型
院系
专业 电路与系统 电磁场与微波技术 刑法学 宪法与行政法学 民商法学 民商法学 物理化学 高分子化学与物理 高分子化学与物理 高分子化学与物理 有机化学 分析化学 无机化学 计算机科学与技术 计算机科学与技术 应用经济学 应用经济学 统计学 马克思主义发展史 生态学 生态学 生态学 生态学 统计学 统计学 数学 数学 汉语言文字学 媒介与文化传播 物理电子学 物理电子学 材料科学与工程 中国哲学 生态学
李文博 陶园 韦玉平 贾金灿 项小书 余成进 魏丕静 郑飞鸿 谢倩倩 姚道林 张国生 张明珠 程磊 陈业禹
申请审核制 资源与环境工程学院 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 硕博连读 法学院 化学化工学院 化学化工学院 计算机科学与技术学院 计算机科学与技术学院 计算机科学与技术学院 经济学院 数学学院 文学院 物理与材料科学学院 资源与环境工程学院 资源与环境工程学院 资源与环境工程学院
博士录取导师 赵吉文 孙玉发 郭志远 程雁雷 朱庆 李明发 程龙玖 夏俊峰 张部昌 杨建军 朱满洲 张忠平 吴杰颖 方贤勇 吴建国 杨仁发 杜鹏程 常伟 吴学琴 刘琳 陈彦 肖亚中 唐汝培 沈爱婷 周礼刚 范益政 蒋威 曾良 芮必峰 叶 申请审核制 电子信息工程学院 申请审核制 法学院 申请审核制 法学院 申请审核制 法学院 申请审核制 法学院 申请审核制 化学化工学院 申请审核制 化学化工学院 申请审核制 化学化工学院 申请审核制 化学化工学院 申请审核制 化学化工学院 申请审核制 化学化工学院 申请审核制 化学化工学院 申请审核制 计算机科学与技术学院 申请审核制 计算机科学与技术学院 申请审核制 经济学院 申请审核制 经济学院 申请审核制 经济学院 申请审核制 马克思主义学院 申请审核制 生命科学学院 申请审核制 生命科学学院 申请审核制 生命科学学院 申请审核制 生命科学学院 申请审核制 数学科学学院 申请审核制 数学科学学院 申请审核制 数学科学学院 申请审核制 数学科学学院 申请审核制 文学院 申请审核制 文学院 申请审核制 物理与材料科学学院 申请审核制 物理与材料科学学院 申请审核制 物理与材料科学学院 申请审核制 哲学系 申请审核制 资源与环境工程学院
2017年博士研究生待录取公示
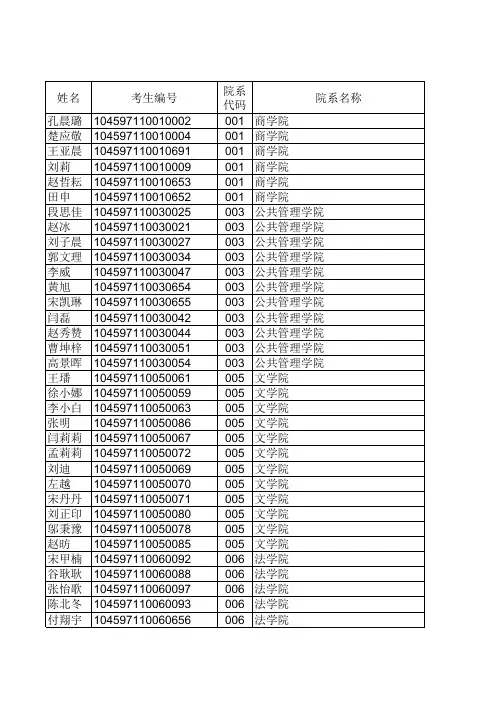
2017年博士研究生待录取公示
专业代码 1204Z2 1204Z2 1204Z2 1204Z2 1204Z2 1204Z2 120400 120400 120400 120400 120400 120400 120400 120400 120400 120400 120400 050104 050104 050104 050104 050104 050104 050104 050104 050104 050104 050104 050104 030103 030103 030103 030103 030103 专业名称 公共经济管理 公共经济管理 公共经济管理 公共经济管理 公共经济管理 公共经济管理 公共管理 公共管理 公共管理 公共管理 公共管理 公共管理 公共管理 公共管理 公共管理 公共管理 公共管理 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 中国古典文献学 宪法学与行政法学 宪法学与行政法学 宪法学与行政法学 宪法学与行政法学 宪法学与行政法学 研究方向 代码 01 01 01 02 02 03 01 01 01 01 01 01 01 02 06 07 08 01 01 02 02 03 03 04 04 04 04 04 04 01 02 03 03 03
山东大学关于修订硕士专业学位研究生培养方案的 - 山东大学研究生院

采用课程学习、专业实践和学位论文相结合的培养方式,注重理论与实际的结合。
鼓励吸收不同学科领域的专家、学者和有丰富实践经验的专业人员,共同承担专业学位研究生的培养工作。
实行双导师制,以校内导师指导为主,校外导师参与实践过程、项目研究、论文写作等多个环节的指导工作。
(四)培养方案按类别(领域)修订,应包括培养目标、培养方向、学制(仅适用于全日制研究生)、培养方式、课程设置及教学要求、实践环节、学位论文等内容,各项内容应具体明确,具有可操作性。
(五)不同培养单位招收同一类别(领域)研究生,在修订培养方案时应在共同协商的基础上确定彼此的共性及差异性。
二、基本框架和内容
对研究生专业实践要实行全过程的管理和服务,重视专业实践环节的实施及监控。专业实践前研究生要提交实践计划,实践期间要参加中期检查,实践结束后要撰写实践报告。各培养单位应制订相应的管理与考核评价办法,确保实践质量。
各培养单位要注重吸纳和利用社会资源,合作建立专业学位研究生工作站,切实为研究生专业实践活动的开展提供可靠的软硬件保障,密切专业学位研究生培养与用人单位实际需求间的联系,积极探索人才培养的供需互动机制。
在职攻读硕士专业学位人员,修满规定的学分,通过论文答辩,经学校学位评定委员会审议通过后,可授予相应硕士专业学位证书。
三、按本意见修订的培养方案从2013年入学的研究生开始执行。由研究生院负责解释。
?? ?? ຫໍສະໝຸດ ?? ?? (3)专业实践8-10学分。具体要求见第六条。
2. 选修课分为专业选修课和非专业选修课。各类别(领域)要开设一定数量的专业选修课,给研究生留有足够的选择空间。专业选修课一般不少于2 门,每门2学分。
学校开设的研究生公共选修课主要包括:
化学博士研究生培养方案

化学博士研究生培养方案(学科、专业代码:0703,授理学学位)一、培养目标1.具有良好的科研道德,严谨、求实、创新、进取的科学态度和作风以及独立从事本学科科学研究的能力;2.具有坚实、宽广的基础理论和系统、深入的专门知识;3.在本学科或专门技术上做出创造性的成果。
二、本学科设置如下研究方向1.无机化学2.化学生物学3.分析化学4.有机化学5.物理化学6.高分子化学7.材料化学三、学习年限本学科、专业博士生的学习年限一般为3-5年。
硕博连读、直攻博研究生的学习年限一般为4-6年。
四、学分要求已获硕士学位博士生总学分要求≥29学分。
硕博连读、直攻博研究生总学分要求≥53学分。
以同等学力报考博士生按硕博连读、直攻博研究生的要求培养,符合课程免修规定的,可申请免修。
五、课程设置及学分分配六、本学科对博士研究生培养提出的具体要求1.博士研究生的培养实行导师负责制,组成以博士生导师为组长的博士研究生指导小组,负责博士研究生的培养和考核工作。
2.对跨一级学科课程的限定(1)跨一级学科课程指本一级学科外的研究生课程,且必须跟班听课并同堂参加考试。
(2)所选的跨一级学科课程不得与硕士期间所修的课程相同。
3.论文选题报告,通过开题得1学分。
选题报告应包括的内容为:(1)课题的来源、意义;(2)课题的国内外研究概况及发展趋势;(3)课题的研究内容和技术方案;(4)理论与实践方面预计的创造性成果;(5)预期成果;(6)主要参考文献。
4.论文中期报告博士生撰写博士学位论文前,要向博士生指导小组或有关学者、专家报告研究工作成果,听取质疑与商讨改进意见,待创造性研究成果获得认同后,方可撰写论文。
5.博士研究生申请论文答辩和资格审查博士论文资格审查由指导教师或博士生指导小组负责进行。
博士研究生申请论文答辩的基本条件:(1)修完所规定的课程学分;(2)完成论文选题报告;(3)完成论文中期报告;(4)在刊物上发表规定数量的论文;(5)完成毕业论文的撰写;(6)通过校内外专家的评审。
考研无机化学(86)专业高校排名
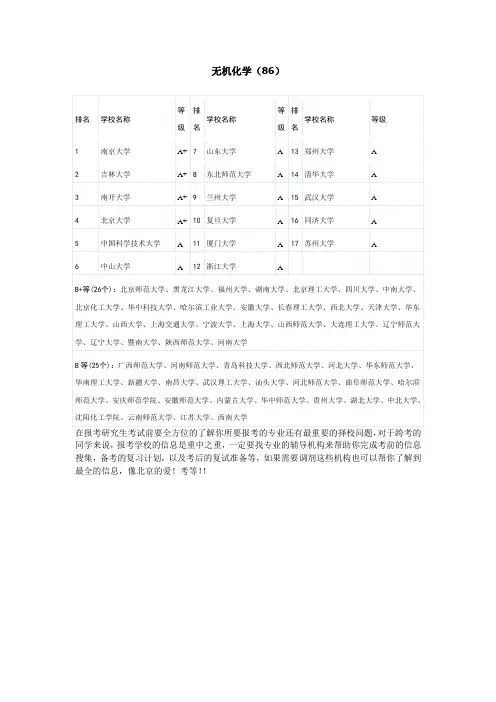
无机化学(86)
排名学校名称
等
级排
名
学校名称
等
级
排
名
学校名称等级
1南京大学A+7山东大学A13郑州大学A
2吉林大学A+8东北师范大学A14清华大学A
3南开大学A+9兰州大学A15武汉大学A
4北京大学A+10复旦大学A16同济大学A
5中国科学技术大学A11厦门大学A17苏州大学A
6中山大学A12浙江大学A
B+等(26个):北京师范大学、黑龙江大学、福州大学、湖南大学、北京理工大学、四川大学、中南大学、北京化工大学、华中科技大学、哈尔滨工业大学、安徽大学、长春理工大学、西北大学、天津大学、华东理工大学、山西大学、上海交通大学、宁波大学、上海大学、山西师范大学、大连理工大学、辽宁师范大学、辽宁大学、暨南大学、陕西师范大学、河南大学
B等(25个):广西师范大学、河南师范大学、青岛科技大学、西北师范大学、河北大学、华东师范大学、华南理工大学、新疆大学、南昌大学、武汉理工大学、汕头大学、河北师范大学、曲阜师范大学、哈尔滨师范大学、安庆师范学院、安徽师范大学、内蒙古大学、华中师范大学、贵州大学、湖北大学、中北大学、沈阳化工学院、云南师范大学、江苏大学、西南大学
在报考研究生考试前要全方位的了解你所要报考的专业还有最重要的择校问题,对于跨考的同学来说,报考学校的信息是重中之重,一定要找专业的辅导机构来帮助你完成考前的信息搜集,备考的复习计划,以及考后的复试准备等,如果需要调剂这些机构也可以帮你了解到最全的信息,像北京的爱!考等!!。
山东大学2017年化学与化工学院博士招生目录_山东大学考研网
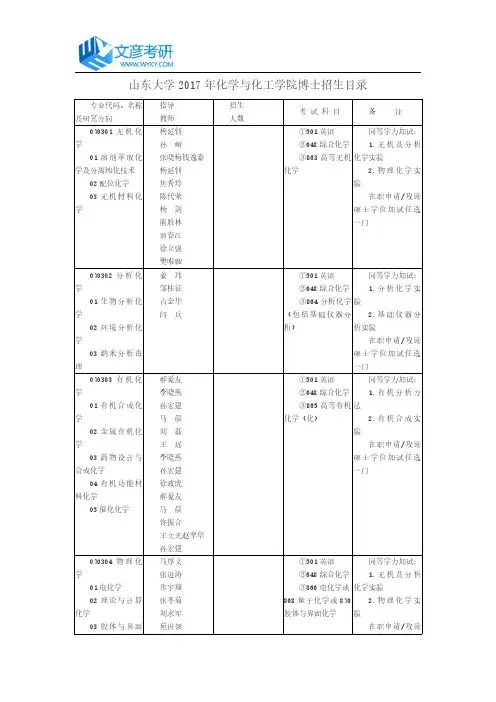
与化学或 671 高等物 化学实验
理化学
2. 物 理 化 学 实
③863 高等无机 验
化学或 899 固态化学
(晶)
侯士峰 王文寿
文章来源:文彦考研
硕士学位试任选一 门
①501 英语
同等学力加试:
②648 综合化学 1. 高 分 子 化 学
③867 高聚物结 与物理基础
构与性能
2. 高 分 子 化 学
与物理基础实验
在职申请/攻读
硕士学位加试任选
一门
①501 英语
同等学力加试:
②643 材料物理 1. 无 机 及 分 析
验
在职申请/攻读
硕士学位加试任选
一门
①501 英语
同等学力加试:
②648 综合化学 1. 分 析 化 学 实
③864 分析化学 验
( 包 括 基 础 仪 器 分 2. 基 础 仪 器 分
析)
析实验
在职申请/攻读
硕士学位加试任选
一门
①501 英语
同等学力加试:
②648 综合化学 1. 有 机 分 析 方
山东大学 2017 年化学与化工学院博士招生目录
专业代码、名称 及研究方向
070301 无 机 化 学
01 溶 剂 萃 取 化 学及分离纯化技术
02 配位化学 03 无 机 材 料 化 学
070302 分 析 化 学
01 生 物 分 析 化 学
02 环 境 分 析 化 学
03 纳 米 分 析 毒 理
郝爱友 李晓燕 孙宏建 马晨 刘磊 王瑶 李晓燕 孙宏建 徐政虎 郝爱友 马晨 佟振合 王文光赵翠华 孙宏建 马厚义 张进涛 步宇翔 张冬菊 刘永军 苑世领
博士研究生培养方案
博士研究生培养方案第1篇博士研究生培养方案一、培养目标本方案旨在培养具有坚定理想信念、扎实理论基础、独立科研能力和国际视野的博士研究生。
通过严格的专业课程学习、科研项目训练及学术交流,使研究生在所学领域达到国内领先、国际一流水平。
二、培养要求1. 掌握宽广的基础理论和系统深入的专门知识;2. 具备独立从事科学研究的能力,创新性解决学术和实际问题;3. 具有良好的学术道德、团队合作精神和国际交流能力;4. 在本学科领域取得具有一定影响力的科研成果。
三、课程设置1. 公共课程:政治理论、英语、数学、计算机等基础课程;2. 专业课程:涵盖本学科领域的核心知识、研究方法及前沿动态;3. 选修课程:跨学科课程、实验方法、学术研讨等,拓宽学术视野。
四、科研训练1. 参与导师科研项目,开展课题研究;2. 定期参加学术会议、研讨会,进行学术交流;3. 申请并承担校级、省级、国家级科研项目;4. 完成博士学位论文,达到高水平学术论文标准。
五、培养过程1. 第一阶段(第一年):基础课程学习、确定研究方向、开展课题研究;2. 第二阶段(第二年):专业课程学习、参与科研项目、进行学术交流;3. 第三阶段(第三年):深化课题研究、撰写博士学位论文、申请科研项目;4. 第四阶段(第四年):完成博士学位论文、进行论文答辩、总结学术成果。
六、考核评价1. 课程考核:采用考试、论文、报告等形式,评估研究生课程学习成果;2. 中期考核:对研究生的学术水平、科研能力、学术道德等方面进行全面评价;3. 博士学位论文预答辩和正式答辩:评估研究生学位论文质量;4. 毕业评价:对研究生培养全过程进行综合评价,确保培养质量。
七、保障措施1. 建立健全导师责任制,强化导师在研究生培养中的指导作用;2. 完善科研条件,为研究生提供良好的学术环境和科研资源;3. 加强学术交流,促进研究生与国际一流学术水平接轨;4. 注重研究生心理健康,提供心理辅导和支持;5. 完善研究生奖助体系,激励研究生学术创新。
山东大学授予博士、硕士学位和培养研究生的学科、专业目录
★△法学理 论 法律史 ★△宪法学 与行政法学 刑法学 ★△民商法 学 诉讼法学 经济法学 环境与资源 保护法学 国际法学 军事法学 ★政治学理 论 ★中外政治 制度 ★▲△科学 社会主义与 国际共产主 义运动 ★中共党史 ★△国际政 治 ★国际关系 ★外交学 △社会学 民俗学 ★△马克思 主义基本原 理 ★马克思主 义发展史 ★马克思主 义中国化研 究 ★国外马克 思主义研究 ★思想政治 教育 ★中国近现 代史基本问 题研究 ☆学生事务 管理与学生 发展指导 高等教育学 应用心理学 体育人文社 会学 体育教育训 练学 ★▲文艺学
1001
100105 100106 100107 100120 100121 100122
100201
100202 100203 100204 100205 100206 100207 1002 ※★临床医 学 100208 100209 100210 100211 100212 100213 100214
★康复医学 与理疗学 ★运动医学 ★麻醉学 ★急诊医学 口腔基础医 学 ★△口腔临 床医学 ★▲流行病 与卫生统计 学 ★劳动卫生 与环境卫生 学 ★营养与食 品卫生学 ★儿少卫生 与妇幼保健 学 ★卫生毒理 学 ★军事预防 医学 ★☆卫生检 验学 ★中西医结 合临床 ★△药物化 学
100702 ★药剂学 100703 ★生药学 ★药物分析 100704 学 ★△微生物 100705 与生化药学 100706 ★药理学 ★☆天然药 100720 物化学 ☆制药工程 100721 学 100722 ☆临床药学 ★△管理科 120100 学与工程 ☆文化产业 120120 管理 120201 会计学 ★△企业管 120202 理 120203 旅游管理 技术经济及 120204 管理 120401 行政管理
化学与化工学院-山东大学本科生院
任选 2 学分 任选 2 学分 任选 2 学分 任选 2 学分 任选 2 学分
00054(00056) 人文学科类(或自然科学类) 2 00055(00057) 社会科学类(或工程技术类) 2 小 计 00090 通识教育选修课组 小 计 sd009201(0-1)0 0102001910 0102002010 0102000620 高等数学(1-2) 大学物理(1-2) 大学物理实验 小 计 无机化学(1-2) 化学分析 仪器分析 有机化学(1-2) 物理化学(1-2) 10 3 3 8 8 1 17 8 4 4 8 8 4 2
总学分:152 学分 ·071·
化学与化工学院
七、修业年限:
4年
八、授予学位:
理学学士学位
九、各类课程学时学分比例
课程性质 课程类别 通识教育必修课程 学科基础平台课程 必修课 专业基础课程 专业必修课程 实践环节 不含实验课程 含实验课程 125 学 分 29 17 56 13 10 36 10 27 3 14 152 432 2531+ 21 周 学 时 739 288 1216 288 21 周 832 160 48 224 2963+21 周 100% 17.76% 82.24% 占总学分百分比 19.08% 11.18% 36.84% 8.55% 6.58% 23.68% 6.58% 1.97% 9.21%
三、培养要求:
系统扎实地掌握化学基础知识和基本理论;熟练地掌握化学实验的基本技能;了解化学的发展历史、学 科前沿和发展趋势;掌握本专业所需的数学、物理、计算机等知识,了解化学工程、生命、材料、能源、环境 等相关领域的基础知识;初步掌握化学研究、开发和应用等基本方法和手段,初步具备发现、提出、分析和解 决化学及相关问题的能力;具有安全意识、环保意识和可持续发展理念;掌握必要的信息技术,能够获取、加 工和应用化学及相关信息;掌握一门外国语,具有国际视野和跨文化交流、竞争与合作能力;具有较强的学习、 表达、交流和协调能力及团队合作精神;具有一定的创新意识和批判性思维;初步具备自主学习、自我发展的 能力,能够适应科学技术和经济社会发展。
山东大学关于硕博连续培养研究生工作的规定
附件1山东大学关于硕博连续培养研究生工作的规定为适应培养高素质创新人才的需要,吸引优秀博士生生源,提高博士生培养质量,根据教育部和国务院学位委员会有关文件精神,结合我校实际情况,对硕博连续培养(以下简称硕博连读)研究生工作做以下规定。
一、开展硕博连读学科、专业的基本条件及审批(一)申请开展硕博连读工作的学科、专业,应是我校具有博士学位授予权的学科、专业。
(二)开展硕博连读工作的博士学位授予学科、专业应有较强的师资队伍,有较好的可供研究生进行学习和科研训练的条件,已建立起从硕士生到博士生的完整课程体系和完善的管理制度。
(三)拟开展硕博连读工作的博士学位授予学科、专业,由所在研究生培养单位提出申请,经所在培养单位学位评定分委员会审核同意,报研究生院批准后方可开展硕博连读研究生的培养工作。
二、硕博连读研究生的人选确定(一)人选必须同时具备下列条件:1、全日制本科毕业且获学士学位;2、参加全国硕士研究生统一入学考试且成绩优秀、或推荐免试入学的硕士研究生;3、全国大学英语六级考试合格(或新计分方法不低于425分)或研究生第一外国语课程考试成绩不低于70分;4、定向、单位委托培养研究生需有定向、委培单位人事部门同意硕博连读的书面意见。
(二)硕博连读研究生人选可在硕士研究生招生录取时确定,复试前由申请人向培养单位提出书面申请,培养单位按学校下达的当年度硕博连读计划数,考核确定硕博连读名单。
确定为硕博连读的研究生应签署相应的协议。
硕博连读研究生人选也可在硕士生入学一年后的硕博连读研究生资格考试时确定。
三、硕博连读工作的基本要求(一)计划开展硕博连读研究生工作的学科、专业应该根据学校关于博士、硕士研究生培养的基本要求以及本规定,制订本专业或本一级学科硕博连读研究生培养方案。
培养方案的内容主要应包括:培养目标、学习年限、课程设置及学分要求、资格考试、综合能力培养、学位论文及成果要求等。
硕博连读研究生培养方案应报研究生院审批。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
山东大学2017年无机化学专业硕博连读研究生培养方案无机化学专业硕博连读研究生培养方案
(学科代码:070301)
一、培养目标
培养德智体全面发展的、在本学科领域具有一定造诣的身心健康的高层次专门人才。
应掌握坚实宽广的化学基础理论和系统的自然科学知识,深入系统地掌握无机化学的专门知识、理论和研究方法,及时了解无机化学及其相关学科的发展趋势;具有良好的科学素养和独立开展科学研究的能力,具有较强的创新意识;至少掌握一门外国语,能熟练阅读本专业的外文资料,具有一定的科技协作管理和进行国际学术交流的能力;能熟练的运用计算机与现代信息工具;毕业后能在高等院校、科研机构和相应的产业部门承担教学、科研、高新技术开发及管理工作。
二、研究方向
1、无机材料化学
2、配位化学
3、能源与环境材料
4、无机材料制备
5、无机/有机复合材料
三、学制与学习年限
硕博连读研究生学制5年,学习年限为5-7年。
四、培养方式
硕博连读研究生的培养实行导师指导和集体培养相结合的方式。
成立研究生指导小组,由3-5名本专业和相关学科的专家组成,其中应有一名校内跨学科的导师或校外导师,研究生导师任组长。
五、应修总学分数
应修总学分不少于40学分。
其中硕士研究生阶段应修学分不少于30学分,必修课不少于18分(含前沿讲座2学分与社会实践2学分)。
博士阶段应修学分不少于10学分(包括博士阶段前沿讲座4学分)。
六、课程设置
硕博连读培养研究生在修完本专业硕士研究生培养方案规定的课程后,应修本专业博士研究生除外国语以外的课程。
(一)必修课
思想政治理论3学分(硕士阶段)
中国马克思主义与当代2学分(博士阶段)
第一外国语3学分、专业外语2学分
学位基础课、学位专业课
社会实践2学分
社会实践:硕士生在读期间应参加一定量的教学实践工作,可辅导本科生课程、参加实验室建设、承接横向课题、参与指导本科生毕业设计或参加社会实践、社会调查活动。
结束后写出总结报告,导师根据报告评定成绩,成绩按优、良、中、及格和不及格五级计分,成绩及格以上记2学分。
前沿讲座6学分。
前沿讲座贯穿硕博连读培养的全过程。
(1)前沿讲座的目的和内容:前沿讲座旨在使研究生了解本学科相关研究方面的重大学术问题和前沿性问题,提高研究生参与学术活动的兴趣和学术交流的能力。
前沿讲座内容包括国内外研究动态介绍、文献讲座、新技术与新成果介绍等。
(2)前沿讲座的形式:“研究生前沿专题讲座”形式有两种:研究生和指导教师参加的、指导教师主持
的学术讨论班;校内外专家主讲的学术讲座。
学术讨论班内容可包括研究生本人做专题综述和工作进展报告,课题组教师或其他研究生做专题综述和工作进展报告,特邀请的国内外本学科或相关学科的专家做前沿学术报告等。
(3)前沿讲座的次数:博士生参加校外专家讲座的次数不得少于15次。
博士生参加本课题组的前沿讲座的次数不得少于25次,其中主讲不得少于6次,主讲者要写出讲稿,讲稿内容要充实,要有个人见解,能够反映所研究领域进展的新动态。
(4)前沿讲座的考核要求和方式:由参加讲座的导师指导小组共同进行考核、评定成绩,并写出评语。
考核按优、良、中、及格、不及格五级计分,考察合格以上记6学分。
(二)选修课:
1、硕士阶段选修课:不少于3门,不少于6学分
学校开设的硕士研究生公共选修课包括:
1)硕士研究生第二外国语,计2学分;
2)体育课,计1学分;
3)心理学课程,计1学分。
2、博士阶段选修课:不少于2门,不少于4学分
学校开设的博士研究生公共选修课包括:
1、马克思主义经典著作选读(2学分)
2、第二外国语(2学分)
博士研究生第一外国语为英语的,第二外国语可作为选修课;第一外国语为非英语的,则第二外国语必修英语。
(三)补修课:
1、无机化学
2、物理化学
跨学科或以同等学力考入的研究生必须补修1-2门本专业本科生必修课,成绩记入本人档案,不计学分。
七、转博资格考试
硕博连读研究生在入学后第三学期末实行转博资格考试,具体按学校有关文件执行。
文章来源:文彦考研。
