(广西专版)2019年中考化学总复习中考6大题型轻松搞定题型复习(六)初高中衔接题练习.doc
(广西专版)2019年中考化学总复习 中考6大题型轻松搞定 题型复习(二)推断题练习
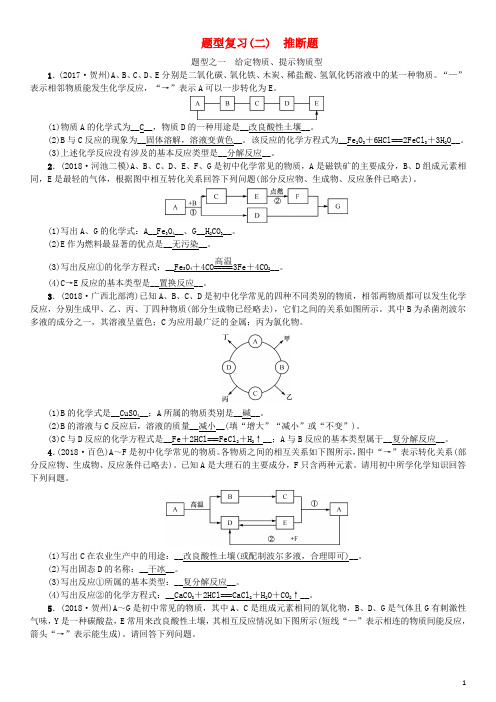
题型复习(二) 推断题题型之一 给定物质、提示物质型1.(2017·贺州)A 、B 、C 、D 、E 分别是二氧化碳、氧化铁、木炭、稀盐酸、氢氧化钙溶液中的某一种物质。
“—”表示相邻物质能发生化学反应,“→”表示A 可以一步转化为E 。
(1)物质A 的化学式为__C__,物质D 的一种用途是__改良酸性土壤__。
(2)B 与C 反应的现象为__固体溶解,溶液变黄色__。
该反应的化学方程式为__Fe 2O 3+6HCl===2FeCl 3+3H 2O__。
(3)上述化学反应没有涉及的基本反应类型是__分解反应__。
2.(2018·河池二模)A 、B 、C 、D 、E 、F 、G 是初中化学常见的物质,A 是磁铁矿的主要成分,B 、D 组成元素相同,E 是最轻的气体,根据图中相互转化关系回答下列问题(部分反应物、生成物、反应条件已略去)。
(1)写出A 、G 的化学式:A__Fe 3O 4__、G__H 2CO 3__。
(2)E 作为燃料最显著的优点是__无污染__。
(3)写出反应①的化学方程式:__Fe 3O 4+4CO=====高温3Fe +4CO 2__。
(4)C→E 反应的基本类型是__置换反应__。
3.(2018·广西北部湾)已知A 、B 、C 、D 是初中化学常见的四种不同类别的物质,相邻两物质都可以发生化学反应,分别生成甲、乙、丙、丁四种物质(部分生成物已经略去),它们之间的关系如图所示。
其中B 为杀菌剂波尔多液的成分之一,其溶液呈蓝色;C 为应用最广泛的金属;丙为氯化物。
(1)B 的化学式是__CuSO 4__;A 所属的物质类别是__碱__。
(2)B 的溶液与C 反应后,溶液的质量__减小__(填“增大”“减小”或“不变”)。
(3)C 与D 反应的化学方程式是__Fe +2HCl===FeCl 2+H 2↑__;A 与B 反应的基本类型属于__复分解反应__。
(广西专版)2019年中考化学总复习 中考6大题型轻松搞定 题型复习(一)函数图象题练习
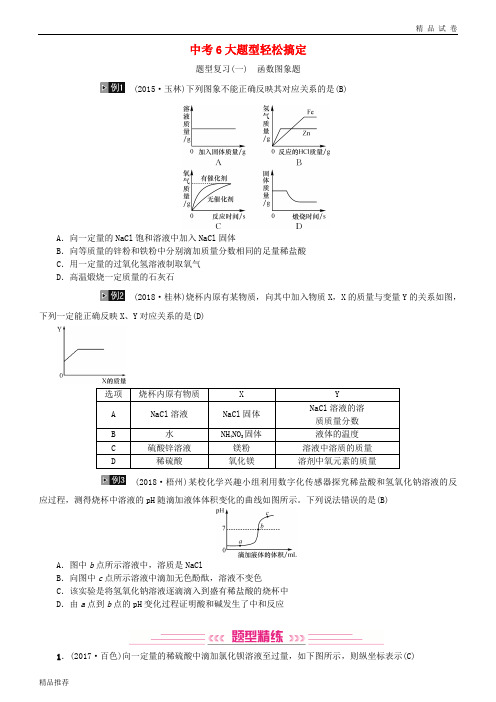
中考6大题型轻松搞定题型复习(一) 函数图象题(2015·玉林)下列图象不能正确反映其对应关系的是(B)A.向一定量的NaCl饱和溶液中加入NaCl固体B.向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸C.用一定量的过氧化氢溶液制取氧气D.高温煅烧一定质量的石灰石(2018·桂林)烧杯内原有某物质,向其中加入物质X,X的质量与变量Y的关系如图,下列一定能正确反映X、Y对应关系的是(D)(2018·梧州)某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。
下列说法错误的是(B)A.图中b点所示溶液中,溶质是NaClB.向图中c点所示溶液中滴加无色酚酞,溶液不变色C.该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中D.由a点到b点的pH变化过程证明酸和碱发生了中和反应1.(2017·百色)向一定量的稀硫酸中滴加氯化钡溶液至过量,如下图所示,则纵坐标表示(C)A.溶液的质量 B.稀硫酸的质量C.硫酸钡的质量 D.溶剂的质量2.(变式题)向氢氧化钡溶液中逐滴加入稀硫酸,某个量y随稀硫酸的加入的变化情况如图所示,则y表示(D)A.沉淀的质量 B.氢氧化钡的质量C.溶液的pH D.溶质的质量3.(例3变式题)某校化学小组在利用硫酸和氢氧化钾溶液探究酸碱中和反应时,利用数字传感器测得烧杯中溶液pH的变化图象如图所示。
下列说法正确的是(D)A.图中c点所示溶液呈碱性B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸的烧杯中D.由b点到c点的变化过程中没有发生化学反应4.(2018·柳州一模)有关a、b两种物质的溶解度曲线如图所示,下列叙述不正确的是(B)A.a物质的溶解度随着温度的升高而增大B.在t2℃时,a、b两种物质的溶液中溶质的质量分数一定相等C.将a、b两种物质的饱和溶液从t3℃降温至t1℃,a有晶体析出,b无晶体析出D.t3℃时,a物质的溶解度大于b物质的溶解度5.(2016·北海)在一密闭容器中,a、b、c、d四种物质在一定条件下发生化学反应,反应前后各物质质量变化如图,下列说法错误的是(D)A.该反应是分解反应B.b可能是催化剂C.反应前后物质的总质量保持不变D.反应生成的c和d质量相等6.(2018·衡阳)现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。
广西专版2019年中考化学总复习中考6大题型轻松搞定题型复习一函数图象题练习【word版】.doc
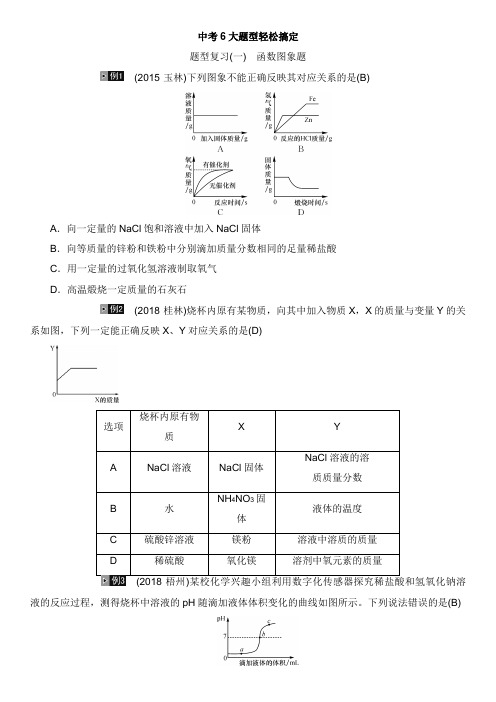
中考6大题型轻松搞定题型复习(一)函数图象题(2015·玉林)下列图象不能正确反映其对应关系的是(B)A.向一定量的NaCl饱和溶液中加入NaCl固体B.向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸C.用一定量的过氧化氢溶液制取氧气D.高温煅烧一定质量的石灰石(2018·桂林)烧杯内原有某物质,向其中加入物质X,X的质量与变量Y的关系如图,下列一定能正确反映X、Y对应关系的是(D)选项烧杯内原有物质X YA NaCl溶液NaCl固体NaCl溶液的溶质质量分数B 水NH4NO3固体液体的温度C 硫酸锌溶液镁粉溶液中溶质的质量D 稀硫酸氧化镁溶剂中氧元素的质量液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。
下列说法错误的是(B)A.图中b点所示溶液中,溶质是NaClB.向图中c点所示溶液中滴加无色酚酞,溶液不变色C.该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中D.由a点到b点的pH变化过程证明酸和碱发生了中和反应1.(2017·百色)向一定量的稀硫酸中滴加氯化钡溶液至过量,如下图所示,则纵坐标表示(C)A.溶液的质量B.稀硫酸的质量C.硫酸钡的质量D.溶剂的质量2.(变式题)向氢氧化钡溶液中逐滴加入稀硫酸,某个量y随稀硫酸的加入的变化情况如图所示,则y表示(D)A.沉淀的质量B.氢氧化钡的质量C.溶液的pH D.溶质的质量3.(例3变式题)某校化学小组在利用硫酸和氢氧化钾溶液探究酸碱中和反应时,利用数字传感器测得烧杯中溶液pH的变化图象如图所示。
下列说法正确的是(D)A.图中c点所示溶液呈碱性B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸的烧杯中D.由b点到c点的变化过程中没有发生化学反应4.(2018·柳州一模)有关a、b两种物质的溶解度曲线如图所示,下列叙述不正确的是(B)A.a物质的溶解度随着温度的升高而增大B.在t2℃时,a、b两种物质的溶液中溶质的质量分数一定相等C.将a、b两种物质的饱和溶液从t3℃降温至t1℃,a有晶体析出,b无晶体析出D.t3℃时,a物质的溶解度大于b物质的溶解度5.(2016·北海)在一密闭容器中,a、b、c、d四种物质在一定条件下发生化学反应,反应前后各物质质量变化如图,下列说法错误的是(D)A.该反应是分解反应B.b可能是催化剂C.反应前后物质的总质量保持不变D.反应生成的c和d质量相等6.(2018·衡阳)现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
题型复习(六) 初高中衔接题一、新信息1.(2017·娄底)在化学上,把由同种元素组成的不同种单质互称为“同素异形体”。
下列各组物质不属于同素异形体的是(D)A .红磷和白磷B .金刚石和石墨C .氧气和臭氧(O 3)D .二氧化硫和三氧化硫2.(2017·来宾)乙醇在一定条件下可氧化为乙醛:2CH 3CH 2OH +O 2――→一定条件2CH 3CHO(乙醛)+2H 2O 。
实际是发生了如下两个反应:反应一:2Cu +O 2――→△2CuO ,反应二:CH 3CH 2OH +CuO ――→△CH 3CHO +H 2O +Cu 。
下列说法错误的是(B)A .Cu 在反应一中是反应物B .Cu 在反应前后化学性质改变C .Cu 在反应二中是生成物D .Cu 在反应中起到催化作用3.(2017·重庆B 卷)我国的高铁技术世界领先。
高铁钢轨采用铝和氧化铁在高温下发生置换反应实现无缝焊接,该反应的化学方程式为__2Al +Fe 2O 3=====高温2Fe +Al 2O 3__。
二、元素周期律4.(2017·柳州)结构决定性质,从原子结构示意图可以推测元素的化学性质。
在元素周期表前20号元素中,最活泼的非金属元素是__F__(填元素符号),判断的依据是__其最外层电子数最多(为7),电子层数最少(为2)__。
5.(2017·泰安)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。
下列各组粒子中属于等电子体的是__BD__(填字母序号)。
A .NO 和O 2B .CO 和 N 2C .SO 2和 CO 2D .PO3-4和SO2-46.(2017·遂宁)浩瀚的海洋中蕴藏着丰富的资源,是巨大的天然宝库。
从海水中提取溴,其中一种方案涉及的化学反应为2NaBr +Cl 2===2NaCl +Br 2,已知非金属单质也有类似金属单质与盐溶液之间的反应规律,由此可判断Cl 2、Br 2的活动性顺序是Cl 2__>__(填“>”“<”或“=”)Br 2。
三、氧化还原反应7.(2017·襄阳)小杰学习时获知“元素化合价发生变化(升降)的化学反应是氧化还原反应”。
据此判断下列基本反应类型一定是氧化还原反应的是(C)A .化合反应B .分解反应C .置换反应D .复分解反应8.(2016·柳州)同学们对原子结构示意图进行深入研究,发现从原子结构示意图可以推出元素的化合价,知道金属元素无负价。
还可以利用化合价来判定氧化还原反应,化学反应中有元素化合价升降的就一定是氧化还原反应。
下列反应就是氧化还原反应,已知水中的氢元素和氧元素化合价没有变化。
A(单质)+H 2O===B(化合物)+C(化合物)请回答:A 是__非金属__(填“金属”或“非金属”)单质,原因是__A 的化合价有升、有降__。
9.(2017·绥化)初中阶段:物质得氧和失氧的反应是氧化还原反应;高中阶段:凡是有元素化合价升降的化学反应都是氧化还原反应。
元素化合价升高的为还原剂,发生氧化反应;元素化合价降低的为氧化剂,发生还原反应;氧化反应和还原反应是同时发生的,这样的反应称为氧化还原反应。
请回答下列问题:(1)根据化合价改变判断下列四种基本反应类型,一定不是氧化还原反应的是__D__。
(填字母序号) A .化合反应 B .分解反应 C .置换反应 D .复分解反应(2)下列化学反应中,属于氧化还原反应的是__B__(填字母序号),该反应的还原剂是__Fe__(填化学式)。
A .Na 2CO 3+CaCl 2===CaCO 3↓+2NaCl B .Fe +CuSO 4===Cu +FeSO 4C .Ca(HCO 3)2=====点燃CaCO 3↓+CO 2↑+H 2OD .CaO +H 2O===Ca(OH)2(3)下列反应中,氧化反应与还原反应在同一元素中进行的是__AD__。
(多选) A .Cl 2+2NaOH===NaCl +NaClO +H 2O B .4P +5O 2=====点燃2P 2O 5C .Zn +CuCl 2===Cu +ZnCl 2D .3NO 2+H 2O===2HNO 3+NO 四、离子反应型10.初中化学中,我们学习了酸和碱发生中和反应的实质是H ++OH -===H 2O 。
如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。
离子方程式的书写一般按以下步骤:(以Na 2SO 4与BaCl 2反应为例)①写出Na 2SO 4与BaCl 2反应的化学方程式:__Na 2SO 4+BaCl 2===BaSO 4↓+2NaCl__;②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。
上述方程式可改写成:2Na ++SO2-4+Ba 2++2Cl -===BaSO 4↓+2Na ++2Cl -;③删去方程式两边不参加反应的离子:Ba 2++SO2-4===BaSO 4↓; ④检查方程式两边各元素的原子个数和电荷总数是否相等。
请回答:(1)下列各组中的离子,在pH =3的水溶液中能大量共存的是__AC__;A .Na +、Mg 2+、Cl -、SO2-4B .Na +、K +、Cl -、OH -C .Na +、Cu 2+、Cl -、SO2-4D .Na +、K +、Cl -、CO2-3(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式__CaCO 3+2H +===Ca 2++H 2O +CO 2↑__;(3)写出一个与离子方程式Mg +2H +===Mg 2++H 2↑相对应的化学方程式__Mg +H 2SO 4===MgSO 4+H 2↑(或Mg +2HCl===MgCl 2+H 2↑)__;(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体、沉淀或__水__生成,反应就能发生。
五、气体的制备11.实验室用下图所示装置制取并收集气体。
A B C D E F 请回答下列各题:(1)乙炔(C 2H 2)气体可用电石(CaC 2块状固体)和水反应来制取,化学方程式为CaC 2+2H 2O===Ca(OH)2+C 2H 2↑,实验室制取乙炔(C 2H 2)气体的发生装置应选用__A__(填序号)。
(2)通常状况下,甲烷是一种无色无味的气体,难溶于水,密度比空气小。
实验室常用醋酸钠和碱石灰两种固体混合加热制得,制取并收集甲烷可选用的装置是__BD(或BF)__(填字母)。
(3)硫化氢(H 2S)气体是一种密度比空气大,能溶于水的有毒物质,其水溶液叫氢硫酸。
实验室常用硫化亚铁(FeS)固体和稀硫酸在常温下发生反应制取硫化氢气体,应选择的发生装置是__A__。
小虹同学认为收集硫化氢气体可用C 或E 装置,但小娟提出了质疑,小娟的理由是__H 2S 气体有毒,会污染空气__。
写出你改进后的收集方法:__用E 装置收集,排出的气体用塑料袋收集(或通入碱溶液)__。
12.实验室用下图所示的装置制取并探究硫化氢气体的性质。
甲 乙 丙 丁(1)甲装置中发生反应的化学方程式为__FeS +H 2SO 4===FeSO 4+H 2S ↑__; (2)实验中收集气体的方法是__向上排空气法__;(3)实验中,丙装置观察到的实验现象是__试液由紫色变为红色(或溶液变成红色)__;(4)丁装置的作用是__吸收多余的硫化氢气体(或防止剧毒的硫化氢气体扩散到空气中)__,反应的化学方程式为__H 2S +2NaOH===Na 2S +2H 2O__,反应的实质是__氢离子和氧氧根离子结合生成水(或H ++OH -===H 2O)__。
六、氨气13.(2014·柳州)通过查阅资料得知,氨气(NH 3)密度比空气小,极易溶于水,其水溶液(氨水)显碱性;在加热条件下,氨气能与氧化铜反应生成铜、水和氮气。
A B C D E F(1)写出氨气与氧化铜反应的化学方程式__2NH 3+3CuO=====△3Cu +N 2+3H 2O__。
(2)用加热固体氯化铵和固体氢氧化钙混合物来制取并收集氨气时,应选择的装置是__CB(或CF)__(填字母序号)。
(3)将收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水中,观察到的现象是__集气瓶内液面上升,溶液变红__。
14.(2016·柳州)氨气(NH 3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性。
实验室里加热氯化铵(NH 4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水。
(1)下列装置是实验室制取气体的一些发生装置,a 仪器为__试管__,b 仪器为__酒精灯__。
制取二氧化碳的发生装置是__D__(填字母序号);制取氨气的发生装置是__C__(填字母序号),收集氨气的方法是__向下排空气法__。
A B C D图1(2)图1是氨气的喷泉实验装置。
打开橡皮管上的夹子,将胶头滴管中的水挤入盛满干燥氨气的烧瓶中,因为氨气极易溶于水,烧瓶内的压强降低,烧杯中的水就会进入烧瓶,形成__红__色的喷泉。
(3)当喷泉实验结束后,测烧瓶内溶液的pH 。
步骤如下:步骤一:用手撕一小段pH 试纸,放到干净的玻璃片上。
步骤二:用蒸馏水润湿pH 试纸。
步骤三:用玻璃棒蘸取待测液滴到pH 试纸上。
步骤四:把试纸显示的颜色与标准比色卡对比,读取pH 。
该实验步骤有几处错误?__一__处,请改正:__步骤二去掉,不用蒸馏水润湿pH 试纸__。
七、氯气15.实验室制取有毒的氯气(Cl 2)时,常用烧碱溶液来吸收多余的氯气,其反应的化学方程式为Cl 2+2NaOH===NaClO +NaCl +H 2O(其中NaClO 是次氯酸钠,ClO -叫次氯酸根)。
试写出工业上以氯气和熟石灰为原料制取漂白粉的化学反应方程式__2Cl 2+2Ca(OH)2===Ca(ClO)2+CaCl 2+2H 2O__。
16.(2017·河南)电解食盐水可得到烧碱、氯气(Cl 2)和一种可燃性气体,反应的化学方程式为__2NaCl +2H 2O=====通电2NaOH +H 2↑+Cl 2↑__;配制质量分数为5%的氯化钠溶液,若量取水时俯视量筒刻度读数(其他操作正确),溶液的质量分数__大于__(填“大于”“小于”或“等于”)5%;现有NaCl 和NaBr 的混合物共2.2 g ,溶于水并加入过量的AgNO 3溶液后,生成AgCl 和AgBr 沉淀共4.75 g ,则原混合物中含钠元素的质量为__0.69__g 。
八、过氧化物17.(2016·柳州)过氧化氢溶液俗称双氧水,在实验室中可用来制取氧气,其反应的化学方程式为__2H 2O 2=====MnO22H 2O +O 2↑__。
