大肠菌群测定原始记录
总大肠菌群原始记录表

总大肠菌群检验数据原始记录
委托书编号:委托单位:
检测项目:总大肠菌群检测依据:GB/T 5750.12-2006 2.1多管发酵法
样品名称:样品数量:
样品编号:样品状态:
收样日期:检测日期:
环境温度:环境湿度:
操作方法:
一、乳糖发酵实验
1、取10ml水样接种到10ml二倍乳糖蛋白胨培养液中,取1ml水样接种到10ml单料乳糖蛋白胨培养液中,另取1ml水样注入到9ml灭菌生理盐水中,混匀后吸取1ml (即0.1ml水样)注入到10ml单料乳糖蛋白胨培养液中,每一稀释度接种5管。对已处理过的出厂自来水,需经常检验或每天检验一次的,可直接种5份10ml水样双料培养基,每份接种10ml水样。
培养温度
培养时间
二倍浓缩乳糖蛋白胨培养液
36±1°C
24h±2h
乳糖蛋白胨培养液
36±1°C
24h±2h
EMB
36±1°C
24h±2h
观察结果
序号
样品编号
乳糖发酵
复发酵
结果报告(MPN/100mL)
10ml
1ml
0.1ml
10ml
1ml
0.1ml
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
操作人:复核人:二、分来自培养:经培养24h后,将产酸产气的发酵管,分别接种于伊红美蓝平板上,36±1°C恒温培养8h-24h,观察形态,挑取数个可疑菌落进行涂片、革兰氏染色、镜检。
20-6.大肠菌群检验原始记录

(3)BGLB肉汤证实试验阳性管数
3
(1)吸取1mL样液于VRBA平板36.0℃培养24h后,是否有沉淀环的紫红色菌落生长
(2)从合适稀释度上挑取典型和可疑菌落数(个)
(3)BGLB肉汤证实试验阳性管数
4
(1)吸取1mL样液于VRBA平板36.0℃培养24h后,是否有沉淀环的紫红色菌落生长大肠菌群检验原始记录来自检验项目大肠菌群
样品状态
□完好□异常
检验
方法
GB 4789.3—2016(第二法)
仪器
设备
样品
处理
□固体样品:无菌操作称取25g加入到225mL无菌生理盐水均质袋中,拍打1~2min
□液体样品:无菌吸管吸取25mL加入到225mL灭菌生理盐水中,充分混匀
样品
序号
培养过程
稀释倍数
结果计算
(2)从合适稀释度上挑取典型和可疑菌落数(个)
(3)BGLB肉汤证实试验阳性管数
5
(1)吸取1mL样液于VRBA平板36.0℃培养24h后,是否有沉淀环的紫红色菌落生长
(2)从合适稀释度上挑取典型和可疑菌落数(个)
(3)BGLB肉汤证实试验阳性管数
琼脂
对照
0 CFU/皿
盐水
对照
0 CFU/mL
检验人:
复核人:
检验日期:
报告CFU/g
100
10-1
10-2
10-3
1
(1)吸取1mL样液于VRBA平板36.0℃培养24h后,是否有沉淀环的紫红色菌落生长
(2)从合适稀释度上挑取典型和可疑菌落数(个)
(3)BGLB肉汤证实试验阳性管数
2
大肠菌群检测原始记录

发酵试验
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
阳性管数
报出值 MPN/ml
审核:
年月
日
编号: 样品名称:
检验依据:GB/T4789.3-2016 培养开始时间: 年 月 培养结束时间: 年 月
稀பைடு நூலகம்度
1
稀释度
项目 管号
1 2 3 1 2 3 1 2 3
项目 管号
2
稀释度
3
稀释度
4
稀释度
1 2 3 1 2 3 1 2 3
项目 管号
1 2 3 1 2 3 1 2 3
项目 管号
1 2 3 1 2 3 1 2 3
项目 管号
1
2
3
5
1
2
3
1
2
3
检验员:
大肠菌群检测原始记录
批次:
日时
日时
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
恒温时间: h 恒温温度:36℃±1℃
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
发酵试验
阳性管数
报出值 MPN/ml
LST肉汤管初 BGLG肉汤管复
发酵试验
大肠菌群、沙门氏菌GBT23780检测原始记录
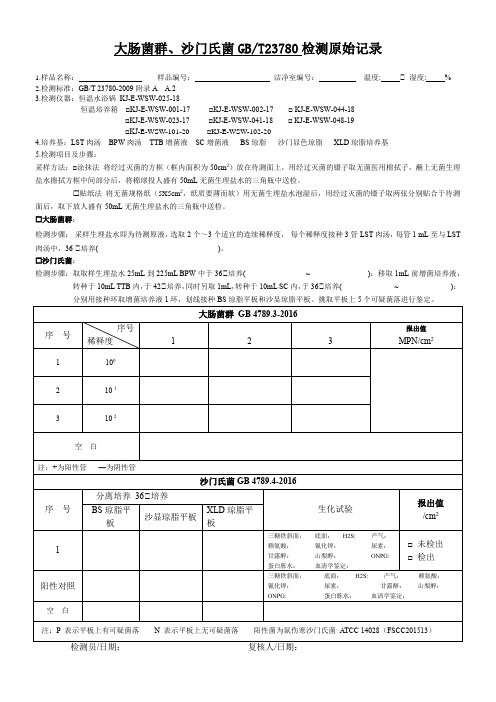
大肠菌群、沙门氏菌GB/T23780检测原始记录1.样品名称:样品编号:洁净室编号:温度: ℃ 湿度: %2.检测标准:GB/T 23780-2009附录A A.23.检测仪器:恒温水浴锅KJ-E-WSW-025-18恒温培养箱□KJ-E-WSW-001-17 □KJ-E-WSW-002-17 □ KJ-E-WSW-044-18□KJ-E-WSW-023-17 □KJ-E-WSW-041-18 □ KJ-E-WSW-048-19□KJ-E-WSW-101-20□KJ-E-WSW-102-204.培养基:LST肉汤BPW肉汤TTB增菌液SC增菌液BS琼脂沙门显色琼脂XLD琼脂培养基5.检测项目及步骤:采样方法:□涂抹法将经过灭菌的方框(框内面积为50cm2)放在待测面上,用经过灭菌的镊子取无菌医用棉拭子,蘸上无菌生理盐水擦拭方框中间部分后,将棉球投人盛有50mL无菌生理盐水的三角瓶中送检。
贴纸法将无菌规格纸(5X5cm2,纸质要薄而软)用无菌生理盐水泡湿后,用经过灭菌的镊子取两张分别贴合于待测面后,取下放人盛有50mL无菌生理盐水的三角瓶中送检。
大肠菌群:检测步骤:采样生理盐水即为待测原液,选取2个~3个适宜的连续稀释度,每个稀释度接种3管LST肉汤,每管1 mL至与LST 肉汤中,36 ℃培养( )。
沙门氏菌:检测步骤:取取样生理盐水25mL到225mL BPW中于36℃培养( ~ );移取1mL前增菌培养液,转种于10mL TTB内,于42℃培养,同时另取1mL,转种于10mL SC内,于36℃培养( ~ );分别用接种环取增菌培养液1环,划线接种BS琼脂平板和沙显琼脂平板。
挑取平板上5个可疑菌落进行鉴定。
检测员/日期:复核人/日期:。
水质 总大肠菌群和粪大肠菌群的测定原始记录

年 月 日颁布
- -J177 水质 总大肠菌群和粪大肠菌群的测定原始记录 第 页共 页
项目编号
温度(℃)
湿度(%RH)
分析方法 水质 总大肠菌群和粪大肠菌群的测定 纸片快速法 HJ 755-2015[检出限:20MPN/L]
仪器名称
检测仪器
恒温培养箱 恒温培养箱
压力蒸汽灭菌器
仪器型号
仪器编号
备注
葡萄球菌,粪大肠菌群阳性对照为大肠埃希氏菌,阴性对照为产气肠杆菌。
[+阳性 -阴性]
检测:
复核:
日期:
年月日
测定样品信息[样品种类:废水 地表水 其他
]
样品编号 样品接种量 Q
ห้องสมุดไป่ตู้样品
样品包装 密封良好 其他
总大肠菌群 阳性对照 阴性对照
粪大肠菌群 样品 阳性对照 阴性对照
空白 对照
mL×5
mL×5
mL×5
MPN 值 M -
(MPN/100mL)
报告值 C -
(MPN/L)
空白对照为纯水,总大肠菌群阳性对照为大肠埃希氏菌,阴性对照为金黄色
公式:
式中:
C 100 M Q
C:水样总大肠菌群或粪大肠菌群
浓度(MPN/L);
M:查 MPN 表得到的 MPN 值
(MPN/100mL);
Q:实际水样最大接种量(mL);
100:为 10×10mL,其中,10 将 MPN 值
的单位 MPN/100mL 转换为 MPN/L,
10mL 为 MPN 最大接种量。
大肠菌检验原始记录
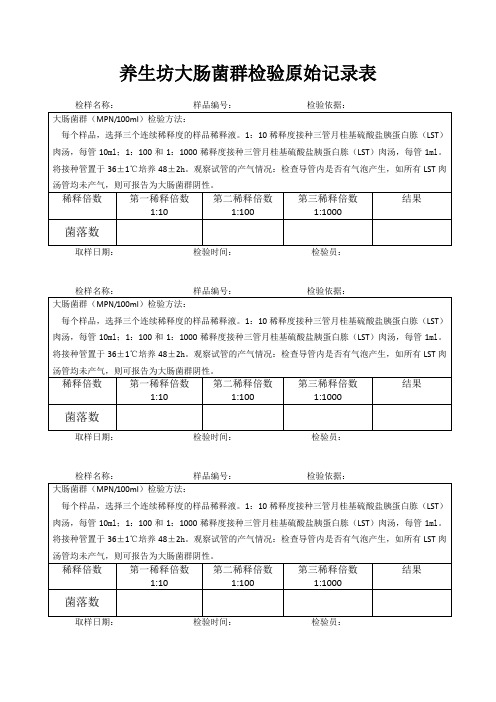
养生坊大肠菌群检验原始记录表检样名称:样品编号:检验依据:大肠菌群(MPN/100ml)检验方法:每个样品,选择三个连续稀释度的样品稀释液。
1:10稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管10ml;1:100和1:1000稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管1ml。
将接种管置于36±1℃培养48±2h。
观察试管的产气情况:检查导管内是否有气泡产生,如所有LST肉汤管均未产气,则可报告为大肠菌群阴性。
稀释倍数第一稀释倍数1:10 第二稀释倍数1:100第三稀释倍数1:1000结果菌落数取样日期:检验时间:检验员:检样名称:样品编号:检验依据:大肠菌群(MPN/100ml)检验方法:每个样品,选择三个连续稀释度的样品稀释液。
1:10稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管10ml;1:100和1:1000稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管1ml。
将接种管置于36±1℃培养48±2h。
观察试管的产气情况:检查导管内是否有气泡产生,如所有LST肉汤管均未产气,则可报告为大肠菌群阴性。
稀释倍数第一稀释倍数1:10 第二稀释倍数1:100第三稀释倍数1:1000结果菌落数取样日期:检验时间:检验员:检样名称:样品编号:检验依据:大肠菌群(MPN/100ml)检验方法:每个样品,选择三个连续稀释度的样品稀释液。
1:10稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管10ml;1:100和1:1000稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管1ml。
将接种管置于36±1℃培养48±2h。
观察试管的产气情况:检查导管内是否有气泡产生,如所有LST肉汤管均未产气,则可报告为大肠菌群阴性。
稀释倍数第一稀释倍数1:10 第二稀释倍数1:100第三稀释倍数1:1000结果菌落数取样日期:检验时间:检验员:。
菌落总数、大肠菌群原始记录

检样细菌总数:
□cfu/mL □cfu/g
大肠菌群最近似值:检验依据 GB/T4789.3
样 品 稀释度 样品接种量 毫升管号 1 10mL 2 3 1 1mL 2 3 1 0.1mL 2 3 标准值: □MPN/100mL □MPN /100g □MPN/mL □MPN /g 结 论: LST 肉汤 初发酵试验 BGLB 肉汤 复发酵
YSJL01-002
菌落总数、大肠菌群检验数据原始记录
样品编号____________
主要仪器设备:□电子天平( )、 □电热恒温培养箱(
第ቤተ መጻሕፍቲ ባይዱ
页共
页
)
)、 □显微镜(
菌落总数:检验依据 GB/T 4789.2
样品稀释度 检 测 值: □cfu/mL □cfu /g 计算平板菌落数 cfu 标 准 值: □cfu/mL □cfu/g 结论:
检样大肠菌群最近似值:
检样大肠菌群最近似值相当于: □MPN/100mL □MPN /100g
备注:
检验人员、检验日期 校核人员、校核日期
大肠菌群检验原始记录第二法
共页;第页
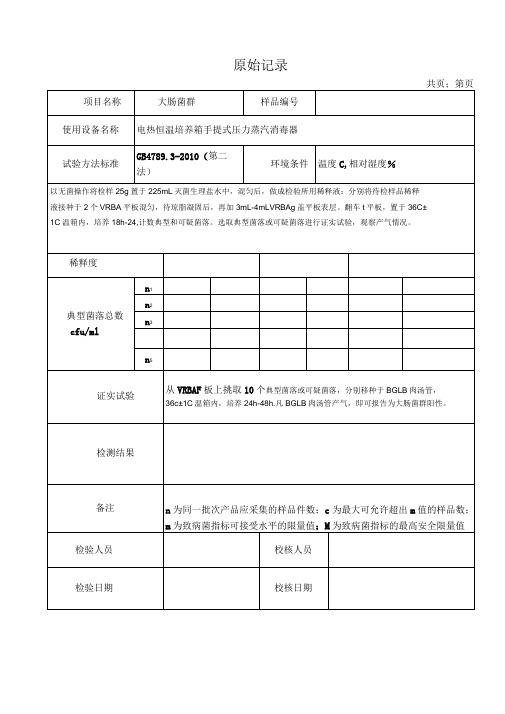
项目名称
大肠菌群
样品编号
使用设备名称
电热恒温培养箱手提式压力蒸汽消毒器
试验方法标准
GB4789.3-2010(第二
法)
环境条件
温度C,相对湿度%
以无菌操作将检样25g置于225mL灭菌生理盐水中,混匀后,做成检验所用稀释液:分别将待检品稀释
液接种于2个VRBA平板混匀,待琼脂凝固后,再加3mL-4mLVRBAg盖平板表层。翻车t平板,置于36C±
1C温箱内,培养18h-24,计数典型和可疑菌落。选取典型菌落或可疑菌落进行证实试验,观察产气情况。
稀释度
典型菌落总数
cfu/ml
n1
n2
n3
n5
证实试验
从VRBAF板上挑取10个典型菌落或可疑菌落,分别移种于BGLB肉汤管,
36c±1C温箱内,培养24h-48h.凡BGLB肉汤管产气,即可报告为大肠菌群阳性。
检测结果
备注
n为同一批次产品应采集的样品件数;c为最大可允许超出m值的样品数;m为致病菌指标可接受水平的限量值;M为致病菌指标的最高安全限量值
检验人员
校核人员
检验日期
校核日期
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
时间:检验地点:本厂化验室
检测样品名称:来源:
生理盐水的配制:8.5g氯化钠加1000ml蒸馏水溶解待用。
1.取225ml生理盐水于标签为1:10的300ml锥形瓶中,
取9ml生理盐水于标签为1:100的50ml锥形瓶中。
2.LST溶液的配制:取LST7.1g加水100ml(双料),溶解至透明,
取1:100的稀释样1ml于标有0.01g的3只试Байду номын сангаас中,
5.培养:放入36℃的培养箱中培养48h。时间起始:
24h产气管数:
48h产气管数:
6.BGLB溶液复发酵试验:配制BGLB溶液,称取BGLB4g溶液100ml水中,均分倒入对应产气标号的标有标示并放有聚气管的试管中,放入灭菌锅灭菌15min。用接种针粘一环产气管液于标有对应的以灭菌的BGLB溶液的试管中,于36℃的培养箱中培养48h。
倒入10ml于3只标有1g的并放有聚气管的试管中;剩余溶液加一倍水配成单料倒入标有0.01g,0.001ml的6只试管中,每只10ml,并放有聚气管(试管要求180×18mm)。
放入灭菌锅灭菌15min.
以上1;2;同时一起灭菌,灭菌起始时间(喷气开始计时):
压力表指针回零后打开放气阀,开盖取出,冷至常温。
培养起始时间:
48h产气管数:
7.检索MPN表结论:
备注:
3.样品稀释:于225ml灭菌的生理盐水中加入样品25g,混匀,配成1:10的稀释样;
从1:10的稀释样中取1ml到入标有1:100的9ml灭菌的生理盐水中混匀,配成1:100稀释样;
4.初发酵试验:取1:10的稀释样10ml于标有1g的3只试管中,
取1:10的稀释样1ml于标有0.1g的3只试管中,
