烃燃烧规律计算
烃的计算

练习
常温常压下,a毫升两种气态烃混合物与足量 氧气混合点燃爆炸后,恢复到原来的状态体 积缩小2a毫升,则两种烃可能是( ) (A) CH4 C2H4 (B) C2H6 C3H6 (C) CH4 C2H6 (D) C2H2 C3H8
做在练习本上
在标准状况下10ml某气态烃在80ml氧气中充 分燃烧后,恢复到标准状况,所得气体的体 积为60ml,该烃是 A、乙烷 B、丙烷 C、丙烯 D、丁烯
烃完全燃烧时耗氧量规律
①物质的量相同的烃,(x+y/4)越大,耗氧 量越大 ②质量相同的烃,y/x越大(相当于含氢量大), 则耗氧量越多, 此时就把CxHy改写成CHy/x,y/x越大耗氧量越 大。 ③质量相同的烃, x/y越大(相当于含碳量大), 则生成的二氧化碳越多,
④ 质量相同的烃, ____越大,则生成的水 越多。 ⑤质量相同的烃, ______相等,则生成的 水和CO2相等。
练习
在常温常压下,取下列四种气态烃各1mol, 分别在足量的氧气中燃烧,消耗氧气最多 的是( )
A、CH4 C、C3H8 B、C2H6 D、C4H10
练习
等质量的下列物质, A、CH4 B、C2H2 C、C2H4 D、C6H6 耗氧量由大到小的是______________. 生成CO2的量有小到大的是_________.
练习
若1mol某气态烃完全燃烧,需用3mol氧气, 则其分子式为_________.
烃的计算
一、烃的燃烧规律
烃的通式:CxHy, 烃燃烧的通式: CxHy + (x+y/4)O2 xCO2+y/2H2O 1、当温度大于100℃时,若物质均是气体, 则有△V=V前-V后 =1- y/4, ①当y=4时,△V=0,体积不变。 ②当y<4时,△V>0,体积减小。 ③当y>4时,△V<0,体积增大。
烃燃烧规律
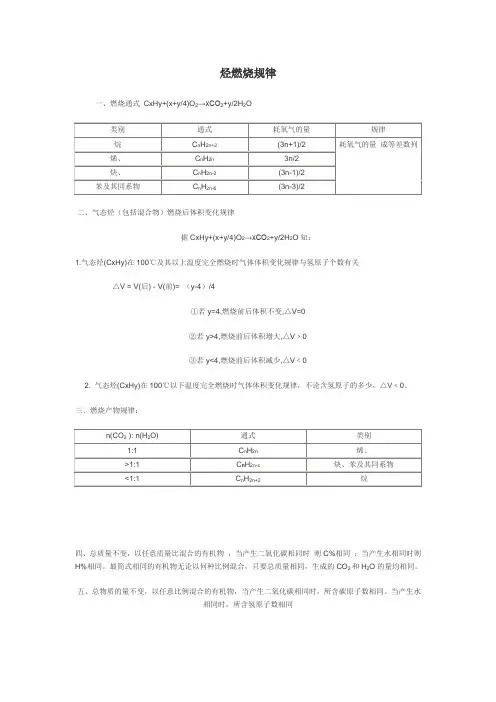
烃燃烧规律一、燃烧通式CxHy+(x+y/4)O2→xCO2+y/2H2O二、气态烃(包括混合物)燃烧后体积变化规律据CxHy+(x+y/4)O2→xCO2+y/2H2O知:1.气态烃(CxHy)在100℃及其以上温度完全燃烧时气体体积变化规律与氢原子个数有关△V = V(后) - V(前)= (y-4)/4①若y=4,燃烧前后体积不变,△V=0②若y>4,燃烧前后体积增大,△V﹥0③若y<4,燃烧前后体积减少,△V﹤02. 气态烃(CxHy)在100℃以下温度完全燃烧时气体体积变化规律,不论含氢原子的多少,△V﹤0。
三、燃烧产物规律:四、总质量不变,以任意质量比混合的有机物,当产生二氧化碳相同时则C%相同;当产生水相同时则H%相同。
最简式相同的有机物无论以何种比例混合,只要总质量相同,生成的CO2和H2O的量均相同。
五、总物质的量不变,以任意比例混合的有机物,当产生二氧化碳相同时,所含碳原子数相同。
当产生水相同时,所含氢原子数相同六、消耗氧气的量的规律1.等物质的量的烃完全燃烧时,其耗氧量的大小取决于(x+y/4)。
2.等质量的烃完全燃烧,其耗氧量的大小取决该烃分子中氢的质量分数,其值越大,耗氧量越大。
设烃的质量为m ,含氢的质量分数为ω,有关系式C~O2~CO2及4H~O2~2H2O可知该厅的耗氧量为:n(O2) = m(1-ω)/12 + mω/4= m/12 +mω/6当m 为定值时,ω值越大,耗氧量就越大。
①对于等质量的烷烃,碳原子数越多,氢的质量分数越小,耗氧量越小,由此可知CH4的耗氧量最多。
②对于等质量的单烯烃,因炭、氧的个数比为定值,股氢的质量分数也为定值,即耗氧量相等。
③对于等质量的炔烃,碳原子数越多,氢的质量分数越大,耗氧量越多,由此可知C2H2的耗氧量最少。
④等质量烷烃、单烯烃、炔烃,因为氢的质量分数关系导致耗氧量的关系如下:“烷烃﹥烯烃﹥炔烃”。
高中化学选修5-烃的燃烧规律

有关烃燃烧的规律一、烷烯炔各类烃含碳(或氢)质量分数的变化规律:1.烷烃:C n H2n+2(n≥1)W(C)=12n/(14n+2)×100% 随n的增大,烷烃W(C)逐渐增大,但永远小于85.7%。
甲烷是烷烃中W(H)最高的。
2.烯烃(或环烷烃):C n H2n(n≥2)W(C)=12n/14n×100%=85.7%即烯烃的W(C)是固定不变的。
3.炔烃(或二烯烃):C n H2n-2(n≥2)W(C)=12n/(14n-2)×100% 随n的增大,炔烃W(C)逐渐减小,但总比烯烃的W(C)高,即总大于85.7%。
乙炔是炔烃中含碳量最高的。
二、烃的燃烧规律:烃的可燃性是烃的一个基本性质,有关烃的燃烧计算和比较是中学化学中常见的习题,掌握烃的燃烧规律,对解决这类习题会起到事半功倍的效果。
烃类燃烧可用通式表示:CxHy + (x+y/4)O2 →xCO2 + y/2H2O1..等物质的量的不同烃燃烧时的耗氧规律:(1)耗O2量取决于(x+y/4),(x+y/4)越大,消耗氧气越多。
(2)产生CO2的量取决于x,x越大,产生CO2的量越多。
(3)产生H2O的量取决于y,y越大,产生H2O的量越多。
例1:等物质的量的CH4、C2H4、C2H2,分别在足量氧气中完全燃烧,以下说法正确的是()A.C2H2含碳量最高,燃烧生成的CO2最多B.C2H2燃烧时火焰最明亮C.CH4含氢量最高,燃烧生成的水最多D.CH4、C2H4燃烧生成的水质量不同,消耗的氧气不同。
例2:1molCxHy(烃)完全燃烧需要5molO2,则X与Y之和可能是( )A.X+Y=5 B.X+Y=7 C.X+Y=11 D.X+Y=92.等质量的不同烃完全燃烧时的耗氧规律:1molC(12g)消耗1mol O2,而4molH(4g)也消耗1molO2,故质量相等的不同烃完全燃烧时,氢元素的质量分数H%越大,消耗O2越多,产生的H2O越多;反之碳元素的质量分数C%越大,消耗O2越少,产生的CO2则越多。
烃的燃烧通式

烃的燃烧通式烃是一类含有碳氢化合物的有机化合物,它们在燃烧过程中可以产生大量的热能。
烃的燃烧过程可用通式表示,该通式描述了在适当的反应条件下,烃与氧气反应产生二氧化碳和水的转化过程。
燃烧通式可以用于描述烃的燃烧反应以及计算与燃烧相关的能量变化。
烃的燃烧通式的一般形式为:CₙHₙ + (n + m/4)O₂ → nCO₂ + (m/2)H₂O其中,CₙHₙ代表烃的化学式,n和m分别代表烃中碳和氢的摩尔数。
通式中的系数n和m表示在适当的物质量条件下与氧气反应时生成的相应物质的摩尔数。
生成物的化学式为nCO₂和(m/2)H₂O,其中n表示生成的CO₂的摩尔数,(m/2)表示生成的H₂O的摩尔数。
在燃烧通式中,燃料(烃)被氧气氧化,生成二氧化碳和水。
例如,对于甲烷(CH₄)的燃烧反应,其燃烧通式可以写为:CH₄ + 2O₂ → CO₂ + 2H₂O在这个例子中,甲烷的一个分子与两个氧气分子发生反应,产生一个二氧化碳分子和两个水分子。
这个通式代表了甲烷的燃烧反应过程,同时给出了燃烧反应中生成物的相对摩尔比例。
烃的燃烧通式可用于描述不同种类的烃燃烧反应。
例如,乙烷的燃烧通式为:C₂H₆ + 7/2O₂ → 2CO₂ + 3H₂O丙烷的燃烧通式为:C₃H₈ + 9/2O₂ → 3CO₂ + 4H₂O通过这些燃烧通式,我们可以了解到燃烧过程中烃与氧气的摩尔比例,以及生成的二氧化碳和水的摩尔比例。
燃烧反应中生成二氧化碳和水的摩尔比例是根据化学方程式中的系数确定的,并符合化学方程式的摩尔比例关系。
除了描述燃烧反应的化学方程,燃烧通式还可以用于计算与燃烧相关的能量变化。
燃烧反应是放热反应,因此燃烧通式中的反应物与生成物之间的能量差是负值。
根据燃烧通式,我们可以计算出燃烧反应的能量变化,这是理解燃烧反应的重要方面。
燃烧通式还可以用于研究燃烧反应的条件和化学动力学。
通过燃烧通式,我们可以确定燃烧反应所需的理论氧化剂量,以及生成物的相对摩尔比例。
烃类完全燃烧的计算规律

烃类完全燃烧的计算规律高中有机化学的学习中,经常涉及烃类完全燃烧的计算的题目。
如何解决这一类题目,既是难点,也是重点内容之一。
为了使同学们熟练解题,系统掌握基础知识,现将有关规律总结如下,供大家参考。
一、烃类完全燃烧的通式CxHy + (x+y/4)O2→xCO2 + (y/2)H2O二、烃类完全燃烧前后体积(分子总数)的变化规律1、同温同压下,1体积烃类完全燃烧,当生成的水为气态时(温度高于100℃)△V = V前– V后= 1 + x + y/4 – x – y/2 =1 – y/4当△V ? 0时, V前? V后,则燃烧前后气体的体积减小,此时y ? 4当△V?0时, V前?V后,则燃烧前后气体的体积减小,此时y ?4当△V =0时, V前= V后,则燃烧前后气体的体积减小,此时y = 4可见,当温度高于100℃时,燃烧前后的体积的变化与碳原子数无关,与氢原子数有关。
例如:150℃时,CH4、C2H4完全燃烧前后的体积不变(即分子数不变),而C2H2燃烧前后的体积变小,C2H6等氢原子数大于4的烃燃烧前后的体积变大。
对于混合气体,求氢原子的平均原子数,亦可适用。
练习1:120℃时,下列气体物质(或混合物)各 a mol,在氧气中完全燃烧,燃烧前后体积不变的有(),燃烧前的体积大于燃烧后的体积的有(),燃烧前的体积小于燃烧后的体积的有()。
A、C2H2B、C2H4与C2H2C、C2H2与C3H6(1:1)D、C3H8与CH4(1:1)E、C2H4与C3H4答案:(C、E); (A、B); (D)2、同温同压下,1体积烃类完全燃烧,当生成的水为液态时(温度低于100℃)。
△V = V前– V后= 1 + x + y/4 – x =1 + y/4则必然△V ? 0, V前? V后,则燃烧前后气体的体积一定减小,这取决于氢原子数,氢原子数越多,体积减少的越多。
例如:在50℃时,1mol的C2H6燃烧前后气体体积减少要比1mol的C2H4体积减少的多。
有机物燃烧规律

1、1000C以上,烃的燃烧通式为:CxHy + (x+y/4)O2 xCO2+y/2H2O。
当y=4时,反应前后体积不变;当y>4时,燃烧后体积增大;当y<4时,燃烧后体积减小。
2、1000C以上,烃的含氧衍生物燃烧通式:CxHyOz + (x+y/4-z/2) xCO2+y/2H2O。
当y=4-2z 时,燃烧前后体积不变;当y>4-2z时,燃烧前后体积增大;当y<4-2z时,无此含氧衍生物。
二、有机物燃烧耗氧量规律1、等质量的烃(CxHy )完全燃烧时,耗氧量的大小与烃中氢元素质量分数的大小有关,且氢元素的质量分数越大,耗氧量越大,即y/x越大,耗氧量越大。
2、等物质的量的烃(CxHy)完全燃烧时,耗氧量的大小取决于(x+y/4)值,(x+y/4)越大,耗氧量越大。
3、一定质量具有相同最简式的有机物混合物完全燃烧时,其耗氧量为定值而与混合物各组分的含量无关,恒等于同质量的某单一组分完全燃烧时的耗氧量。
三、有机物燃烧后生成CO2和H2O的规律1、在1000C以上时,若有机物完全燃烧生成的CO2和H2O的体积相等(或物质的量相等),有机物分子中所含的氢原子数是碳原子数的2倍。
如CnHn(烯烃或环烷烃)、CnH2nO(醛或酮)、CnH2nO2(羧酸或酯)、葡萄糖和果糖等。
2、在1000C以上时,若有机物完全燃烧生成的CO2和H2O的体积(或物质的量)之比为2:1,有机物分子中的碳原子数必和氢原子数相等。
如C2H2、C6H6、C6H5OH、C8H8等。
3、在1000C以上时,若有机物完全燃烧生成的CO2和H2O的体积(或物质的量)之比为1:2,有机物分子中氢原子数必是碳原子数的4倍。
如CH4、CH3OHCO(NH2)2等。
四、有机混合物燃烧时耗氧量与生成物的量关系规律1、混合物总物质的量一定时:①A、B两种有机物不论以何种比例混合,只要物质的量之和不变,完全燃烧时消耗的O2和生成的CO2的物质的量也不变。
烃完全燃烧的三大规律
y y 烧前后体积不变,得 1+(x+4)=x+2(120 ℃),解得 y=4。依题 y 意,4 体积 O2 为适量或过量,故 x+4≤4 y y 烃燃烧通式为 CxHy+(x+4)O2――→xCO2+2H2O 依上式可得如下规律: y y (1)物质的量相同的烃,(x+4)越大,耗氧量越多,若两种烃(x+4) 相等,则耗氧量相同。 y (2)质量相同的烃,x越大(含氢量越大),则耗氧量越多,若两种烃 y 的x相等,质量相等时,则耗氧量相同。
有关,可能增大,可能不变,也可能减小。
典例5
120 ℃时,1体积某烃和4体积O2混合,完全燃烧后,恢
复到原来的温度和压强,测得反应前后气体的体积不变。该烃分
子中所含的碳原子数不可能是( D )
A.1
解析
B.2
C.3
D.4
点燃 y y 烃燃烧通式为 CxHy+(x+4)O2――→xCO2+2H2O(g), 由燃
则 2CO 2 x
点燃 + O2――→2CO2 1 x/2 2 x
ΔV 1 x/2
CH4 y
+
点燃 2O2――→CO2+2H2O(g) 2y y 2y
根据题意,x+y=a,x/2=a/4
则有x=y=a/2
若要保证气体完全燃烧,O2必须足量,即b≥x/2+2y,即b≥5a/4。
答案 ①0.33 ②b≥5a/4
x (3)质量相同的烃,y越大(含碳量越大),则生成的 CO2 越多,若 x 两种烃的y相等, 质量相等时, 则生成的 CO2 和 H2O 的量均相等。
典例6 A.CH4
等质量的下列烃完全燃烧时,消耗氧气量最多的是( A ) B.C2H6 C.C3H6 D.C6H6
解析 12 g碳和4 g氢分别完全燃烧都消耗1 mol O2,显然,含氢
人教版高中化学选择性必修第3册 第2章 微专题1 烃的燃烧规律及有关计算
微专 题强 化训 练
点击右图进入…
18
Thank you for watching !
8
由①②③式知,在 25 ℃、101 kPa 时, 1 mL C2H6 完全燃烧,气体会减少1+72-2mL=2.5 mL; 1 mL C2H2 完全燃烧,气体会减少1+52-2mL=1.5 mL; 1 mL C3H6 完全燃烧,气体会减少1+92-3mL=2.5 mL;
9
设 C2H6 和 C3H6 共 x mL,C2H2 为 y mL,可列方程组: x+y=32 2.5x+1.5y=72 解得 x=24,y=8。 故原混合烃中乙炔的体积分数为382×100%=25%。]
32 mL 与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温
度和压强,气体总体积缩小了 72 mL,原混合烃中乙炔的体积分数
为( )
A.12.5%
B.25%
C.50%
D.75%
7
B [乙烷、乙炔和丙烯完全燃烧的化学方程式分别为 C2H6+72O2―点―燃→2CO2+3H2O……① C2H2+52O2―点―燃→2CO2+H2O……② C3H6+92O2―点―燃→3CO2+3H2O……③
12 g 1 mol
4g
1 mol
当烃的质量相同时,xy越大,耗氧量越大(最简式相同的烃,无论
以何种比例混合,耗氧量都相同)。
3
(3)气态烃燃烧时气体体积的变化 ①若温度大于 100 ℃,即 H2O 为气态,则1+x+4y可当作参加 反应的气体体积,x+2y可当作生成的气体体积,故体积变化 ΔV=1 -4y,则当
12
2.取 10 mL 无论以何种比例混合的两种气态烃的混合气体,在
50 mL 的氧气中充分燃烧生成 CO2 和液态 H2O,燃烧后所得气体的 体积为 35 mL,则该混合气体可能为 ( )
烃(CxHy)的燃烧规律.
练习
1.CH4,C2H2,C2H4,C2H6,C3H4,C3H6完全 燃烧,反应后温度为120 ℃ ,则反应后, 体积不变的是哪种气体?体积减小的是哪 种气体?体积增=0
y>4时, △V>0 y<4时, △V<0
体积不变的是CH4,C2H4,C3H4 体积减小的是C2H2 体积增大的是C2H6,C3H6
而且,Vm在相同条件下,数值相同, 可以得到结论 M/M(H2)=36; 所以,M=72g/mol;
而该烷烃的摩尔质量M=14n+2,得到等式:14n+2=72,
解得n=5,
所以,该烷烃的分子式为:C5H12
练习
某烃,其蒸汽的密度是相同条件下一氧化碳
的密度2倍,测得含碳量为85.7%,试求该 烃的分子式。
解:根据题意,可以得到结论:
M/M(CO)=2 ; M=56g/mol
设该烃的分子式为CxHy;根据含碳量,得:
12x/56=85.7%
y/56=(1-85.7)%
解得:x=4;
y=8
所以,该烃的分子式为:C4H8
2.根据烃的燃烧通式确定
例:某烃0.1mol完全燃烧,将产物通人浓硫 酸,增重5.4g,再通入到NaOH溶液中,增 重8.8g,试确定该烃的分子式。
烃(CxHy)的燃 烧规律
1.等物质的量的烃完全燃烧耗氧量比较的规律:
对于等物质的量的任意烃(CxHy) ,完全燃 烧,耗氧量的大小取决于(x+y/4) 的值的大 小,该值越大,耗氧量越多。
原理:
烃的燃烧通式为: CxHy + (x+y/4)O2 →xCO2 + y/2 H2O 若烃的物质的量相同,则,烃前面的系数必然相同, 因此,耗氧量的大小直接决定于氧气前面的系数。
烃燃烧规律
• 规律 :当温度高于 规律3 温度高于100度时,恢复至状态反应后 度 总体积变化情况: 总体积变化情况 烃分子中氢原子数=4,总体积不变 • (1)烃分子中氢原子数 总体积不变 烃分子中氢原子数 总体积不变. • (2)烃分子中氢原子数<4,总体积减少3)烃分子中氢原子数>4,总体积增大。 总体积增大。 )烃分子中氢原子数> 总体积增大 y y • ⊿v C x H y + ( x + )O 2 → xC O 2 + H 2O
烃燃烧规律
• 规律 等物质的量的烃完全燃烧,耗氧量 规律1 等物质的量的烃完全燃烧 的烃完全燃烧, 决定于 x+y/4
y y C x H y + ( x + )O2 → xCO2 + H 2 O 4 2
• 规律 等质量的烃 规律2 等质量的烃CxHy燃烧,y/x越大, 燃烧, 越大 越大, 燃烧 则耗氧量越多。 则耗氧量越多。
4 2
•
1
x+y/4
x
y/2
1-y/4
• 思考:1g 乙烯 和1g 丙烯完全燃烧,耗氧 思考: 丙烯完全燃烧, 量? • 规律 .最简式相同的有机物混合物,只要 规律4.最简式相同的有机物混合物 有机物混合物, 总质量一定,不论以何种质量比混合, 总质量一定,不论以何种质量比混合,完 全燃烧是耗氧量为定值。 全燃烧是耗氧量为定值。
1
• • • •
1 丙烯使溴水褪色 2 2-甲基 丁烯加聚 甲基-2-丁烯加聚 甲基 3 新戊烷和氯气的第 步取代 新戊烷和氯气的第1步取代 4 丙烯和水的加成(写主要产物) 丙烯和水的加成(写主要产物)
• 5写支链上有 个C的庚烷同分异构庚烷有几 写支链上有2个 的庚烷同分异构庚烷有几 写支链上有 并标出各有几种一氯取代物? 种? 并标出各有几种一氯取代物?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
规律:
⑴对于烃CxHy,只要X+Y/4相等; ⑵若是烃CxHy和烃的含氧衍生物采用组 合法,将含氧衍生物写成
CxHy•n(CO2) • m(H2O)。
练习:下列有机物不管它们以任意物质的量的
比混合,只要混合物的总物质的量一定,则完全 燃烧时,消耗氧气的量恒定不变的是( D )
A.C2H4和C2H6O2
C、C3H6
D、C6H6
例2:等质量的CH4,C2H4,C2H6,C3H4,C3H6
完全燃烧,耗氧量最大的是哪个?
CH4
2、最简式相同的有机物,不论以何种比 例混合,只要混合物总质量一定,完全燃 烧后生成的CO2和H2O及耗氧量就一定。
(1)所有的烯烃:如C2H4和C5H10 等 (2)同分异构体,
同状况下测得),该混合物可能是( B )
A.乙烷,乙烯
B.甲烷,乙烯
C.甲烷,丙烯
D.乙烷,丙烯
5.根据烃的燃烧通式确定
例:有两种气态烷烃的混合物,在 标准状况下,其密度为1、16g/L,则 关于混合物的说法正确的是 A、一定有甲烷 B、一定有乙烷 C、可能是甲烷和己烷的混合物 D、可能是乙烷和丙烷的混合物
• 2、取总质量一定的下列各组物质混合后,
无论以何种比例混合,其充分燃烧后得到
的二氧化碳和水的量为恒值的是 D
A.C2H2 C2H6 C.C3H6 C3H8
B. CH4 C3H8 D. C2H4 C4H8
例4:CH4,C2H2,C2H4,C2H6,C3H4,C3H6完全燃 烧,反应后温度为120℃ ,则反应后,体 积不变的是哪种气体?体积减小的是哪种 气体?体积增大的是哪种气体?
例3.由A、B两种烃组成的混合物,当混合物总质
量一定时,无论A、B以何种比例混合,完全燃
烧消耗氧气的质量为一恒量。对A、B两种烃有
下面几种说法:①互为同分异构体;②互为同
系物;③具有相同的最简式;④两种烃中碳的
质量分数相同。正确的结论是( B )
A.①②③④
B.①③④
C.②③④
D.③④
例3:等物质的量的下列有机物完全燃
或增加(y/4 – 1)
●H2O为气态:体积不变 y = 4(CH4 C2H4 C3H4) 体积减小 y < 4(C2H2) 体积增大 y > 4(C2H6 C3H8)
练习
1、在压强一定,温度150 ℃ 条件下,某 有机物完全燃烧,反应前后压强不发生变 化,该有机物可能是( AC ) A、CH4 B、C2H6 C、C2H4 D、C2H2
B. CH4 C3H6 D. C2H2 C3H6
3、烃完全燃烧前后气体体积变化规律:
(利用差量法确定分子中的含H数)
CxHy +(x+y/4)O2 →xCO2 + y/2H2O ΔV
1
x+y/4
x
减少(1 + y/4)(t<100℃)
(t>100℃)
1
x+y/4
x y/2(气) 减少(1 - y/4)
B.C4H6和C3H8
C.C5H10O和C3H6O D.C3H6和C3H8O
练习:1、下列有机物不管它们以任意物质的量
的比混合,只要混合物的总物质的量一定,则完 全燃烧时,消耗氧气的量恒定不变的是( D)
A.C2H4和C2H6O2 C.C5H10O和C3H6O
B.C4H6和C3H8 D.C3H6和C3H8O
体积不变的是CH4,C2H4,C3H4
体积减小的是C2H2
体积增大的是C2H6,C3H6
练习
2、两种气态烃以任意比例混合,在105℃时1 L
该混合烃与9 L氧气混合,充分燃烧后恢复到原
状态,所得气体体积仍是10 L,下列各组混合烃
中不符合此条件的是 B(D )
A. CH4 C2H4 C. C2H4 C3H4
一、烃的燃烧规律
燃烧通式: CxHy + (x+y/4) O2
xCO2 + y/2 H2O
1、等物质的量的烃、等质量的烃完全燃烧时:
CxHy
等物质 的量
耗氧量
X+y/4
生成CO2量 生成H2O量
x
y
等质量 y/x
x/y
y/x
例1、等物质的量的下列烃完全燃烧时,消耗O2
最多的是( D
)
A、CH4
B、C2H6
烧耗氧量相同的有( AC )
A.C2H4和C3H6O3 B.CH4和C2H4O
C.C6H6和C5H10
D.C3H6和C4H8O2
解析: C2H4和C3H6O3 ,其中C3H6O3
可以组合成C2H4•H2O •CO2,而C6H6和 C5H10 ,x+y/4相等。故它们在等物质的 量时完全燃烧耗氧量相同。
4. 烃的混合物计算H4
;
若M混<28(烷、烯的混合物),则一定
有 CH4
。
(2)若平均分子组成中,存在1<n(C)<2,则一定
有 CH4 ;若平均分子组成中,存在2<n(H)<4,
则一定有
。C2H2
例5:某两种气态烃的1 L混合气体,完全燃 烧生成1.4 L CO2和2.0 L水蒸气(体积均在相
