胆矾结晶水的 测定
胆矾中结晶水含量误差分析
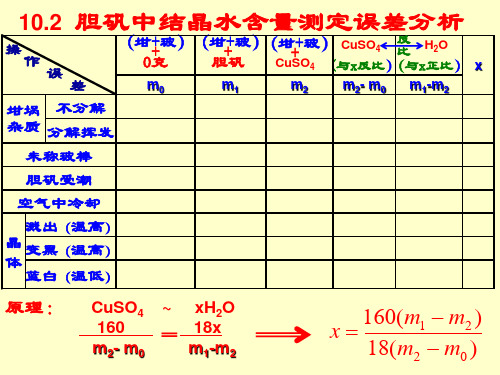
胆矾中结晶水含量测定误差分析 反
m0 m1 m2 m2- m0 m1-m2
(坩+玻)(坩+玻) 坩+玻) CuSO4 ( 比 H2O + + + CuSO4 (与x反比) 与x正比) x 0克 胆矾 反比) 正比) (
差 坩埚 不分解 杂质 分解挥发 未称玻棒 胆矾受潮 空气中冷却 溅出(温高) 晶 变黑(温高) 体 蓝白(温低)
↑ ↑ ↓
↑ ↑ ↓
↑ 无 ↓↓
无 ↓ ↓
无 ↑ ↑
无 ↑
原理: 原理:
CuSO4 160 m 2- m 0
~
xH2O 18x m 1- m 2
160(m − m2 ) 1 x= 18(m2 − m0 )
10.2
操 作 误
胆矾中结晶水含量测定误差分析 反
m0 m1 m2 m2- m0 m1-m2
(坩+玻)(坩+玻) 坩+玻) CuSO4 ( 比 H2O + + + CuSO4 (与x反比) 与x正比) x 0克 胆矾 反比) 正比) (
差 坩埚 不分解 杂质 分解挥发 未称玻棒 胆矾受潮 空气中冷却 溅出(温高) 晶 变黑(温高) 体 蓝白(温低)
↑ ↑
↑ ↑
↑
无
无
无
原理: 原理:
CuSO4 160 m 2- m 0
~
xH2O 18x m 1- m 2
160(m − m2 ) 1 x= 18(m2 − m0 )
10.2
操 作 误
差 坩埚 不分解 杂质 分解挥发 未称玻棒 胆矾受潮 空气中冷却 溅出(温高) 晶 变黑(温高) 体 蓝白(温低)
胆矾结晶水的测定实验报告

胆矾结晶水的测定实验报告胆矾结晶水的测定实验报告胆矾是一种常见的无机化合物,化学式为CuSO4·5H2O,它是一种含水结晶物质。
在本次实验中,我们的目标是测定胆矾中结晶水的含量。
本文将详细介绍实验的步骤、原理以及结果分析。
实验步骤:1. 实验前准备:准备好所需的胆矾样品、称量瓶、烧杯、热水浴、称量器等实验器材。
2. 称重:首先,将称量瓶放在天平上,并记录下称量瓶的质量。
然后,将一定量的胆矾样品精确称量到称量瓶中,并记录下总质量。
3. 加热:将称量瓶中的胆矾样品放入烧杯中,并加入适量的蒸馏水。
随后,将烧杯放入热水浴中,加热至溶液沸腾。
4. 干燥:等待溶液完全沸腾后,继续加热一段时间,使胆矾样品充分干燥。
这一步骤的目的是去除样品中的结晶水。
5. 冷却:将烧杯从热水浴中取出,放置在室温下进行冷却。
等待样品完全冷却后,记录下烧杯的质量。
6. 计算:根据实验数据,计算出胆矾样品中结晶水的质量百分比。
实验原理:胆矾是一种含有结晶水的盐类,其化学式中的“5H2O”表示每个胆矾分子中含有5个结晶水分子。
因此,测定胆矾中结晶水的含量,实际上是测定样品中结晶水分子的质量。
在实验中,我们首先将胆矾样品加热,使其结晶水蒸发。
通过称量瓶和烧杯的质量变化,可以推算出胆矾样品中结晶水的质量。
根据质量变化的比例关系,我们可以计算出结晶水的质量百分比。
结果分析:在本次实验中,我们使用了10克的胆矾样品进行测定。
经过加热和干燥,最终得到的烧杯质量为8克。
根据质量变化的比例关系,我们可以计算出结晶水的质量为2克。
通过计算,我们可以得出结晶水的质量百分比为20%。
这意味着在10克的胆矾样品中,有2克的质量来自于结晶水分子。
结论:通过本次实验,我们成功地测定了胆矾样品中结晶水的含量。
实验结果表明,在10克的胆矾样品中,结晶水的质量百分比为20%。
胆矾结晶水的测定对于化学实验和工业生产中的溶液浓度控制具有重要意义。
通过准确测定结晶水的含量,我们可以更好地控制溶液的浓度,确保实验和生产过程的准确性和稳定性。
《10.2结晶水合物中结晶水含量的测定(第一课时)》教案

《10.2结晶⽔合物中结晶⽔含量的测定(第⼀课时)》教案《10.2结晶⽔合物中结晶⽔含量的测定(第⼀课时)》教案松江四中李婉⼀、设计思路1.教材分析本节课是沪科版《化学》⾼⼆年级第⼀学期第⼗章“学习⼏种定量测定⽅法”第⼆节“结晶⽔合物中结晶⽔含量的测定”第⼀课时内容。
第⼗章共有三个定量实验:“测定1mol⽓体的体积”“结晶⽔合物中结晶⽔含量的测定”“酸碱滴定”,其中“测定1mol⽓体的体积”是拓展型课程内容,因此“结晶⽔合物中结晶⽔含量的测定”就成为本章的第⼀个定量实验,是学⽣学习定量测定⽅法的第⼀课,也是学⽣学习的第⼀种定量测定⽅法——重量法。
因此,本节课设计思路:既然是第⼀课,那么本节课的任务是带领学⽣进⼊定量测定实验的殿堂,在完成本节课后对定量实验的核⼼——“精准性”留下深刻的印象。
教学设计让学⽣在测定物质组成的过程中,始终围绕着“精准性”徐徐展开内容,感受“精准性”在定量测定中的意义和价值,为后⾯学习“中和滴定”和拓展型课程中的“⽓体摩尔体积的测定”、“⼩苏打中碳酸氢钠的含量测定”打好基础。
2.教学基本要求分析《上海市⾼中化学学科教学基本要求》中指出:⾼中阶段共学习5个定量实验,按基础性课程和拓展型课程的顺序,分别是“配制⼀定物质的量浓度的溶液”、“结晶⽔合物中结晶⽔含量的测定”、“中和滴定”、“⽓体摩尔体积的测定?”、“⼩苏打中碳酸氢钠的含量测定?”。
其中对“结晶⽔合物中结晶⽔含量的测定”的学习⽔平要求:知识⽔平C级,技能⽔平C级;即知识达到运⽤层⾯,能将所学内容应⽤到新的情境中,并⽤于解决简单的问题;技能达到设计层⾯,能根据具体情境的需要,选择、组合相关实验操作,解决问题。
虽然,在⾼⼀年级学习“配制⼀定物质的量浓度的溶液”时初次接触了定量实验,但对定量实验的“精准性”核⼼只有⼀个模糊的印象,技能⽔平也只要求达到B级:能规范、熟练地完成某种操作的⽔平。
⽽本节课要在其基础上,技能⽔平有所提⾼,要求达到C级设计⽔平;但是在具体要求⼀栏的描述中,并没有出现设计⽅案四个字,⽽是解释实验原理、复述恒重操作要点的概念和操作要点、描述实验步骤、归纳仪器使⽤要点。
胆矾结晶水的测定

③加热脱结晶水。加热坩埚, 不用盖盖子,用玻璃棒不断 搅拌,加热到硫酸铜晶体变白 (不要变灰,变灰就是氧化铜了)。 用到的仪器有____________________________
④干燥器内冷却:把装有样品的坩埚马上放到 干燥器中干燥,不盖盖子(切忌不能放在空气 中干燥),干燥好了盖上坩埚盖子。为什么不 能放在空气中干燥_____________________
实验目的:结晶水合物中结晶水含量的测定
实验原理:CuSO4·XH2O △ CuSO4+XH2O 实验流程:
①研磨 ②称量:准确称量一干燥洁净的瓷坩锅质量(m0)。 再称:称量瓷坩埚+硫酸铜晶体的质量(m1) ③加热脱结晶水 ④干燥器内冷却 ⑤再称:在干燥器内冷却后,称量瓷坩埚+硫酸铜粉 末的质量(m2) ⑥重复③~⑤至恒重[再加热脱结晶水→干燥器内再冷 却→再称重] ⑦计算
主要步骤: ①研磨:将颗粒较大的固体研磨成颗粒较小的 固体,方便加热时快速失水。用到的仪器有 _____________
②称重[样品(m1-m0)克]:天平调零后先称干燥 的坩埚包括盖子的质量,记录读数m0,然后在坩 埚中加入硫酸铜晶体盖上盖子,再称量,记录读 数m1。用到的仪器有 ___________量瓷坩埚+硫酸 铜粉末的质量(m2)。 ⑥重复③~⑤至恒重。(恒重:托盘天平,前后 两次重量不相差0.1克可视为恒重。)
⑦计算:根据实验数据计算硫酸 铜晶体中结晶水的质量分数和化学 式中的X值。一般情况,定量实验要 多测几次,求平均值,以减少误差。
【练一练】根据实验室中测定硫酸铜晶体结晶水含量 的实验,填写下列空白。 (1)从下列仪器选出所需仪器________________ (用标 号字母填写)。 (A)托盘天平(带砝码) (B)研钵 (C)试管夹 (D)酒 精灯 (E)蒸发皿 (F)玻璃棒 (G)坩埚 (H)干燥器 (I)石棉网 (J)三脚架 除上述仪器外,还需要的仪器是__________________.
胆矾中CuSO4.5H2O含量的测定(

任务分析 任务分析
胆矾的制备
1.由孔雀石(碱式碳酸铜)制备五水硫酸铜 由孔雀石(碱式碳酸铜) 由孔雀石
2.一种新的制备方法,该方法是将废铜放入配 一种新的制备方法, 一种新的制备方法 制的有铁离子的稀硫酸溶液中, 制的有铁离子的稀硫酸溶液中,加热并鼓入空 气进行催化反应制得硫酸铜。 气进行催化反应制得硫酸铜。用过的母液可以 反复使用,没有废水、废气、废渣, 反复使用,没有废水、废气、废渣,不产生环 境污染。利用该方法制备硫酸铜, 境污染。利用该方法制备硫酸铜,生产工艺简 材料消耗少,产率高。 单,材料消耗少,产率高。
2Cu 2 + + 5 I − = 2CuI ↓ + I 3−
子任务2 子任务2: 0.1mol/L Na2S2O3 标准滴定溶液制备方案 思考
1.如何配制和保存Na2S2O3溶液? 1.如何配制和保存 如何配制和保存Na2S2O3溶液 溶液? 水中的CO2、细菌和光照都能使其分解, 答:水中的CO2、细菌和光照都能使其分解,水中的氧也能 将其氧化。故配制Na2S2O3溶液时 先将蒸馏水煮沸, 溶液时, 将其氧化。故配制Na2S2O3溶液时,先将蒸馏水煮沸,以除 去水中的CO2和O2,并杀死细菌;冷却后加入少量Na2CO3 去水中的CO2和O2,并杀死细菌;冷却后加入少量Na2CO3 使溶液呈弱碱性以抑制Na2S2O3的分解和细菌的生长 的分解和细菌的生长。 使溶液呈弱碱性以抑制Na2S2O3的分解和细菌的生长。保存 于棕色瓶中。 于棕色瓶中。 2.为什么要加入NH4SCN?为什么不能过早地加入? 2.为什么要加入 为什么要加入NH4SCN?为什么不能过早地加入? CuI沉淀表面吸附 ,这部分I2不能被滴定 沉淀表面吸附I2 不能被滴定, 答:因CuI沉淀表面吸附I2,这部分I2不能被滴定,会造成结 果偏低。加入NH4SCN溶液 溶液, CuI转化为溶解度更小的 果偏低。加入NH4SCN溶液,使CuI转化为溶解度更小的 CuSCN, CuSCN不吸附 从而使被吸附的那部分 释放出 CuSCN,而CuSCN不吸附I2从而使被吸附的那部分I2释放出 不吸附I2从而使被吸附的那部分I2 提高了测定的准确度。但为了防止I2对SCN-的氧化, 来,提高了测定的准确度。但为了防止I2对SCN-的氧化,而 NH4SCN应在临近终点时加入 NH4SCN应在临近终点时加入。 应在临近终点时加入。
10.2结晶水合物中结晶水含量的测定(一)

数据记录:
名称
/P54 质量(g) 第一次 第二次
瓷坩埚质量(m0) 瓷坩埚+硫酸铜晶体质量(m1) 瓷坩埚+无水硫酸铜质量(m2’) 瓷坩埚+无水硫酸铜质量(m2’’) 瓷坩埚+无水硫酸铜质量(m2) 无水硫酸铜质量(m2-m0) 结晶水质量(m1-m2)
数据处理和结论:
m(CuSO 4) m( H 2O) : 1: x M (CuSO 4) M ( H 2O)
CuSO4 CuO SO3
650 C
依据以上原理,设计实验方案以确定硫酸铜晶体的 组成? 实验步骤:⑴称量硫酸铜晶体 ⑵加热分解 ⑶称量无水硫酸铜 ⑷计算
讲解:定量测定中有的数据可以直接测量,如硫酸铜晶 体的质量;有的数据不能直接测量,需要通过间接方 式测量,如CuSO4· 2O晶体中CuSO4的质量和H2O的 xH 质量。对于间接测量,一般运用化学反应,测量可测 物质或易测物质的有关数据,再通过计算来实现。
五水合硫酸铜俗称胆矾、蓝矾,是一种蓝色晶体。 CuSO4· 2O可用作纺织品媒染剂、农业杀虫剂、水 5H 的杀菌剂,饲料添加剂,并用于镀铜等。 下面我们就以硫酸铜晶体中结晶水含量的测定为 例,研究晶体中结晶水含量的测定的方法、原理。
一、结晶水含量测定的原理:
思考:根据CuSO4· 2O的化学式,如何计算结晶水的百 5H 分含量?
冷却时放在干燥器中进行,是为了避免在冷却过 程中吸收空气中的水份。
为防止固体飞溅,需在研钵中将硫酸铜晶体研碎。
导读:P54/学生实验 思考:测定硫酸铜晶体中结晶水含量的实验步骤? ⒈研磨:在研钵中将硫酸铜晶体研碎; ⒉称量:准确称量一干燥洁净的瓷坩埚质量(m0); ⒊再称量:称量瓷坩埚+约2 g硫酸铜晶体的质量(m1); ⒋加热:放在泥三角上慢慢加热,直至蓝色晶体全部 变成白色粉末,并放在干燥器中冷却; ⒌恒重操作:在干燥器中冷却后,称量瓷坩埚+硫酸 铜粉末的质量(m2);直至两次称量结果相差不超过 0.001 g; ⒍另取硫酸铜晶体,再作一次测定; ⒎数据处理、误差分析、完成实验报告。
高中化学-结晶水含量的测定(教师版)
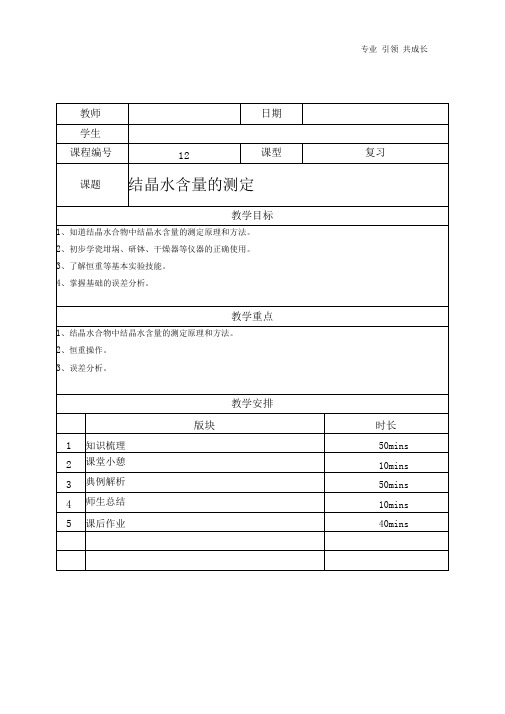
CuSO 4· xH 2O CuSO 4 + xH 2O CuSO 4 650℃CuO + SO 3m(CuSO 4 ):m(H2O) 1:x160m(H 2O) 18m(CuSO)160(m 1 m 2 ) 18m 2式中: m 1=m(CuSO 4· xH 2O),m 2=m(CuSO 4)、实验仪器和装置1.瓷坩埚、坩埚钳、泥三角瓷坩埚用于加热或灼烧固体物质, 加热、 灼烧时应放在泥三角上进 行。
热的瓷坩埚及坩埚盖取放时要用坩埚钳。
2.干燥器干燥器用于保存干燥的物质。
由普通厚玻璃制成,内有带孔瓷板,脱水后的白色 CuSO 4粉末和坩埚要放在干燥器里进行冷却, 因为 CuSO 4 具有很强的吸湿性, 在空气中会重新吸水形成水合物。
结晶水含量的测定知识梳理、实验原理结晶水合物受热能够失去结晶水,硫酸铜晶体(蓝色)在110℃开始失去部分结晶水, 150℃时失去全部结晶水,生成白色的无水硫酸铜。
650℃硫酸铜分解成黑色的氧化铜。
如无水氯 玻璃盖与容器应与磨砂面保持吻合。
容器内下部装有干燥剂【知识拓展】化学干燥剂脱水原理分为两种:℃与水可逆地结合生成水合物,如氯化钙、硫酸镁等;℃干燥剂与水发生不可逆的化学反应,生成新的化合物。
注意:选用干燥剂时,必须注意不与被干燥的物质发生化学反应,不溶于被干燥的物质中。
三、实验1.实验操作(1)研磨:在研钵中用研棒将硫酸铜晶体研碎。
(2)称量:准确称量干燥的瓷坩埚的重量,并记下瓷坩埚的质量m0,并用此坩埚准确称取一定质量已研碎的硫酸铜晶体,并记下坩埚钳和硫酸铜晶体的质量m1。
(3)加热:加热晶体,使其失去全部结晶水(由蓝色完全变为白色)。
(4)称量:在干燥器内冷却后称量,并记下瓷坩埚和无水硫酸铜的质量m2。
(5)再加热、再称量至恒重:把盛有无水硫酸铜的瓷坩埚再加热,再放入干燥器里冷却后再称量,并记下瓷坩埚和无水硫酸铜的质量,到两次称量的质量相差不超过0.001g 为止。
高中化学-结晶水含量的测定(教师版)
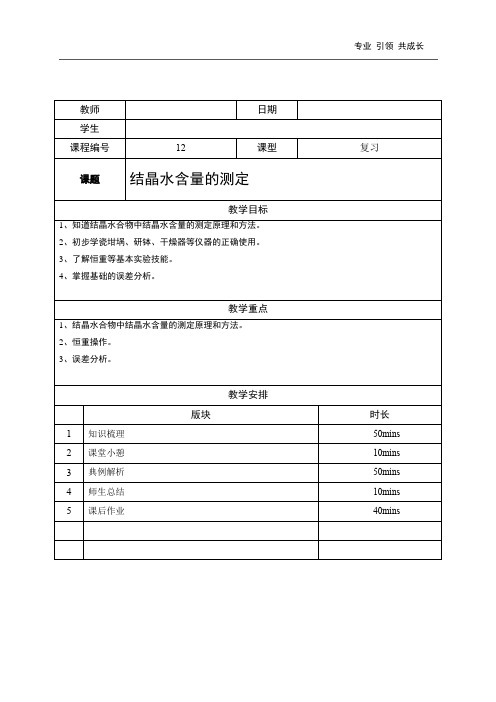
一、实验原理结晶水合物受热能够失去结晶水,硫酸铜晶体(蓝色)在110℃开始失去部分结晶水,150℃时失去全部结晶水,生成白色的无水硫酸铜。
650℃硫酸铜分解成黑色的氧化铜。
CuSO 4·xH 2O −→−∆CuSO 4 + xH 2OCuSO 4 −−→−℃650 CuO + SO 3x O H m CuSO m :118)(160)(24=:24160m(H O)x 18m(CuSO )=22118)(160m m m x -=式中:m 1=m(CuSO 4·xH 2O),m 2=m(CuSO 4)二、实验仪器和装置1.瓷坩埚、坩埚钳、泥三角瓷坩埚用于加热或灼烧固体物质,加热、灼烧时应放在泥三角上进行。
热的瓷坩埚及坩埚盖取放时要用坩埚钳。
2.干燥器干燥器用于保存干燥的物质。
由普通厚玻璃制成,内有带孔瓷板,玻璃盖与容器应与磨砂面保持吻合。
容器内下部装有干燥剂(如无水氯化钙、碱石灰、浓硫酸等)。
脱水后的白色CuSO 4粉末和坩埚要放在干燥器里进行冷却,因为CuSO 4具有很强的吸湿性,在空气中会重新吸水形成水合物。
结晶水含量的测定知识梳理()1220160(m m )18m m --【知识拓展】化学干燥剂脱水原理分为两种:℃与水可逆地结合生成水合物,如氯化钙、硫酸镁等; ℃干燥剂与水发生不可逆的化学反应,生成新的化合物。
注意:选用干燥剂时,必须注意不与被干燥的物质发生化学反应,不溶于被干燥的物质中。
三、实验1.实验操作(1)研磨:在研钵中用研棒将硫酸铜晶体研碎。
(2)称量:准确称量干燥的瓷坩埚的重量,并记下瓷坩埚的质量m 0,并用此坩埚准确称取一定质量已研碎的硫酸铜晶体,并记下坩埚钳和硫酸铜晶体的质量m 1。
(3)加热:加热晶体,使其失去全部结晶水(由蓝色完全变为白色)。
(4)称量:在干燥器内冷却后称量,并记下瓷坩埚和无水硫酸铜的质量m 2。
(5)再加热、再称量至恒重:把盛有无水硫酸铜的瓷坩埚再加热,再放入干燥器里冷却后再称量,并记下瓷坩埚和无水硫酸铜的质量,到两次称量的质量相差不超过0.001g 为止。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CuSO4+XH2O
主要步骤: ①研磨:将颗粒较大的固体研磨成颗粒较小的 固体,方便加热时快速失水。用到的仪器有 _____________
②称重[样品(m1-m0)克]:天平调零后先称干燥 的坩埚包括盖子的质量,记录读数m0,然后在坩 埚中加入硫酸铜晶体盖上盖子,再称量,记录读 数m1。用到的仪器有 _________________________
实验目的:结晶水合物中结晶水含量的测定 实验原理:CuSO4· XH2O 实验流程:
①研磨 ②称量:准确称量一干燥洁净的瓷坩锅质量(m0)。 再称:称量瓷坩埚+硫酸铜晶体的质量(m1) ③加热脱结晶水 ④干燥器内冷却 ⑤再称:在干燥器内冷却后,称量瓷坩埚+硫酸铜粉 末的质量(m2) ⑥重复③~⑤至恒重[再加热脱结晶水→干燥器内再冷 却→再称重] ⑦计算
【练一练】根据实验室中测定硫酸铜晶体结晶水含量 的实验,填写下列空白。 (2)某学生实验后得到 加热后质 加热前质量 以下数据: 量 请写出结晶水含量(X%) W3(容器+ 的计算公式(用W1、W2、 W1(容 W2(容 无水硫酸 W3表示)x%=____。 器) 器+晶体) 铜) (3)该生测定结果是偏高 5.4克 7.9克 6.8克 还是偏低?______。 从下列分析中选出该学生产生实验误差的原因可能是 ___________。(填写字母) A.加热前称量时容器未完全干燥; B.最后两次加热后的质量相差较大(大于0.1克); C.加热后容器未放入干燥器中冷却; D.加热过程中晶体有少量溅失。
⑤再称:在干燥器内冷却后,称量瓷坩埚+硫酸 铜粉末的质量(m2)。 ⑥重复③~⑤至恒重。(恒重:托盘天平,前后 两次重量不相差0.1克可视为恒重。)
⑦计算:根据实验数据计算硫酸 铜晶体中结晶水的质量分数和化学 式中的X值。一般情况,定量实验要 多测几次,求平均值,以减少误差。
【练一练】根据实验室中测定硫酸铜晶体结晶水含量 的实验,填写下列空白。 (1)从下列仪器选出所需仪器________________ (用标 号字母填写)。 (A)托盘天平(带砝码) (B)研钵 (C)试管夹 (D)酒 精灯 (E)蒸发皿 (F)玻璃棒 (G)坩埚 (H)干燥器 (I)石棉网 (J)三脚架 除上述仪器外,还需要的仪器是__________________.
③加热脱结晶水。加热坩埚, 不用盖盖子,用玻璃棒不断 搅拌,加热到硫酸铜晶体变白 (不要变灰,变灰就是氧化铜了)。 用到的仪器有____________________________ ④干燥器内冷却:把装有样品的坩埚马上放到 干燥器中干燥,不盖盖子(切忌不能放在空气 中干燥),干燥好了盖上坩埚盖子。为什么不 能放在空气中干燥_____________________
