亲核取代反应及其影响因素
亲核取代反应的历程及影响因素
2. 底物 + 亲核试剂
中性分子 中性分子
RX +
NH3 H2O HOR'
R+NH3X- NH3
RO+H2
RO+R' H
- H+ - H+
RNH2 + NH+4XROH ROR'
3. 底物为正离子:
RN+(CH3)3 + OH+ H2S
ROH + N(CH3)3 R+SH + N(CH3)3
Organic Chem
νC-F νC-Cl νC-Br νC-I
1000-1350 cm -1 (S) 700-750 cm-1 (m) 485-610 cm-1 (m) 485-610 cm-1 (m)
1.24-1.55
R CH2
CH2
CH2
X
1.03-1.08
2.16-4.4
例: H3C CH2 CH2 Cl
54
3
2
1
2-甲基-4-溴戊烷
H3C CH CH CH2 CH3
12
34
5
3-甲基-2-氯戊烷
(取代基离两端等距离,
优先考虑列出的基团 )
Organic Chem
H3C
4
1
CH2Cl
CH2 CH CH2 CH3
3
2
2-乙基-1-氯丁烷
Br
H3C CH CH CH CH3
54
3
2
1
4-溴-2-戊烯
优先使双键的位次最小
也可按所含卤原子数目分为:
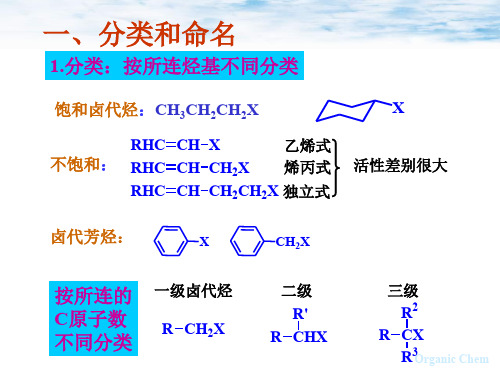
一卤代物: R-X 二卤代物: CH2X2 多卤代物: CHX3,CX4 2.命名: 系统命名法
影响亲核取代反应的因素

影响亲核取代反应的因素影响亲核取代反应的因素摘要亲核取代反应是有机化学中⼀类重要的反应,饱和碳原⼦上的亲核取代反应可按S N1和S N2两种不同历程进⾏。
亲核取代反应的两种历程,在反应中同时存在,相互竞争。
对同⼀反应物来说,在不同的反应条件下反应速率是不同的;在相同的条件下,不同的反应物的活性也不同。
本⽂讨论了影响亲核取代反应的因素,并总结了某些规律。
关键词亲核取代反应速率影响因素卤代烃的亲核取代反应是⼀类重要的反应。
由于这类反应可⽤于各种官能团的转变以及碳碳键的形成,因此在有机合成中具有⼴泛⽤途。
本⽂将以卤代烃的亲核取代反应为例,讨论影响亲核取代反应的因素,即亲核取代反应的反应活性。
⼤量研究表明,亲核取代反应的活性与反应物的结构(包括烃基和离去基团的结构)、亲核试剂的亲核性和溶剂的性质等因素都有密切的联系。
1反应物的结构1.1烃基的结构烃基的影响体现在两个⽅⾯,⼀个是电⼦效应,另⼀个是空间(⽴体)效应。
⼀般来说,烃基的电⼦效应对S N1反应的影响更⼤,烃基的空间效应对S N2反应的影响更显著。
1.1.1在S N2反应中,烃基的空间效应影响占主导地位,α—碳或β—碳上⽀链增加,阻碍了亲核试剂从离去基团的背⾯进攻,且会造成过渡态拥挤程度增加,降低了过渡态的稳定性,使反应速率明显下降。
例如,不同的烷基发⽣S N2反应的平均相对速度如下:R-CH3-CH3CH2-(CH3)2CH-相对速度30 1 2.5?10-2卤代烃按S N2机理进⾏的活性次序是:烯丙型、苄基型、甲基卤代烷>伯>仲>叔>⼄烯型、芳卤、桥头卤代烷在烯丙卤、苄卤的S N2反应中,当亲核试剂进攻α-碳原⼦时,其反应过渡态应该有p轨道的重叠,旁边的碳碳双键能帮助它分散电荷,起稳定作⽤。
在⼄烯型、芳卤的S N2反应中,因其分⼦中存在着p-π共轭,使碳卤键键长缩短,键能增加,卤原⼦不易离去。
桥头卤代烷因桥环的⽴体障碍,亲核试剂不能从背⾯进攻α-碳原⼦,故不易发⽣S N2反应。
化学反应中的亲核取代反应

化学反应中的亲核取代反应化学反应是物质之间发生变化的过程,其中亲核取代反应是一种重要的反应类型。
亲核取代反应是指一个亲核试剂与一个电子不足的反应物发生反应,亲核试剂中的亲核基团取代掉反应物中的一个离去基团。
这种反应在有机合成中具有广泛的应用,可以用于合成各种有机化合物。
亲核取代反应可以分为两类:亲核试剂为中性物质的亲核取代反应和亲核试剂为离子的亲核取代反应。
中性物质的亲核取代反应通常发生在有机化合物中,而离子的亲核取代反应则发生在无机化合物或离子中。
中性物质的亲核取代反应中,亲核试剂通常是一种带有孤对电子的原子或分子,如氨、水、醇等。
这些亲核试剂通过与反应物中的电子不足的原子或分子发生反应,形成新的化学键。
例如,氨与醛反应可以生成胺,水与酰氯反应可以生成醛或酮。
离子的亲核取代反应中,亲核试剂通常是带有正电荷的离子,如氢离子、钠离子等。
这些亲核试剂通过与反应物中的带有负电荷的离子或原子发生反应,形成新的化学键。
例如,氢离子与氢氧根离子反应可以生成水,钠离子与氯离子反应可以生成氯化钠。
亲核取代反应的速率通常受到多种因素的影响,如反应物浓度、温度、溶剂等。
在一些情况下,亲核取代反应可能会出现竞争性反应,即不同的亲核试剂与反应物中的不同位置发生取代反应。
这时,反应的选择性就成为一个重要的问题。
在有机合成中,亲核取代反应可以用于合成各种有机化合物,包括药物、农药、染料等。
通过选择不同的反应条件和亲核试剂,可以实现对目标化合物的选择性合成。
亲核取代反应还可以用于构建碳-碳键和碳-杂原子键,从而构建复杂的有机分子。
总之,亲核取代反应是化学反应中的一种重要反应类型,广泛应用于有机合成中。
通过选择不同的亲核试剂和反应条件,可以实现对目标化合物的选择性合成。
亲核取代反应的研究对于发展新的有机合成方法和合成新的有机化合物具有重要意义。
有机化学基础知识点亲核取代反应的机理

有机化学基础知识点亲核取代反应的机理在有机化学领域中,亲核取代反应是一类重要的反应类型,它涉及一个亲核试剂与有机物中电子不足的位点之间的亲核攻击和断裂反应。
亲核取代反应机理的理解对于合成新颖的有机化合物以及研究有机反应有着至关重要的意义。
本文将介绍亲核取代反应的一些基础知识点,并详细解析其机理。
一、亲核试剂的选择亲核取代反应中,亲核试剂的选择通常是根据底物的特性来确定的。
常见的亲核试剂包括氢离子(H^-)、氧化物离子(O^-)、卤素离子(Cl^-、Br^-、I^-)等。
不同的亲核试剂对应着不同的反应类型和机理。
二、亲核取代反应的机理亲核取代反应的机理大致分为两步:亲核攻击和断裂反应。
1. 亲核攻击在亲核取代反应中,亲核试剂通过自身的强电子亲合性,攻击有机底物上的电子不足的位点(如C=O双键、C-X键等)。
亲核试剂的亲核攻击会导致分子内电子重新分布,形成新的共价键。
2. 断裂反应亲核攻击后,原有的化学键会发生断裂,底物分子会发生结构改变。
通常情况下,在亲核取代反应中,断裂反应是一个带有正电荷的离去基团的离去,形成新的化学键。
三、亲核取代反应的分类和示例亲核取代反应可以根据亲核试剂的种类和底物中亲电子受体的特点进行分类。
下面将以常见的亲核试剂和底物为例,介绍几种典型的亲核取代反应:1. 氢离子(H^-)的亲核取代反应氢离子亲核取代反应是有机化学中最基础的反应类型之一,常用来合成醇、胺等化合物。
例如,酯的水解反应就是氢离子亲核取代反应的一个典型例子:[示例反应方程式]2. 水氧离子(OH^-)的亲核取代反应水氧离子亲核取代反应广泛应用于合成醇、酚等化合物。
这类反应以醇的合成反应为代表,其机理与氢离子亲核取代反应类似。
3. 卤素离子(Cl^-, Br^-, I^-)的亲核取代反应卤素离子亲核取代反应是常见的有机反应类型,用于制备卤代烃等化合物。
其中,氯离子亲核取代反应最为常见。
以氯离子的亲核取代反应为例,其机理如下:[示例反应方程式]四、亲核取代反应的影响因素亲核取代反应的速度和产率受多种因素的影响,包括溶剂、温度、底物结构等。
亲核取代反应及其影响因素

亲核取代反应及其影响因素航03班 林三春 2010011556摘要:本文分为四部分。
第一部分论述了亲核取代反应的组成部分:亲核试剂、离去基团、反应底物,特地列出了常见的亲核试剂、常见的离去基团。
第二部分论述了亲核取代反应机理,主要论述了四种:SN1、SN2、离子对机理和邻近基团参与机理,其中还包括各种机理的实验现象验证,以及对反应产物的影响,如对构型的影响。
第三部分论述了亲核反应的影响因素,主要有烃基、离去基团、溶剂和亲核试剂四种,详细地说明了这四种因素如何影响反应。
给出了判断离去基团的好坏,以及比较亲核试剂的亲核性的方法。
最后一部分论述了亲和取代反应与消除反应的竞争关系,其中包括SN1与E1竞争,SN2与E2竞争。
主要以卤代烃为例阐述的。
在论述的同时,还附有适当的图示,以及实验数据,通过比较等手段,使得论述更加有说服力。
全文通过这四个部分,详细、全面地介绍了亲核取代反应。
正文:亲核取代反应,简称SN 亲核取代反应,通常发生在带有正电或部分正电荷的碳上,碳原子被带有负电或部分负电的亲核试剂(Nu:-)进攻而取代。
一、亲核取代反应的重要组成成分:亲核取代反应中涉及到的三个重要组成成分为:亲核试剂、离去基团、反应底物。
称为反应底物。
进攻反应底物的试剂CH30Na (或CH3O —)是带着电子对与碳原子结合成键的,它本身具有亲核性,称为亲核试剂,一般用Nu 表示。
这类反应之所以称为亲核取代也正是因为它是由亲核试剂进攻反应底物而引起的取代反应。
反应底物上的溴原子带着电子对从碳原子上离去,所以Br-;称为离去基团,一般用L 表示。
该取代反应是在与溴相连的那个碳原子上进行的,常称该碳原子为中心原子,或反应中心。
.一般的亲核取代反应可以用如下的通式表示: 。
其中R —L 为反应底物,L —为离去基团,Nu —为亲核试剂,弯箭头表示电子转移的方向。
1、亲核试剂:亲核性是指:带负电荷或孤对电子的试剂即亲核试剂对亲电子原子的进攻的能力。
影响亲核取代反应的因素

影响亲核取代反应的因素2010-04-27 08:55饱和碳原子上的亲核取代反应可按SN1和SN2两种不同历程进行。
亲核取代反应的两种历程,在反应中同时存在,相互竞争。
但对一种反应物来说, 在一定条件下, 与亲核试剂作用时, 我们能否知道, 反应究竟按什么历程进行?如果对不同的反应物, 我们能否预计哪一个快, 哪一个慢?对于这样类似的一系列问题, 通过许多科学家的研究, 现在已经找到明确而肯定的答案。
研究表明, 反应历程和反应活性与反应物中的烃基结构, 离去基团性质, 亲核试剂性质以及溶剂性质等因素都有关系, 下面分别讨论。
5.5.1烃基结构的影响影响反应历程的因素很多,卤代烃本身结构是主要因素之一。
在卤代烃分子中,反应中心是a-C原子。
a-C原子上电子密度的高低,直接影响反应历程。
如果a-C原子上电子密度低,则有利于Nu-进攻,有利于反应按双分子历程进行。
反之,如果a-C原子上电子密度高,则有利于卤素夺取电子而以X-的形式离解,所以有利于按单分子历程进行反应.从反应中间体来看如果能形成稳定的正离子,则有利于反应按SN1历程进行。
反之,则有利于SN2历程。
烃基结构对亲核取代反应的影响, 可以通过分析烃基的电子效应和空间效应来确定。
先看看SN1和SN2两个决速步骤中过渡态的结构(见表5.8)。
表5.8 SN1和SN2过渡态结构反应历程SN2SN1过渡态结构电荷分散集中体积比反应物拥挤比反应物宽松在卤代烃的亲核取代反应中, 烃基的立体效应和电子效应对SN1和SN2影响程度不同。
对SN2历程,烃基的立体效应是主要的,而对SN1历程,烃基的电子效应是主要的。
5.5.1.1 烃基的立体效应由于SN2历程中形成的过渡态比较拥挤, 所以SN2历程对烃基的立体效应比较敏感。
(1)当中心碳原子上的支链增多时, 不利于SN2反应, 有利于SN1反应。
考虑立体因素时,伯卤代烃有利于SN2反应,叔卤代烃有利于SN1反应。
亲核取代的反应机理
亲核取代的反应机理亲核取代反应是有机化学中常见的一种反应类型。
这种反应是指:一个亲核试剂(通常是一个碱或是一个有机分子中的一个带负电荷的基团)进攻一个化学键上的一个有机基团,从而替换掉原来的原子或是基团。
这个反应在有机化学合成中非常重要,因为它可以用来构建新分子,并且可以控制其立体化学性质和化学反应性质。
在这篇文章中,我们将讨论亲核取代反应的机理,了解在这个反应中哪些因素会影响反应速率和选择性。
亲核取代反应的机理分为三个步骤:1)亲核进攻;2)失去离去基团;3)质子转移。
1) 亲核进攻:在亲核试剂进攻有机基团前,亲核试剂必须先与有机分子中的一个另一个原子形成一个键,这个反应称为亲核加成反应。
这样可以形成一个更好的亲核试剂,以便亲核试剂可以更容易地进攻到有机基团上。
在这个阶段,亲核试剂进攻有机基团时,该反应的速率取决于亲核试剂的浓度,相对于其反应物在反应体系中的相对位置以及反应体系的温度和压力。
2) 失去离去基团:亲核试剂进攻有机基团的结构不稳定,因为它们的电子云被扰乱了。
为了恢复这个结构稳定性,反应体系中的另外一个原子或基团必须被去除。
这个反应称为离去反应。
离去反应的速率取决于离去基团的稳定性和离去基团与碳原子之间的键的强度。
3) 质子转移:在这个阶段中,质子转移是由离去基团周围的一个质子转移到亲核试剂上。
这个反应的速率取决于质子可转移的可能性和质子从离去基团到亲核试剂转移的过度态的稳定性。
通过三个步骤的亲核取代反应可以产生一个新的有机分子,并且立体化学性质和化学反应性质可以控制。
在这个反应中,选择性是一个重要的因素,并且可以使用物化性质诸如温度、溶剂常数、极性等参数来控制反应的选择性。
有机化学中的亲核取代反应
有机化学中的亲核取代反应有机化学是研究碳化合物及其衍生物的科学,涵盖了广泛的知识和反应类型。
在有机化学中,亲核取代反应是一类重要的反应类型,它在有机合成中起着至关重要的作用。
本文将介绍有机化学中的亲核取代反应,包括基本概念、机理和实际应用。
亲核取代反应是一种核酸(亲核试剂)与一个带正电荷或部分正电荷的碳原子相互作用的反应。
亲核试剂指的是具有孤对电子或由共轭体系提供可用孤对电子的分子或离子。
在反应中,亲核试剂攻击带正电荷的碳原子,将其替换为亲核试剂中的原子或基团。
亲核取代反应可以分为以下几种类型:1. SN1反应(亲核取代一型):SN1反应是一种两步反应,首先发生离解步骤,生成一个离子中间体,然后亲核试剂与离子中间体发生反应。
SN1反应的速率仅取决于离解步骤,与亲核试剂无关。
2. SN2反应(亲核取代二型):SN2反应是一种一步反应,亲核试剂直接攻击带正电荷的碳原子,并将其替换。
SN2反应的速率与亲核试剂的浓度成正比。
3. SNi反应(亲核取代离解负离子反应):SNi反应类似于SN1反应,但离解步骤形成负离子中间体。
4. 过渡态化合物的亲核取代反应:过渡态化合物的亲核取代反应是一类特殊的反应,其中反应物形成一个比中间体更稳定的产物。
这种反应常见于环化合物的开环反应。
亲核取代反应在有机合成中有广泛的应用。
例如,通过SN2反应,可以合成含有新碳-亲核试剂键的化合物。
此外,亲核取代反应还可以用于合成酯、醚、胺等有机物。
通过选择适当的亲核试剂和反应条件,可以实现高效的选择性反应。
需要注意的是,亲核取代反应的机理和速率常受到多种因素的影响,包括亲核试剂的性质、反应物的结构和环境条件等。
因此,合理选择反应条件对于实现期望的反应结果非常重要。
总结起来,有机化学中的亲核取代反应是一类重要的反应类型,它在有机合成中具有广泛的应用。
通过理解亲核取代反应的基本概念和机理,我们可以更好地应用这些反应,合成有机化合物,并推动有机化学领域的进一步发展。
第三节 亲核取代反应历程
离子的碱性: X 离子的碱性:I - < Br- < Cl离子离去倾向: X 离子离去倾向:I - >Br- > Cl卤代烷反应活性顺序是:
R I > R Br > R Cl
(三)亲核试剂的影响
SN 2反应 反应 SN 1反应 反应
亲核试剂的亲核能力 , 亲核试剂的亲核能力↑, 亲核能力 浓度↑,反应υ↑。 浓度 ,反应 。
1.双分子亲核取代反应(S 2)历程 历程: 1.双分子亲核取代反应(SN2)历程 双分子亲核取代反应
HO + CH3 Br
CH3OH + Br
动力学特征: 动力学特征 υ = k [ CH3Br ] [ OH- ],二级反应 ,
OH-
CH3Br
空间位阻最小 静电斥力最小
H
H
Br
H HO C H H
(四)溶剂极性
1) SN 2反应 反应
Nu R L
-
2) SN 1反应 反应
C L]
δ Nu R L
[Nu
δ
R L
[R
δ
L]
δ 慢
R+ LNu
溶剂的极性变化所起的作用很小
O H Nu R O H R
H O
R
溶剂极性的提高, 溶剂极性的提高,利于碳正离子 及卤负离稳定 使反应速率加快。 稳定, 及卤负离稳定,使反应速率加快。
溶剂极性 的影响
的极性对反应不利。 的极性对反应不利。
小结:影响亲核取代机理的因素 小结:
R X C H 3X , 1o 强亲核性, 高浓度 非质子性, 小极性
:
对SN2有利 的因素
Nu 溶剂
: :
有机化学基础知识点亲核取代反应的机理和规律
有机化学基础知识点亲核取代反应的机理和规律有机化学是一门研究碳元素的化合物及其反应的学科。
其中,亲核取代反应是有机化学中一类重要的反应类型,它在有机合成、药物开发以及材料科学等领域起着关键性作用。
本文将重点介绍亲核取代反应的机理和规律,帮助读者更好地理解和应用这一有机化学基础知识点。
一、亲核取代反应的基本概念和机理亲核取代反应是一种典型的酸碱反应,即亲核试剂(通常是含有亲核试剂的阴离子)攻击了一个电子亏损的反应物,将其取代出来,形成新的化学键。
这种反应过程中,亲核试剂的亲电性中心与电子亏损的反应物的亲电性中心发生作用,从而实现取代反应。
亲核取代反应的机理可归纳为以下几个步骤:1. 亲核试剂的进攻:亲核试剂中具有亲电性的部分与电子亏损的反应物发生反应,亲核试剂的亲电性中心接近反应物的亲电性中心。
2. 形成临时五元环中间体:亲核试剂与反应物亲电性中心的结合形成一个临时的五元环中间体。
具体形成过程中,亲核试剂中的亲电性碳离子(通常是负离子)与反应物中的亲电性碳离子形成新的化学键。
3. 断裂反应物化学键:在形成临时的五元环中间体过程中,反应物中的一个化学键断裂,释放出一个亲核试剂与离去基团。
4. 形成新的化学键:离去基团离开后,亲核试剂中的亲电性碳离子与反应物中的亲电性碳离子形成新的化学键,得到产物。
二、亲核取代反应的规律和影响因素亲核取代反应的速率和产物选择性受到多种因素的影响。
下面介绍一些常见的规律和影响因素:1. 亲核试剂的选择:不同的亲核试剂具有不同的亲电性中心和亲核性,因此在不同的反应中选择适合的亲核试剂是十分重要的。
2. 电子密度和空间位阻效应:反应物中存在不同的亲电性中心时,选择攻击电子密度较高的中心更有利于反应进行。
此外,反应物或产物中的取代基团的位阻效应也会影响反应速率和选择性。
3. 溶剂选择:不同的溶剂对反应速率和产物选择性有一定影响。
一些溶剂可以稳定或降低亲核试剂的亲电性,从而影响反应速率和选择性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
亲核取代反应及其影响因素摘要:饱和碳原子上的亲核取代反应主要有两种:单分子亲核取代反应(S N1)与双分子亲核取代反应(S N2)。
大多数反应介于这两种极端情况之间。
人们提出离子对机理与邻近基团参与的理论来解释反应情况与构型变化的问题。
亲核取代反应的反应速度,与烃基的数量、离去集团的大小、亲核试剂的活性以及溶剂的极性等有关。
一般来说,烃基数量少,离去基团大,亲核试剂亲核性强,溶剂的极性弱,对S N2反应有利;烃基数量多,离去基团大,溶剂的极性强,对S N1反应有利。
另外,亲核取代反应和对应的消除反应(单分子消除反应E1、双分子消除反应E2与S N1、S N2)互为竞争性反应。
强碱和较高的温度有利于消除,弱碱和强亲核试剂有利于取代;有利于碳正离子生成的条件,有利于按单分子机理进行;不利于底物异裂的条件,有利于双分子反应。
正文:一、烷基结构的影响1.烷基的结构对S N2 反应的影响反应中,如果中心碳原子上连接的取代烷基(支链)越多,它们对亲在卤代烷的SN2核试剂从碳卤键背后进攻中心碳原子的空间位阻就越大,使得发生有效碰撞的概率大为下降;而在过渡态时众多的支链与中心碳原子要保持在同一个平面内,其张力是很大的,这就使形反应的活性下降,反应速成过渡态需要有非常高的活化能,这些都将导致卤代烷进行SN2率减小。
例如,I-与下面各溴代烷的丙酮溶液中于25℃发生S N2 反应时的相对反应速率为:反应的速率也有明显的影响,即卤如果在卤代烷的β- 碳原子上连有支链烷基时,对SN2代烷中心碳( α- 碳)原子上连接的烷基体积越大,其空间位阻越大,不利于亲核试剂的攻击。
反应时,在其它条件相同时,不同结构卤代烷的反应活性综上所述,卤代烷进行SN2次序为:2.烷基的结构对S N1 反应的影响在S N1 反应中,由于决定反应速率的步骤是碳正离子的生成。
因此,烷基子离子越稳,越易形成,生成时的活化能越低,反应速率也越快,由于烷基正离子稳定性的顺序是:(CH3)3C+>(CH3)2CH+>CH3CH2+>CH3+所以,在S反应中,卤代烷的活性顺序为:R3CX > R2CHX > RCH2X > CH3X N1(3°>2°>1°>CH3X),例如:卤代烷与AgNO溶液的反应被认为是S N1 机理。
3/EtOH二、离去基团(卤原子)的影响由于S和S N2 反应的慢步骤都包括C-X 键的断裂,因此离去基团X-的性质对N1S N1 和S N2 产生相似的影响,但由于在S N2 反应中,参与过渡态形成的还有亲核试剂,故和卤原子离去的难易除与本身性质有关外,还与亲核试剂的性质有关。
卤原子的性质对SN1S N2 反应影响的程度不同,其中对S N1 反应的影响更为突出。
总之,离去基的离去倾向越大,碳卤键越易于变形断裂,亲核取代反应速度越快。
从C-X 键解离能和可极化度的大小,可知卤代烷的活性次序为:RI>RBr>RCl>RF ( S N1 和S N2 一致)其中,I-最好的离去基团,F-的离去能力最差。
三、亲核试剂的影响反应的慢步骤(第一步)只与卤代烷的浓度有关,故亲核试剂对S N1 反应的由于SN1反应的慢步骤则与卤代烷和亲核试剂均有关系,试剂的亲核能力越强或影响不大。
而SN2机理进行的亲核试剂的浓度越大,则它与卤代烷中心碳原子的成键能力越大,反应按SN2趋势越大,反应活性越高。
试剂的亲核性大小主要是由两个因素决定的。
一个是试剂的碱性(给电子性),一个试剂的极化度(变形性)。
这两个因素对试剂的亲核性的影响通常是一致的;但也有不一致的情况,这时往往是后者起主导作用,但也与溶剂性质有关。
一般有如下规律。
1.同一周期的原子作为亲核中心时,试剂的亲核性与碱性有相同的强弱次序:2.同一族的原子作为亲核中心时,变形性大者(原子半径大、电负性小者),呈现出较强的亲核性;这与碱强弱次序相反:3.卤素负离子在质子型溶剂中表现出的上面所述的亲核性次序是与卤负离子的溶剂化作用有关的;卤负离子的体积越小,负电荷就越集中,它与质子型溶剂化作用程度越大,导反应,(如使用二甲致卤负离子的亲核性大为下降。
如果在非质子型极性溶剂中进行SN2基亚砜或二甲基甲酰胺)由于X-与溶剂分子不发生溶剂化作用,X-的负电荷是完全裸露,这时它们的亲核性与碱性的强弱次序是相同的:4.亲核试剂的体积大小对它的亲核性也有明显的影响;体积大者,在反应中空间位阻增大,亲核性下降。
四、溶剂板性的影响反应的速度控制步骤是它电离生成正碳离子一步;在这个步骤中,从反应卤代烷SN1物到正碳离子是一个正电荷不断形成的过程;而在过渡状态,卤代烷已发生了C-X 键的部分异裂,并在中心碳和卤原子上出现了部分的正负电荷,形成了高度极化的状态。
极性溶剂分子对高度极化的过渡状态的溶剂化作用,可使卤代烷的过渡状态因电荷分离而引起的热力学能和升高有所缓解,并有助于碳卤键的进一步彻底解离。
对于生成的正碳离子及卤负离子,极性溶剂分子也将对它们分别起到溶剂化作用,使它们所带的电荷得到进一步的分散而更趋于稳定,所以溶剂的性质对S反应的控制步骤的影响是相当重要的。
溶剂的极性大,溶N1反应)的剂解的速度也越快。
例如,叔氯丁烷在25℃时与不同溶剂中进行溶剂解(即SN1相对速度为:CH3OH HCOOH H2O溶剂:CH3COOH介电常数: 6 33 58 78相对速度: 1 4 5000 150000RX→ [ Rδ+……Xδ-] → R++X-而在S N2 反应中,增加溶剂的极性对S N2 反应不利,反应中体系的极性通常没有变化,只是发生电荷的分散,增加溶剂的极性反而使因为SN2极性大的亲核试剂溶剂化。
Nu++R x → [ Nuδ+……R……Xδ-] → NuR+X-机理进行。
因此,在极性小的非质子溶剂(如丙酮)中有利用反应按SN2一般情况下,在极性不太小的溶剂(如无水的乙醇溶液)中,叔卤代烷主要按S机N1机理进行,仲卤代烷同理进行,而在极性较小的溶剂(如乙醇)中,伯卤代烷主要按SN2时按照两种机理进行,一般是以S为主,改变溶剂的极性常可改变反应机理。
如在极性N2机理进行,而在极性较小的非质子溶剂中,很大的溶剂(如甲酸)中,伯卤代烷可以按SN1叔卤代烷则可按照S机理进行。
N2综上所述,卤代烷在进行SN反应时所遵循的有关规律和特点是:反应时,活性次序为:3°>2°>1°>CH3X,而且反应产物有外消旋化并卤代烷的进行SN1可出现重排产物。
卤代烷进行S反应时,活性次序为:CH3X>1°>2°>3°,而且反应产物N2发生立体构型的转化,但没有重排产物。
S N2反应离去基的离去活性越大,卤代烷的SN反应活性越高;试剂的亲核性越强,对越有利;而溶剂的极性越大,对S反应越有利;试剂浓度的增大对S N2 反应有利;提高N1反应的温度可加快SN反应的速度,但对仲卤代烷显得尤为主要。
亲核取代与消除反应的竞争卤烃的亲核取代反应与消除反应是一对竞争反应。
有利于S的反应条件,同样对E2N2反应,消除反应也有利。
因而在取代反应的同时常伴随消除反应。
一级卤代烃主要发生SN2产物较少,当β位上连有苄基或烯丙基时,则会增加E2反应速率,提高消除反应产率。
例如,溴乙烷在55℃时,在乙醇溶剂中与乙醇钠作用,取代产物占99%,而烯烃只占1%;当β位上的一个氢被苄基取代后的β-苯基溴乙烷,在同样条件下的反应,取代产物只占4.4%,消除产物却占95.6%。
反应速率减慢,有利于β-碳上连有支链的一级卤代烃和二级卤代烃,空间位阻导致SN2亲核试剂对β-氢的进攻,导致消除反应增多。
从电性效应考虑,试剂的亲核性强,易于发生S反应;试剂的碱性强,浓度大,有利于E2反应。
从立体效应考虑,试剂的本积大,N2则不利于亲核取代反应,而有利于E2反应。
由于三级卤代烃主要发生单分子反应,难发生S N2反应,如遇有强碱,则是以E2消除反应为主。
与E1反应混合物之比主要取决于空间效应。
卤烃中取代基越大,越有利于消除反SN1应。
例如,下面三个氯代烷的溶剂解反应,随着取代基的空间效应增大,消除产物的比例越来越大:总这,亲核取代反应与消除反应的取向与卤烃的结构有直接关系。
直链一级卤烃易进行S N2反应,不易发生消除反应,只有强碱条件下才可发生消除反应。
二级卤烃及β碳上有支链的一级卤烃进行S的反应速度较慢,在低极性溶剂中,强亲核试剂条件下有利于S N2反N2反应,在应,在低极性溶剂,强碱性试剂条件下,有利于E2反应。
三级卤烃难以进行SN2和E1混合产物。
生成物的强碱条件下有利于E2反应。
三级卤烃在无强碱存在时,得到SN1相对比率依条件决定,逐渐增大碱的浓度,将增加消除反应比率。
反应趋势如下所示。
参考文献1.汪焱钢.亲和加成反应.湖北.高等教育出版社.1994。
