2020届高三化学复习备考:10年高考工艺流程真题汇编
全国新课标三卷高考化学工艺流程试题分类汇编

全国新课标三卷高考化学工艺流程试题汇编(新课标Ⅲ)2020新课标Ⅲ.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni 、Al 、Fe 及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO 4·7H 2O):溶液中金属离子开始沉淀和完全沉淀的pH 如下表所示:回答下列问题:(1)“碱浸”中NaOH 的两个作用分别是______________。
为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。
写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代H 2O 2的物质是______________。
若工艺流程改为先“调pH”后“转化”,即“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH)2的K sp =______________(列出计算式)。
如果“转化”后的溶液中Ni 2+浓度为1.0 mol·L −1,则“调pH”应控制的pH 范围是______________。
(5)硫酸镍在强碱溶液中用NaClO 氧化,可沉淀出能用作镍镉电池正极材料的NiOOH 。
写出该反应的离子方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
2020新课标Ⅲ.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。
回答下列问题:相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
2020年高考化学专题复习 化学工艺流程题

2020年高考复习化学工艺流程题题型特点本题型以现代工业生产为基础,与化工生产成本、产品提纯、环境保护等相融合,考查物质的制备、检验、分离、提纯等基本实验原理在化工生产中的实际应用,要求考生依据流程图分析原理、紧扣信息、抓住关键、准确答题。
这类试题具有较强的实用性和综合性,能较好地考查学生信息获取能力、分析问题能力、语言表达能力和计算能力等。
突破点一化工工艺流程题的分析【解题策略】1.粗读试题(1)读题头,得目的。
题头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括副产品),以及提供需要用到的信息。
(2)读题干、析过程。
题干部分主要用框图形式将原料到产品的主要生产工艺流程表示出来。
题干信息有三个层次:读得懂的;读得不太懂但根据上下文可以勉强懂的;完全读不懂的。
关键是突破第二层次,对于读得不太懂但根据上下文可以勉强懂的部分需要学生运用已有的基础知识,根据学习过的化学反应原理,联系实际工业生产及题目信息等进行知识的整合,最终得到结论。
(3)读题尾、看措施:题尾主要是根据生产过程中涉及的化学知识设计成系列问题,构成一道完整的化学试题。
阅读题尾时要将设问中的提示性信息,用笔画出来,以便在后面精读试题时随时提醒自己与之联系。
2.精读试题在粗读试题的基础上,结合流程图以外的文字描述、表格信息、后续设问中的提示性信息,在流程图上随手画出相关信息,以便在解题时随时进行联系和调用;同时思考几个问题:从原料到产品依次进行了什么反应,利用了什么原理(氧化还原?溶解度?溶液中的平衡?),每一步操作进行到什么程度最佳,每一步除目标物质外还产生了什么杂质或副产物,杂质或副产物用什么方法除去等等,体会出题者设问的角度、意图。
只要掌握了这一题型的一般特点和解题策略,无论流程如何陌生复杂,在高考中即使遇到情境陌生的流程图题,也能够驾驭自如,迎刃而解。
1[2019·全国卷Ⅲ]高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如图G2-1所示。
专题07 无机综合及工业流程-2020年高考化学十年真题精解(全国Ⅰ卷)(解析版)
精解07无机综合及工业流程2020考纲考点2020考纲要求(4)物质结构和元素周期律①了解元素、核素和同位素的含义。
②了解原子的构成。
了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。
③了解原子核外电子排布规律。
④掌握元素周期律的实质。
了解元素周期表(长式)的结构(周期、族)及其应用。
⑤以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
⑥以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
⑦了解金属、非金属元素在周期表中的位置及其性质递变规律。
⑧了解化学键的定义。
了解离子键、共价键的形成。
①能正确书写化学方程式和离子方程式,并能进行有关计算。
⑥了解氧化还原反应的本质。
了解常见的氧化还原反应。
掌握常见氧化还原反应的配平和相关计算。
3.常见无机物及其应用ⅠⅠIII IIIIII III IIIⅡIII III(1)常见金属元素(如Na 、Mg 、Al 、Fe 、Cu 等)①了解常见金属的活动顺序。
②了解常见金属及其重要化合物的制备方法,掌握其主要性质及其应用。
③了解合金的概念及其重要应用。
(2)常见非金属元素(如H 、C 、N 、O 、Si 、S 、Cl 等)①了解常见非金属元素单质及其重要化合物的制备方法,掌握其主要性质及其应用。
②了解常见非金属元素单质及其重要化合物对环境的影响。
(3)以上各部分知识的综合应用。
ⅡⅡⅠIIIⅠIII本节考向题型研究汇总题型考向考点/考向考试要求选择题元素周期律III填空题无机综合III考向题型研究物质结构1.(2017·全国I·T12)短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。
由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。
下列说法不正确的是()A.X的简单氢化物的热稳定性比W的强B.Y的简单离子与X的具有相同的电子层结构C.Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红D.Z与X属于同一主族,与Y属于同一周期【答案】C【解析】四种主族元素都在短周期,W的简单氢化物可用作制冷剂,则W为N元素。
2020届高三考前冲刺工艺流程题专项训练(含答案)

(6)从废旧碱性锌锰电池中可以回收利用的物质有 _____________________(写两种)。 7.亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、 印染和食品工业.它在碱性环境中稳定存在。某同学查阅资料后 设计生产 NaClO2 主要流程如下:
(1)Ⅰ中发生反应的还原剂是___________,气体 a 的名称是 ___________ (2) Ⅱ 中 反 应 的 离 子 方 程 式 是 _________________________________________ (3)A 的化学式是___________ (4)Ⅲ中电极 X 是___________,(填“阴极”“阳极”),其上 发生的电极反应为 ____________________________。离子交换膜 N 是____(填“阴” “阳”)离子交换膜。(5)ClO2 是一种高效水处理剂,可用亚氯 酸钠和稀盐酸为原料制备: 5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O,该反应中氧化剂和还原剂
(1)反应①的尾气可以再利用,写出应用该尾气制得的两种重 要化学试剂:____________。(2)如果在实验室模拟操作 1 和 操作 2,则需要使用的主要玻璃仪器有:_______________。 (3)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶 液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式 为_______________。 (4)工业上制备还原性气体 CO 和 H 2 的反应原理为 CO 2+CH 42CO +2H 2,CH 4+H 2O CO +3H 2。含甲烷体积分数为 80%的 a L(标准状况)天然气与足 量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为 90%,用产生的还原性气体(CO 和 H 2)还原 MoO 3 制钼,理论上 能生产钼的质量为____________。 5.二氟磷酸锂(LiPO 2F 2)作为电解液添加剂能够有效提升锂电 池的循环性能。在氮气气氛下,在 PFA(全氟烷氧基树脂)烧瓶中 加入高纯 LiPF 6 和 Li 2CO 3 固体,以碳酸二甲酯作溶剂制备 LiPO 2F 2,其流程如下:
2020届高三化学大题练——化学工艺流程题
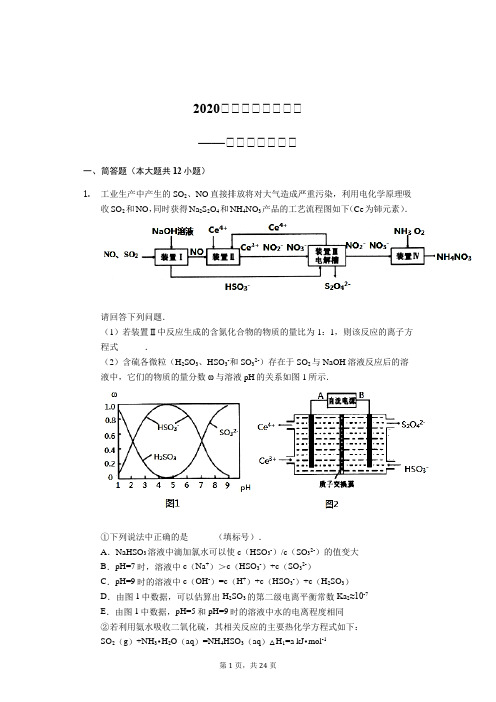
2020届届届届届届届届——届届届届届届届一、简答题(本大题共12小题)1.工业生产中产生的SO2、NO直接排放将对大气造成严重污染,利用电化学原理吸收SO2和NO,同时获得Na2S2O4和NH4NO3产品的工艺流程图如下(Ce为铈元素).请回答下列问题.(1)若装置Ⅱ中反应生成的含氮化合物的物质的量比为1:1,则该反应的离子方程式______.(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω与溶液pH的关系如图1所示.①下列说法中正确的是______(填标号).A.NaHSO3溶液中滴加氯水可以使c(HSO3-)/c(SO32-)的值变大B.pH=7时,溶液中c(Na+)>c(HSO3-)+c(SO32-)C.pH=9时的溶液中c(OH-)=c(H+)+c(HSO3-)+c(H2SO3)D.由图1中数据,可以估算出H2SO3的第二级电离平衡常数Ka2≈10-7E.由图1中数据,pH=5和pH=9时的溶液中水的电离程度相同②若利用氨水吸收二氧化硫,其相关反应的主要热化学方程式如下:SO2(g)+NH3•H2O(aq)=NH4HSO3(aq)△H1=a kJ•mol-1NH3•H2O (aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l)△H2=b kJ•mol-1 2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq)△H3=c kJ•mol-1反应2SO2(g)+4NH3•H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)△H=______kJ•mol-1.③取装置Ⅰ中的吸收液VmL,用cmol/L的酸性高锰酸钾溶液滴定.吸收液溶液应装在______(填“酸式”或“碱式”)滴定管中,判断滴定终点的方法______.(3)装置Ⅲ的作用之一是再生Ce4+,其原理如图2所示.图中B为电源的______(填“正”或“负”)极.左侧反应室中发生的主要电极反应式为______.(4)已知进入装置Ⅳ的溶液中NO2-的浓度为0.4mol/L,要使1m3该溶液中的NO2-完全转化为NH4NO3,该过程中转移电子数目为______.2.2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛.(1)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理.已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为______;(2)氧化铁是重要工业颜料,下面是制备氧化铁的一种方法,其流程如下:①操作Ⅰ的名称是______;操作Ⅱ为洗涤,洗涤操作的具体方法为______;②滤液A中加入稍过量的NH4HCO3溶液生成沉淀同时有一种气体产生,写出其化学方程式:______;(3)如果煅烧不充分,产品中将有FeO存在,称取3.0g氧化铁产品,溶解,在250mL 容量瓶中定容;量取25.00mL待测溶液于锥形瓶中,用酸化的0.01000mol/L KMnO4溶液滴定至终点,重复滴定2-3次,消耗KMnO4溶液体积的平均值为20.00mL,①该实验中的KMnO4溶液需要酸化,用于酸化的酸是______(填字母序号).a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸②计算上述产品中Fe2O3的质量分数为______.3.某学习小组利用废旧电池拆解后的碳包滤渣(含MnO2、C、Hg2+等)制取硫酸锰晶体( MnSO4•H2O ),实验流程如下:已知:(1)25℃时,几种硫化物的溶度积常数如下:物质 FeS MnS HgS 溶度积 5×10-18 4.6×10-14 2×10-54(2)25℃时,几种金属氢氧化物沉淀时的PH 如下:Fe (OH )2 Fe (OH )3Mn (OH )2 开始沉淀时的PH 6.3 2.78.3 沉淀完全时的PH 8.43.7 9.8 请回答下列问题:(1)“浸取”时加热的作用是______;写出“浸取”时生成MnSO 4、Fe 2(SO 4)3 反应的离子方程式:______.(2)若“浸取”在25℃时进行,加入足量FeS ,则FeS (s )+Hg 2+(aq )⇌HgS (s )+Fe 2+ (aq )的平衡常数K 为______.(3)过滤I 过程中,需要使用的玻璃仪器有烧杯、______,滤渣I 的主要成分为FeS 、S 和______(化学式).(4)“氧化”时加入MnO 2 的作用是______,也可用H 2O 2 代替MnO 2 ,H 2O 2 的电子式为______.(5)“中和”过程,应该调节溶液PH 为______,写出该过程产生滤渣II 的离子方程式:______(6)获得MnSO 4•H 2O 的“一系列操作”是______、过滤、洗涤、干燥.(7)1150℃时,MnSO 4•H 2O 在氩气氛围中进行焙烧的分解产物是Mn 3O 4、硫的氧化物等,分解反应的化学方程式是:______,在MnSO 4•H 2O 进行焙烧时,除加热仪器外,还需要的仪器中主要成分属硅酸盐的有______.4. 草酸钴用途广泛,可用于指示剂和催化剂制备.一种利用水钴矿[主要成分为Co 2O 3,含少量Fe 2O 3、Al 2O 3、MnO 、MgO 、CaO 等]制取CoC 2O 4•2H 2O 工艺流程如图1:已知:①浸出液含有的阳离子主要有H +、Co 2+、Fe 2+、Mn 2+、Ca 2+、Mg 2+、Al 3+等; ②部分阳离子以氢氧化物形式沉淀时溶液的pH 见表:沉淀物 Fe (OH )3 Fe (OH )2 Co (OH )2 Al (OH )3 Mn (OH )2完全沉淀的pH3.79.69.2 5.29.8(1)浸出过程中加入Na2SO3的目的是将______还原(填离子符号).(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,产物中氯元素处于最低化合价.该反应的离子方程式为______.(3)请用平衡移动原理分析加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是:______.(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是______;使用萃取剂适宜的pH是______.A.接近2.0 B.接近3.0 C.接近4.0(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知K sp(MgF2)=______.=7.35×10-11、K sp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)c(Ca2+)(6)为测定制得的无水草酸钴样品的纯度,现称取样品mg,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用cmol/L高锰酸钾溶液去滴定,当溶液由______(填颜色变化),共用去高锰酸钾溶液VmL(CoC2O4的摩尔质量147g/mol),计算草酸钴样品的纯度为______.5.图l表示“侯氏制碱法”工业流程,图2表示各物质的溶解度曲线.回答下列问题:(1)图中X的化学式为______ .(2)沉淀池中发生反应的化学方程式为______ ,该反应先向饱和食盐水中通入______ (填化学式)至饱和,再通入另一种气体,若顺序颠倒,后果是______ .(3)沉淀池的反应温度控制在30~35℃,原因是______ .(4)母液中加入CaO后生成Y的化学方程式为______ .(5)氯碱工业是指电解饱和食盐水,这里的碱是指______ (填化学式),其另外两种气体产物可以用于工业上制取纯硅,流程如图3:①整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应,写出该反应的化学方程式______ .②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%.则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是______ .6.Ⅰ.工业上常利用电解含有铁、钯、铜等金属的粗银棒精炼银,示意图如下:(1)阴极反应式为______。
2020届高三工艺流程题考前冲刺二
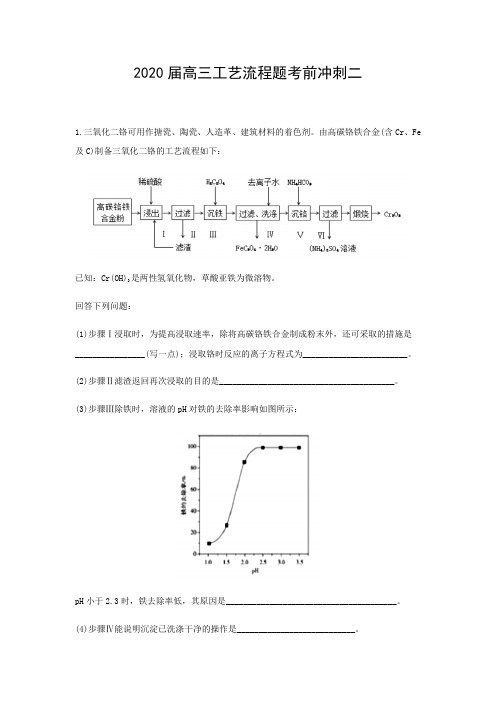
2020届高三工艺流程题考前冲刺二1.三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。
由高碳铬铁合金(含Cr、Fe 及C)制备三氧化二铬的工艺流程如下:已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是________________(写一点);浸取铬时反应的离子方程式为________________________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图所示:pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是___________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
2.CoCl2·6H2O是一种饲料营养强化剂。
一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式。
2020高考化学工艺流程题特殊考点汇编
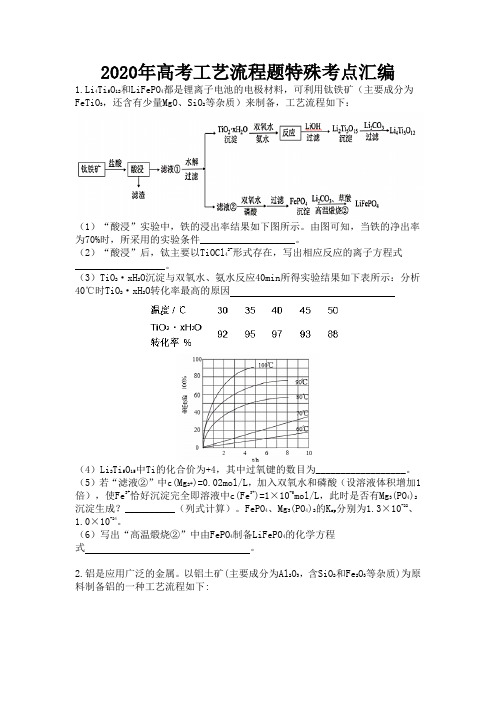
2020年高考工艺流程题特殊考点汇编1.Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:(1)“酸浸”实验中,铁的浸出率结果如下图所示。
由图可知,当铁的净出率为70%时,所采用的实验条件___________________。
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:分析40℃时TiO2·xH2O转化率最高的原因(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5mol/L,此时是否有Mg3(PO4)2沉淀生成?__________(列式计算)。
FePO4、Mg3(PO4)2的K sp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式。
2.铝是应用广泛的金属。
以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________(填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。
2019-2020年高考化学复习备考工艺流程试题汇总
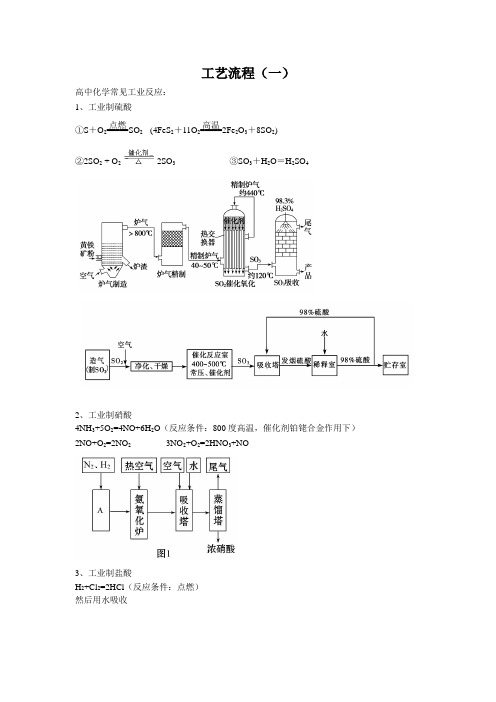
工艺流程(一)高中化学常见工业反应: 1、工业制硫酸①S +O 2=====点燃SO 2 (4FeS 2+11O 2=====高温2Fe 2O 3+8SO 2) ②2SO 2 + O 22SO 3 ③SO 3+H 2O =H 2SO 42、工业制硝酸4NH 3+5O 2=4NO+6H 2O (反应条件:800度高温,催化剂铂铑合金作用下) 2NO+O 2=2NO 2 3NO 2+O 2=2HNO 3+NO3、工业制盐酸H 2+Cl 2=2HCl (反应条件:点燃) 然后用水吸收4、工业制烧碱(氯碱工业)2NaCl+2H 2O=H 2+Cl 2+2NaOH (电解饱和食盐水)5、工业制取漂白粉(漂粉精)、漂白液 2Ca(OH)2+2Cl 2=CaCl 2+Ca(ClO)2+2H 2O 2 NaOH +Cl 2=NaCl+NaClO+H 2O6、工业制纯碱(侯氏).侯氏制碱法 NaCl +NH 3+CO 2+H 2O =NaHCO 3+NH 4Cl 1)NH 3+H 2O+CO 2=NH 4HCO 32)NH 4HCO 3+NaCl=NaHCO 3+NH 4Cl (NaHCO 3结晶析出) 3)2NaHCO 3=====△Na 2CO 3+CO 2↑+H 2O7、工业制金属铝2Al 2O 3===========950~970 ℃通电,Na 3AlF 64Al +3O 2↑利用反应 SiO 2+2C=====高温Si+2CO↑能得到不纯的粗硅。
粗硅需进行精制,才能得到高纯度硅。
首先,使Si 跟Cl 2起反应: Si+2Cl 2=SiCl 4(400 ℃~500 ℃)生成的SiCl4液体通过精馏,除去其中的硼、砷等杂质。
然后,用H 2还原SiCl 4: SiCl 4+2H 2=====高温Si+4HCl 这样就可得到纯度较高的多晶硅。
9.硅酸盐工业(制普通玻璃)生石灰 (高温煅烧石灰石) CaCO 3=====高温CaO+CO 2↑玻璃工业(玻璃窑法) Na 2CO 3 + SiO 2=====高温Na 2SiO 3 +CO 2↑ CaCO 3 + SiO 2=====高温CaSiO 3 +CO 2↑ 10.高炉炼铁3CO +Fe 2O 3=====高温2Fe +3CO 2 11.工业制取水煤气 C+H 2O=====高温CO+H 212.粗铜的精炼 电解:阳极用粗铜阳极:Cu -2e -=Cu 2+阴极:Cu 2++2e -=Cu 13、工业制氨气N 2(g)+3H 2(g) 2NH 3(g)注:催化剂为铁触媒MgCl 2(熔融)Mg +Cl 2↑15.海水提溴Cl 2+2Br -===2Cl -+Br 2Br 2+SO 2+2H 2O===2HBr +H 2SO 416.化石燃料的综合利用石油煤原料 原油煤 原理分馏、裂化、裂解干馏产品溶剂油、汽油、煤油、柴油、重油、润滑油、凡士林、乙烯、丙烯、丁烯等工艺流程(二)1.锌可作为食品锌强化剂的原料。
