高考化学工艺流程题汇总
高考化学工艺流程题目专项练习

高考化学工艺流程题目专项练习1.废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。
湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。
某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是________。
循环使用的NH4Cl 在反应Ⅰ中的主要作用是_________________________________________。
【答案】H2SO4防止由于溶液中的c(OH-)过高,生成Cu(OH)2沉淀【解析】操作④得到的H2SO4可以利用到反应Ⅲ中,所以第三处循环的试剂为H2SO4;NH4Cl水解溶液呈酸性,可以中和溶液中的OH―,防止由于溶液中的c(OH-)过高,生成Cu(OH)2沉淀。
2.毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:pH pHCa2+Mg2+Fe3+开始沉淀时的pH 11.9 9.1 1.9完全沉淀时的pH 13.9 11.1 3.2加入NH3·H2O调节pH=8可除去________(填离子符号),滤渣Ⅱ中含________(填化学式)。
加入H2C2O4时应避免过量,原因是_____________________________________________________________。
已知:K sp(BaC2O4)=1.6×10-7,K sp(CaC2O4)=2.3×10-9。
【答案】Fe3+Mg(OH)2、Ca(OH)2H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少【解析】根据流程图及表格中数据可知,加入NH3·H2O调节pH=8时,只有Fe3+完全沉淀而除去。
加入NaOH,调pH=12.5,对比表格中数据可知,此时Mg2+完全沉淀,Ca2+部分沉淀,所以滤渣Ⅱ中含Mg(OH)2、Ca(OH)2。
(完整版)高考化学工艺流程题

工艺流程题专题(教师版)考察形式:流程图、表格图像、文字叙述问题类型:措施、成分、物质、原因能力考查:获取信息的能力、分解问题的能力、表达能力知识基础:基本生产理论,金属、非金属及其化合物、有机物的性质,实验基本操作无机工业流程图题能够以真实的工业生产过程为背景,体现能力立意的命题指导思想,能够综合考查各方面的基础知识及将已有知识灵活应用在生产实际中解决问题的能力。
【例】某工厂生产硼砂过程中产生的固体废料,主要含有MgCO 3、MgSiO 3、CaMg(CO 3)2、Al 2O 3和Fe 2O 3等,回收其中镁的工艺流程如下:原 料:矿石(固体)预处理:酸溶解(表述:“浸出”)除 杂:控制溶液酸碱性使金属离子形成沉淀核心化学反应是:控制条件,调节PH ,使Mg 2+全部沉淀解题技巧: 明确整个流程及每一部分的目的 → 仔细分析每步发生的反应及得到的产物 → 结合基础理论与实际问题思考 → 注意答题的模式与要点在解这类题目时:1、要粗读试题,尽量弄懂流程图,但不必将每一种物质都推出。
2、再精读试题,根据问题去精心研究某一步或某一种物质。
3、要看清所问题,不能答非所问,并注意语言表达的科学性在答题时应注意:前一问回答不了,并不一定会影响回答后面的问题。
一、分析流程图需要掌握的技巧是:浏览全题,确定该流程的目的——由何原料获得何产物(副产物),对比原料和产物;了解流程图以外的文字描述、表格信息、后续设问中的提示性信息,并在下一步分析和解题中随时进行联系和调用;解析流程图并思考:从原料到产品依次进行了什么反应?利用了什么原理(氧化还原?溶解度?溶液中的平衡?)。
每一步操作进行到什么程度最佳?每一步除目标物质外还产生了什么杂质或副产物?杂质或副产物是怎样除去的?Ⅱ分离提纯Ⅰ预处理 Ⅱ分离提纯Ⅲ 还原二、无机化工题:要学会看生产流程图,对于比较陌生且复杂的流程图,宏观把握整个流程,不必要把每个环节的原理都搞清楚,针对问题分析细节。
高三化学 化学工艺流程题(含答案

高高高高高高高高高高—高高高高高高高01高高高VIB高高高高高高高一、单选题(本大题共2小题,共4分)1.以铬铁矿为原料[Fe(CrO2)2]可制备K2Cr2O7和金属铬。
实验流程如下:下列说法中,不正确的是()A. 焙烧时不能使用陶瓷容器B. Na2S的作用是调节溶液的酸碱度和将重铬酸钠还原为氢氧化铬C. 在酸性溶液中CrO42−比Cr2O72−稳定D. 操作①包括过滤和洗涤。
实验室洗涤沉淀的操作是沿玻璃棒加水至浸没沉淀,待水自然滤出,重复2∼3次【答案】C【解析】【分析】本题考查实验制备方案设计,为高考常见题型,侧重考查学生的分析能力、实验能力,注意把握实验的原理以及物质的性质,把握实验操作的方法,难度中等。
【解答】A.高温下二氧化硅与碳酸钠反应,生成硅酸钠和二氧化碳,则焙烧时不能使用陶瓷容器焙烧,故A正确;B.Na2Cr2O7溶液中加入Na2S,发生氧化还原反应生成Cr(OH)3,同时调节溶液的pH,故B正确;C.在酸性溶液中Cr2O72−比CrO42−稳定,故C错误;D.实验室洗涤沉淀的操作是沿玻璃棒加水至浸没沉淀,待水自然滤出,重复2∼3次操作正确,故D正确。
故选C。
2.某电镀污泥含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量金等,某小组设计如下资源综合利用的方案:已知:碲和硫位于同主族,煅烧时Cu 2Te 发生的反应为,滤渣中TeO 2溶于稀硫酸发生的反应为TeO 2+H 2SO 4=TeOSO 4+H 2O 。
下列说法错误的是( )A. “高温煅烧”电镀污泥时铜、碲和铬元素都被氧化B. “酸化”时可向溶液中加入硫酸C. “固体1”的主要成分为CuD. “滤液3”可以循环利用【答案】C【解析】【分析】本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯方法、流程中发生的反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大。
2024高考化学工艺流程专题
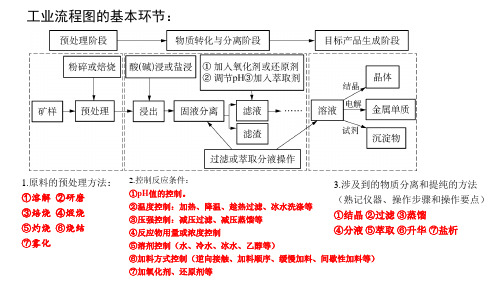
②还原焙烧:指在低于炉料熔点和还原气氛条件下,使矿石中的金属氧化物转变为相应 低价金属氧化物或金属的焙烧过程。 该焙烧过程中,一般要在矿石中附加细小的炭粒作还原剂。 还原焙烧目前主要用于处理难选的铁、锰、镍、铜、锡、锑等矿物原料。
产物 ②控制反应速率 ③控制反应物转化率和产品产率 ④控制环境温度 ⑤抑制(促进)离子 的水解 ⑥降低生产成本酸浸时酸过量的目的:为了提高矿石中某金属元素的浸取率;抑制**离 子的水解等。对有多种反应物的体系,增大便宜、易得的反应物的浓度目的是:提高其他物质 的利用率,使反应充分进行;降低生产成本等。如:增大浓度可以加快反应速率,使平衡发生 移动等。(应结合具体问题进行具体分析)。(2)控制加料的方法:逆向接触、加料顺序、缓 慢加料、间歇性加料等。
(2023·全国甲卷第26题)BaTiO3是一种压电材料。以BaSO4为原料,采用下 列路线可制备粉状BaTiO3。
回答下列问题:(1)“焙烧”步骤中碳粉的主要作用是_______。(2)“焙烧”后固体产物 有BaCl2、易溶于水的BaS和微溶于水的CaS。
“浸取”时主要反应的离子方程式为_______。 (1)“焙烧”步骤中,BaSO4与过量的碳粉及过量的氯化钙在高温下焙烧得到CO、BaCl2、BaS 和CaS,BaSO4被还原为BaS,因此,碳粉的主要作用是做还原剂,将BaSO4还原。(2)S2-易发生 水解生成HS-,
4.研磨:增大固体样品与溶液的接触面积,加快反应(浸取)速率或使反应更充分。
真题思演维练模型和方法模型
专题12 工艺流程综合题-三年(2022-2024)高考化学真题分类汇编(全国通用)(教师卷)

专题12工艺流程综合题考点三年考情(2022-2024)命题趋势考点1工艺流程综合题◆物质分离和提纯类工艺流程题:2024广东卷、2024湖南卷、2024河北卷、2024新课标卷、2024全国甲卷、2024黑吉辽卷、2024安徽卷、2023新课标卷、2023湖北卷、2023辽宁卷、2023广东卷、2023浙江卷、2022湖南卷、2022湖北卷、2022重庆卷、2022全国乙卷◆物质制备类工艺流程题:2024北京卷、2024甘肃卷、2024浙江卷6月、2024江苏卷、2024山东卷、2024湖北卷、2024浙江卷1月、2023全国甲卷、2023全国乙卷、2023湖南卷、2023山东卷、2023北京卷、2023浙江卷、2022全国甲卷、2022福建卷、2022辽宁卷、2022广东卷、2022北京卷、河北卷化学工艺流程题是将化工生产中的生产流程用框图形式表示出来,并根据生产流程中有关的化学知识步步设问。
化工流程题以现代工业生产为基础,与化学反应原理、产品提纯、环境保护等相融合,具有考查知识面广、综合性强、思维容量大的特点。
这类题型不但综合考查考生在中学阶段所学的元素及其化合物知识以及物质结构、元素周期律、氧化还原反应、化学用语、电解质溶液、化学平衡、电化学、实验操作等知识,而且更重要的是能突出考查考生的综合分析判断能力、逻辑推理能力,且这类试题陌生度高,文字量大,包含信息多,思维能力要求高。
近年高考有关考查要点和设问方式没有大的变化,注意的是有关化学方程式的书写的考查,有加强的趋势,一般有2~3个小问会涉及方程式的书写。
考法01物质分离提纯类工艺流程题1.(2024·广东卷)镓(Ga )在半导体、记忆合金等高精尖材料领域有重要应用。
一种从电解铝的副产品炭渣(含C Na Al F 、、、和少量的Ga Fe K Ca 、、、等元素)中提取镓及循环利用铝的工艺如下。
工艺中,LAEM 是一种新型阴离子交换膜,允许带负电荷的配离子从高浓度区扩散至低浓度区。
高三化学 化学工艺流程题(含答案

高高高高高高高高高高—高高高高高高高01高高高VIB高高高高高高高一、单选题(本大题共2小题,共4分)1.以铬铁矿为原料[Fe(CrO2)2]可制备K2Cr2O7和金属铬。
实验流程如下:下列说法中,不正确的是()A. 焙烧时不能使用陶瓷容器B. Na2S的作用是调节溶液的酸碱度和将重铬酸钠还原为氢氧化铬C. 在酸性溶液中CrO42−比Cr2O72−稳定D. 操作①包括过滤和洗涤。
实验室洗涤沉淀的操作是沿玻璃棒加水至浸没沉淀,待水自然滤出,重复2∼3次【答案】C【解析】【分析】本题考查实验制备方案设计,为高考常见题型,侧重考查学生的分析能力、实验能力,注意把握实验的原理以及物质的性质,把握实验操作的方法,难度中等。
【解答】A.高温下二氧化硅与碳酸钠反应,生成硅酸钠和二氧化碳,则焙烧时不能使用陶瓷容器焙烧,故A正确;B.Na2Cr2O7溶液中加入Na2S,发生氧化还原反应生成Cr(OH)3,同时调节溶液的pH,故B正确;C.在酸性溶液中Cr2O72−比CrO42−稳定,故C错误;D.实验室洗涤沉淀的操作是沿玻璃棒加水至浸没沉淀,待水自然滤出,重复2∼3次操作正确,故D正确。
故选C。
2.某电镀污泥含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量金等,某小组设计如下资源综合利用的方案:已知:碲和硫位于同主族,煅烧时Cu 2Te 发生的反应为,滤渣中TeO 2溶于稀硫酸发生的反应为TeO 2+H 2SO 4=TeOSO 4+H 2O 。
下列说法错误的是( )A. “高温煅烧”电镀污泥时铜、碲和铬元素都被氧化B. “酸化”时可向溶液中加入硫酸C. “固体1”的主要成分为CuD. “滤液3”可以循环利用【答案】C【解析】【分析】本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯方法、流程中发生的反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大。
专题16工艺流程题——三年(2020-2022)高考真题化学分项汇编(全国通用)(原卷版)

专题16 工艺流程题1.(2022·全国甲卷)硫酸锌(4ZnSO )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。
硫酸锌可由菱锌矿制备。
菱锌矿的主要成分为3ZnCO ,杂质为2SiO 以及Ca 、Mg 、Fe 、Cu 等的化合物。
其制备流程如下:本题中所涉及离子的氯氧化物溶度积常数如下表: 离子3+Fe2+Zn 2+Cu 2+Fe 2+MgspK384.010-⨯ 176.710-⨯ 202.210-⨯168.010-⨯ 111.810-⨯回答下列问题:(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X 调溶液pH=5,最适宜使用的X 是_______(填标号)。
A .32NH H O ⋅ B .2Ca(OH) C .NaOH 滤渣①的主要成分是_______、_______、_______。
(4)向80~90℃的滤液①中分批加入适量4KMnO 溶液充分反应后过滤,滤渣②中有2MnO ,该步反应的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓24H SO 反应可以释放HF 并循环利用,同时得到的副产物是_______、_______。
2.(2022·全国乙卷)废旧铅蓄电池的铅膏中主要含有4PbSO 、2PbO 、PbO 和Pb 。
还有少量Ba 、Fe 、Al 的盐或氧化物等。
为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表: 难溶电解质4PbSO3PbCO4BaSO3BaCOspK82.510-⨯ 147.410-⨯ 101.110-⨯ 92.610-⨯一定条件下,一些金属氢氧化物沉淀时的pH 如下表: 金属氢氧化物 3Fe(OH)2Fe(OH)3Al(OH)2Pb(OH)开始沉淀的pH 2.3 6.8 3.5 7.2 完全沉淀的pH 3.28.34.69.1回答下列问题:(1)在“脱硫”中4PbSO 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择23Na CO 的原因________。
(完整版)高考化学工艺流程题汇总,推荐文档

高考化学工艺流程题一、解读考试说明,探究命题思路1、化学工艺流程题为何取代传统无机框图题?传统无机框图题多年来一直是高考化学试卷中备受青睐的热门题型,但由于该类试题人为设计成分较多、问题编制模式过于单一、逻辑推理味道浓厚而化学味道淡薄,取而代之的是创新的工业生产流程题。
工业生产流程题取材于真实的、广阔的工业生产和日常生活,问题设计更加灵活,更有化学味,是落实新课程高考对考生素质和能力要求的具体体现,能够考查考生“将与化学相关的实际问题分解,综合运用相关知识和科学方法,解决生产、生活实际和科学研究中的简单化学问题的能力”。
正是新课程突出化学是一门实用性、创造性的科学,化学高考试题的发展趋势必然是重视与生产、生活的紧密联系,化学工艺流程题便成为近年来北京高考的新亮点和主流题型。
2、化学工艺流程题考查三维目标1)知识和技能(1由例题分析,初步认识工业生产流程题的特点。
(2了解工业生产流程题的解题思路和应具备的能力要求。
2)过程和方法采用例举、讨论、演绎、归纳等方式。
3)情感态度和价值观(l通过对工业生产流程题“真实性”的分析,培养学生的化学素养。
(2开展多种形式的讨论交流活动,培养学生的互助合作精神。
3、解流程题的步骤和方法首先,浏览全题,确定该流程的目的;——由何原料获得何产物(副产物),对比原料和产物。
其次,精读局部,明确反应原理——确定各步的反应物、生成物。
第三,针对问题再读图,明确要求——科学表述、规范书写。
4、考查要点:1)物质性质及其相互转化关系2)元素及其化合物的转化网络3)物质的分离和提纯的方法结晶——固体物质从溶液中析出的过程(蒸发溶剂、冷却热饱和溶液、浓缩蒸发)过滤——固、液分离蒸馏——液、液分离分液——互不相溶的液体间的分离萃取——用一种溶剂将溶质从另一种溶剂中提取出来。
升华——将可直接气化的固体分离出来。
盐析——加无机盐使溶质的溶解度降低而析出4)电解质溶液基本理论弱酸、弱碱的电离、水的电离、盐类水解、沉淀平衡5)氧化还原反应原料→产品6)方法:应用三大守恒写出陌生方程式,并能够进行简单计算电子守恒、电荷守恒、元素守恒法二、高考是怎么样考的?——研究试题,把握标高2009——2011年北京化学工艺流程题统计【例1】(2009北京理综,26,15分)以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):Ⅰ. 从废液中提纯并结晶出FeSO 4·7H 2O。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学工艺流程题汇总
(2010安徽)27.(14分)
锂离子电池的广泛应用使回收利用锂货源成为重要课题:某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)进行资源回收研究,设计实验流程如下:
⑴第②步反应得到的沉淀X的化学式为。
(1)第②步反应得到的沉淀X的化学式为。
(2)第③步反应的离子方程式
是。
(3)第④步反应后,过滤Li2CO3所需的玻璃仪器
有。
若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:
、。
(4)若废旧锂离子电池正极材料含LiNB2O4的质量为18.1 g第③步反应中加入
答案:27、(1)Al(OH)3
(2)4LiMn2O4+O2+4H+=4Li++8MnO2+2H2O
(3)漏斗玻璃棒烧杯;滤纸破损、滤液超过滤纸边缘等(其它合理答案均可)
(4)或
(2010北京)26.(14分)
某氮肥厂氨氮废水中的氮元素多以NH4+和的形式存在,该废水的处理流程如下:
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:。
②用化学平衡原理解释通空气的目的:。
(2)过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成。
两步反应的能量变化示意图如下:
①第一步反应是反应(选题“放热”或“吸热”),判断依据是。
②1mol NH4+(aq)全部氧化成NO3—(aq)的热化学方程式
是。
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。
若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是。
答案:(14分)
(1)①NH4++OH-===
②废水中的NH3被空气带走,使NH3+H2O
D的平衡向正反应方向移动,利于除氨
(2)①放热
△H=-273kJ/mol<0(反应为的总能量大于生成物的总能量)
②NH4+(aq)+2O2(g)===2H+(aq)+NO3-(aq)+H2O(l)
△ H=-346kJ/mol
③5:6
(2010广东)32.(16分)碳酸锂广泛应用于陶瓷和医药等领域,以β-锂辉石(主要成分为Li2O·Al2O3·4SiO2)为原料制备Li2CO3的工艺流程如下:
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH值分别为、、和。
Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g 和1.3g。
(1) 步骤I前,以β-锂辉石要粉碎成细颗粒的目的是___________________
(2) 步骤I中,酸浸后得到的酸性溶液中含有Li+、SO42-,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_________(填“石灰石”、“氯化钙”或“称硫酸”)以调节溶液的pH值为,沉淀部分杂质离子,然后分离得到浸出液。
(3) 步骤II中,将适量的H2O2溶液、石灰乳和碳酸钠溶液依次加入浸出液中,可除去的杂质金属离子有______________________。
(4) 步骤III中,生成沉淀的离子方程式为________________________。
(5) 从母液中可回收的主要物质是__________________。
(2010福建卷)24.硫酸锌可作为食品锌强化剂的原料。
工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3 MgO、CaO等,生产工艺流程示意如下:
(1)将菱锌矿研磨成粉的目的是_____。
(2)完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3 +□CI-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______。
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。
K^S*#O%
a.大理石粉 b.石灰乳 c.纯碱溶
液 d.烧碱溶液
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。
(2010江苏卷)16.(10分)钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3、BaSO4、Ba(FeO2)3等]。
某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取BaNO3,其部分工艺流程如下:
(1)酸溶后溶液中pH=1,Ba(FeO2)3与HNO3的反应化学方程式
为。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,
原因
是、。
(3)该厂结合本厂实际,选用的X为(填化学式);中和Ⅰ使溶液中(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的
是。
(2010四川理综卷)29.(16分)四川攀枝花蕴藏丰富的钒、钛、铁资源。
用钛铁矿渣(主要成分为TiO2、FeO、Fe2O3,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的主要步骤如下:
请回答下列问题:
硫酸与二氧化钛反应的化学方程式是____________________________________。
(1向滤液I中加入铁粉,发生反应的离子方程式为:
_________________________、____________________。
(2)在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液pH达,钛盐开始水解。
水解过程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二氧化钛沉淀。
请用所学化学平衡原理分析通入高温水蒸气的作用:
_______________________________________________。
过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐、___________、______________、_______________________(填化学式),减少废物排放。
(4)A可用于生产红色颜料(Fe2O3),其方法是:将556a kgA(摩尔质量为278 g/mol)溶于水中,加入适量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体;再向红褐色胶体中加入3336b kg A和112c kg铁粉,鼓入足量空气搅拌,反应完成后,有大量Fe2O3附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。
若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料_______________________kg。
