最新慢性阻塞性肺疾病
慢阻肺2024年新疗法解读

慢阻肺2024年新疗法解读1. 引言慢性阻塞性肺疾病(慢阻肺,COPD)是一种常见的慢性疾病,全球发病率及死亡率均较高。
其主要特点是气道慢性炎症、气道阻塞和气流受限。
目前,我国慢阻肺患者已超过1亿,给公共卫生系统带来了沉重的负担。
近年来,随着医学研究的深入,慢阻肺的新疗法不断涌现。
本文将对2024年慢阻肺的新疗法进行解读,以期为临床实践和患者治疗提供参考。
2. 慢阻肺2024年新疗法概述2.1 生物制剂生物制剂在慢阻肺治疗中的应用逐渐受到关注。
2024年,几种新型生物制剂取得了显著的研究成果,如:抗肿瘤坏死因子-α(TNF-α)抑制剂、白三烯受体拮抗剂等。
这些生物制剂可有效减轻气道炎症,改善肺功能,为慢阻肺患者提供了新的治疗选择。
2.2 吸入性药物吸入性药物一直是慢阻肺治疗的重要手段。
2024年,新型吸入性药物的研发取得了突破性进展,如:长效 muscarinic antagonist (LAMA)和长效β2-adrenergic agonist(LABA)的联合应用,以及前列腺素E2(PGE2)受体拮抗剂等。
这些新型吸入性药物可有效缓解症状,改善肺功能,降低急性加重风险。
2.3 免疫疗法免疫疗法在慢阻肺治疗中的应用逐渐受到关注。
2024年,研究人员发现,通过调节患者免疫系统,可减轻气道炎症,改善肺功能。
其中,细胞因子疗法、免疫调节剂等新型免疫疗法取得了显著的疗效,为慢阻肺患者带来了新的希望。
2.4 基因治疗基因治疗在慢阻肺治疗领域的研究取得了重要进展。
2024年,研究人员发现,通过修复或替换受损的基因,可以有效改善慢阻肺患者的肺功能。
虽然基因治疗目前仍处于临床试验阶段,但已显示出良好的前景。
3. 结论2024年慢阻肺新疗法的出现,为临床实践和患者治疗提供了更多选择。
生物制剂、吸入性药物、免疫疗法和基因治疗等新型疗法在慢阻肺治疗中的应用,有望显著改善患者症状,提高生活质量,降低急性加重风险。
然而,这些新疗法的临床应用仍需进一步研究和验证。
2024年慢性阻塞性肺病最新治疗指南(全文)

2024年慢性阻塞性肺病最新治疗指南(全文)2024年慢性阻塞性肺病(COPD)最新治疗指南引言慢性阻塞性肺病(Chronic Obstructive Pulmonary Disease,简称COPD)是一种以气流受限为特征的进行性气道炎症性疾病,主要包括慢性支气管炎和肺气肿。
COPD是全球范围内导致慢性呼吸衰竭和死亡的主要病因之一。
为了提高COPD的诊疗水平,制定科学、规范的治疗指南至关重要。
本文档旨在整理2024年COPD最新治疗指南,为临床实践提供参考。
诊断病因学诊断1. 详细询问病史,了解患者吸烟史、环境污染史、感染史等相关因素。
2. 进行胸部X线检查、肺功能检查、呼气一氧化氮(FeNO)检测等,以评估气道炎症和气流受限程度。
3. 根据诊断标准,确定COPD的类型和严重程度。
并发症诊断1. 慢性呼吸衰竭:通过动脉血气分析、血氧饱和度等检查评估。
2. 慢性肺源性心脏病:通过心电图、超声心动图等检查评估。
3. 其他并发症:如肺结核、肺炎等,需根据相应疾病的特点进行诊断。
治疗药物治疗1. 支气管舒张剂:包括β2受体激动剂、抗胆碱能药物等,用于缓解气道痉挛,改善呼吸功能。
2. 糖皮质激素:长期使用可降低气道炎症,改善肺功能,减少急性加重发作。
3. 磷酸二酯酶-4(PDE4)抑制剂:具有抗炎作用,可用于治疗COPD。
4. 抗生素:用于治疗感染引起的急性加重。
非药物治疗1. 戒烟:对改善COPD患者预后具有重要意义。
2. 氧疗:长期氧疗可改善患者生活质量,降低肺功能恶化的速度。
3. 康复锻炼:包括呼吸锻炼、有氧运动等,有助于提高患者呼吸功能和体力。
4. 营养支持:合理膳食,补充蛋白质、维生素等营养物质。
手术治疗1. 肺大泡切除术:适用于肺大泡导致的呼吸困难等症状。
2. 肺移植:适用于严重COPD、药物治疗无效的患者。
预防和随访1. 加强宣教,提高患者对COPD的认识,加强自我管理。
2. 定期随访,监测肺功能、血气分析等指标,评估病情变化。
最新慢性阻塞性肺疾病评分(CAT)
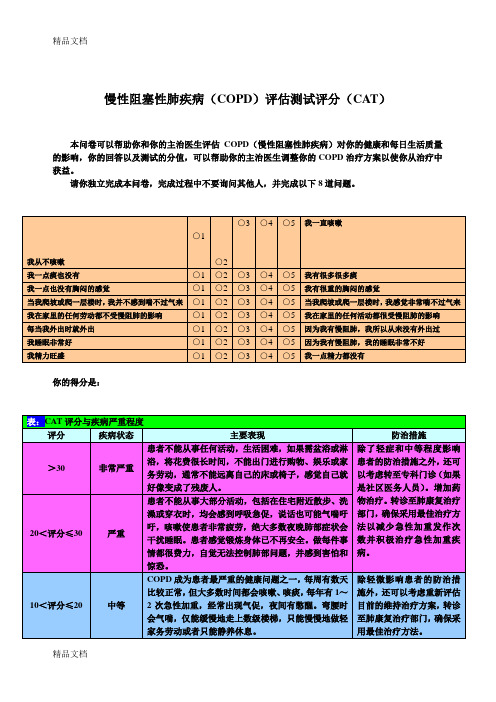
请你独立完成本问卷,完成过程中不要询问其他人,并完成以下8道问题。
四、影响的宏观环境分析在现代文化影响下,当今大学生对新鲜事物是最为敏感的群体,他们最渴望为社会主流承认又最喜欢标新立异,他们追随时尚,同时也在制造时尚。“DIY自制饰品”已成为一种时尚的生活方式和态度。在“DIY自制饰品”过程中实现自己的个性化追求,这在年轻的学生一代中尤为突出。“DIY自制饰品”的形式多种多样,对于动手能力强的学生来说更受欢迎。
防治措施
>30
非常严重
患者不能从事任何活动,生活困难,如果需盆浴或淋浴,将花费很长时间,不能出门进行购物、娱乐或家务劳动,通常不能远离自己的床或椅子,感觉自己就好像变成了残废人。
除了轻症和中等程度影响患者的防治措施之外,还可以考虑转至专科门诊(如果是社区医务人员)。增加药物治疗。转诊至肺康复治疗部门,确保采用最佳治疗方法以减少急性加重发作次数并积极治疗急性加重疾病。
体现市民生活质量状况的指标---恩格尔系数,上海也从1995年的53.4%下降到了2003年的37.2%,虽然与恩格尔系数多在20%以下的发达国家相比仍有差距,但按照联合国粮农组织的划分,表依据恩格尔系数,将恩格尔系数在40%-50%定为小康水平的消费,20%-40%定为富裕状态的消费)。慢性阻塞性肺疾病(COPD)评估测试评分(CAT)
包括戒烟、每年接种流感疫苗、减少暴露于急性加重危险因素以及通过进一步临床评价,保障所采取的治疗措施。
(六)DIY手工艺品的“创作交流性”
PS:消费者分析调研课题:我从不咳嗽
2023年度慢阻肺最新临床指南解读

2023年度慢阻肺最新临床指南解读1. 引言慢性阻塞性肺疾病(慢阻肺,COPD)是全球范围内导致慢性呼吸衰竭和死亡的主要病因之一。
近年来,随着对慢阻肺研究的深入,临床指南也在不断更新和完善。
本文将为您详细解读2023年度慢阻肺最新临床指南,帮助您了解慢阻肺的诊断、评估和治疗的最新进展。
2. 慢阻肺的诊断2.1 病史和临床表现2023年度慢阻肺指南强调了对患者病史和临床表现的重视。
医生应询问患者是否有慢性咳嗽、咳痰、气促和呼吸困难等症状,以及是否有吸烟等危险因素的暴露史。
此外,医生还应关注患者是否有反复发作的肺部疾病,如肺炎和支气管炎等。
2.2 肺功能检查肺功能检查是诊断慢阻肺的关键手段。
指南建议,对于有吸烟史或有慢性呼吸道症状的患者,应进行肺功能检查。
肺功能检查应包括用力肺活量(FVC)和一秒钟用力呼气容积(FEV1)的测量。
如果FEV1/FVC比率低于70%,可诊断为慢阻肺。
3. 慢阻肺的评估3.1 症状评估症状评估是慢阻肺管理的重要组成部分。
指南推荐使用慢阻肺评估测试(CAT)或改良版慢阻肺评估测试(mMRC)等工具对患者症状进行评估。
根据症状严重程度,将患者分为轻度、中度、重度和极重度。
3.2 肺功能评估肺功能评估主要包括对FEV1和FVC的测量。
根据FEV1/FVC比率,将患者分为GOLD 1-4级,以指导治疗方案的选择。
4. 慢阻肺的治疗4.1 药物治疗药物治疗是慢阻肺治疗的核心。
2023年度慢阻肺指南推荐使用长效β2受体激动剂(LABA)和长效 muscarinic 受体拮抗剂(LAMA)作为首选治疗。
对于中度至重度慢阻肺患者,指南还推荐使用联合疗法,如LABA+LAMA或LABA+糖皮质激素(ICS)等。
4.2 非药物治疗非药物治疗包括肺康复、氧疗和营养支持等。
指南强调,肺康复训练可改善患者肺功能和生活质量,应作为慢阻肺治疗的组成部分。
对于重度至极重度患者,长期氧疗可提高生存率和生活质量。
COPD(慢性阻塞性肺病)诊治指南(2023年中文版)

COPD(慢性阻塞性肺病)诊治指南(2011 中文版)1000字COPD(慢性阻塞性肺病)是一种严重的慢性呼吸系统疾病,其病理生理学特征为不完全可逆的气道阻塞和肺部组织的炎症反应。
COPD患者的气流受限主要由两个互补的病理生理学机制所致:气道炎症和气道变形及纤维化。
例如,慢性支气管炎及肺气肿属于 COPD 的常见表现形式。
在全球, 目前约有过10%的成年人患有 COPD, 到了2030年, COPD可能成为第三位导致死亡的疾病,同时, COPD 对经济的负担和社会层面的影响包括工作能力的减退、减少社会接触和生活质量受损等, 而且 COPD 的发病率也在逐年增加。
因此,针对 COPD 患者的诊断、治疗和预防显得格外重要。
COPD的诊断主要依靠病史、临床表现、肺功能检测和影像学检查等方法。
病史是对 COPD 诊断的基础,病人有咳嗽、气促、咳痰等症状。
检查还需考虑典型的病因、诱因和危险因素等,肺功能检测能够测定COPD胸腔的体积和肺泡的扩张程度等数据。
影像学检查在COPD诊断和评估患者状况的过程中非常重要,例如X线和 CT 检查能够检测出肺部异常结构和细节。
大多数COPD患者肺功能明显受损,用呼吸道疾病问卷筛查CO(COPD Assessment Test)。
COPD的治疗策略可以分为非药物治疗和药物治疗。
非药物治疗包括戒烟、充足的营养和体减、充足的休息和锻炼、控制症状和预防加重等方面。
同时,需要患者和家属一同合作来减轻症状和改善生活质量。
药物治疗包括短效和长效吸入支气管扩张剂、糖皮质激素、免疫抑制剂和粘液溶解剂等主要药物。
根据2011中国肺科学会编制的COPD诊治指南, 对于COPD的治疗应综合考虑气道炎症和气道变形及纤维化的复杂性。
因此,治疗应该围绕这个复杂性展开,而非是单一的药物。
在药物治疗方面,COPD病人的药物选择应该分析患者状况,包括既往病史、用药史、胸部影像学和肺功能等来确定。
选择合理的药物,可以有效地改善患者的症状和减轻他们的痛苦。
2024版慢性阻塞性肺疾病ppt课件

2024/1/25
个体化治疗和精准医学将在慢性阻塞 性肺疾病的治疗中发挥越来越重要的 作用
新的治疗手段和药物的不断涌现将为 慢性阻塞性肺疾病的治疗提供更多选 择
26
THANKS
感谢观看
2024/1/25
27
2024/1/25
16
心血管合并症风险评估及干预措施
2024/1/25
风险评估
通过心电图、超声心动图等检查手 段,评估患者心血管合并症的风险, 如心肌缺血、心力衰竭等。
干预措施
针对患者具体病情,采取相应治疗 措施,如控制高血压、改善心肌供 血、减轻心脏负荷等,以降低心血 管事件的发生率。
17
其他并发症(如骨质疏松等)防范建议
耐量。
2024/1/25
药物治疗选择
根据症状严重程度、急性加重风险、 副作用等因素选择合适药物。
药物治疗调整
根据症状缓解程度、副作用等及时 调整治疗方案。
12
非药物治疗方法探讨
01
02
03
氧疗
对于严重低氧血症患者, 长期氧疗可提高生存率。
2024/1/25
机械通气
对于严重呼吸衰竭患者, 机械通气可维持生命。
4
流行病学及危害程度
流行病学
COPD是全球范围内的一种常见疾病,尤其在吸烟人群中更为普遍。其发病率 和死亡率均较高,严重影响患者的生活质量和预期寿命。
危害程度
COPD可导致患者呼吸困难、咳嗽、咳痰等症状,严重影响患者的日常活动和 生活质量。随着病情的发展,患者可能出现呼吸衰竭、肺心病等严重并发症, 甚至危及生命。
19
康复期目标设定和实施方案
最新:慢性阻塞性肺疾病的社区健康管理(全文)

最新:慢性阻塞性肺疾病的社区健康管理(全文)慢性阻塞性肺疾病(慢阻肺)是长期终生的慢性疾病,给患者家庭和社会造成沉重负担。
目前全球患者已达6亿人次,我国约有9990万人,>60岁人群患病率高达27%。
研究显示,轻中度气流受限和无症状或症状隐匿的患者多数未得到及时的诊断和治疗。
社区医疗卫生机构与居民联系紧密,医疗环境友好,有利于进行包括早期干预、用药及生活方式指导、营养及康复治疗等在内的一系列长期规范管理。
《慢性阻塞性肺疾病基层诊疗指南(2018年)》指出,慢阻肺的预防、高危/疑似患者的识别、筛查、患者教育、康复治疗和长期随访等任务应交给基层医疗卫生机构,开展双向转诊;终末期患者可以在社区医院及医养结合的家庭病床治疗。
社区全科医生关注并长期规范疾病管理、康复有利于提高患者的生命质量及活动耐力,改善临床症状及急性发作,获得良好的成本效益。
因此,有必要完善更加规范合理的慢阻肺社区管理。
本文通过阐述目前国内外慢阻肺社区健康管理现状并对其未来发展与挑战进行展望,以期提高我国慢阻肺健康管理水平以及慢阻肺患者生命质量。
一、我国慢阻肺社区健康管理现状1.慢阻肺相关卫生政策2009年我国启动国家基本公共卫生服务项目,由基层医疗卫生机构向包含慢性病患者在内的重点人群提供免费自愿的基本服务;根据《关于做好2023年基本公共卫生服务项目工作的通知》,目前人均服务补贴经费已增加至79元。
2014年,《中国居民慢性病与营养监测工作方案(试行)》指出,要掌握我国不同地区、不同年龄及不同性别居民慢阻W的患病或发病现况,并抽取125个点开展监测试点。
自此,慢呦市逐渐开始得到了国家的重视。
2017年,《慢阻肺分级诊疗技术方案》颁布,明确了其分级诊疗的重点任务和服务流程,慢阻肺成为第二批纳入分级诊疗的试点疾病;同年,《中国防治慢性病中长期规划(2017—2025年)》明确提出,提高40岁以上居民肺功能检测率、加强慢性呼吸系统疾病筛查干预、积极推进慢性呼吸系统疾病患者分级诊疗等策略措施,将慢阻肺的监测纳入居民慢性病与营养监测项目,开展慢阻肺及相关危险因素流行情况的常规监测;同年,在国家卫生计生委医政医管局和基层司的指导下,由中国健康促进与教育协会、国家呼吸临床研究中心、中日友好医院呼吸专科医联体、国家卫生计生委远程医疗培训管理中心主办、中国医师协会呼吸医师分会协办的〃幸福呼吸〃中国慢阻肺分级诊疗项目正式开展。
慢性阻塞性肺疾病的最新诊疗进展

慢性阻塞性肺疾病的最新诊疗进展慢性阻塞性肺疾病(简称慢阻肺)是一种常见的、可预防和治疗的慢性呼吸系统疾病,其特征为持续存在的呼吸道症状和气流受限。
随着医学研究的不断深入,慢阻肺的诊疗技术也在不断更新和发展。
一、诊断方法的改进过去,慢阻肺的诊断主要依赖于患者的症状、肺功能检查以及胸部X 光等检查手段。
然而,如今的诊断方法更加多样化和精准化。
1、高分辨率 CT 检查高分辨率 CT 能够更清晰地显示肺部的细微结构变化,对于早期慢阻肺的诊断以及评估疾病的严重程度具有重要意义。
它可以帮助医生发现小气道病变、肺气肿的分布范围等,为制定个性化的治疗方案提供更准确的依据。
2、生物标志物检测血液和痰液中的某些生物标志物,如 C 反应蛋白、白细胞介素-6 等,有助于判断炎症的程度和疾病的进展。
此外,呼出气体中的一氧化氮浓度检测也逐渐成为一种辅助诊断方法。
3、综合评估工具除了单纯的肺功能指标,现在更强调使用综合评估工具来全面评估患者的病情。
例如,BODE 指数(包括体重指数、气流阻塞程度、呼吸困难程度和运动能力)能够更准确地预测患者的预后和死亡风险。
二、治疗药物的新进展1、长效支气管扩张剂长效抗胆碱能药物和长效β₂受体激动剂的应用越来越广泛。
这些药物作用时间长,能够更有效地缓解症状,改善患者的生活质量。
而且,新型的长效支气管扩张剂具有更好的安全性和耐受性。
2、吸入糖皮质激素联合治疗对于症状严重、频繁急性加重的患者,吸入糖皮质激素与长效支气管扩张剂的联合治疗方案显示出了较好的疗效。
但需要注意的是,长期使用糖皮质激素可能会带来一些副作用,因此用药需要权衡利弊。
3、磷酸二酯酶-4 抑制剂这类药物可以通过抑制炎症细胞的活性来减轻炎症反应,对于某些特定类型的慢阻肺患者可能具有一定的治疗效果。
4、靶向药物治疗随着对慢阻肺发病机制的深入研究,一些靶向药物正在研发和临床试验阶段。
例如,针对特定炎症通路的药物有望为慢阻肺的治疗带来新的突破。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
慢性阻塞性肺疾病(COPD)慢性阻塞性肺疾病(chronic obstructive pulmoriary disease,COPD)是一组气流受限为特征的肺部疾病,气流受限不完全可逆,呈进行性发展,但是可以预防和治疗的疾病。
COPD主要累及肺部,但也可以引起肺外各器官的损害。
COPD是呼吸系统疾病中的常见病和多发病,患病率和病死率均居高不下。
1992年在我国北部和中部地区,对102230名农村成人进行了调查,COPD的患病率为3%。
近年来对我国7个地区20245名成年人进行调查,COPD的患病率占40岁以上人群的8.2%。
因肺功能进行性减退,严重影响患者的劳动力和生活质量。
COPD造成巨大的社会和经济负担,根据世界银行/世界卫生组织发表的研究,至2020年COPD将成为世界疾病经济负担的第五位。
【病因与发病机制】确切的病因不清楚。
但认为与肺部对香烟烟雾等有害气体或有害颗粒的异常炎症反应有关。
这些反应存在个体易感因素和环境因素的互相作用。
(一)吸烟为重要的发病因素,吸烟者慢性支气管炎的患病率比不吸烟者高2-8倍,烟龄越长,吸烟量越大,COPD患病率越高。
烟草中含焦油、尼古丁和氢氰酸等化学物质,如本章第一节所述香烟可损伤气道上皮细胞和纤毛运动,促使支气管黏液腺和杯状细胞增生肥大,黏液分泌增多,使气道净化能力下降。
还可使氧自由基产生增多,诱导中性粒细胞释放蛋白酶,破坏肺弹力纤维,诱发肺气肿形成。
(二)职业粉尘和化学物质接触职业粉尘及化学物质,如烟雾、变应原、工业废气及室内空气污染等,浓度过高或时间过长时,均可能产生与吸烟类似的COPD。
(三)空气污染大气中的有害气体如二氧化硫、二氧化氮、氯气等可损伤气道黏膜上皮,使纤毛清除功能下降,黏液分泌增加,为细菌感染增加条件。
(四)感染因素与慢性支气管炎类似,感染亦是COPD发生发展的重要因素之一。
(五)蛋白酶-抗蛋白酶失衡蛋白水解酶对组织有损伤、破坏作用;抗蛋白酶对弹性蛋白酶等多种蛋白酶具有抑制功能,其中a1-抗胰蛋白酶(a1-AT)是活性最强的一种。
蛋白酶增多或抗蛋白酶不足均可导致组织结构破坏产生肺气肿。
吸人有害气体、有害物质可以导致蛋白酶产生增多或活性增强,而抗蛋白酶产生减少或灭活加快;同时氧化应激、吸烟等危险因素也可以降低抗蛋白酶的活性。
先天性a1-抗胰蛋白酶缺乏,多见于北欧血统的个体,我国尚未见正式报道。
(六)氧化应激有许多研究表明COPD患者的氧化应激增加。
氧化物主要有超氧阴离子(O2-)、羟根(OH)、次氯酸(HClO)、H2O2和一氧化氮(NO)等。
氧化物可直接作用并破坏许多生化大分子如蛋白质、脂质和核酸等,导致细胞功能障碍或细胞死亡,还可以破坏细胞外基质;引起蛋白酶-抗蛋白酶失衡;促进炎症反应,如激活转录因子NF-κB,参与多种炎症因子的转录,如IL-8、TNF-а、NO诱导合成酶和环氧化物诱导酶等。
(七)炎症机制气道、肺实质及肺血管的慢性炎症是COPD的特征性改变,中性粒细胞、巨噬细胞、T 淋巴细胞等炎症细胞均参与了COPD发病过程。
中性粒细胞的活化和聚集是COPD炎症过程的一个重要环节,通过释放中性粒细胞弹性蛋白酶、中性粒细胞组织蛋白酶G、中性粒细胞蛋白酶3和基质金属蛋白酶引起慢性黏液高分泌状态并破坏肺实质。
(八)其他如自主神经功能失调、营养不良、气温变化等都有可能参与COPD的发生、发展。
COPD发病机制见图2-6-1。
【病理改变】COPD的病理改变主要表现为慢性支气管炎及肺气肿的病理变化。
支气管黏膜上皮细胞变性、坏死,溃疡形成。
纤毛倒伏、变短、不齐、粘连,部分脱落。
缓解期黏膜上皮修复、增生、鳞状上皮化生和肉芽肿形成。
杯状细胞数目增多肥大,分泌亢进,腔内分泌物储留。
基底膜变厚坏死。
支气管腺体增生肥大,腺体肥厚与支气管壁厚度比值常大于0.55-0.79(正常小于0.4)。
各级支气管壁均有多种炎症细胞浸润,以中性粒细胞、淋巴细胞为主。
急性发作期可见到大量中性粒细胞,严重者为化脓性炎症,黏膜充血、水肿、变性坏死和溃疡形成,基底部肉芽组织和机化纤维组织增生导致管腔狭窄。
炎症导致气管壁的损伤-修复过程反复发生,进而引起气管结构重塑、胶原含量增加及瘢痕形成,这些病理改变是COPD气流受限的主要病理基础之一。
肺气肿的病理改变可见肺过度膨胀,弹性减退。
外观灰白或苍白,表面可见多个大小不一的大疱。
镜检见肺泡壁变薄,肺泡腔扩大、破裂或形成大疱,血液供应减少,弹力纤维网破坏。
细支气管壁有炎症细胞浸润,管壁黏液腺及杯状细胞增生、肥大,纤毛上皮破损、纤毛减少。
有的管腔纤细狭窄或扭曲扩张,管腔内有痰液存留。
细支气管的血管内膜可增厚或管腔闭塞。
按累及肺小叶的部位,可将阻塞性肺气肿分为小叶中央型(图2-6-2),全小叶型(图2-6-3)及介于两者之间的混合型三类。
其中以小叶中央型为多见。
小叶中央型是由于终末细支气管或一级呼吸性细支气管炎症导致管腔狭窄,其远端的二级呼吸性细支气管呈囊状扩张,其特点是囊状扩张的呼吸性细支气管位于二级小叶的中央区。
全小叶型是呼吸性细支气管狭窄,引起所属终末肺组织,即肺泡管、肺泡囊及肺泡的扩张,其特点是气肿囊腔较小,遍布于肺小叶内。
有时两型同时存在一个肺内称混合型肺气肿。
多在小叶中央型基础上,并发小叶周边区肺组织膨胀。
【病理生理】在早期,一般反映大气道功能的检查如第一秒用力呼气容积(FEV1)、最大通气量、最大呼气中期流速多为正常,但有些患者小气道功能(直径小于2mm的气道)已发生异常。
随着病情加重,气道狭窄,阻力增加,常规通气功能检查可有不同程度异常。
缓解期大多恢复正常。
随疾病发展,气道阻力增加、气流受限成为不可逆性。
慢性支气管炎并发肺气肿时,视其严重程度可引起一系列病理生理改变。
早期病变局限于细小气道,仅闭合容积增大,反映肺组织弹性阻力及小气道阻力的动态肺顺应性降低。
病变累及大气道时,肺通气功能障碍,最大通气量降低。
随着病情的发展,肺组织弹性日益减退,肺泡持续扩大,回缩障碍,则残气量及残气量占肺总量的百分比增加。
肺气肿加重导致大量肺泡周围的毛细血管受膨胀肺泡的挤压而退化,致使肺毛细血管大量减少,肺泡间的血流量减少,此时肺泡虽有通气,但肺泡壁无血液灌流,导致生理无效腔气量增大;也有部分肺区虽有血液灌流,但肺泡通气不良,不能参与气体交换。
如此,肺泡及毛细血管大量丧失,弥散面积减少,产生通气与血流比例失调,导致换气功能发生障碍。
通气和换气功能障碍可引起缺氧和二氧化碳储留,发生不同程度的低氧血症和高碳酸血症,最终出现呼吸功能衰竭。
【临床表现】(一)症状起病缓慢、病程较长。
主要症状:1.慢性咳嗽随病程发展可终身不愈。
常晨间咳嗽明显,夜间有阵咳或排痰。
2.咳痰一般为白色黏液或浆液性泡沫性痰,偶可带血丝,清晨排痰较多。
急性发作期痰量增多,可有脓性痰。
3.气短或呼吸困难早期在劳力时出现,后逐渐加重,以致在日常活动甚至休息时也感到气短,是COPD的标志性症状。
4.喘息和胸闷部分患者特别是重度患者或急性加重时出现喘息。
5.其他晚期患者有体重下降,食欲减退等。
(二)体征早期体征可无异常,随疾病进展出现以下体征:1.视诊胸廓前后径增大,肋间隙增宽,剑突下胸骨下角增宽,称为桶状胸。
部分患者呼吸变浅,频率增快,严重者可有缩唇呼吸等;2.触诊双侧语颤减弱。
3.叩诊肺部过清音,心浊音界缩小,肺下界和肝浊音界下降。
4.听诊两肺呼吸音减弱,呼气延长,部分患者可闻及湿性啰音和(或)干性啰音。
【实验室检查】(一)肺功能检查是判断气流受限的主要客观指标,对COPD诊断、严重程度评价、疾病进展、预后及治疗反应等有重要意义。
1.第一秒用力呼气容积占用力肺活量百分比(FEV1/FVC)是评价气流受限的一项敏感指标。
第一秒用力呼气容积占预计值百分比(FEV1%预计值),是评估COPD严重程度的良好指标,其变异性小,易于操作。
吸入支气管舒张药后FEV1/FVC<70%及FEV1<80%预计值者,可确定为不能完全可逆的气流受限。
2.肺总量(TLC)、功能残气量(FRC)和残气量(RV)增高,肺活量(VC)减低,表明肺过度充气,有参考价值。
由于TLC增加不及RV增高程度明显,故RV/TLC增高。
3.一氧化碳弥散量(DLco)及DLco与肺泡通气量(VA)比值(DLco/VA)下降,该项指标对诊断有参考价值。
(二)胸部X线检查COPD早期胸片可无变化,以后可出那肺纹理增粗、紊乱等非特异性改变,也可出现肺气肿改变。
X线胸片改变对COPD诊断特异性不高,主要作为确定肺部并发症及与其他肺疾病鉴别之用。
(三)胸部CT检查CT检查不应作为COPD的常规检查。
高分辨CT,对有疑问病例的鉴别诊断有一定意义。
(四)血气检查对确定发生低氧血症、高碳酸血症、酸碱平衡失调以及判断呼吸衰竭的类型有重要价值。
(五)其他COPD合并细菌感染时,外周血白细胞增高,核左移。
痰培养可能查出病原菌;常见病原菌为肺炎链球菌、流感嗜血杆菌、卡他莫拉菌、肺炎克雷伯杆菌等。
【诊断与严重程度分级】主要根据吸烟等高危因素史、临床症状、体征及肺功能检查等综合分析确定。
不完全可逆的气流受限是COPD诊断的必备条件。
吸入支气管舒张药后FEV1/FVC<70%及FEV1<80%预计值可确定为不完全可逆性气流受限。
有少数患者并无咳嗽、咳痰症状,仅在肺功能检查时FEV1/FVC<70%,而FEV1≥80%预计值,在除外其他疾病后,亦可诊断为COPD。
根据FEV1/FVC、FEV1%预计值和症状可对COPD的严重程度做出分级(表2-6-1)。
COPD病程分期:急性加重期(慢性阻塞性肺疾病急性加重)指在疾病过程中,短期内咳嗽、咳痰、气短和(或)喘息加重,痰量增多,呈脓性或黏液脓性,可伴发热等症状,稳定期则指患者咳嗽、咳痰、气短等症状稳定或症状较轻。
【鉴别诊断】(一)支气管哮喘多在儿童或青少年期起病,以发作性喘息为特征,发作时两肺布满哮鸣音,常有家庭或个人过敏史,症状经治疗后可缓解或自行缓解。
哮喘的气流受限多为可逆性,其支气管舒张试验阳性。
某些患者可能存在慢性支气管炎合并支气管哮喘,在这种情况下,表现为气流受限不完全可逆,从而使两种疾病难以区分。
(二)支气管扩张有反复发作咳嗽、咳痰特点,常反复咯血。
合并感染时咯大量脓性痰。
查体常有肺部固定性湿性啰音。
部分胸部X片显示肺纹理粗乱或呈卷发状,高分辨CT可见支气管扩张改变。
(三)肺结核可有午后低热、乏力、盗汗等结核中毒症状,痰检可发现抗酸杆菌,胸部X线片检查可发现病灶。
(四)弥漫性泛细支气管炎大多数为男性非吸烟者,几乎所有患者均有慢性鼻窦炎;X胸片和高分辨率CT显示弥漫性小叶中央结节影和过度充气征,红霉素治疗有效。
(五)支气管肺癌刺激性咳嗽、咳痰,可有痰中带血,或原有慢性咳嗽,咳嗽性质发生改变,胸部X线片及CT可发现占位病变、阻塞性肺不张或阻塞性肺炎。
