纯化水(药典)
药典纯化水

中国药典纯化水标准纯化水在医药卫生行业作为一种应用最广泛的原辅料,由于其应用的普遍性与重要性,一直被《中国药典》所收载。
作为原辅料,根据其制备工艺及质量特征,经过不断的修改与论证,自药典出版起,均将硝酸盐检查列为必检项目之一。
中国药典[1]化学指标:符合中华人民共和国药典2010版制药纯化水要求卫生学检查:微生物10CFU/100ml内毒素0.25EU/ml电导率≤2μS/cm ( 电阻率≥0.5 M Ω*CM)本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
1,性状:本品为无色的澄清液体;无臭,无味。
2,检查酸碱度:取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3,硝酸盐:取本品5ml置试管中,于水浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml 相当于1ugNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000006%)。
4,亚硝酸盐:取本品10ml,置纳氏管中,对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml与盐酸萘乙二胺溶液(0.1→100)1ml,产生粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.75g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1ugNO2)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(0.000002%)。
5,氨:取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氨化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.00003%)。
纯化水质量标准、检查项目表及验证检测周期2019.10.29文件

在表中列出,采用线性内插法计算得到限度值,所测定的电导率值应不大于限度值。
表1温度和电导率的限度表
温度(℃)010导率
2.43.64.35.15.46.57.18.19.19.79.79.710.2 (μS/cm )
硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液
产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取
1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于
1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000
项目标准检测依据
性状无色澄清、无臭、无味
加甲基红指示液不显红色,加溴麝酸碱度
香草酚蓝指示液不显蓝色
硝酸盐≤0.000006%
亚硝酸盐≤0.000002%
氨≤0.00003%2015版
易氧化物粉红色不完全消失《中国药典》
不挥发物遗留残渣不得过1mg
重金属0.00001%
电导率
总有机碳≤0.5mg/L
微生物限度菌落总数≤100cfu/ml
易氧化物:取纯化水100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,
再煮沸10分钟,粉红色不得完全消失。
不挥发物:取纯化水100ml,置105℃恒重的蒸发皿中,在水浴上蒸干,并在105℃干燥
至恒重,遗留残渣不得过1mg。
重金属:取纯化水100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml
各国药典纯化水标准
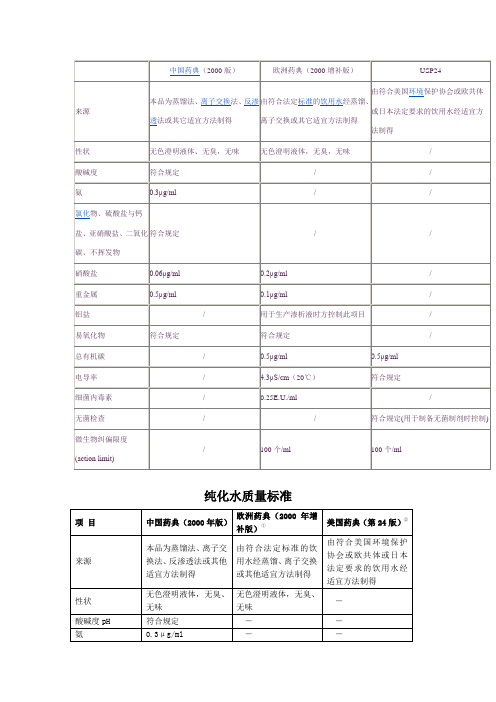
由符合美国环境保护协会或欧共体或日本法定要求的饮用水经适宜方法制得
性状
无色澄明液体,无臭、无味
无色澄明液体,无臭、无味
-
酸碱度pH
符合规定
-
-
氨
0.3μg/ml
-
-
氨化物、硫酸盐与钙盐、亚硝酸盐、不挥发物
符合规定
-
-
二氧化碳
符合规定
-
-
硝酸盐
0.06μg/ml
100个/ml
100个/ml
中国药典(2000版)
欧洲药典(2000增补版)Байду номын сангаас
USP24
来源
本品为蒸馏法、离子交换法、反渗透法或其它适宜方法制得
由符合法定标准的饮用水经蒸馏、离子交换或其它适宜方法制得
由符合美国环境保护协会或欧共体或日本法定要求的饮用水经适宜方法制得
性状
无色澄明液体、无臭,无味
无色澄明液体,无臭,无味
/
酸碱度
符合规定
/
/
氨
0.3μg/ml
/
/
氯化物、硫酸盐与钙盐、亚硝酸盐、二氧化碳、不挥发物
符合规定
/
/
硝酸盐
0.06μg/ml
0.2μg/ml
/
重金属
0.5μg/ml
0.1μg/ml
/
铝盐
/
用于生产渗析液时方控制此项目
/
易氧化物
符合规定
符合规定
/
总有机碳
/
0.5μg/ml
0.5μg/ml
电导率
/
4.3μS/cm(20℃)
中国药典2020版二部纯化水微生物检查

中国药典2020版二部纯化水微生物检查
【原创实用版】
目录
1.概述
2.纯化水的微生物检查标准
3.微生物检查的方法
4.微生物检查的注意事项
5.总结
正文
1.概述
在中国药典 2020 版二部中,对于纯化水的微生物检查有严格的标准和要求。
纯化水是制药过程中常用的一种水源,其微生物质量直接关系到药品的质量和安全性。
因此,对纯化水的微生物检查是药品生产质量管理的重要环节。
2.纯化水的微生物检查标准
根据中国药典 2020 版二部的规定,纯化水的微生物检查需要符合以下标准:
- 菌落总数:≤10cfu/ml
- 大肠埃希菌:不得检出
- 铜绿假单胞菌:不得检出
- 霉菌和酵母:≤1cfu/ml
3.微生物检查的方法
微生物检查通常采用以下方法:
- 菌落计数法:通过在培养基上培养,观察形成的菌落数来计算菌落总数。
- 试管法:将纯化水分别注入试管,然后在一定条件下培养,观察是否有微生物生长。
- 薄膜过滤法:将纯化水通过薄膜过滤器,然后将滤膜在培养基上培养,观察是否有微生物生长。
4.微生物检查的注意事项
在进行微生物检查时,需要注意以下几点:
- 采样:采样时应遵循无菌操作,避免污染。
- 培养条件:培养时应根据不同微生物的生长要求,设置合适的温度、湿度和时间。
- 结果判断:判断结果时应以菌落总数、大肠埃希菌、铜绿假单胞菌和霉菌酵母的检出情况为主要依据。
5.总结
中国药典 2020 版二部对纯化水的微生物检查有严格的标准和要求,微生物检查的方法有多种,但都需要遵循无菌操作和合适的培养条件。
纯化水水质各国药典标准

电导率
--
------
4.3μs/cm(20℃)
符合规定
细菌内毒素
--
-----
0.25E.U./ml
--
微生物限度
--
100cfu/ml
--
符合规定(用于制备无菌制剂时控制
微生物超标纠正标准
--
100个/ml
100个/ml
①、欧洲药典中总有机碳(TOC)和易氧化物项目,可任选一项监控。
②、美国药典中规定:a、企业自用的纯化水监测TOC和电导率。商业用的纯化水应符合无菌纯水的试验要求表中所列为企业自用纯化水的监测项目。b、纯化水不得用于制备肠外制剂。
③、微生物超标纠正标准是指微生物污染达到某一数值,表明纯化水系统已经偏离了正常运行的条件,应采取纠偏措施,使系统回到正常的运行状态。
性状
无色澄明液体、无臭、无味
无色澄明液体、无臭、无味
无色澄明液体,无臭、无味
--
酸碱度pH
符合规定(定性检测)
符合规定(定性检测)
--
--
氯化物、硫酸盐与钙盐、二氧化碳、
符合规定(定性检测)
符合规定(定性检测)
--
--
硝酸盐
0.06 mg/l
0.06 mg/l
0.2μg/ml
--
亚硝酸盐
0.02 mg/l
纯化水水质标准
项目
中国药典(2005年版)
中国药典(2010年版)
欧州药典(2012年版)
美国药典(第38版)
来源
本品为蒸馏法、离子交换法、反渗透法或其他适宜方法制得
本品为蒸馏法、离子交换法、反渗透法或其他适宜方法制得
由符合法定标准的饮用水经蒸馏离子交换或其他适宜方法制得
中国药典纯化水用途

中国药典纯化水用途
中国药典中规定的纯化水用途主要有以下几个:
1. 药品制造:纯化水在药品制造中是一个非常重要的原材料。
它被用来制备药物溶液、药物基质和药物载体等。
纯化水需要满足一定的纯度和微生物指标要求,以确保最终产品的质量和安全性。
2. 实验室研究:在科学研究和实验室中,纯化水用于制备实验溶液、培养基和其他实验需要的用水。
因为纯化水的纯度高,可以避免对实验结果的干扰。
3. 医疗卫生:纯化水在医疗卫生领域中用途广泛。
它被用于清洗和冲洗医疗器械、器皿和空间,以保持医疗环境的卫生和无菌。
此外,纯化水还可以作为医疗设备的冷却介质和洗涤剂。
4. 化妆品和个人护理产品制造:纯化水在化妆品和个人护理产品制造过程中广泛应用。
它可以用来制备产品配方中的溶液,调节产品的pH值,稀释和冲洗原料等。
总之,纯化水在制药、实验室、医疗卫生和化妆品制造等领域起着非常重要的作用。
纯化水标准(版中国药典)
纯化水【1】【试剂】10%氯化钾:取10g氯化钾溶加100ml水使溶解,即得。
稀硫酸:取硫酸57ml,加水稀释至1000ml,即得。
应含H2SO4 9.5%~10.5%甲基红指示剂:取甲基红0.1g,加0.05mol/L氢氧化钠溶液 5.3ml使溶解,再加水稀释至100ml,即得。
溴麝香草酚蓝指示剂:取溴麝香草酚蓝0.1g,加0.05mol/L氢氧化钠溶液3.2,ml使溶解,再加水稀释至200ml,即得。
0.1%二苯胺硫酸溶液:取0.1g二苯胺,加入100ml硫酸(98%)使之溶解,即得。
稀盐酸:取盐酸243ml,加水稀释至1000ml,即得。
应含HCl9.5%~10.5%高锰酸钾滴定液(0.02mol/L):取高锰酸钾3.2g,加水1000ml,煮沸15分钟,密塞,静置2天以上,用垂熔玻璃滤器过滤,摇匀。
高锰酸钾滴定液标定:准确称取于摄氏110度烘过两小时的草酸钠0.2g,置于烧杯中,加5%硫酸120ml,加热至80-90摄氏度,用高锰酸钾标准溶液滴至微红色(在1分钟内不消失)即为终点。
c=5m/v*0.0670式中c-高锰酸钾标准溶液的浓度(mol/L); m-称取草酸钠重量(g); v-滴定时消耗高锰酸钾溶液体积(ml);0.0670-Na2C2O4(草酸分子量)/2*1/1000。
本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭。
【检査】酸碱度取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50°C水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml ,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每lml相当于1μg NO 3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后纯化水的颜色比较,不得更深(0.000006%)。
纯化水注射用水质量标准
项 目
法定标准
企 业 内 控 标 准
《中华人民共和国药典》2010年版二部411页
性 状
应为无色的澄明液体,无臭,无味。
应为无色的澄明液体,无臭,无味。
检查
酸碱度
应符合规定
应符合规定
硝酸盐
不得过0.000006%
不得过0.000006%
亚硝酸盐
不得过0.000002%
不得过0.000002%
应为无色的澄明液体,无臭,无味。
检
查
pH
应为5.0~7.0
应为5.0~7.0
氨
不得过0.00002%
不得过0.00002%
硝酸盐
不得过0.000006%
不得过0.000006%
亚硝酸盐
不得过0.000002%
不得过0.000002%
电导率
应≤1.1µs/cm(20℃)
应≤1.0µs/cm(20℃)
总有机碳
不得过0.50mg/L
不得过0.50mg/L
不挥发物
遗留残渣不得过1mg
遗留残渣不得过1mg
重金属
不得过0.00001%
不得过0.00001%
细菌内毒素
应小于0.25EU/ml
应小于0.25EU/ml
微生物限度
细菌、霉菌和酵母菌总数每100ml不得过10个
细菌、霉菌和酵母菌总数每100ml不得过8个
细菌、霉菌和酵母菌应≤100CFU/ml
细菌、霉菌和酵母菌应≤80CFU/ml
细菌内毒素
---
应小于0.25EU/ml
备注:“总有机碳”和“易氧化物”两项任做一项。
注射用水质量标准
项 目
中国药典纯化水检验标准
中国药典纯化水检验标准一、酸碱度按照中国药典规定,纯化水的酸碱度应该符合以下要求:pH值在5.0-7.0之间,以保证其符合药典规定的范围。
测试酸碱度的样品应该在使用之前进行取样,并且使用酸碱度试纸进行检测。
二、硝酸盐硝酸盐是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的硝酸盐含量不得超过0.00005%。
测试硝酸盐的样品应该在使用之前进行取样,并且使用硝酸盐试纸进行检测。
三、亚硝酸盐亚硝酸盐也是纯化水中常见的污染物之一,其含量过高会对人体健康产生影响。
因此,中国药典规定纯化水中的亚硝酸盐含量不得超过0.00001%。
测试亚硝酸盐的样品应该在使用之前进行取样,并且使用亚硝酸盐试纸进行检测。
四、氨氨是一种有毒物质,其含量过高会对人体健康产生影响。
因此,中国药典规定纯化水中的氨含量不得超过0.00005%。
测试氨的样品应该在使用之前进行取样,并且使用氨试纸进行检测。
五、氯化物氯化物是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的氯化物含量不得超过0.001%。
测试氯化物的样品应该在使用之前进行取样,并且使用氯化物试纸进行检测。
六、硫酸盐硫酸盐是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的硫酸盐含量不得超过0.001%。
测试硫酸盐的样品应该在使用之前进行取样,并且使用硫酸盐试纸进行检测。
七、钙钙是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的钙含量不得超过0.002%。
测试钙的样品应该在使用之前进行取样,并且使用钙试纸进行检测。
八、镁镁是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的镁含量不得超过0.002%。
测试镁的样品应该在使用之前进行取样,并且使用镁试纸进行检测。
中国药典2020版二部纯化水微生物检查
中国药典2020版二部纯化水微生物检查摘要:I.引言- 介绍中国药典2020 版二部- 阐述纯化水微生物检查的重要性II.纯化水微生物检查的标准- 引用《中国药典》2020 年版二部中有关纯化水微生物检查的标准- 详细解析标准中的关键要点III.检查方法- 描述纯化水微生物检查的具体步骤- 介绍所需的实验材料和设备- 详细说明实验操作流程IV.结果处理与分析- 介绍如何处理和分析检查结果- 阐述如何根据检查结果判断纯化水是否合格V.结论- 总结纯化水微生物检查的关键要点- 强调实施纯化水微生物检查的重要性正文:引言中国药典2020 版二部对药品的生产、质量控制等方面做出了严格的规定。
其中,纯化水微生物检查是确保药品生产过程中水质安全的重要环节。
纯化水在药品生产中有着广泛的应用,如制药工艺中的溶剂、清洗剂等。
因此,对纯化水微生物进行检查,可以有效防止微生物污染,保证药品的质量和安全。
纯化水微生物检查的标准根据《中国药典》2020 年版二部,纯化水微生物检查的标准如下:1.检查项目:总细菌数、霉菌和酵母菌数、大肠埃希氏菌。
2.检查方法:采用薄膜过滤法,将纯化水样品过滤后,在适当的培养基上进行微生物培养。
3.检查频率:每批纯化水进行一次微生物检查。
4.合格标准:纯化水中总细菌数不得超过100CFU/mL,霉菌和酵母菌数不得超过10CFU/mL,大肠埃希氏菌不得检出。
检查方法纯化水微生物检查的具体步骤如下:1.取样:从纯化水储存和使用系统中分别取样。
2.过滤:采用薄膜过滤法,将样品过滤至滤膜上。
3.培养:将滤膜放入适当的培养基中,恒温培养一定时间。
4.计数:对培养后的菌落进行计数,并计算各项指标。
结果处理与分析1.对于检查结果,应按照《中国药典》2020 年版二部的要求进行判定。
2.若纯化水中的总细菌数、霉菌和酵母菌数或大肠埃希氏菌有一项不合格,则该批纯化水视为不合格。
3.根据检查结果,对纯化水进行处理,如重新制备、消毒等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3.培养条件:
培养温度(℃)
开始时间
结束时间
33.0
2018年__月__日
2018年__月__日
4.计算与结论:
原液
10-1
10-2
10-3
10-4
10ቤተ መጻሕፍቲ ባይዱ5
空白
结果
标准限量
结论判定
需氧菌总数
□CFU/mL
1#
□ 合格
□不合格
□ 实测
2#
检验:复核:共页第页
检验原始记录(续)
样品总编号:
检验日期
环境条件
温度:℃相对湿度:%气压:
参数检验
依据
《中国药典》2015版
需氧菌总数检测:
1.实验步骤:
取100mL待测水样经0.45μm孔径滤膜处理,取处理水样为原液,根据实验需求对待测水样进行稀释,混匀,过滤。吸取1mL处理液于无菌平皿内,每个稀释度做两个平皿,加入R2A琼脂培养基,33℃±1℃培养5d。
