稳定性试验箱URS
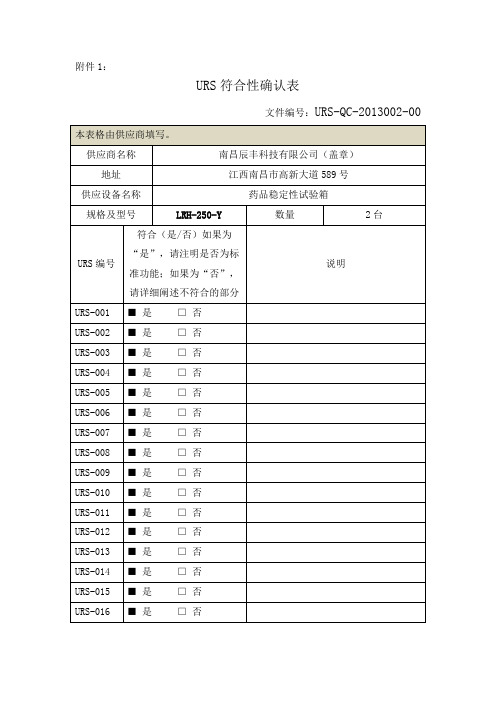
05 药品稳定性试验箱URS符合性确认表
附件1:
URS符合性确认表
文件编号:URS-QC-2013002-00
本表格由供应商填写。
供应商名称
南昌辰丰科技有限公司(盖章)
地址
江西南昌市高新大道589号
■是□否
URS-022
■是□否
URS-023
■是□否
URS-024
■是□否
URS-025
■是□否
URS-026
■是□否
URS-027
■是□否
URS-028
■是□否
URS-029
■是□否
URS-030
■是□否
URS-031
■是□否
URS-032
■是□否
URS-033
■是□否
URS-034
■是□否
URS-035
供应设备名称
药品稳定性试验箱
规格及型号
LRH-250-Y
数量
2台
URS编号
符合(是/否)如果为“是”,请注明是否为标准功能;如果为“否”,请详细阐述不符合的部分
说明
URS-001
■是□否
URS-002
■是□否
URS-003
■是□否
URS-004
■是□否
URS-005
■是□否
URS-006
■是□否
URS-007
■是□否
URS-008
■是□否
URS-009
■是□否
URS-是□否
URS-012
■是□否
URS-013
步入式稳定性试验箱URS

步入式稳定性试验箱用户需求说明User Requirement Specification文件编号:URS-2017-002版本2.0.0江苏药业有限公司审批REVIEW AND APPROV AL您的签名表明:您完全认可该用户需求标准中所有的技术要求,并确定这些技术要求符合相应的法规、工艺的要求。
目录1.目的32.标准33.缩略语34.设计要求45.安装要求46.质量控制47.控制系统48.EHS控制59.服务和维修510.包装及运输611.设备吊装712.验证和文件712.1.验证712.2.文件要求813.质保要求914.付款及发货条件101.目的药业A号楼二楼(南坝塘路1号A楼二层)设计和建造用于稳定性研究(温/湿度有效控制范围:温度10℃~60℃,湿度30%RH~90%RH)的步入式稳定性试验箱一间,有效体积为8~12m³。
供应商需要执行一系列的预先确定的、系统的工作,以使其设备供货、安装和服务满足本文件要求。
供应商同意此URS,将表明所有的要求应在其技术文件(报价)中体现。
本文旨在:●描述用户对步入式稳定性试验箱的要求;●为供应商提供设计所需要的信息;●在本项目中,供应商须提供全新的设计、构造、安装、验证、运行和维护的系统及设备,并能产出符合所有相关法规、药典要求的步入式稳定性试验箱;●系统及设备的设计、构造和安装须满足现场建筑物、安全和环境法规的执行要求。
本文为步入式稳定性试验箱的必须要求,但不限于此文件定义的内容。
本用户需求要求承包方提供步入式稳定性试验箱的设计、材料供应、施工安装、调试和4Q验证(DQ/IQ/OQ/PQ),并提供相应的文件。
2.标准《GB-T 10589-2008 低温实验箱技术条件》《药品生产质量管理规范》(2010年修订)(卫生部令第79号)《中国药典》(2015年版)四部9001 原料药与制剂稳定性试验指导原则ICH Guideline Q1C(R2)STABILITY TESTING OF NEW DRUG SUBSTANCES AND PRODUCTS3.缩略语DQ:Design Qualification设计确认IQ:Installation Qualification安装确认OQ:Operation Qualification运行确认PQ:Performance Qualification性能确认SAT:Site Acceptance Test现场验收FAT:Factory Acceptance Test工厂验收4.设计要求5.安装要求6.质量控制7.控制系统8.EHS控制9.服务和维修10.包装及运输11.设备吊装12.验证和文件12.1.验证12.2.文件要求供应商提供以下但不限于这些文件,作为供应包的一部分提供给用户,书面文件一式13.质保要求14.1、供应商认为URS需增加或更改内容,请供方提供书面说明或技术交流,供应商根据需要可以修改补充URS相关内容。
四箱式综合药品稳定性试验箱设备工艺原理

四箱式综合药品稳定性试验箱设备工艺原理引言稳定性试验是药物研发和药物生产的重要过程,目的在于评估药物在储存过程中的质量稳定性,以确保这些药物在其有效期内保持所需的药理活性和物理化学性质。
为了保证药物的质量控制,需要合适的稳定性试验箱来进行药品的稳定性测试。
本文将介绍四箱式综合药品稳定性试验箱设备工艺原理。
设备原理四箱式综合药品稳定性试验箱是一种模拟不同环境条件下药物质量变化的设备。
其主要原理是根据ICH稳定性试验指南Q1A(R2)和Q1B的规定,模拟稳定性试验条件,进行药物质量变化的评估。
四箱式综合药品稳定性试验箱由四个独立的箱体组成,包括高温高湿箱体、高温干燥箱体、低温干燥箱体和常温箱体。
这些箱体可以根据需要进行单独或同时操作,以模拟不同环境条件下的药物储存情况。
箱体内设有温度、湿度和压力控制系统,以确保箱内环境参数的准确控制。
此外,箱体内还设有容量不同的货架,以容纳不同规格的药品样品。
设备工艺流程四箱式综合药品稳定性试验箱工艺流程如下:1.样品装载:将要进行稳定性试验的药品样品装入不同规格的货架上。
2.环境设定:根据试验要求,设置箱内高温高湿、高温干燥、低温干燥和常温环境参数。
3.稳定性试验:将药品样品放入四箱式综合药品稳定性试验箱,并在箱内稳定性试验中评估药物质量的变化。
箱体根据设定的环境参数,模拟不同环境条件下药物质量变化。
4.数据记录:记录箱内环境参数和药品的质量变化数据。
5.结果分析:根据记录的数据,分析药物在不同环境条件下的质量变化情况,并进行结果报告。
箱体操作四箱式综合药品稳定性试验箱操作相对简单,主要包括以下几个方面:1.电源控制:开启并关闭试验箱的电源开关。
2.货架设置:根据药品样品的不同规格,设置相应的货架以放置样品。
3.环境参数设置:根据要求,设置不同的温度、湿度和压力参数。
4.稳定性试验操作:将要进行稳定性试验的药品样品装入箱体中,并设定试验时间。
注意事项四箱式综合药品稳定性试验箱在使用时需要注意以下几个事项:1.设备操作前需要根据药品试验要求正确设置箱体内的环境参数,以确保试验结果的准确性。
关于药品稳定性试验箱的正确选择

关于药品稳定性试验箱的正确选择通常客户用药品稳定性试验箱是为了完成如下几种实验:①新药研发;②药品留样(常见的温度在+25℃±2℃,湿度在60±5%RH);③样品低温保存试验(常见为5℃储存);④样品的加速实验(常见温度+40℃±2℃,湿度75±5%RH,光照条件:4500±500LX);⑤样品是出口还是内销(原料药出口的可能性更大哦)。
3、确定实验需要控制的三大参数要求①温度范围:药品稳定性试验箱从做的实验以及样品来考虑,一般不会需要太高的温度,通常我们看到的温度范围是0-65℃;当然如果药品稳定性试验箱是用来做加速实验需要带上光照功能的话,实验的温度范围则还会分为有光照10-50℃,无光照4-50℃;当然也会出现更宽泛的,但一般使用的温度就在这个温度范围之中,极少需要超出这个温度范围的;工程师在此提示您,产品选择合适的,而不是选择厂家给你的更宽泛的参数,看上去是优势,其实对你来说都一样哦~~②湿度范围:同样的,药品稳定性试验箱从做的实验以及样品来考虑,一般湿度范围在:40~95%RH,谚禾公司在此提醒大家,在我们选择药品箱之前,要了解自己实验过程中需要用到的温度是什么?在此温度下,要控制多少的湿度,不妨确定出几个常见的温湿度点,然后去选择合适自己使用的药品箱哦,这样既可以选择适合自己的,也可以节省成本。
③光照功能:确定自己的实验是否需要用到光照功能,如果不需要,当然只要选择控制温度和湿度的药品箱就行了;如果需要,让我们拿药品的加速实验做个参考,在药典中规定的加速稳定性实验的光照条件是4500±500LX,所以光照强度只要能做到这个参数;一般就没什么问题了,市面上的药品箱,带光照功能的,好一些的可以做到0~6000LX之间,误差可以做到500LX以下。
其余行业,一般都会有自己需要的参数,可以将这个参数提供给厂家,让厂家的人员帮助我们选型。
药物稳定性试验箱的参数特点是怎样的呢 试验箱操作规程

药物稳定性试验箱的参数特点是怎样的呢试验箱操作规程药物稳定性试验箱是具有恒温、恒湿功能的高精度试验室设备,广泛应用于各种药物、化工原材料、木材、建材的有效性及老化试验;以及霉菌、组织细胞、微生物、抗生药物稳定性试验箱是具有恒温、恒湿功能的高精度试验室设备,广泛应用于各种药物、化工原材料、木材、建材的有效性及老化试验;以及霉菌、组织细胞、微生物、抗生物的培育及其它生物工程、卫生防疫、制药、化工、食品、饮料、农业、畜牧,水产等科研部门、大专院校的理想之选的稳定性试验。
药物稳定性试验箱应用简介:药品稳定性试验箱用于制药业、医学、生物技术行业和全部包括生命科学的相关工业的潜心讨论。
25℃/60%RH湿度长期稳定性试验条件。
在试验中加快达到试验效果,是制药行业的稳定性试验系统领域,紧要模拟环境气候中温度、湿度、光照试验。
药物稳定性试验箱产品特点:1、智能培育箱掌控电路微电脑PID温度掌控器,控温精准明确牢靠,波动少。
2、大屏幕彩色显示屏同时显示时钟、温度,动态图标直观指示培育箱运行情形。
3、安全牢靠双重限温(±4℃及上限70℃)保护。
4、环保节能保温层接受硬质聚氨酯整体灌注,坚固耐用,高效节能。
5、自诊断功能故障自动诊断,故障代码直观指示。
6、预留RS485接口便利以后计算机查阅或自动打印记录温度历史数据或曲线。
7、时钟显示和定时功能便于察看培育时间,可设置0—9999分钟的定时时间。
8、精准明确的湿度掌控湿度检测精准明确到0.1%。
9、八级(强光)四级(弱级)光照每天24时段可编程掌控(也可简单设置成每天一、二、三段,操作更简单),模拟2000药典药物稳定性试验引导原则所需要的培育环境。
—专业分析仪器服务平台,试验室仪器设备交易网,仪器行业专业网络宣扬媒体。
相关热词:等离子清洗机,反应釜,旋转蒸发仪,高精度温湿度计,露点仪,高效液相色谱仪价格,霉菌试验箱,跌落试验台,离子色谱仪价格,噪声计,高压灭菌器,集菌仪,接地电阻测试仪型号,柱温箱,旋涡混合仪,电热套,场强仪万能材料试验机价格,洗瓶机,匀浆机,耐候试验箱,熔融指数仪,透射电子显微镜。
稳定性试验箱URS

稳定性试验箱用户需求说明编制:日期:审核:日期:批准:日期:目录1.目的 (2)2.范围 (2)3.缩写列表 (2)4.仪器标准 (2)5.仪器安装地点描述 (2)6.设计、施工范围 (2)7.用户及系统要求 (2)7.1URS01:检验能力和精度要求 (3)7.2URS03:电气要求 (4)7.3URS04:安全要求 (4)7.4URS05:自控系统要求 (5)7.5URS06:材质及配套附机要求 (6)7.6URS07:文件要求 (6)7.7URS08:对供应商的要求 (7)7.8URS09:服务与维修要求 (7)7.9 URS10:时间要求 (7)7.10URS11:其它要求 (8)7.11URS12:附件 (8)8.审批 (9)1.目的该旨在从项目和系统的角度阐述用户对稳定性试验箱的需求,主要包括相关法规符合度和用户的具体需求,这份是构建起项目和系统的文件体系的基础,同时也是该仪器设计、安装和效验的可接受标准的依据,未列出的具体要求,以最新相关版本的法律或行业标准为依据。
2.范围2.1用户需求(URS)及其附件是对稳定性试验箱的设计、生产、安装、检查和测试、文件、交付的说明和最低要求。
2.2该仪器的主要用途是:能够及时、有效、真实的记录药品稳定性试验过程。
4.缩写列表5.仪器标准仪器必须合以下标准、规范:4.1中国GMP 及其附录(2010版)4.2中国药典4.3安全标准所有电气仪器的电线和电缆必须依据ICE标准安全:达到国内相关标准及CE标准要求6.仪器安装地点描述该仪器准备安装在实验室内,温度18-26℃,湿度45-60%,周围无强烈振动,无强烈电磁场影响。
周围无高浓度粉尘及腐蚀性物质,无阳光直接照射或其它热源直接辐射。
7.设计、施工范围供应商的仪器设计开展和工作应完全符合本用户需求及其附件以及相关标准和规范。
7.1仪器供应商的设计内容和施工范围:◎该仪器的设计、辅助工器具的准备等;◎如有变更,必须严格按照变更控制进行;◎提供相关验证资料(包括认证需要的验证和确认文件);◎安装、调试;◎安装、调试所需要的所有配件、仪器和工具;◎操作、维护与维修、验证的培训;◎后续服务。
稳定性试验箱校验方案说明

稳定性试验箱校验方案说明一、校验目的二、校验内容1.温度控制功能的校验:利用温度标准计或者精密温度计,将温度控制点设置在试验箱内,记录温度梯度和控制精度,并与设备的标称温度进行比较。
2.湿度控制功能的校验:利用湿度计将湿度控制点设置在试验箱内,记录湿度变化和控制精度,并与设备的标称湿度进行比较。
3.温度均匀性的校验:在试验箱内不同位置放置多个温度探头,并记录各位置的温度变化,评估试验箱的温度均匀性。
4.湿度均匀性的校验:在试验箱内不同位置放置多个湿度探头,并记录各位置的湿度变化,评估试验箱的湿度均匀性。
5.其他功能校验:包括通风、振动、气压等功能的校验,根据设备的具体规格和性能要求进行验证。
三、校验方法1.温度和湿度控制功能的校验:利用标准温湿度计、计时器和数据采集系统,将温度和湿度控制点设置在试验箱内,并进行稳定性的控制;记录控制过程中的温度和湿度变化,并与标准值进行比较,评估设备的控制精度和稳定性。
2.温度和湿度均匀性的校验:在试验箱内不同位置放置多个温度和湿度探头,记录各位置的温度和湿度变化,并进行统计分析,评估试验箱的均匀性。
3.其他功能的校验:根据设备的具体功能要求,进行相应的测试和校验,例如通风功能可以使用风速计进行测量,振动功能可以采用振动仪进行检测,气压功能可以使用压力计进行验证。
四、校验结果评定1.温度和湿度控制功能的评定:根据国家相关标准和技术要求,对设备的控温和控湿精度进行评定,同时考虑设备的稳定性和可靠性。
2.温度和湿度均匀性的评定:通过对试验箱内不同位置的温度和湿度数据进行统计分析,评估设备的均匀性表现,并与相关标准进行比较。
3.其他功能的评定:根据设备的具体规格和性能要求,对其功能进行评定,包括通风、振动和气压等。
五、校验周期和记录1.校验周期:对于稳定性试验箱,建议每年进行一次全面的校验;对于高精度要求的设备,可以根据实际情况适当缩短校验周期。
2.校验记录:根据国家相关标准和技术要求,对校验过程进行详细记录,包括校验日期、校验人员、校验结果等信息,并保存至少五年以上。
稳定性试验箱URS

稳定性试验箱用户需求说明编制:日期:审核:日期:批准:日期:目录1.目的 (2)2.范围 (2)3.缩写列表 (2)4.仪器标准 (2)5.仪器安装地点描述 (2)6.设计、施工范围 (2)7.用户及系统要求 (2)7.1URS01:检验能力和精度要求 (3)7.2URS03:电气要求 (4)7.3URS04:安全要求 (4)7.4URS05:自控系统要求 (5)7.5URS06:材质及配套附机要求 (6)7.6URS07:文件要求 (6)7.7URS08:对供应商的要求 (7)7.8URS09:服务与维修要求 (7)7.9 URS10:时间要求 (7)7.10URS11:其它要求 (8)7.11URS12:附件 (8)8.审批 (9)1.目的该旨在从项目和系统的角度阐述用户对稳定性试验箱的需求,主要包括相关法规符合度和用户的具体需求,这份是构建起项目和系统的文件体系的基础,同时也是该仪器设计、安装和效验的可接受标准的依据,未列出的具体要求,以最新相关版本的法律或行业标准为依据。
2.范围2.1用户需求(URS)及其附件是对稳定性试验箱的设计、生产、安装、检查和测试、文件、交付的说明和最低要求。
2.2该仪器的主要用途是:能够及时、有效、真实的记录药品稳定性试验过程。
5.仪器标准仪器必须合以下标准、规范:4.1中国GMP 及其附录(2010版)4.2中国药典4.3安全标准所有电气仪器的电线和电缆必须依据ICE标准安全:达到国内相关标准及CE标准要求6.仪器安装地点描述该仪器准备安装在实验室内,温度18-26℃,湿度45-60%,周围无强烈振动,无强烈电磁场影响。
周围无高浓度粉尘及腐蚀性物质,无阳光直接照射或其它热源直接辐射。
7.设计、施工范围供应商的仪器设计开展和工作应完全符合本用户需求及其附件以及相关标准和规范。
7.1仪器供应商的设计内容和施工范围:◎该仪器的设计、辅助工器具的准备等;◎如有变更,必须严格按照变更控制进行;◎提供相关验证资料(包括认证需要的验证和确认文件);◎安装、调试;◎安装、调试所需要的所有配件、仪器和工具;◎操作、维护与维修、验证的培训;◎后续服务。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
稳定性试验箱用户需求说明
编制:日期:
审核:日期:
批准:日期:
目录
1.目的 (2)
2.范围 (2)
3.缩写列表 (2)
4.仪器标准 (2)
5.仪器安装地点描述 (2)
6.设计、施工范围 (2)
7.用户及系统要求 (2)
7.1URS01:检验能力和精度要求 (3)
7.2URS03:电气要求 (4)
7.3URS04:安全要求 (4)
7.4URS05:自控系统要求 (5)
7.5URS06:材质及配套附机要求 (6)
7.6URS07:文件要求 (6)
7.7URS08:对供应商的要求 (7)
7.8URS09:服务与维修要求 (7)
7.9 URS10:时间要求 (7)
7.10URS11:其它要求 (8)
7.11URS12:附件 (8)
8.审批 (9)
1.目的
该旨在从项目和系统的角度阐述用户对稳定性试验箱的需求,主要包括相关法规符合度和用户的具体需求,这份是构建起项目和系统的文件体系的基础,同时也是该仪器设计、安装和效验的可接受标准的依据,未列出的具体要求,以最新相关版本的法律或行业标准为依据。
2.范围
2.1用户需求(URS)及其附件是对稳定性试验箱的设计、生产、安装、检查和测试、文件、交付的说明和最低要求。
2.2该仪器的主要用途是:能够及时、有效、真实的记录药品稳定性试验过程。
4.缩写列表
5.仪器标准
仪器必须合以下标准、规范:
4.1中国GMP 及其附录(2010版)
4.2中国药典
4.3安全标准
所有电气仪器的电线和电缆必须依据ICE标准
安全:达到国内相关标准及CE标准要求
6.仪器安装地点描述
该仪器准备安装在实验室内,温度18-26℃,湿度45-60%,周围无强烈振动,无强烈电磁场影响。
周围无高浓度粉尘及腐蚀性物质,无阳光直接照射或其它热源直接辐射。
7.设计、施工范围
供应商的仪器设计开展和工作应完全符合本用户需求及其附件以及相关标准和规范。
7.1仪器供应商的设计内容和施工范围:
◎该仪器的设计、辅助工器具的准备等;
◎如有变更,必须严格按照变更控制进行;
◎提供相关验证资料(包括认证需要的验证和确认文件);
◎安装、调试;
◎安装、调试所需要的所有配件、仪器和工具;
◎操作、维护与维修、验证的培训;
◎后续服务。
8.用户及系统要求
编号要求内容必需/期望
URS9-1 仪器生产周期为自预付款到达供应商账户之日起三十个工作
日内。
必需
编号要求内容必需/期望URS11-1 供应商需对URS响应表详细填写。
必需
8.审批
用户需求(URS)审核备案表
附件1:供应商对URS响应表
注:1、如果符合要求,请在供应商响应栏填“是”并详细说明符合条件的理由;如果不符合要求,请在供应商响应栏填“否”,并在偏离说明栏详细阐述不符合部分的原因。
2、请在URS响应表上盖公章并寄回。
精品文档。
11欢迎下载
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求。
