化学必修一推断题汇编
完整word版,高一必修一化学期末推断题专练

專題推斷題解題技巧推斷題解題技巧:看其顏色,觀其狀態,察其變化。
1. 常見物質の顏色:多數氣體為無色,多數固體化合物為白色,多數溶液為無色。
2. 一些特殊物質の顏色:黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亞鐵)藍色:CuSO4•5H2O、Cu(OH)2、含Cu2+ 溶液、液態固態O2(淡藍色)紅色:Cu(亮紅色)、Fe2O3(紅棕色)、紅磷(暗紅色)黃色:硫磺(單質S)、含Fe3+の溶液(棕黃色)綠色:FeSO4•7H2O、含Fe2+の溶液(淺綠色)、堿式碳酸銅[Cu2(OH)2CO3]紫黑色:KMnO4無色氣體:N2、CO2、CO、O2、H2、CH4有色氣體:Cl2(黃綠色)、NO2(紅棕色)有刺激性氣味の氣體:NH3(此氣體可使濕潤pH試紙變藍色)、SO2、HCl有臭雞蛋氣味:H2S產生酸霧:HCl、HNO33. 常見一些變化の判斷:①白色沉澱且不溶於稀硝酸或酸の物質有:BaSO4、AgCl(就這兩種物質)②藍色沉澱:Cu(OH)2、CuCO3③紅褐色沉澱:Fe(OH)3Fe(OH)2為白色絮狀沉澱,在空氣中很快變成灰綠色沉澱,再變成Fe(OH)3紅褐色沉澱④沉澱能溶於酸並且有氣體(CO2)放出の:不溶の碳酸鹽。
例如CaCO3⑤沉澱能溶於酸但沒氣體放出の:不溶の堿。
例如Cu(OH)24. 燃燒時の主要現象①在氧氣中:硫——藍紫色火焰;鐵——火星四射;木炭——發白光。
②在空氣中:鎂帶——耀眼の白光;紅磷——“白煙”;硫、氫氣——淡藍色火焰;CO、CH4——藍色火焰5、酸和對應の酸性氧化物の聯繫:①酸性氧化物和酸都可跟堿反應生成鹽和水:CO2 + 2NaOH = Na2CO3 + H2O(H2CO3 + 2NaOH = Na2CO3 + 2H2O)SO2 + 2KOH = K2SO3 + H2OH2SO3 + 2KOH = K2SO3 + 2H2OSO3 + 2NaOH = Na2SO4 + H2OH2SO4 + 2NaOH = Na2SO4 + 2H2O②酸性氧化物跟水反應生成對應の酸:(各元素の化合價不變)CO2 + H2O = H2CO3 SO2 + H2O = H2SO3SO3 + H2O = H2SO4 N2O5 + H2O = 2HNO3(說明這些酸性氧化物氣體都能使濕潤pH試紙變紅色)6. 堿和對應の鹼性氧化物の聯繫:①鹼性氧化物和堿都可跟酸反應生成鹽和水:CuO + 2HCl = CuCl2 + H2OCu(OH)2 + 2HCl = CuCl2 + 2H2OCaO + 2HCl = CaCl2 + H2OCa(OH)2 + 2HCl = CaCl2 + 2H2O②鹼性氧化物跟水反應生成對應の堿:(生成の堿一定是可溶於水,否則不能發生此反應)K2O + H2O = 2KOH Na2O +H2O = 2NaOHBaO + H2O = Ba(OH)2 CaO + H2O = Ca(OH)2③不溶性堿加熱會分解出對應の氧化物和水:Mg(OH)2 MgO + H2O Cu(OH)2 CuO + H2O2Fe(OH)3 Fe2O3 + 3H2O 2Al(OH)3 Al2O3 + 3H2O1 某實驗室の廢液中,可能含有氯化鐵、氯化鈉、硫酸鈉、鹽酸、氫氧化鈉、硝酸鋇中の一種或幾種。
必修一无机化学推断题

必修一无机化学推断题1、由短周期元素组成的单质A 、B 、C 和甲、乙、丙、丁、戊五种化合物有下图所示转换关系,工业上电解熔融的甲可制取金属A 。
请回答: (1)写出下列物质的化学式:A 甲 。
(2)写出乙物质的溶液中通入过量CO 2的现象: ; (3)写出丁与过量氨水反应的离子方程式: 。
2、下图中A ~H 均为中学化学中常见的物质,它们之间有如下转化关系。
其中A 为金属单质,B 为非金属单质,A 与水反应生成C 和最轻的气体D ,C 的焰色反应呈黄色。
请回答以下问题:(1)C 的电子式为_____________。
(2)F 的化学式为_____________。
(3)写出某种金属与C 反应生成D 的化学方程式________________________。
(4)写出H 与G 的稀溶液反应生成F 的离子方程式________________________。
3、下图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。
已知:A 、C 、D 、F 均为单质,C 、E 、F 、G 常温下是气体,J 为白色沉淀,既能溶于B ,又能溶于E ;物质B 、G 可以使湿润的红色石蕊试纸变蓝,且B 的焰色反应呈黄色。
反应④是化肥工业的重要反应。
请回答下列问题:(1)A 的元素在元素周期表中的位置是 ,物质B 的电子式为 。
(2)上述反应①~⑥中,属于化合反应的是 。
(3)反应⑤的离子方程式为 。
(4)在I 的水溶液滴加B 溶液至过量的过程中,所观察到的现象为 。
通过量CO 2通过量NH 3C乙 NaOH 溶液A+B甲NaOH 溶液HCl 溶液乙丁丙戊4、已知A ~H 是中学化学中的常见物质,A 、C 、G 是金属,E 、F 是氧化物,B 溶于水得蓝色溶液,它们有如下图所示的关系(反应中生成的水已略去)。
试回答下列问题。
(1)推断填写物质化学式:A 是 ,D 是 ,H 是 。
高一化学推断题练习试题集

高一化学推断题练习试题答案及解析1.X、Y、Z三种短周期元素,两两之间能组成5种化合物A、B、C、D、E;X、Y、Z三种元素可组成化合物F。
已知:化合物A、B、C中原子个数比都为1︰1;B为淡黄色固体,C、E常温下均为无色液体;A是化学式为XZ的离子化合物,A与E反应生成F和一种气体;D是化学式为X2Y的离子化合物,D的阴、阳离子具有相同的电子层结构且与E分子所含电子数相等。
请回答下列问题:(1)X元素的名称是__________,它在周期表中的位置____________。
(2)X、Y、Z的原子半径从大到小的顺序是(用元素符号表示)____________________(3)写出F的电子式______________________________(4)已知X单质、A、B、D均为固体,分别与E反应都生成同一种物质,其中X单质、A、B分别与E的反应均是氧化还原反应。
请写出X单质、B分别与E反应的化学方程式__________________________________,;B中含有的化学键是;(5)请写出由化合物C制取Y的单质反应的化学方程式_______________________________。
【答案】(1)钠(1分)第三周期第I A族(2分)(2) Na>O>H (2分)【解析】由题可以知道X、Y、Z分别为Na、O、H,A、B、C、D、E分别为NaH、、、、,所以(1)X元素的名称是钠,在周期表中的位置为第三周期第I A族;(2)X、Y、Z的原子半径从大到小的顺序是Na>O>H ;(3)F为NaOH,其电子式为;(4)X单质、B分别与E反应的化学方程式为、,B为,其中含有的化学键是;(5)化合物C制取Y的单质反应的化学方程式为。
【考点】元素周期表点评:本题考查了元素周期表中部分元素的性质及其化合物,该题难度不大。
2.某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。
高一化学推断题练习试题集

高一化学推断题练习试题答案及解析1.(6分)已知:A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成食品包装材料。
(1)A的结构简式为。
(2)D分子中的官能团是,(3)写出下列反应的化学方程式②④【答案】(1)CH2=CH2(1分)(2)羧基或—COOH(1分)(3)②2H3CH2OH+O22H3CHO+2H2O(2分)④ nCH2=CH2。
(2分)【解析】根据题意可知A是乙烯CH2=CH2;B是乙醇CH3CH2OH;C是乙醛CH3CHO;D是乙酸CH3COOH,E是乙酸乙酯CH3COOCH2CH3;F是聚乙烯。
(1)A的结构简式为CH2=CH2;(2)D分子中的官能团是羧基或—COOH;(3)②反应的化学方程式是2H3CH2OH+O22H3CHO+2H2O;④反应的化学方程式是nCH2=CH2。
【考点】考查有机物的结构、性质、转化及方程式的书写的知识。
2.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
请回答下列问题:(1)写出下列物质的化学式:B_________、丙_________、乙_________。
(2)写出下列反应的离子方程式:反应①_____________________________________________;反应⑤_____________________________________________;反应⑥_____________________________________________。
【答案】(1)Al、HCl、Cl2(2)2Na+2H2O=2Na++2OH-+H2↑;Cl2+2Fe2+=2Fe3++2Cl-;Fe3++3OH-=Fe(OH)3↓【解析】金属A的焰色反应是黄色,说明A是Na。
钠和水反应生成氢氧化钠和氢气,则甲是氢气,D是氢氧化钠。
高中化学推断题100题
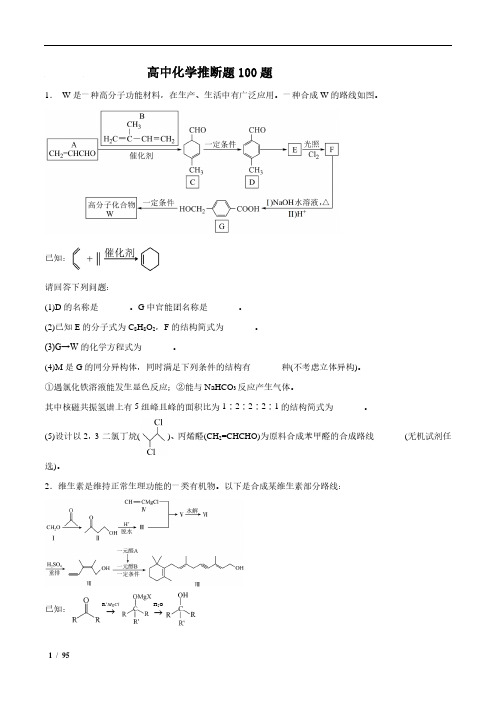
高中化学推断题100题1. W 是一种高分子功能材料,在生产、生活中有广泛应用。
一种合成W 的路线如图。
已知:请回答下列问题:(1)D 的名称是_______。
G 中官能团名称是_______。
(2)已知E 的分子式为C 8H 8O 2,F 的结构简式为_______。
(3)G→W 的化学方程式为_______。
(4)M 是G 的同分异构体,同时满足下列条件的结构有_______种(不考虑立体异构)。
①遇氯化铁溶液能发生显色反应;②能与NaHCO 3反应产生气体。
其中核磁共振氢谱上有5组峰且峰的面积比为1∶2∶2∶2∶1的结构简式为_______。
(5)设计以2,3-二氯丁烷()、丙烯醛(CH 2=CHCHO)为原料合成苯甲醛的合成路线_______(无机试剂任选)。
2.维生素是维持正常生理功能的一类有机物。
以下是合成某维生素部分路线:已知:R MgCl'→2H O→(1)化合物Ⅶ的分子式为________,该分子中处在同一平面的碳原子数为________。
(2)分析一元醛A 的结构特征,预测其可能的化学性质,完成下表 序号 结构特征 反应的试剂 反应形成的新结构 反应类型① -CHO Ag(NH 3)2OH _____ _____ ②_____________________(3)写出由化合物Ⅲ和Ⅳ反应生成化合物V 的方程式:________。
(4)化合物Ⅱ的同分异构体中能发生银镜反应但不能发生水解反应的共________种,其中核磁共振氢谱有3组峰,且峰面积比为6:1:1的同分异构结构简式为________。
(5)聚苯乙烯树脂是一种良好的保温材料,请以苯甲醛为原料,设计路线合成其单体苯乙烯____,其他试剂任选。
3.化合物H 是用于合成某种镇痛药的医药中间体,利用烃A 合成H 的某路线如下图所示:已知:Fe/HCl22R NO R NH ⎯−−⎯⎯→ 回答下列问题:(1)A 的化学名称为___________;D 中的官能团名称为___________。
化学必修一推断题

推断题1、已知甲、乙、丙为常见单质,A 、B 、C 、D 、X 、Y 、Z 为常见化合物,Y 的相对分子质量比Z 小16,乙与丙的相对分子质量相同,B 的相对分子质量比D 的小2,B 与X 的相对分子质量相同,各物质的转化关系如下图(反应条件已略去)(1)丙和B 的分子式分别为 和 。
(2)Y 转化为Z 的化学方程式 。
(3)B 与D 反应的化学方程式 。
2、下图中①~○11分别代表有关反应中的一种物质,请填写以下空白。
(1)①、③、④的化学式分别是______、______、______。
(2)⑧与⑨反应的化学方程式是______。
3、请写出A 、B 、C 的化学式:A B 、 、C 。
置于空气中NaOH 溶液B C (红褐色)ΔDE (白色)AACl 2NaOH 溶液盐酸4、下图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。
已知:A、C、D、F均为单质,C、E、F、G常温下是气体,J为白色沉淀,既能溶于B,又能溶于E;物质B、G可以使湿润的红色石蕊试纸变蓝,且B的焰色反应呈黄色。
反应④是化肥工业的重要反应。
请回答下列问题:⑴A的元素在元素周期表中的位置是▲,物质B的电子式为▲。
⑵上述反应①~⑥中,属于化合反应的是▲,反应⑤的离子方程式为▲。
⑶在I的水溶液滴加B溶液至过量的过程中,所观察到的现象为▲。
5、某些金属氧化物跟熔融烧碱反应可生成盐,根据图2化学反应方框图填空:(1)单质F是________;(2)写出由E生成G的离子方程式(或化学方程式)_______;(3)溶液I中所含金属离子是_____ ___;(4)由C E+F若改用浓酸,则不能选用的浓酸是(写分子式)________。
6、下图①~分别代表反应中的一种物质,请填空白:(1)①、③、④的化学式分别是 。
(2)⑧与⑨反应的化学方程式是_____ ___。
【课后作业】1.下列框图题中,已知A 、E 、F 、H 是单质,其中只有A 是固体,其它都是气体,且H 是呈黄绿色;B 是最常见液体,G 的焰色反应呈黄色,L 是白色沉淀,M 是红褐色沉淀。
高一化学推断题含答案(已整理分类,独一无二版本)
(一)元素推断题1、周期表前20号元素中,它们形成离子化合物时,原子数之比为1﹕2,且阴阳离子的电子层结构相同。
写出这些化合物的化学式__________________________________________ 。
2、A 、B 两元素,A 的原子序数为X,A 、B 所在周期的元素种类分别为m 和n ,若A 和B 同主族,当B 在A 的上一周期时,B的原子序数为__________________。
B 在A 的下一周期时,B 的原子序数为_____________。
3、A 、B 、C 、D 为短周期元素,A 和B 同周期相邻,A 和C 同主族相邻,ABC 三种元素的原子序数之和为31,D 元素与ABC 既不同周期又不同主族,请回答:(1)元素符号 A ________B _________C_________D____________ . (2)A 、B 、D 组成为D 4B 2A 3的离子化合物,其水溶液的PH 值小于7的原因是(3)比较B 、D 形成的化合物与A 、D 形成的阴离子结合质子能力强弱_______. 请用方程式表示_____________________________________________________________(4)用电子式表示D 2A 形成过程___________________________________________。
4.有A 、B 、C 、D 四种短周期的非金属元素(其单质也可分别用A 、B 、C 、D 表示),四种元素的原子序数按B 、D 、C 、A 顺序增大,D 、C 元素在周期表中位置相邻。
在一定条件下,B 可以分别和A 、C 、D 化合生成甲、乙、丙化合物,C 和D 化合可得丁。
已知乙、丙两个分子中各含有10个电子,并且甲、乙、丙、丁、戊有如下的变化关系:请填写下列空格:(1)甲的浓溶液与一种黑色粉末共热可得A ,则甲为_______,乙为___________。
高一化学推断题练习试题集
高一化学推断题练习试题答案及解析1.A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,D是具有果香气味的烃的衍生物。
A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
(1)工业上,由石油获得石蜡油的方法是______,由石蜡油获得A是___ __变化(“物理”或“化学”)。
(2)写出反应B+C→ D的化学方程式: _____________________________ __。
(3)丁烷是由石蜡油获得A的过程中的中间产物之一,写出它的两种同分异构体的结构简式:。
【答案】(1)分馏(或蒸馏)化学(2) CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O。
(3)正丁烷异丁烷(结构简式)【解析】据题意可知A为乙烯、B为乙醇、C为乙酸、D为乙酸乙酯。
从石蜡油里获得乙烯主要是通过石蜡油的裂解得到,所以是化学变化。
乙醇与乙酸在浓硫酸做催化剂的条件下,乙醇脱掉羟基中的氢,而乙酸脱掉羧基中的羟基,所以产物为乙酸乙酯和水。
同分异构体特点是分子式相同结构不同。
【考点】考查有机物合成的相关知识点。
2.(10分)下列框图中,已知A、E、F、H是单质,其中只有A是固体,其它都是气体,且H 是呈黄绿色;B是最常见液体,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。
部分反应的某些产物未标出。
(1)写出H的化学式:、C的电子式:。
(2)写出D与I溶液发生反应的离子方程式:。
(3)写出L→M的化学方程式:。
(4)检验J中的阳离子时,不宜选用下列试剂中的(填选项字母)。
A.Fe粉 B.NaOH溶液 C.KSCN溶液【答案】(1)Cl2(2)Fe3O4+ 8H+ = Fe2+ + 2Fe3+ + 4H2O(3)4Fe(OH)2 + O2+ 2H2O = 4Fe(OH)3(4)A【解析】根据题意可知A的Fe;B是H2O;D是Fe3O4;E是H2;H是Cl2;I是HCl;C是Na2O2;Na2O2与水反应得到G:NaOH和F:O2;Fe3O4与HCl发生反应得到FeCl2、FeCl3; FeCl2与Cl2发生反应得到FeCl3;FeCl3与Fe发生反应得到FeCl2.因此J是FeCl3;K是FeCl2。
高一化学推断题专项训练(附答案)
高一化学推断题专项训练一、推断题1.X、Y、D、E、F……都是中学化学中的常见物质,已知Y是单质,X是化合物,溶液E中滴入KSCN 溶液呈红色。
这些物质间的相互关系如框图所示,根据框图及提示的信息回答下列问题:1.Y和X的浓溶液反应的条件是___________,若无该条件,反应将很难进行,其原因是______________________。
2.写出F→G+X的离子方程式________________________。
3.L转化为I的化学方程式是_________________________。
4.在试管中制备L,为了能观察到L的颜色,需要进行特殊的操作,该特殊的操作是____________________________。
5.将Cu放入0.1mol·L-1 Fe(NO3)3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为________。
2.已知X、Y为有刺激性气味的气体,有以下转化关系,部分产物未标出。
试回答:1.写出下列物质的化学式X________、Y________、A________、B________、C________。
2.反应①的化学方程式为__________,反应②的离子方程式为__________。
3、下图表示几种物质间的转化关系(部分物质已略去),其中A、C为无色气体。
1.化合物W可能是或,C是,F是。
2.反应①中若消耗7.8gNa 2O 2,则转移的电子数为。
3.反应③的离子方程式: 。
4.A与CuO在加热条件下能发生反应生成N 2和Cu,请写出该反应的化学方程式:4.图中每一个方格表示相关的一种反应物或生成物,其中B是一种单质,其余物质都是含B元素的化合物。
C是一种钠盐,E是C对应的酸,B的结构类似于金刚石,D是B的氧化物(其他不含B元素的生成物、各步反应添加的必要试剂和反应条件已略去)。
元素推断题题目大全高中
元素推断题题目大全高中1. 推断该元素是碱金属还是碱土金属2. 推断该元素的周期3. 推断该元素在同一周期中的布居规律4. 推断该元素的电子亲和能力5. 推断该元素的电离能力6. 推断该元素的电负性7. 推断该元素的原子半径8. 推断该元素的离子半径9. 推断该元素是单质还是化合物10. 推断该元素在自然界中的存在形式11. 推断该元素的合成方法12. 推断该元素的物理性质13. 推断该元素的化学性质14. 推断该元素的氧化态范围15. 推断该元素的反应活性16. 推断该元素的应用领域17. 推断该元素对人体的影响18. 推断该元素的放射性质19. 推断该元素在核反应中的应用20. 推断该元素的稳定性。
1. 推断该元素是碱金属还是碱土金属这个推断可以根据该元素所在的周期表位置进行判断。
如果在第一和第二周期,这个元素很可能是碱金属;如果在第三到第八周期,这个元素可能是碱土金属或其他元素。
如果推断不出来,可以进一步查找该元素物理化学特征。
2. 推断该元素的周期这个推断可以根据该元素的原子序数进行判断。
每个元素原子序数都唯一,按顺序排列即为周期,可以通过周期表示或周期表来进行确认。
3. 推断该元素在同一周期中的布居规律元素在同一周期中的电子数相同,通常遵循A型布局规律,即元素的外层电子排布规律为$s^1$、$s^2p^1$、$s^2p^2$、$s^2p^3$、$s^2p^4$、$s^2p^5$和$s^2p^6$。
该元素的布局规律可以根据其所处的周期表序数来推断。
4. 推断该元素的电子亲和能力电子亲和能力指的是原子能够吸收电子形成阴离子的程度。
如果原子能够轻松地接受电子,那么它的电子亲和能力就会比较高。
可以通过该元素的电子结构、化学成分、原子数和元素周期来推断该元素的电子亲和能力。
5. 推断该元素的电离能力电离能力指的是从原子中脱离电子所需的能量。
如果原子的电离能力很高,说明它的化学反应比较不活泼;如果电离能力很低,说明它的化学反应比较活泼。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
推断题一、解无机推断题的解题思路无机推断题的一般解题思路是:迅速浏览整体扫描产生印象寻找突破口注意联系大胆假设全面分析(正推或逆推)验证确认。
解题的关键是仔细审题,依物质的特性或转化特征来确定“突破口...”,顺藤摸瓜,进而完成全部未知物的推断。
一般而言,推断题的思维方法可分四种:一是顺向思维,从已有条件一步步推出未知信息;第二种是逆向思维,从问题往条件上推,作假设;第三种则是从自己找到的突破口进行发散推导。
第四种考生还可同时找到几个突破口,从几条解题线索着手,配合推断。
第五虽然没有明显突破口,但其性质或转化关系像某种物质,这时应大胆假设,带入验证。
推断题最后都要代入检验....其准确性。
二、无机框图题的应对策略及解题方法1.夯实基础:框图题重点考察元素及化合物知识,一般基于中学阶段常见物质与反应,故要熟练掌握一些代表性物质的基本性质:如色、态、味、化学性质等。
同时框图题设计的问题通常围绕化学基本用语,周期表,物质结构等化学基本知识,因此注重基础是求解推断题的前提,避免出现推得出而写不出的现象。
2.抓住特性:所谓抓物质特性,就是在中学化学知识范围内,根据某些物质特有的性质来判断其存在与否的一种方法。
值得一提的是,为了验证结论的正确性,须对结论进行严密的论证和检验,这样才能确保万无一失。
我们可以从以下几个典型特性入手:2.1抓特殊现象:例如,气体燃烧呈苍白色火焰的必为H2和Cl2;向一溶液中滴入碱液,先产生白色沉淀,进而变成灰绿色,最后变为红褐色沉淀,则该溶液中一定含Fe2+;遇空气迅速由无色变为红棕色的气体必为NO等等;使湿红石蕊试纸变蓝的气体为NH3等等。
2.2抓特征反应:考例1已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。
元素X、Y、Z的原子序数依次递增。
②X在A、B、C、D中都不呈现它的最高化合价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是,Z是。
(2)写出③中反应的化学方程式:。
(3)写出④中反应的化学方程式:。
小结:平时要有意识的对一些特征反应进行总结1.与碱反应的常见单质:Al、Si、X2(Cl2、Br2、I2)、S。
2.两种化合物反应可生成一种金属单质的反应通常为:CO与金属氧化物的反应。
3.一种分解生成三种物质的反应物通常为:NaHCO3、NH4HCO3、(NH4)2CO3、KMnO4、HNO3。
2.3抓特征数据:考例2已知甲、乙、丙为常见单质,A、B、C、D、X、Y、Z为常见化合物,Y的相对分子质量比Z小16,乙与丙的相对分子质量相同,B的相对分子质量比D的小2,B与X的相对分子质量相同,各物质的转化关系如下图(反应条件已略去)(1)丙和B的分子式分别为和。
(2)Y转化为Z的化学方程式。
(3)B与D反应的化学方程式。
【小结】平时要记住一些特征数据,如式量差16通常为一个氧原子,式量为100的通常有CaCO3,KHCO3 ,Mg3N2等。
有10个电子的微粒常有CH4,NH3,H2O,HF,Ne,NH4+,H3O+,OH-,Na+,Mg2+,Al3+等。
除了以上特征外,我们还可以从寻找特征的反应条件,框图中高频出现的物质,特殊的化学式等作为入题口,进行推断。
3.化整为零:考例3下图中①~○11分别代表有关反应中的一种物质,请填写以下空白。
(1)①、③、④的化学式分别是______、______、______。
(2)⑧与⑨反应的化学方程式是______。
解析:粗读题目,将整块网络图看在眼里,难免被11个数码搞得心慌意乱。
细读题目,要清醒地看到④、⑥、⑦、②的重复出现。
把整块框图画分成Ⅰ→Ⅳ小块,如图所示:第Ⅰ块中,Na2O2是个突破口,能与Na2O2反应的气体应该是CO2,由此估计②可能是CO2,④可能是O2。
由①加热得气体混合物,该气体混合物通过浓硫酸后,得到气体②,可认为①为碳酸铵或碳酸氢铵(中学学过的物质受热得到气体混合物的,当属这两种盐)。
第Ⅱ块中,气体混合物通过碱石灰后,CO2和H2O均被除去,③应为NH3,③与④在催化剂、高温条件下,生成⑥和的反应为⑥与④反应,生成⑦,反应为:2NO+O2=====2NO2由此可知⑥为NO,⑦为NO2,为H2O。
⑦与反应生成⑥和⑧,应该是3NO2+H2O=2HNO3+NO,由此可知⑧为HNO3。
第Ⅲ块中,⑧与⑨反应,生成⑦、②和,只有⑨是未知的,HNO3与什么物质反应能生成NO2,CO2和H2O呢?显然⑨应该是碳。
第Ⅳ块中,②与Mg条在点燃条件下反应生成⑨和⑩,可确定⑨为碳(发生的反应当然,也可以按Ⅰ、Ⅳ、Ⅱ、Ⅲ块的顺序思考。
本题使用了11种物质,用了11个序号,涉及9步反应(或操作),组成了元素化合物的框图题,考查四种主族元素的典型反应之间的相互关系及相关的化学用语。
此题还反映出考生在正确书写指定物的化学式方面的缺陷,由于“NH 4+”与“NH 3”不分、“NH 3”与“NH 3·H 2O ”不分,把本应该得到的分数丢失了。
由此我们得到启示,要走出元素化合物框图的误区,就要熟练掌握重要元素的单质及化合物的典型反应,正确书写反应的化学方程式、离子方程式,做到知识存储有序,便于迅速准确提取。
4.转变思维:对某些框图题,可根据题给条件,采用“顺藤摸瓜”的思维方法,步步推断,从而直截了当,快速突破。
对某些框图题,可根据题给条件,采用逆向思维的方法,反向分析推断,从而打破常规,巧妙突破。
考例4 A .B .C .D 四种有机物,在一定条件下有如下转化关系:反应① 反应 ② 反应③已知D 的分子式为C 4H 8O 2,试推断A 、B 、C 、D 各是什么物质。
(写结构简式) A B C D 完成下列反应方程式反应①反应 ② (2)某金属A 及其化合物之间有如下的转化关系:请写出A 、B 、C 的化学式:A B 、 、C 。
5.相信自己:置于空气中NaOH 溶液B C (红褐色)ΔDE (白色)AACl 2NaOH 溶液盐酸对某些框图题,按照关系推出物质时,考生会发现某些物质书本上并未提及,是新物质,这时考生在确定其它转化并无毛病时,自己要相信自己的结论。
万一不能把整个题目都推导出来,也别丢弃了少数题空。
考例5下图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。
已知:A、C、D、F均为单质,C、E、F、G常温下是气体,J为白色沉淀,既能溶于B,又能溶于E;物质B、G可以使湿润的红色石蕊试纸变蓝,且B的焰色反应呈黄色。
反应④是化肥工业的重要反应。
请回答下列问题:⑴A的元素在元素周期表中的位置是▲,物质B的电子式为▲。
⑵上述反应①~⑥中,属于化合反应的是▲,反应⑤的离子方程式为▲。
⑶在I的水溶液滴加B溶液至过量的过程中,所观察到的现象为▲。
解析:考生对自己的推断可能不确定,但可以先假定,再验证,因此要保持一定的自信。
6.认真答题:推出结果,不忘检验。
通过一系列思维活动推断出结果后,必须将结果放人原题检验,完全符合为正确,如有一处不符,说明有错误,则再思考。
在答题时必须注意:①答名称,还是答符号、化学式;②答离子方程式,还是化学方程式;③答现象,还是答结论;④答规律,还是答具体物质或具体内容。
解析与答案:考例1解析:此题虽然不是框图推断,但考查了学生分析推理能力。
我们可以从A单质与某种常见一元强碱溶液反应,由此可推断A可能是Cl2;再由特征反应:化合物D受热催化分解,可制得元素Y的单质,可知Y的单质为O2,D为KClO3。
根据X元素有多种价态且元素Y、X、Z的原子序数依次递增,可知Y为O,X为Cl,Z为K。
答案:(1)Cl(氯),K(钾)(2)2KOH+Cl2====KCl+ KClO+H2O(3)考例2解析:甲、乙、丙为常见单质,且乙与丙的相对分子质量相同,Y的相对分子质量比Z小16,即Z比Y 多一个氧原子。
再根据甲转为A,A转为B和乙转为C,C转为D都要与丙反应,应该能判断出这两个过程为两步氧化,初步推断丙为O2,乙为S,C为SO2,D为SO3,A、B均为氧化物。
又根据C与A反应生成Y,即与SO2与A反应生成Y,则A为碱性氧化物,可知甲为金属钠,A为Na2O,X为Na2S。
答案:(1)O2,Na2O2 (2)2Na2SO3+ O2====2Na2SO4(3)2SO3+ 2Na2O2====2Na2SO4+ O2考例3答案:(1)①为NH4HCO3[或(NH4)2CO3],③为NH3,④为O2(2)C+4HNO3=2H2O+4NO2↑+CO2↑考例4(1)A、CH3CH2OH C、CH3COOH D、CH3COOCH2CH3 (2)A、Fe B、FeCl3 C、Fe(OH)3考例5答案:⑴第三周期、ⅠA族Na+[ O H]-⑵④ Al3++3NH3·H2O=Al(OH)3↓+3NH4+ ⑶有白色沉淀产生,后渐渐溶解至消失三、无机框图题的应对策略及解题方法1.顺推法:顺推是根据题设条件和转化关系方框图,从最初反应物入手,利用给定反应物的结构和性质特点,顺着转化关系往后推,从而解决问题。
例1.图1每一方框中的字母代表一种反应物或生成物:附表各物质的量C D I起始组成/mol 640某时刻组成/mol 332物质A跟B反应生成物E、F和G,物质C跟D反应生成物质I,某温下该反应起始和某时刻的反应混合物组成如附表所示。
请填写下列空白:⑴物质H的分子式____ ___;⑵反应①的化学方程式__ _____;⑶反应②的化学方程式(须注明反应条件)是____ ____。
2.逆推法:有的推断题,最初条件意义并不明确,但某一结果有较明确的含义,求解时,从这一结果入手,采用逆推模式,逆向逐层推理,可顺利达到解决问题的目的。
例2.某些金属氧化物跟熔融烧碱反应可生成盐,根据图2化学反应方框图填空:(1)单质F是________;(2)写出由E生成G的离子方程式(或化学方程式)_______;(3)溶液I中所含金属离子是_____ ___;(4)由C E+F若改用浓酸,则不能选用的浓酸是(写分子式)________。
3.假想验证法:假设思维模式是由题设条件和转化关系图找出题目突破口,并对有关内容建立假设,再将假设结果代入题中验证分析,由此可使问题得以解决。
例3.下图①~分别代表反应中的一种物质,请填空白:(1)①、③、④的化学式分别是。
(2)⑧与⑨反应的化学方程式是_____ ___。
四、基础知识梳理1、物理性质a.两性物质: Al (OH )3、Al 2O 3b.单质:Al○12物质转化关系的特殊性。
无机物之间有一些重要的衍变关系,在物质之间按照一定规律反应时,会形成一定的特征的转化关系:a.直线型转化:两次被氧化 (物质的相对分子质量增加16)323222HNO NO NO NH OH O O −−→−−→−−→−(气体) 金属、非金属的变化规律:b.交叉型转化:c.三角形转化:○13产生白烟的化学反应:NH 3+HCl==NH 4Cl 。
