第三节 电解池
人教化学选修4第四章第3节 电解池(共28张PPT)

二、电解原理的应用
应用一:氯碱工业即电解饱和食盐水
阳极:2Cl- 阴极:2H+ +
2e-= Cl2如↑ 何检验两极产物? 2e- = H2↑
总反应:
电解
2NaCl + 2H2O==
CC
存在问题: 2NaOH + H2↑+ Cl22↑
H2+ Cl2=2HCl爆炸 氯气溶于水与水反应 氯气与NaOH反应产物不纯更纯
AgNO3溶液
当阳极金属与电解质溶液中的金属 阳离子相同,则为电镀
例:在50mL 0.2mol/L的硫酸铜溶液中插入两个
电极,通电电解(不考虑水分蒸发),则:
⑴若两极均为铜片,试说明电解过程中溶液
溶质浓度将怎样变化 不变
。
⑵若阳极为纯锌,阴极为铜片,阳极反应式
是 Zn -2e-=Zn2+
⑶如果两极均为铜片且不考虑H+在阴极上放电,
3、构成电解池的条件: ① 直流电源;
② 阴、阳电极
③ 电解质溶液或熔融电解质; ④ 形成闭合回路。
⑤非自发进行的氧化还原反应
原电池与电解池的比较
比较内容
原电池
电解池
装置举例 铜锌原电池
电解氯化铜
电极名称 正极、负极
阴极、阳极
电极反应 负极氧化反应 正极还原反应
能量转变 将化学能转变成电能
阳极氧化反应 阴极还原反应
实质:电解水
溶液pH变化: 增大 溶液复原方法:加入H2O
1、复习提问:
电极名称_阴__极____ C
反应类型_还__原____
C 电极名称__阳__极___
反应类型__氧__化___
电极反应_Cu_2+ _+_2e_- _= C_u 实验现象_红_色__固__体_
选修四第四章第三节电解池(52张)

四、电解电极反应式的书写
电解溶质型
HCl溶液
阳极:2Cl- - 2e- = Cl2↑
阴极:2H++2e- = H2↑
总反应:2HCl
通电
===
H2
↑
+Cl2
↑
通电
2H++2Cl- === H2 ↑ +Cl2 ↑
电解水型 阳极:4OH- - 4e- = 2H2O + O2 ↑
阴极:4H+ + 4e- = 2H2 ↑
电解溶质和水 放氧生酸型
阳极:4OH- - 4e- = 2H2O + O2 ↑ 阴极: Cu 2++ 2e -= Cu
总反应:
通电
CuSO4溶液
22CCuuS2+O+24+H22HO2O=通=电====4H2+H+O2 2S↑O+42+COu2 ↑+2Cu
电解质溶液用惰性电极电解的示例:
电解
举例
2.原理 (1)通电前: Cu2+、Cl-、H+、OH-自由移动 通电后: 定向移动
(2)电极上的反应
阴极: Cu2+ + 2e- = Cu (还原反应)
阳极: 2Cl--2e- =Cl2↑(氧化反应)
总反应: Cu2+ + 2Cl-电解
电解
Cu
+Cl2↑
CuCl2 Cu +Cl2↑
放电
粒子在电极上失去或获得电子发生氧化还原反应的过程。
类型 物质类别 实例
电极反应
溶液pH 溶液复 变化 原方法
含氧酸
仅溶剂 强碱 水电解
选修4第四章第三节电解池

想一想、做一做
[例]以石墨棒为电极,请写出分别电解下列溶液时,在 阴、阳两极上发生的电极反应式及总的化学方程式。 (1)NaCl溶液: 阳极:2Cl--2e-=Cl2↑ 阴极:2H++2e-=H2↑ (2H2O 总反应:2Cl-+2H
2H++2OH-)
O = Cl2↑+H2↑+2OH2
电解
(2)CuSO4溶液: OH-在哪一极产生? 阳极:4OH--4e-=2H2O+O2↑ (4H2O 4H++4OH-) 2+ +4e-=2Cu 阴极:2Cu
2、电解无氧酸溶液(氢氟酸除外)、不活泼金属的 无氧酸盐溶液,如电解盐酸、CuCl2溶液等 电解盐酸 阳极: 2Cl -- 2e-=Cl2↑ 阴极: 2H+ +2e-= H2 ↑
总反应:2HCl = Cl2↑ + H2↑ 类型:电解电解质型 实质:电解质本身被电解 电解后溶液中溶质的质量分数 减小 ,若要恢复 原来的组成和浓度,需加入一定量的 溶质 (通入一 定量的HCl气体)
活性金属 > S2->I->Br->Cl->OH->含氧酸根>F-
除Pt、Au
电极反应:
阳极: 2Cl- - 2e- = Cl2↑
(氧化反应)
阴极
Cu -
-- + e +
阳极
eoooo oooo oooo oooo oooo oooooooooooo ooooooooooo
阴极: Cu2+ + 2e- = Cu
4、根据金属活动顺序表,Cu不能发生如下反应:
Cu + 2H2O=Cu(OH)2↓+ H2↑。但选择恰当电极材料
第三节电解池课件精修ppt
3.两极都用银片作电极电解AgNO3时,阳极的产
物是 Ag+;阴极的产物是 Ag 。
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
4.试写出下列装置中所发生的电极反应式。
石墨
石墨 粗铜
纯铜 纯铜
铁
CuSO4溶液 (A)
②若阳极是惰性电极,还原性强的阴离子在阳极放电,
阴极材料不发生任何变化。
阴离子放电(失电子)顺序:
S2–>I–>Br–>Cl– > OH– > (NO3-、SO42– 等)含氧
酸根离子>F-
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
3、电冶金(使用电解法冶炼像钠、镁、铝等活泼金属的
方法)
制取金属铝
电解熔融状态的氧化铝。
阳极:6O 2- -12e- == 3O2↑
阴极: 4Al 3+ + 12e- == 4Al
总反应:2Al2O3(熔融)
通电
冰晶石
4Al + 3O2 ↑
助熔剂:冰晶石(Na3AlF6 六氟合铝酸钠)
阳极材料(碳)和熔融氧化铝需要定期补充
操作步骤: 1.在烧杯中注入CuCl2溶液 2.连接电极,将两根石墨棒插入溶液中 3.接通直流电源,在烧杯上方放一个湿润的
淀粉KI试纸,观察阴极和阳极的实验现象 并记录。
注意: 1.在实验过程中,两电极要始终放在溶液中,
且两电极不能接触; 2.电压要调至6V; 3.实验结束,关闭电源,将导线从电源上取下。
高中化学选修四电解池知识点

第三节电解池一、电解原理1、电解池:把电能转化为化学能的装置叫做电解池或电解槽。
2、电解:电流(外加直流电)通过电解质溶液而在阴阳两极引起氧化还原反应(被动的不是自发的)的过程3、放电:当离子到达电极时,失去或获得电子,发生氧化还原反应的过程。
反应条件:①连接直流电源②阴阳两极阴极:与电源负极相连;极:与电源正极相连。
③两极处于电解质溶液或熔融电解质中④两电极形成闭合回路4、电子流向:电源负极一电解池阴极一离子定向运动(电解质溶液)一电解池阳极一电源正极5、电极名称及反应:阳极:与直流电源的正极相连的电极,发生氧化反应失去电子;阴极:与直流电源的负极相连的电极,发生还原反应得到电子。
7、电解本质:电解质溶液的导电过程,就是电解质溶液的电解过程8、反应规律:阳极:活泼金属一电极失电子6“ Pt除外);惰性电极一溶液中阴离子失电子阴离子失电子能力:活泼金属(除Pt, Au)>S2->|->Br->Cl->OH->含氧酸根(NO3->SO42-)>F-阳离子得电子能力:Ag+>Hg2+>Fe3+>Cu2+>H+ (酸)>Pb2+>Sn2+>Fe2+>Zn2+>H+ (水)>Al3+>Mg2+>Na+>Ca2+>K+ (即金属活泼性顺序表的逆向)规律:铝前(含铝)离子不放电,氢(酸)后离子先放电,氢(酸)前铝后的离子看条件。
9、四类电解型的电解规律(当阳极为惰性电极时)①电解水型(强碱,含氧酸,活泼金属的含氧酸盐),pH由溶液的酸碱性决定,溶液呈碱性则pH增大,溶液呈酸性则pH减小,溶液呈中性则pH不变。
电解质溶液复原一加适量水。
②电解电解质型(无氧酸,不活泼金属的无氧酸盐),无氧酸pH变大,不活泼金属的无氧酸盐pH不变。
电解质溶液复原一加适量电解质。
③放氢生碱型(活泼金属的无氧酸盐),pH变大。
人教版化学选修四第四章第三节电解池(共13张PPT)

加酚酞溶液变红
实验装置
2.电镀
(1).
定义
利用电解原理在某些金属的表面镀上 一薄层其它金属或合金的过程。
(2). 电镀材料的选择
阴极——镀件 阳极——镀层金属
电镀液——含有镀层金属离子的溶液
(3).电极反应式
阴极:Cu2++ 2e- = Cu
阳极: Cu - 2e- = Cu2+ (4).电镀的特点
择决定命运,环境造就人生!
电解
==MgLeabharlann +Cl2↑
(3)制取金属铝
电解熔融氧化铝
阳极: 6O2- - 12e- = 3O2↑
阴极: 4Al3+ + 12e- = 4Al
总反应:
电解
2Al2O3 ==
4Al
+
3O2↑
小结:电解池、电解精炼池、电镀池的比较
电解池
电镀池
电解精炼池
定义
将电能转变成化学能 的装置。
应用电解原理在某些 金属表面镀上一层其 它金属的装置。
①阳极本身参加电极反应 ②电解质溶液的浓度保持不变
3、粗铜的电解精炼
-+
以粗铜为阳极,以纯铜 纯铜
粗铜
为阴极, 以CuSO4溶液 为电解液进行电解
阳极: Zn Zn-2e- = Zn2+
Fe Ni
Fe -2e- = Ni -2e- =
Fe2+ Ni2+
CuSO4溶液
阳极泥: 相对不活泼的金
Cu Cu-2e- = Cu2+ 属以单质的形式沉积在电
离子放电顺序:
阳离子 H+ > Na+ 阴离子 Cl- > OH-
电解池知识点

第三节 电解池1.电解(1)定义:使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程。
在此过程中,电能转化为化学能。
(2)特点:①电解是不可逆的;②电解质导电一定发生化学变化。
2.电解池(1)概念:电解池是把电能转化为化学能的装置。
(2)电解池的构成条件 ①有与电源相连的两个电极。
②两个电极插入电解质溶液(或熔融电解质)中。
③形成闭合回路。
(3)电极名称及电极反应式以用惰性电极电解CuCl 2溶液为例:总反应方程式:CuCl 2=====电解Cu +Cl 2↑。
(4)电解池中电子和离子的移动方向①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流向电源的正极。
②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。
3.电解产物的判断及有关反应式的书写(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)再分析电解质水溶液的组成,找全离子并分阴、阳两组(勿忘水溶液中的H +和OH -)。
(3)排出阴、阳两极的放电顺序4.电解本质:电解质溶液的导电过程,就是电解质溶液的电解过程☆规律总结:电解反应离子方程式书写: 稀溶液中离子放电顺序: 阳离子放电顺序Ag +>Hg 2+>Fe 3+>Cu 2+>H +(指酸电离的)>Pb 2+>Sn 2+>Fe 2+>Zn 2+>H 2O>Al 3+>Mg 2+>Na +>Ca 2+>K + 阴离子的放电顺序是惰性电极时:活性金属>S2->SO32->I->Br->Cl->OH->H2O>NO3->SO42-(等含氧酸根离子)>F-是活性电极时:电极本身溶解放电注意先要看电极材料,是惰性电极还是活性电极,若阳极材料为活性电极(Fe、Cu)等金属,则阳极反应为电极材料失去电子,变成离子进入溶液;若为惰性材料,则根据阴阳离子的放电顺序,依据阳氧阴还的规律来书写电极反应式。
人教化学选修4第四章第3节 电解池(共19张PPT)
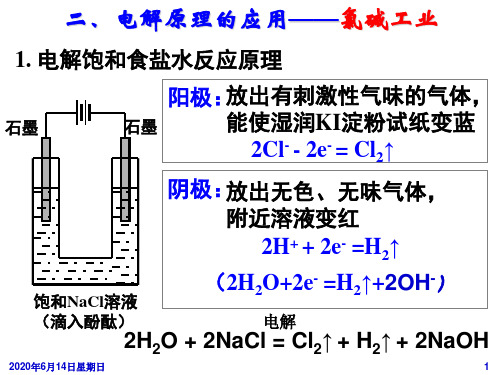
Cl2
H2
(2)电解饱和食盐水
2的Cl离-+子2方H2程O式=电=是解==2;OH淡-盐+水H2↑+Cl2N↑a+ (3)电解时用盐酸控
溶液A
制阳极区溶液的pH
氯 H减在 衡 酸C少气的移2l~O氯与作动,3气水用原,增在反_理用_大水应解_化H_中:释学_C_的C盐l平_的l_溶2+浓;解H度,2可O有使精利制平于饱衡和氯逆H气水向C的(移含l+溢少动出,。
2020年6月14日星期日
10
二、电解原理的应用——电解精炼铜
2020年6月14日星期日
11
二、电解原理的应用——电冶金
电解是最强有力的氧化还原手段,用于 冶炼Na、Ca、Mg、Al这样活泼的金属
钠的冶炼 (熔融NaCl作电解质)
阳极:2Cl--2e-=Cl2↑ 阴极:2Na++2e-=2Na 总反应: 2NaCl(熔融)通==电=2Na+Cl2↑
Cu
以粗铜为阳极,以纯铜
Zn Fe
纯铜 Cu
为阴极, 以CuSO4溶液 为电解液进行电解。
Ni Ag
Au
②电解后CuSO4浓度的变化 CuSO4浓度减小
CuSO4溶液
阳极: Zn -2e-=Zn2+ Fe-2e-=Fe2+
Ni -2e-=Ni2+ Cu-2e-=Cu2+
阴极: Cu2+ +2e-=Cu
2020年6月14日星期日
NaCl
量NaOH) 19
阴极:
4Al 3+ + 12 e- =4Al 阳极:
C
Fe
6O 2- -12e - =3O2↑ 总反应: 2Al2O3(熔融)通==电=4Al+3O2↑
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
思考回忆
1、电解质是指在_____________能够导电的化合物。
水溶液 熔融 2、电离是指电解质在_____________ 或__________ 自由移动离子 状态下离解成____________ 的过程。 把化学能转化为电能 3、原电池是_____________
水溶液或熔融状态下
的装置 。
23
电子流向
极
(外电路)负极 → 正极 (外电路)正极→负极 负极:Zn - 2e- =Zn2+(氧化反应)
电流方向
电极反应 能量转化 应用
正极:2H+ + 2e- =H2↑(还原原应) 化学能→ 电能 设计电池、金属防腐
三、电解原理的应用
1.电解食盐水 思考:
(1)通电前,饱和食盐水中存在哪些离子?这些离子的运动情况 怎样? (2)通电后,溶液中的离子运动发生了什么变化? (3)通电后,溶液中的在阴、阳放电的是什么离子? (4)电解后,在阴极区和阳极区分别得到的产物是什么?怎样初 步检验两极产物的生成?
电解后溶液中溶质的质量分数 增大 ,若要恢复 原来的浓度,只需加入一定量的 水 即可。
16
电解
⑵电解无氧酸溶液(氢氟酸除外)、不活泼金属的 无氧酸盐溶液,如电解盐酸、CuCl2溶液等 电解盐酸
阳极: 2Cl -- 2e-=Cl2↑ 阴极: 2H+ +2e-= H2 ↑ 电解 总反应:2HCl== Cl2↑ + H2↑
电解一段时间以后,甲、乙两池中溶液的 pH值均减小,而在①和④两极,电极产物 的物质的量之比为1︰2的是
甲
甲
乙
乙
• A B • 甲 KOH H2SO4 • 乙 CuSO4 AgNO3 D
C D Na2SO4 CuSO4 HCl HNO3
21
3.为下图所示装置中,a、b都是惰性电极, 通电一段时间后,b极附近溶液呈红色。下 列说法正确的是 AC A.X是正极,Y是负极 B.X是负极,Y是正极 C.CuSO4溶液的pH值逐渐减小 D.CuSO4溶液的pH值不变
电解
⑷电解活泼金属的无氧酸盐溶液时,电解质和水 都有一部分被电解,如电解NaCl溶液等。
阳极 (C): 2Cl -- 2e-=Cl2↑
阴极 (C): 2H+ +2e-= H2 ↑ 总反应:2NaCl+2H2O==2NaOH+ Cl2↑ + H2↑ 电解后原溶液中溶质的质量分数减小,若要恢 复原来的组成和浓度,需通入一定量的HCl。
28
泥沙 Mg2+、 Ca2+、 Fe3+ 、 SO42-
、
Na+、
Cl-、
沉降
除泥沙
Na+、 Cl-、 .Mg2+、 Ca2+、 Fe3+ 、 SO42略过量 BaCl2 溶液 除SO42-
Na+、
Cl-、Ca2+
、
略过量NaOH 溶液
Ba2+ 、引入OH-
除Fe3+ Mg2+
,
Na+、 Cl-、 Mg2+、 Ca2+、 Fe3+ 、引入Ba2+
通电
2H2↑ + O2↑
13
阴极: 2H+ + 2e- == H2 ↑
2Cl 2e == Cl2↑ 阳极:
2HCl 总反应:
通电
H2 ↑+ Cl2↑
14
阴极:2Cu 2+ + 4e- = 2Cu 阳极:4OH- - 4e- = 2H2O + O2↑ 总反应: 2Cu(NO3)2 + 2H2O
通电
25
氯碱工业:离子交换膜法制烧碱210
(1)生产设备名称:离子交换膜电解槽 阴极:碳钢 阳极:钛 阳离子交换膜:只允许阳离子通过(Cl-、OH -离子和气体不能通过),把电解槽隔成阴 极室和阳极室。 (2)离子交换膜的作用: a、防止氢气和氯气混合而引起爆炸; b、避免氯气和氢氧化钠反应生成 ,而影响 氢氧化钠的产量。
纯铜
阳极泥: 相对不活泼的金 粗铜 含杂质(Zn Fe Ni Ag Au 等) 属以单质的形式沉积在电 粗铜 阳极: 解槽底,形成阳极泥 2+ -
CuSO4溶液
Zn Fe Cu Ag Au
Zn→ Zn +2e Fe → Fe2++2eCu→ Cu2++2e阳极泥
阴极:
Cu2+ + 2e- → Cu
30
4、写出下列物质的电离方程式 CuCl2 H2O NaHSO4 CH3COONH4
2
一、电解原理 演示实验 微粒移动方向
结论:电解质通电前在水溶液中自由移动的阴、阳离
自由 子作______________ 运动;在外电源的作用下(直流 电),改作_________ 移动而导电。在导电的同时,在 定向 阳、阴两极发生氧化—还原反应,即被电解,电离是 电解 __________ 的前题。
电镀:电镀是利用电解原理在某些金属表面镀 上一薄层其他金属或合金的过程,
①电极: 阳极——镀层金属 或惰性电极 阴极——待镀金属制品 铁 片 铜 片
硫酸铜溶液
②电镀液:含有镀层金属离子的电解质溶液。 溶液中CuSO4的浓度保持不变或变小
31
4、电冶金
略过量 2+. Ba2+ 除 Ca Na2CO3 溶液
Na+、 Cl-、
适量HCl溶液 调节PH 除 CO32- 、OH-
Na+、 Cl29
CO32-
、
OH-
2.铜的电解精炼
一般火法冶炼得到的粗铜中含有多种杂质(如锌、铁、镍、银、金等),这种 粗铜的导电性远不能满足电气工业的要求,如果用以制电线,就会大大降低电线的 导电能力。因此必须利用电解的方法精炼粗铜。
6
3、构成电解池的条件:
①直流电源; 与电源负极相连的电极为阴极 ②电极 与电源正极相连的电极为阳极
③电解质溶液或熔融电解质; ④ 形成闭合的回路
7
4.电解池电极反应规律(阳氧阴还)
(1)阴极:得电子,还原反应
①电极本身不参加反应
②一定是电解质溶液中阳离子“争”得电子
(2)阳极:失电子,氧化反应
<
>
Cu2+ SO4
2-
②、然后写电极反应式 : 阴极: 2Cu2++4e=2Cu 阳极: 4OH- -4e=O2↑+2H2O ③、最后使得失数相等,两极半反应相加得总方程式; 2Cu2++2H 或
2O
电解 电解
2Cu+O2↑+4H+ 2Cu+O2↑+2H2SO4
(电解离子方程式) (电解化学方程式 11 )
2
CuCl2
电解
Cu +Cl2↑
4
1、电解原理
在外加直流电源的作用下,电解质的阴阳离子在 阴阳两极发生氧化还原反应的过程,叫电解。
明 确
⑴
电流是发生氧化—还原反应的根源、动力。 阴阳离子在做定向运动导电的同时,也就 在两极发生了氧化还原反应,生成了新物 质; 而金属导电是由自由电子的定向运动形成, 无反应发生,无新物质生成,两者有本质 区别。
3. 电镀
电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合 金的过程,它是电解原理的又一重要应用。电镀可以使金属更 加美观耐用,增强防锈抗腐能力。例如,钢铁是人们最常用的 金属,但钢铁有个致命的缺点,就是它们易被腐蚀。防止钢铁 发生腐蚀的一种最常用方法就是在其表面镀上其他金属,如锌、 铜、铬、镍等。
19
电解
1.如上图所示,通电后A极上析出Ag,对该装置的有关 叙述正确的是 B A.P是电源的正极 B.F极上发生的反应为:4OH- - 4e-=2H2O+O2↑ C.电解时,甲、乙、丙三池中,除E、F两极外,其余电 极均参加了反应 D.通电后,甲池的PH减小,而乙、丙两池溶液的PH不变
20
2.用铂电极电解下表中各组物质的水溶液,
2CuSO4+2H2O
练习:完成下列溶液的电极反应。 (以石墨为电极电解) 硫酸溶液: 盐酸: NaOH溶液: CuBr2溶液: KCl溶液: Cu(NO3)2溶液: Na2SO4溶液:
12
阳极:4OH- - 4e- = 2H2O + O2↑ 阴极:4H+ + 4e- = 2H2↑ 总反应:2H2O
3
电解氯化铜原理
直流电源 I 电极 负极 e电源 正极 eI
(析出Cu) 阴极 被还原
阳极 (放出Cl2↑) Cu2+ Cl– 被氧化 Cl– 失2e-
电解质
得2e-
CuCl2 = Cu2++2Cl–
电极反应
阴极: Cu2+ + 2e = Cu (还原反应)
阳极: 2Cl--2e =Cl2↑ (氧化反应) 总反应: Cu2+ + 2Cl- 电解 Cu +Cl ↑(氧化还原反应)
2Cu + 4HNO3+ O2↑
15
二、电解规律(用惰性电极电解时)
⑴电解含氧酸、强碱溶液、活泼金属的含氧酸盐溶液时,
如电解H2SO4、HNO3、NaOH、Na2SO4等溶液
例如:电解硫酸钠溶液
阳极 : 4OH--4e-=2H2O +O2↑ 阴极: 4H+ +4e-=2H2 ↑ 总反应:2H2O== O2↑ +2H2↑ 实质:电解水
26
Cl2 +
H2 - NaOH溶液
淡盐水
阳 极
Cl2 Na+ Cl—
H+
阴 极 碳钢网
