2013年普通高等学校招生全国统一考试理科综合四川卷化学word校对
2013年四川卷,含答案)

2013年普通高等学校招生全国统一考试(四川卷)1.化学与生活密切相关,下列说法不正确的是A.二氧化硫课广泛用于食品的漂白B.葡萄糖可用于补钙药物的合成C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌2.下列物质分类正确的是A.SO2、SiO2 CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.福尔马林、水玻璃、氨水均为混合物3.下列离子方程式正确的是A.Cl2通入水中:Cl2+H2O = 2H++Cl-+ClO-B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜做电极电解CuSO4溶液:2Cu2++2H2O2Cu+O2↑+4H+D.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O4.同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。
下列说法正确的是A. W、Y、Z的电负性大小顺序一定是Z>Y>WB. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>ZC.Y、Z形成的分子的空间构型可能是正四面体D.WY2分子中σ键与π键的数目之比是2︰15.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:实验编号起始浓度/(mol·L-1)反应后溶液的pHc(HA)c(KOH)①0.10.19②x0.27下列判断不正确的是A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol·L—1K W-91X10C. 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1D. 实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)6.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表:t/min2479n(Y)/mol0.120.110.100.10下列说法正确的是A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)C.该温度下此反应的平衡常数K=1.44D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大7.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是A.该合金中铜与镁的物质的量之比是2 ︰1B.该浓硝酸中HNO3的物质的量浓度是14.0mol/LC. NO2和N2O4 的混合气体中,NO2 的体积分数是80%D. 得到2.54沉淀时,加入NaOH溶液的体积是600mL8.(11分)X、Y、Z、R为前四周期元素且原子序数依次增大。
2013年四川高考理综试卷及答案

2013年高考四川卷化学试卷及答案1.化学与生活密切相关,下列说法不正确...的是A.二氧化硫课广泛用于食品的漂白B.葡萄糖可用于补钙药物的合成C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌2.下列物质分类正确的是A.SO2、SiO2CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.福尔马林、水玻璃、氨水均为混合物3.下列离子方程式正确的是A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜做电极电解CuSO4溶液:2Cu2++2H2O2Cu+O2↑+4H+D.Na2S2O3溶液中加入稀硫酸:2S2O-23+4H+=SO-24+3S↓+2H2O4.同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。
下列说法正确的是A.W、Y、Z的电负性大小顺序一定是Z>Y>WB.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>ZC.Y、Z形成的分子的空间构型可能是正四面体D.WY2分子中σ键与π键的数目之比是2︰15.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:实验编号起始浓度/(mol·L-1)反应后溶液的pH C(HA) c(KOH)①0.1 0.1 9②x 0.2 7下列判断不正确...的是A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)B .实验①反应后的溶液中:c(OH -)=c(K +)-c(A -)=mol ·L -1C .实验②反应后的溶液中:c (A -)+c (HA)>0.1mol·L -1 D .实验②反应后的溶液中:c (K +)=c (A -)>c (OH -)=c (H +)6.在一定温度下,将气体X 和气体Y 各0.16mol 充入10L 恒容密闭容器中,发生反应 X(g)+Y(g)2Z(g)△H<0, 一段时间后达到平衡,反应过程中测定的数据如下表:t/min 2 4 7 9 n(Y)/mol0.120.110.100.10下列说法正确的是A .反应前2min 的平均速率ν(Z)=2.0×10-3mol·L -1·min -1B .其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)C .该温度下此反应的平衡常数K =1.44D .其他条件不变,再充入0.2molZ ,平衡时X 的体积分数增大7.1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL 、质量分数为63%的浓硝酸中,得到NO 2和N 2O 4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH 溶液,当金属离子全部沉淀时,得到2.54g 沉淀,下列说法不正确...的是 A .该合金中铜与镁的物质的量之比是2︰1 B .该浓硝酸中HNO 3的物质的量浓度是14.0mol/L C .NO 2和N 2O 4的混合气体中,NO 2的体积分数是80% D .得到2.54沉淀时,加入NaOH 溶液的体积是600mL8.(11分)X 、Y 、Z 、R 为前四周期元素且原子序数依次增大。
化学高考真题-2013四川

2013年高考理综试题(四川卷)化学部分1.化学与生活密切相关,下列说法不正确的是A.二氧化硫可广泛用于食品的增白B.葡萄糖可用于补钙药物的合成C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌2.下列物质分类正确的是A.SO2、SiO2、CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.福尔马林、水玻璃、氨水均为混合物3.下列离子方程式正确的是A.Cl2通入水中:Cl2 + H2O = 2H++ Cl-+ ClO-B.双氧水中加入稀硫酸和KI溶液:H2O2 + 2H++ 2I-= I2 + 2H2OC.用铜作电极电解CuSO4溶液:2Cu2++ 2H2O 2Cu + O2↑+ 4H+D.Na2S2O3溶液中加入稀硫酸:2S2O32-+ 4H+= SO42-+ 3S↓+ 2H2O4.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4∶3,Z原子比X原子的核外电子数多4。
下列说法正确的是A.W、Y、Z的电负性大小顺序一定是Z>Y>WB.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>ZC.Y、Z形成的分子的空间构型可能是正四面体D.WY2分子中σ键与п键的数目之比是2∶15.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:实验编号起始浓度/(mol•L-1)反应后溶液的pH c(HA) c(KOH)①** **9②x **7下列判断不正确的是A.实验①反应后的溶液中:c(K+) > c(A-) > c(OH-) > c(H+)B.实验①反应后的溶液中:c(OH-) = c(K+)—c(A-) =C.实验②反应后的溶液中:c(A-) + c(HA) > 0.1mol/L D.实验②反应后的溶液中:c(K+) = c(A-) > c(OH-) = c(H+)6.在一定温度下,将气体X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应X(g) + Y(g) 2Z(g)△H < 0,一段时间后达到平衡。
13年高考真题——(四川卷)解析版

2013年高考真题——(四川卷)解析版2013年全国高考理科综合化学参考答案及解析 1. 化学与生活密切相关,下列说法不正确的是...A.二氧化硫可广泛用于食品的增白B.葡萄糖可用于补钙药物的合成C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌【答案】A 【解析】二氧化硫有一定毒性,少量用于漂白,此题应该选A。
2. 下列物质分类正确的是A.SO2、SiO2、CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.福尔马林、水玻璃、氨水均为混合物【答案】D 【解析】不是酸性氧化物,B氧化铁不是胶体,C,CCl4属于非电解质。
3. 下列离子方程式正确的是A.Cl2通入水中:Cl2 + H2O === 2H+ + Cl +ClO ——B.双氧水中加入稀硫酸和KI溶液:H2O2 + 2H+ + 2I === I2 + 2H2O —C.用铜作电极电解CuSO4溶液:2Cu2+ + 2H2O === 2Cu + O2↑+ 4H+D.Na2S2O3溶液中加入稀硫酸:2S2O32 4H+ === SO42 + 3S↓ + 2H2O ——电解【答案】B 【解析】A的HClO 是弱电解质不拆,做电解池电极时参加反应失电子做阳极,不是水中的氢氧根失去电子。
4. 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X 原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4。
下列说法正确的是A.W、Y、Z的电负性大小顺序一定是Z>Y>W B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z 1 C.Y、Z形成的分子空间构型可能是正四面体D.WY2分子中δ键与π键的数目之比是2:1 【答案】C 【解析】因为最外层电子数W:X≒4:3,故W最外层电子数为4,X的为3,又因为WXYZ的原子序数依次增加,可以推出:X:Al W:C Z:Cl 所以W为C,X为Al,Z 为Cl,Y可能为Si、P、S,所以C选项SiCl4为正四面体,正确。
2013年普通高等学校招生全国统一考试·全国卷Ⅰ 理科综合化学部分

2013年普通高等学校招生全国统一考试·全国卷Ⅰ理科综合·化学部分(分值:100分)注意事项:1.高考试题中理科综合试卷总分300分,时间150分钟,本试卷只呈现化学部分。
2.本试卷分第Ⅰ卷和第Ⅱ卷两部分,卷Ⅰ为选择题,卷Ⅱ为非选择题。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 K 39 Mn 55第Ⅰ卷(选择题,共42分)一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7.化学无处不在,下列与化学有关的说法不正确的是( )A.侯氏制碱法的工艺过程中应用了物质溶解度的差异B.可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气C.碘是人体必需微量元素,所以要多吃富含高碘酸的食物D.黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成8.香叶醇是合成玫瑰香油的主要原料,其结构简式如右:下列有关香叶醇的叙述正确的是( )A.香叶醇的分子式为C10H18OB.不能使溴的四氯化碳溶液褪色C.不能使酸性高锰酸钾溶液褪色D.能发生加成反应不能发生取代反应9.短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是( )A.W2-、X+B.X+、Y3+C.Y3+、Z2- D .X+、Z2-10.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,下列说法正确的是( )A.处理过程中银器一直保持恒重B.银器为正极,Ag2S被还原生成单质银C.该过程中总反应为2Al+3Ag2S6Ag+Al2S3D.黑色褪去的原因是黑色Ag2S转化为白色AgCl11.已知K sp(AgCl)=1.56×10-10,K sp(AgBr)=7.7×10-13,K sp(Ag2CrO4)=9.0×10-12。
2013年普通高等学校招生全国统一考试 四川卷(理工类)
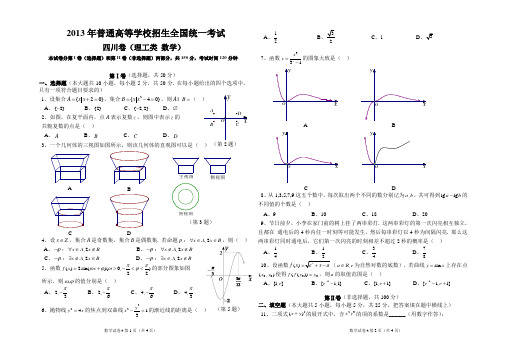
(第2题) 2013年普通高等学校招生全国统一考试四川卷(理工类 数学)本试卷分第I 卷(选择题)和第II 卷(非选择题)两部分,共150分,考试时间120分钟.第Ⅰ卷(选择题,共50分)一、选择题(本大题共10小题,每小题5分,共50分. 在每小题给出的四个选项中,只有一项符合题目要求的)1、设集合{20}A x x =+=,集合2{40}B x x =-=,则A B = ( A 、{2}- B 、{2} C 、{2,2}- D 、∅2、如图,在复平面内,点A 表示复数z ,则图中表示z 的 共轭复数的点是( )A 、AB 、BC 、CD 、D3、一个几何体的三视图如图所示,则该几何体的直观图可以是( )4、设x Z ∈,集合A 是奇数集,集合B 是偶数集. 若命题p :,2x A x B ∀∈∈,则( ) A 、p ⌝:,2x A x B ∀∈∉ B 、p ⌝:,2x A x B ∀∉∉ C 、p ⌝:,2x A x B ∃∉∈ D 、p ⌝:,2x A x B ∃∈∉5、函数()2sin()(0,)22f x x ππωϕωϕ=+>-<<的部分图象如图所示,则,ωϕ的值分别是( ) A 、2,3π-B 、2,6π-C 、4,6π-D 、4,3π 6、抛物线24y x =的焦点到双曲线2213y x -=的渐近线的距离是( ) A 、12B 、2C 、1D7、函数331x x y =-的图象大致是( )8、从1,3,5,7,9这五个数中,每次取出两个不同的数分别记为,a b ,共可得到lg lg a b -的不同值的个数是( )A 、9B 、10C 、18D 、209、节日前夕,小李在家门前的树上挂了两串彩灯. 这两串彩灯的第一次闪亮相互独立,且都在 通电后的4秒内任一时刻等可能发生,然后每串彩灯以4秒为间隔闪亮. 那么这两串彩灯同时通电后,它们第一次闪亮的时刻相差不超过2秒的概率是( )A 、14B 、12C 、34D 、7810、设函数()f x =,a R e ∈为自然对数的底数). 若曲线sin y x =上存在点00(,)x y 使得00(())f f y y =,则a 的取值范围是( )A 、[1,]eB 、1[1,1]e --C 、[1,1]e +D 、1[1,1]e e --+ 第Ⅱ卷(非选择题,共100分)二、填空题(本大题共5小题,每小题5分,共25分,把答案填在题中横线上) 11、二项式5()x y +的展开式中,含23x y 的项的系数是______(用数字作答);俯视图侧视图主视图(第3题)AB CD (第5题)ABCD(第18题)12、在平行四边形ABCD 中,对角线AC 与BD 交于点O ,AB AD AO λ+=,则λ=____;13、设sin 2sin αα=-,(,)2παπ∈,则tan 2α的值是______;14、已知()f x 的定义域为R 的偶函数,当0x ≥时,2()4f x x x =-,那么,不等式(2)5f x +<的解集是______;15、设12,,,n P P P 为平面α内的n 个点,在平面α内的所有点中,若点P 到点12,,,n P P P 的距离之和最小,则称点P 为点12,,,n P P P 的一个“中位点”. 例如,线段AB 上任意点都是端点,A B 的中位点. 现有下列命题:①若三个点,,A B C 共线,C 在线段AB 上,则C 是,A B 的中位点; ②直角三角形斜边的中点是该直角三角形三个顶点的中位点; ③若四个点,,,A B C D 共线,则它们的中位点存在且唯一; ④梯形对角线的交点是该梯形四个顶点的唯一中位点.其中的真命题是______.(写出所有真命题的序号)三、解答题(本大题共6小题,共75分. 解答应写出文字说明、证明过程或演算步骤) 16、(本小题满分12分)在等差数列{}n a 中,138a a +=,且4a 为2a 和9a 的等比中项,求数列{}n a 的首项、公差及前n 项和.17、(本小题满分12分)在ABC ∆中,角,,A B C 的对边分别为,,a b c ,且232c o sc o ss i n ()s i n c o s ()25A BB A B B AC ---++=-.(1)求cos A 的值;(2)若a =5b =,求向量BA 在BC方向上的投影.18、(本小题满分12分)某算法的程序框图如图所示, 其中输入的变量x 在1,2,3,…,24这24个整数中等可能 随机产生.(1)分别求出按程序框图正确编程运行时输出y 的值 为i 的概率(1,2,3)i P i =;(2)甲、乙两同学依据自己对程序框图的理解,各自 编写程序重复运行n 次后,统计记录了输出y 的值为i(1,2,3)i =的频数. 以下是甲、乙所作频数统计表的部分数据.甲的频数统计表(部分)乙的频数统计表(部分)当2100n =时,根据表中的数据,分别写出甲、乙所编程序各自输出y 的值为(1,2,3)i i =的频率(用分数表示),并判断两位同学中哪一位所编程序符合算法要求的可能性较大; (3)将按程序框图正确编写的程序运行3次,求输出y 的值为2的次数ξ的分布列及数学期望.19、(本小题满分12分)如图,在三棱柱111ABC A B C -中,侧棱1AA ⊥底面ABC ,12AB AC AA ==,120BAC ∠=︒,1,D D 分别是线段,BC11B C 的中点,P 是线段AD 的中点.(1)在平面ABC 内,试作出过点P 与平面1A BC 平行 的直线l ,说明理由,并证明直线l ⊥平面11ADD A ; (2)设(1)中的直线l 交AB 于点M ,交AC 于点N , 求二面角1A A M N --的余弦值.20、(本小题满分13分)已知椭圆C :22221(0)x y a b a b+=>>的两个焦点分别为1(1,0)F -,2(1,0)F ,且椭圆C经过点41(,)33P .(1)求椭圆C 的离心率;(2)设过点(0,2)A 的直线l 与椭圆C 交于,M N 两点,点Q 是线段MN ,且222211AQAMAN=+,求点Q 的轨迹方程.21、(本小题满分14分)已知函数22,0()ln ,0x x a x f x x x ⎧++<=⎨>⎩,其中a 是实数. 设11(,())A x f x ,22(,())B x f x 为该函数图象上的两点,且12x x <(1)指出函数()f x 的单调区间;(2)若函数()f x 的图象在点,A B 处的切线互相垂直,且20x <,求21x x -的最小值;(3)若函数()f x 的图象在点,A B 处的切线重合,求a 的取值范围.C 11(第19题)。
2013四川高考理综化学部分试题及答案(word版)

绝密★启用前2013年普通高等学校招生全国统一考试(四川卷)理科综合·化学理科综合考试时间共150分钟。
试卷满分300分,其中物理110分,化学100分,生物90分。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(费选择题)。
第Ⅰ卷5至6页,第Ⅱ卷7至8页,共4页。
考生作答时,需将答案答在答题卡上,在本卷第Ⅱ卷、草稿纸上答题无效。
考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H 1 N 14 O 16 Mg 24 Al 27 S 32 K 39 Cu 64第Ⅰ卷(选择题共42分)注惹事项:必须使用2B铅笔将答题卡上将所选答案对应的标号涂黑。
Ⅰ卷共7题,每题6分。
在每题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列说法不正确...的是A.二氧化硫课广泛用于食品的漂白B.葡萄糖可用于补钙药物的合成C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌【解析】SO2 可被人体吸收进入血液,对全身产生毒性作用,它能破坏酶的活力,影响人体新陈代谢,对肝脏造成一定的损害。
慢性毒性试验显示,SO2 有全身性毒性作用,故SO2不可用于食品漂白,A错。
葡萄糖酸钙常被用做补钙剂,B正确;聚乙烯可做食品的包装,而聚氯乙烯不可,C正确;“84”消毒液的有效成分就是NaClO,可用于环境消毒,D正确。
【答案】A【考点】化学知识在日常生活中的应用。
2.下列物质分类正确的是A.SO2、SiO2 CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.福尔马林、水玻璃、氨水均为混合物【解析】CO属于不成盐氧化物,故A错;氯化铁溶液不属于胶体,是溶液,故B错;四氯化碳属于非电解质;福尔马林是甲醛的水溶液、水玻璃是硅酸钠的水溶液、氨水是氨气的水溶液,都属于混合物,D正确。
【答案】D【考点】物质的成分及分类。
3.下列离子方程式正确的是A.Cl2通入水中:Cl2+H2O = 2H++Cl-+ClO-B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜做电极电解CuSO 4溶液:2Cu 2++2H 2O 2Cu +O 2↑+4H + D.Na 2S 2O 3溶液中加入稀硫酸:2S 2O 32-+4H +=SO 42-+3S ↓+2H 2O【解析】HClO 是电解质,不能拆,故A 错;B 选项中的产物正确,元素、电荷和得失电子都守恒,正确;用Cu 作电极电解时,作阳极的铜要优先失去电子发生氧化反应,故C 错;D 选项中的电荷不守恒。
【2013高考真题+理综+化学】【四川卷】

2 013年普通高等学校招生全国统一考试(四川卷)理科综合·化学理科综合考试时间共150分钟。
试卷满分300分,其中物理110分,化学100分,生物90分。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(费选择题)。
第Ⅰ卷5至6页,第Ⅱ卷7至8页,共4页。
考生作答时,需将答案答在答题卡上,在本卷第Ⅱ卷、草稿纸上答题无效。
考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H 1 N 14 O 16 Mg 24 Al 27 S 32 K 39 Cu 64第Ⅰ卷(选择题共42分)注惹事项:必须使用2B铅笔将答题卡上将所选答案对应的标号涂黑。
Ⅰ卷共7题,每题6分。
在每题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列说法不正确...的是A.二氧化硫可广泛用于食品的漂白B.葡萄糖可用于补钙药物的合成C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌2.下列物质分类正确的是A.SO2、SiO2、CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.福尔马林、水玻璃、氨水均为混合物3.下列离子方程式正确的是A.Cl2通入水中:Cl2+H2O = 2H++Cl-+ClO-B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜做电极电解CuSO4溶液:2Cu2++2H2O2Cu+O2↑+4H+D.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O4.同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。
下列说法正确的是A. W、Y、Z的电负性大小顺序一定是Z>Y>WB. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>ZC.Y、Z形成的分子的空间构型可能是正四面体D.WY2分子中σ键与π键的数目之比是2︰15.实验编号起始浓度/(mol·L-1)反应后溶液的pH c(HA)c(KOH)①0.1 0.1 9②x 0.2 7 ...A.实验①反应后的溶液中:c(K +)>c(A -)>c(OH -)>c(H +)B.实验①反应后的溶液中:c(OH -)=c(K +)-c(A -)=mol ·L —1C. 实验②反应后的溶液中:c(A -)+c(HA)>0.1mol ·L -1D. 实验②反应后的溶液中:c(K +)=c(A -)>c(OH -) =c(H +)6.在一定温度下,将气体X 和气体Y 各0.16mol 充入10L 恒容密闭容器中,发生反应t/min2 4 7 9 n(Y)/mol0.120.110.100.10下列说法正确的是A.反应前2min 的平均速率ν(Z)=2.0×10-3mol ·L -1·min -1 B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正) C.该温度下此反应的平衡常数K=1.44D. 其他条件不变,再充入0.2molZ ,平衡时X 的体积分数增大7.1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL 、质量分数为63%的浓硝酸中,得到NO 2和N 2O 4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH 溶液,当金属离子全部沉淀时,得到2.54g 沉淀,下列说法不正确...的是 A.该合金中铜与镁的物质的量之比是2 ︰1B.该浓硝酸中HNO 3的物质的量浓度是14.0mol/LC. NO 2和N 2O 4 的混合气体中,NO 2 的体积分数是80%D. 得到2.54沉淀时,加入NaOH 溶液的体积是600mL第Ⅱ卷(非选择题 共 58分)注意事项:必须使用0.5毫米黑色墨迹签字笔在答题卡上题目所指示的答题区域内作答,答在试题卷上、草稿纸上无效。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2013年普通高等学校招生全国统一考试(四川卷)
理科综合·化学
理科综合考试时间共150分钟。
试卷满分300分,其中物理110分,化学100分,生物90分。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(费选择题)。
第Ⅰ卷5至6页,第Ⅱ卷7至8页,共4页。
考生作答时,需将答案答在答题卡上,在本卷第Ⅱ卷、草稿纸上答题无效。
考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H 1 N 14 O 16 Mg 24 Al 27 S 32 K 39 Cu 64
第Ⅰ卷(选择题 共 42分)
注惹事项:
必须使用2B 铅笔将答题卡上将所选答案对应的标号涂黑。
Ⅰ卷共7题,每题6分。
在每题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列说法不正确...的是 A.二氧化硫课广泛用于食品的漂白 B.葡萄糖可用于补钙药物的合成 C.聚乙烯塑料制品可用于食品的包装 D.次氯酸钠溶液可用于环境的消毒杀菌 2.下列物质分类正确的是
A.SO 2、SiO 2 CO 均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物 3.下列离子方程式正确的是
A.Cl 2通入水中:Cl 2+H 2O = 2H ++Cl -+ClO -
B.双氧水加入稀硫酸和KI 溶液:H 2O 2+2H ++2I -
=I 2+2H 2O C.用铜做电极电解CuSO 4溶液:2Cu 2++2H 2O
2Cu +O 2↑+4H +
D.Na 2S 2O 3溶液中加入稀硫酸:2S 2O 32-
+4H +
=SO 42-
+3S ↓+2H 2O
4.同周期元素W 、X 、Y 、Z 的原子序数依次增大,W 、X 原子的最外电子层电子数之比为4︰3,Z 原子比X 原子的核外电子数多4。
下列说法正确的是 A. W 、Y 、Z 的电负性大小顺序一定是Z>Y>W
B. W 、X 、Y 、Z 的原子半径大小顺序可能是W>X>Y>Z
C.Y 、Z 形成的分子的空间构型可能是正四面体
D.WY 2分子中σ键与π键的数目之比是2︰1
5.
下列判断不正确...
的是 A.实验①反应后的溶液中:c(K +)>c(A -)>c(OH -)>c(H +) B.实验①反应后的溶液中:c(OH -
)=c(K +
)-c(A -
)=
mol ·L —1
K W
1X10
-9
C. 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D. 实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
6.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
2Z(g)
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
7.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确
...的是
A.该合金中铜与镁的物质的量之比是2 ︰1
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54沉淀时,加入NaOH溶液的体积是600mL
第Ⅱ卷(非选择题共58分)
注意事项:
必须使用0.5毫米黑色墨迹签字笔在答题卡上题目所指示的答题区域内作答,答在试题卷上、草稿纸上无效。
Ⅱ卷共4题
8.(11分)
X、Y、Z、R为前四周期元素且原子序数依次增大。
X的单质与氢气可以化合生成气体G,其水溶液pH>7;Y单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。
Y、Z分别与钠元素可以形成化合物Q和J,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀I;Z与氢元素形成的化合物与G反应生成M。
请回答下列问题:
⑴M固体的晶体类型是。
⑵Y基态原子的核外电子排布式是①;G分子中X原子的杂化轨道的类型是②。
⑶I的悬浊液加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是。
⑷R的一种含氧酸根RO42-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是。
9.(15分)
为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。
为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。
可选用第试剂KSCN溶液、K3[Fe(CN)6]溶液、氯水。
Ⅱ. AgNO3的热稳定性性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。
当反应结束以后,试管中残留固体为黑色。
⑵装置B的作用是。
⑶经小组讨论并验证该无色气体为O2,其验证
方法是。
⑷【查阅资料】Ag2O和粉末的Ag均为黑色;
Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:ⅰAg;ⅱAg2O;ⅲAg和Ag2O
【实验评价】根据上述实验,不能确定固体产物成分的实验是①(填实验编号)
【实验结论】根据上述实验结果,该小组得出的AgNO3固体热分解的产物有②。
10.(17分)
有机化合物G是合成维生素类药物的中间体,其结构简式为:
G的合成线路如下:
其中A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:
请回答下列问题:
⑴G的分子式是①;G中官能团的名称是②。
⑵第①步反应的化学方程式是。
⑶B的名称(系统命名)是。
⑷第②~⑥步中属于取代反应的有(填步骤编号)。
⑸第④步反应的化学方程式是。
⑹写出同时满足下列条件的E的所有同分异构体的结构简式。
①只含有一种官能团;②链状结构且无—O—O—;③核磁共振氢谱只有2种峰。
11、(15分)
明矾石经处理后得到明矾[ KAl(SO4)2·12H2O]。
从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4 +2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是。
(2)从水浸后的滤液中得到K2SO4晶体的方法
是。
(3)A12O3在一定条件下可制得AIN,其晶体结构如右图所示,该晶体中Al的
配位数是
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时
NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式
是。
(5)焙烧产生的SO2可用于制硫酸。
已知25℃、101 kPa时:
2SO 2(g) +O2(g)2SO3(g) △H1= 一197 kJ/mol;
2H2O (g)=2H2O(1) △H2=一44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=一545 kJ/mol。
则SO3 (g)与H2O(l)反应的热化学方程式是①。
焙烧948t明矾(M=474 g/mol ),若SO2的利用率为96%,可生产质量分数为98%的硫酸②t。
