2020年有机化学(第三版 马祥志主编)课后习题答案
有机化学课后习题参考答案完整版

有机化学课后习题参考答案完整版⽬录第⼀章绪论 0第⼆章饱和烃 (1)第三章不饱和烃 (5)第四章环烃 (13)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应⽤ (33)第⼋章醇酚醚 (43)第九章醛、酮、醌 (52)第⼗章羧酸及其衍⽣物 (63)第⼗⼀章取代酸 (71)第⼗⼆章含氮化合物 (78)第⼗三章含硫和含磷有机化合物 (86)第⼗四章碳⽔化合物 (89)第⼗五章氨基酸、多肽与蛋⽩质 (100)第⼗六章类脂化合物 (105)第⼗七章杂环化合物 (114)Fulin 湛师第⼀章绪论1.1扼要归纳典型的以离⼦键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于⽔中所得的溶液与NaBr 及KCl 各1mol 溶于⽔中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在⼀起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么?答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于⽔中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离⼦各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在⽔中是以分⼦状态存在,所以是两组不同的混合物。
1.3碳原⼦核外及氢原⼦核外各有⼏个电⼦?它们是怎样分布的?画出它们的轨道形状。
当四个氢原⼦与⼀个碳原⼦结合成甲烷(CH 4)时,碳原⼦核外有⼏个电⼦是⽤来与氢成键的?画出它们的轨道形状及甲烷分⼦的形状。
答案:C+624H CCH 4中C 中有4个电⼦与氢成键为SP 3杂化轨道,正四⾯体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电⼦式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H H HCC HH HH 或b.H C H c.H N Hd.H S H e.H O NOf.OC H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OS H H或1.5下列各化合物哪个有偶极矩?画出其⽅向。
有机化学第三版答案_上册

1) 链引发
1 3 0 ℃
① ( C H 3 ) 3 C O - O C ( C H 3 ) 3
2 ( C H 3 ) 3 C O
︱ C H 3
② (C H 3 )3 C O+C H 3 -︱ C -C H 3
(C H 3 )3 C -O H+C H 3 -︱ C H -C H 3
2) 链增长
21
2)异已烷
∣ CH3
CH3CHCH2CH2CH3
∣ CH3 ∣ CH2CHCH2CH2CH3 Cl
20%
∣CH3
CH3∣CCH2CH2CH3 17%
Cl
∣CH3 CH3CHC∣HCH2CH3
Cl
26.5%
∣CH3 CH3CHCH2∣CHCH3
26.5%
Cl
∣CH3
CH3CHCH2CH2∣ CH2
π键具有对称面,就是σ键平面. 3. 丙烷CH3CH2CH3的分子按碳的四面体分布,试画出个原 4. 子的分布示意.
HH H H
H
H
HH
6
4、只有一种结合方式:2个氢、1个碳、1个氧 (H2CO) ,试把分子的电子式画出来。
H HC O
5、丙烯CH3CH = CH2中的碳,哪个的sp3杂化,哪 个是sp2杂化?
(Z)-3-ethyl-2-methyl-3-heptene
(2) H
CH2Cl
CH3 C=C CH3
顺-1-氯-2-甲基-2-丁烯
cis-1-chloro-2-methyl-2-butene (E)-1-氯-2-甲基-2-丁烯
(E)-1-chloro-2-methyl-2-butene
35
(3 ) (C H 3 )3 C C H = C H 2
高教版有机化学第三版答案3

⑶.浓 H2SO4 作用后,加热水解. (答案)
课 后 答 案 网
⑷.HBr (答案)
(遵循马氏规则)
⑸.HBr
(有过氧化物) (答案)
课 后 答 案 网
⑸.HBr (有过氧化物) (答案)
6.写出下列各烯烃的臭氧化还原水解产物: (答案) (答案)
(答案)
课 后 答 案 网
7.裂化汽油中含有烯烃用什么方法能除去烯烃? (答案)
解:室温下,用浓 H2SO4 洗涤,烯烃与 H2SO4 作用生成酸性硫酸酯而溶 于浓 H2SO4 中,烷烃不溶而分层,可以除去烯烃。
8.试写出下列反应中的(a)及(b)的构造式: (1) (a)+Zn (b)+ZnCl
(答案)
(a):
(b): CH3CH2CH=CH2
(2)
(答案)
(a) :(CH3CH2CH2)3B
(b): CH3CH2CH2OH
9.试举出区别烷烃和烯烃的两种化学方法:(答案) 解:方法一:使酸性 KMnO4 溶液褪色为烯烃, 烷烃无此反应.
方法二:室温下无光照,迅速使 Br2/CCl4 溶液褪色者为烯烃, 烷烃无此反应.
2.命名下列化合物, 如有顺反异构体则写出构型式,并标以 Z,E (1)
(答案)
4-甲基-2-乙基-1-戊烯
⑵ CH3(C2H5)C=C(CH 3)CH2CH2CH3 (答案)
3,4-二甲基-3-庚烯
(Z)-3,4- 二甲基-3-庚烯
(E)-3,4- 二甲基-3-庚烯
课 后 答 案 网
⑶
∴离子的稳定性 3O>2O,因此,3O 碳正离子比 2O 碳正离子容易形成,综
生物化学第三版课后习题详细解答

生物化学(第三版)课后习题详细解答第三章氨基酸提要α-氨基酸是蛋白质的构件分子,当用酸、碱或蛋白酶水解蛋白质时可获得它们。
蛋白质中的氨基酸都是L型的。
但碱水解得到的氨基酸是D型和L型的消旋混合物。
参与蛋白质组成的基本氨基酸只有20种。
此外还有若干种氨基酸在某些蛋白质中存在,但它们都是在蛋白质生物合成后由相应是基本氨基酸(残基)经化学修饰而成。
除参与蛋白质组成的氨基酸外,还有很多种其他氨基酸存在与各种组织和细胞中,有的是β-、γ-或δ-氨基酸,有些是D型氨基酸。
氨基酸是两性电解质。
当pH接近1时,氨基酸的可解离基团全部质子化,当pH在13左右时,则全部去质子化。
在这中间的某一pH(因不同氨基酸而异),氨基酸以等电的兼性离子(H3N+CHRCOO-)状态存在。
某一氨基酸处于净电荷为零的兼性离子状态时的介质pH称为该氨基酸的等电点,用pI 表示。
所有的α-氨基酸都能与茚三酮发生颜色反应。
α-NH2与2,4-二硝基氟苯(DNFB)作用产生相应的DNP-氨基酸(Sanger反应);α-NH2与苯乙硫氰酸酯(PITC)作用形成相应氨基酸的苯胺基硫甲酰衍生物( Edman反应)。
胱氨酸中的二硫键可用氧化剂(如过甲酸)或还原剂(如巯基乙醇)断裂。
半胱氨酸的SH基在空气中氧化则成二硫键。
这几个反应在氨基酸荷蛋白质化学中占有重要地位。
除甘氨酸外α-氨基酸的α-碳是一个手性碳原子,因此α-氨基酸具有光学活性。
比旋是α-氨基酸的物理常数之一,它是鉴别各种氨基酸的一种根据。
参与蛋白质组成的氨基酸中色氨酸、酪氨酸和苯丙氨酸在紫外区有光吸收,这是紫外吸收法定量蛋白质的依据。
核磁共振(NMR)波谱技术在氨基酸和蛋白质的化学表征方面起重要作用。
氨基酸分析分离方法主要是基于氨基酸的酸碱性质和极性大小。
常用方法有离子交换柱层析、高效液相层析(HPLC)等。
习题1.写出下列氨基酸的单字母和三字母的缩写符号:精氨酸、天冬氨酸、谷氨酰氨、谷氨酸、苯丙氨酸、色氨酸和酪氨酸。
第三版无机化学教材课后习题答案

17. 简单说明 答
键和 π 键的主要特征是什么?
18. 试比较如下两列化合物中正离子的极化能力的大小: ① ZnCl 2 , Fe Cl2 , CaCl 2 , KCl 。 ② SiCl 4 , AlCl 答
3
, PCl 5 , MgCl 2, NaCl 。
19. 试用离子极化的观点,解释下列现象: ① AgF 易溶于水, AgCl , AgF , AgI 难溶于水,溶解度由 AgF 到 AgI 依次减小。
答
10. 下列说法是否正确?不正确的应如何改正? ( 1) ( 2) ( 3) ( 4) 答 s 电子绕核运动,其轨道为一圆周,而电子是走 主量子数 n 为 1 时,有自旋相反的两条轨道; 主量子数 n 为 4 时,其轨道总数为 16,电子层电子最大容量为 32; 主量子数 n 为 3 时,有 3s, 3p , 3d 三条轨道。 S 形的;
2
14. 已知 NO 2,CO 2,SO2 分子其键角分别为 道的杂化类型? 答
132 °, 180°, 120 °,判断它们的中心原子轨
。 15. 写出 NO ,NO ,NO 答
+
分子或离子的分子轨道式,
指出它们的键级, 其中哪一个有磁性?
16. 举例说明金属导体,半导体和绝缘体的能带结构有何区别? 答
+
试用离子键理论说明由金属钾和单质氯反应, 方向性和饱和性?
形成氯化钾的过程?如何理解离子键没有
△ H 1=83 kJ・ mol △ H2 =419 kJ・ mol
1
1
1 2
H2(g) → H(g)
△ H 3=218kJ ・ mol
1
K (g) + H K(s) + 解
有机化学第三版课后习题答案

有机化学第三版课后习题答案有机化学是化学中的一个重要分支,研究有机化合物的结构、性质和合成方法。
在学习有机化学的过程中,课后习题是一个非常重要的环节,通过解答习题可以加深对知识的理解和掌握。
本文将针对《有机化学第三版》的课后习题进行解答,帮助读者更好地学习有机化学。
第一章:有机化学基础知识1. 有机化学的定义是什么?有机化学是研究有机化合物的结构、性质和合成方法的科学。
2. 有机化合物的特点是什么?有机化合物的特点是含有碳元素,并且具有较为复杂的结构和多样的性质。
3. 有机化合物的命名方法有哪些?有机化合物的命名方法包括系统命名法、常用命名法和特殊命名法等。
4. 有机化合物的结构有哪些?有机化合物的结构包括直链、支链、环状和立体异构等。
第二章:有机化合物的化学键和立体化学1. 有机化合物中的化学键有哪些?有机化合物中的化学键包括共价键、极性共价键和离子键等。
2. 有机化合物的立体化学有哪些?有机化合物的立体化学包括手性、立体异构和对映异构等。
3. 请解释手性和对映异构的概念。
手性是指分子或离子的镜像不能通过旋转重叠的现象,分为左旋和右旋。
对映异构是指具有相同分子式、相同结构式,但不能通过旋转重叠的镜像异构体。
第三章:有机化合物的反应性1. 有机化合物的反应类型有哪些?有机化合物的反应类型包括加成反应、消除反应、取代反应和重排反应等。
2. 请解释加成反应和消除反应的概念。
加成反应是指两个或多个分子结合形成一个新的分子的反应。
消除反应是指一个分子分解成两个或多个小分子的反应。
3. 请解释取代反应和重排反应的概念。
取代反应是指一个官能团被另一个官能团取代的反应。
重排反应是指分子内部原子或官能团的重新排列而形成新的分子的反应。
第四章:有机化合物的合成方法1. 有机化合物的合成方法有哪些?有机化合物的合成方法包括加成合成、消除合成、取代合成和重排合成等。
2. 请解释加成合成和消除合成的概念。
加成合成是指通过两个或多个分子的加成反应合成目标化合物的方法。
有机化学课后答案
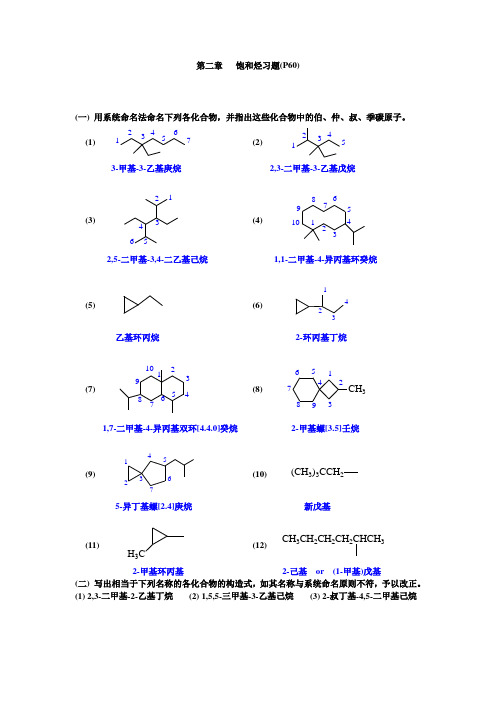
第二章饱和烃习题(P60)(一) 用系统命名法命名下列各化合物,并指出这些化合物中的伯、仲、叔、季碳原子。
(1) 1234567(2)123453-甲基-3-乙基庚烷2,3-二甲基-3-乙基戊烷(3)123456(4) 101234567892,5-二甲基-3,4-二乙基己烷1,1-二甲基-4-异丙基环癸烷(5) (6)1234乙基环丙烷2-环丙基丁烷(7)12345678910(8)123456789CH3 1,7-二甲基-4-异丙基双环[4.4.0]癸烷2-甲基螺[3.5]壬烷(9)1234567(10) (CH3)3CCH25-异丁基螺[2.4]庚烷新戊基(11)H3C (12)CH3CH2CH2CH2CHCH32-甲基环丙基2-己基or (1-甲基)戊基(二) 写出相当于下列名称的各化合物的构造式,如其名称与系统命名原则不符,予以改正。
(1) 2,3-二甲基-2-乙基丁烷(2) 1,5,5-三甲基-3-乙基己烷(3) 2-叔丁基-4,5-二甲基己烷CH 3CCHCH 3CH 3CH 3CH 2CH 32CH 2CHCH 2C CH 3CH 33CH 32H 5CH 32CH C(CH 3)333CH 32,3,3-三甲基戊烷2,2-二甲基-4-乙基庚烷 2,2,3,5,6-五甲基庚烷(4) 甲基乙基异丙基甲烷(5) 丁基环丙烷(6) 1-丁基-3-甲基环己烷CH CH 3CH 2CH 3CHCH 3CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2CH 3CH 32,3-二甲基戊烷 1-环丙基丁烷 1-甲基-3-丁基环己烷 (三) 以C 2与C 3的σ键为旋转轴,试分别画出2,3-二甲基丁烷和2,2,3,3-四甲基丁烷的典型构象式,并指出哪一个为其最稳定的构象式。
解:2,3-二甲基丁烷的典型构象式共有四种:( I )( II )( III )CH 33CH 333CH 33CH (最稳定构象)( IV )(最不稳定构象)( III )( II )CH 3CH 3H 3CH 3H3CH 3CH2,2,3,3-四甲基丁烷的典型构象式共有两种:3H 333H 33CH 333(最稳定构象)( I )( II )(四) 将下列的投影式改为透视式,透视式改为投影式。
高教版有机化学第三版答案4

(2)1,3- 丁二烯和 HBr 加成时,1,4-加成比 1,2-加成产物稳定?
(答案)
⑵平衡控制
18.用什么方法区别乙烷,乙烯,乙炔用方程式表示?
(答案)
解:
课 后 答 案 网
方程式:
19.写出下列各反应中“?”的化合物的构造式: (答案) (答案) (答案)
(答案)
CH
ΔH=? (答案)
同理: ΔHФ=EC≡C–EC=C=835.1-610-345.6=-120.5KJ/mol
(3) CH3C CH+HBr--
CH3-C=CH2 ΔH=? (答案)
ΔH=E +EH-Br-EC=C-EC-Br-EC-H =835.1+368.2-610-284.5-415.3=-106.5 KJ/mol
课 后 答 案 网
(2)CH3CH=C=CHCH3
无顺反异构体
(答案)
(3) CH3C
CCH3
(答案)
无顺反异构体
⑷ CH
C-CH=CH-CH3
(答案)
顺式 (Z) 反式(E)
5.利用共价键的键能计算如下反应在 2500C 气态下的反应热.
⑴ CH CH + Br2
CHBr=CHBr
第四章炔烃和二烯烃
1、写出 C6H10 的所有炔烃异构体的构造式,并用系统命名法命名之
课 后 答 案 网
www.khd(答案)
2、命名下列化合物:
(1) (CH3)3C
CCH2C(CH3)3
2,2,6,6-四甲基-3-庚炔
(2)C4H9-C C-CH3
(答案)
(答案)
2-庚炔
⑶ CH3CH=CHCH(CH3)C
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
作者:空青山作品编号:89964445889663Gd53022257782215002 时间:2020.12.13第一章 绪论习题参考答案1. 某化合物的分子量为60,含碳40.1%、含氮6.7%、含氧53.2%,确定该化合物的分子式。
解:① 由各元素的百分含量,根据下列计算求得实验式1:2:133.3:7.6:34.3162.53:17.6:121.40== 该化合物实验式为:CH 2O② 由分子量计算出该化合物的分子式216121260=+⨯+该化合物的分子式应为实验式的2倍,即:C 2H 4O 22. 在C —H 、C —O 、O —H 、C —Br 、C —N 等共价键中,极性最强的是哪一个?解:由表1-4可以查得上述共价键极性最强的是O —H 键。
3. 将共价键⑴ C —H ⑵ N —H ⑶ F —H ⑷ O —H 按极性由大到小的顺序进行排列。
解:根据电负性顺序F > O > N > C ,可推知共价键的极性顺序为: F —H > O —H > N —H > C —H4. 化合物CH 3Cl 、CH 4、CHBr 3、HCl 、CH 3OCH 3中,哪个是非极性分子? 解:CH 4分子为高度对称的正四面体空间结构,4个C —H 的向量之和为零,因此是非极性分子。
5. 指出下列化合物所含官能团的名称和该化合物所属类型。
CH 3OH(2)碳碳三键,炔烃 羟基 ,酚(4)COOH酮基 ,酮 羧基 ,羧酸(6) CH 3CH 2CHCH 3OH醛基 ,醛 羟基 ,醇(7) CH 3CH 2NH 2氨基 ,胺6. 甲醚(CH 3OCH 3)分子中,两个O —C 键的夹角为111.7°。
甲醚是否为极性分子?若是,用表示偶极矩的方向。
解:氧原子的电负性大于碳原子的电负性,因此O —C 键的偶极矩的方向是由碳原子指向氧原子。
甲醚分子的偶极矩是其分子中各个共价键偶极矩的向量之和,甲醚分子中的两个O —C 键的夹角为111.7°,显然分子是具有极性的,其偶极矩的方向如下图所示。
37. 什么叫诱导效应?什么叫共轭效应?各举一例说明之。
(研读教材第11~12页有关内容)8. 有机化学中的离子型反应与无机化学中的离子反应有何区别?解:无机化学中的离子反应是指有离子参加的反应,反应物中必须有离子。
(1) CH 3CH 2C CH(3) CH 3COCH 3(5) CH 3CH 2CHO而有机化学中的离子型反应是指反应物结构中的共价键在反应过程中发生异裂,反应物本身并非一定是离子。
第二章 链烃习题参考答案1. 写出分子式为C 6H 14的化合物的所有碳链异构体的构造式,并按系统命名法命名。
解:① 所有可能的碳架如下:C C C C C C C C C C CC CC C C C CC C C C C C C C C CCC② 所有异构体的构造式及名称:CH 3CH 2CH 2CH 2CH 2CH 3 CH 3CHCH 2CH 2CH 3CH 3CH 3CH 2CHCH 2CH 3CH 3己烷 2—甲基戊烷 3—甲基戊烷CH 3CH CH CH 3CH 3 C CH 2CH 3CH 3CH 3CH 3CH 32,3—二甲基丁烷 2,2—二甲基丁烷2. 写出下列化合物的结构式或名称,并指出分子中的1°、2°、3°、4°碳原子。
CH 3CHCH 2CHCH 3CH 3 C CH 3CH 3CH 3(1) 2,4—二甲基戊烷 (2) 2,2—二甲基丙烷CH 3CH 31°1°1°1°3°3°2°1°1°1°1°4°CH 3 C C CH 2CH 3CH 3CH 2CH 3CH 3CH 2CH 31°1°1°1°1°1°4°4°2°2°2°(3) 2,2—二甲基—3,3—二乙基戊烷(4) CH 3CH 2CH CHCH 2CH 3CH 3 CH CH 3CH CH 3CH 31°1°1°1°1°1°1°2°2°3°3°3°3° 2,5—二甲基—3,4—二乙基己烷CH 3(5) (CH 3CH 2)2CH CH(CH 2CH 3)23,4—二乙基己烷1°1°3°3°2°2°(6) (CH 3)3C CH C(CH 3)32,2,3,4,4—五甲基戊烷 1°1°1°4°4°3°3. 将下列化合物的结构式改写成键线式CH 3CH 3(1) CH 3 CH CH 2 CH 2 CHCH 2CH 3CH3(2) CH 3CH CHCH 2CH CHCH 2CHCH3(3) (CH 3)2CHCH 2CH 2CH(CH 2CH 3)24. 写出分子式为C 5H 10的所有开链异构体的结构式,并用系统命名法命名。
CH 2 CHCH 2CH 2CH 3C CCH 3HCH 2CH 3HC CCH 2CH 3CH 3H H1—戊烯顺—2—戊烯反—2—戊烯CH 3CH 3HCH 3CH 2 CHCHCH 3CH 3CH 2 CCH 2CH 3C CCH 33—甲基—1—丁烯2—甲基—1—丁烯2—甲基—2—丁烯5. 完成下列反应式(1) (CH 3)2CHCH CH 2 + Br 2 (CH 3)2CHCH CH 2BrCl 4BrCH 3Cl(2) CH 3CH 2C CH 2 + HCl CH 3CH 2C CH 3CH 3(3)C C2CH 3CH 3CH 3H① O 2CH 3CHO + CH 3CCH 2CH 3O(4) CH 3CH 2CH CH 2 + H 2O CH 3CH 2CH CH 3OHH +(5) CH 3CH 2C CH + HCl(过量CH 3CH 2CCl 2CH 3(6) CH 3CH 2C CH4H 2OCH 3CH 2COOH + CO 2(7) CH 3CH 2C CHCu(NH 3)2+CH 3CH 2C CCu(8)+COOHCOOH6. 用化学方法鉴别下列各组化合物 (1) 乙烷、乙烯、乙炔解答:分别将三种气体通入溴水中,不能使溴水褪色的是乙烷。
将能使溴水褪色的两种气体分别通入银氨溶液中,能使之产生白色沉淀的气体是乙炔,另一个是乙烯。
(2) 丁烷、1—丁炔、2—丁炔解答:分别将三种待测物分别与高锰酸钾酸性溶液混合,不能使高锰酸钾紫红色褪色的是丁烷。
将能使高锰酸钾褪色的两种待测物分别与银氨溶液混合,能使之产生白色沉淀的是1—丁炔,另一个是2—丁炔。
(3) 1,3—丁二烯、1—丁炔解答:分别将两种待测物与氯化亚铜氨溶液混合,能使之产生棕红色色沉淀的是1—丁炔,另一个是1,3—丁二烯。
7. 以乙炔、丙炔为原料,合成下列化合物(其他试剂任选)。
(1) 1,2—二氯乙烷HC CH + Cl 2(适量)ClCH CHCl ClCH CHCl + H 2NiClCH 2CH 2Cl(2) 异丙醇PtCH 3C CH + H 2O HgSO 4H 2SO 4CH 3CCH 3O CH 3CCH 3O+ H 2CH 3CHCH 3OH(3) 2,2—二氯丙烷CH 3C CH + 2HCl加热催化剂CH 3CCH 3ClCl(4) 乙烯基乙炔224HC CH + HC CHCH 2 CH C CH(5) 丙酮CH 3C CH + H 2OHgSO 4H 2SO 4CH 3CCH 3O(6) 苯2 [(C 653 P]23HC CH50℃ , 1.5~2MPa(7) 乙烯基乙醚碱150~180℃ , 0.1~0.5MPaHC CH + CH 3CH 2CH 2 CHOCH 2CH 38. 如何除去乙烷中含有的少量丙烯?解答:将含有少量丙烯的乙烷气体通入硫酸溶液中,其中的丙烯杂质因与硫酸发生加成反应而被吸收。
9. 丁烷和异丁烷分子中哪个氢原子最容易发生卤代反应?为什么? 解答:异丁烷分子中的叔氢原子最易发生卤代反应。
有大量实验结果表明,在取代反应中,各种类型氢原子的反应活性顺序为:3°H > 2°H > 1°H 。
10. 用杂化轨道理论简述甲烷、乙烯、乙炔的分子结构。
解答:(1) 甲烷的结构根据杂化轨道理论,甲烷分子中的碳原子采取sp 3杂化,4个价电子分别位于4个sp 3杂化轨道中。
4个sp 3杂化电子云在空间呈正四面体排布,各个sp 3杂化电子云的大头分别指向四面体的四个顶点。
C 与H 成键时,4个H 原子的s 电子云沿着4个sp 3杂化电子云的大头重叠形成4个s-sp 3σ键,因此形成的甲烷分子是正四面体型的,键角为109°28/ 。
(2)乙烯的结构乙烯分子中的碳原子采取sp 2杂化,4个价电子中有3个分别位于3个sp 2杂化轨道中,1个位于2p 轨道中。
3个sp 2杂化电子云在空间呈平面三角形分布,各sp 2杂化电子云的大头指向三角形的3个顶点,2p 电子云对称轴垂直穿过3个sp 2杂化电子云所在的平面。
11. 乙烯和乙炔都能使溴水褪色,两者的反应速度有何区别?为什么会有此不°同?解答:乙烯使溴水褪色的速度较乙炔的快。
乙炔碳碳键长(0.120nm )较乙烯碳碳键的键长(0.133nm )短,因此乙炔分子中的π键较乙烯的π键稳定,反应活性低、反应速度慢。
12. 乙烯既能使高锰酸钾溶液褪色,也能使溴水褪色。
这两个实验的本质有无区别?作者:空青山作品编号:89964445889663Gd53022257782215002 时间:2020.12.13解答:这两个实验有着本质的区别,乙烯使高锰酸钾溶液褪色是因为乙烯与高锰酸钾发生了氧化还原反应,乙烯使高锰酸钾还原而褪色;乙烯使溴水褪色是因为乙烯与溴发生了加成反应,生成了无色的溴代烷烃。
13. 写出分子式C 4H 6的开链构造异构体的结构式,并用系统命名法命名。
CH 3CH 2C CH CH 2 CH CH CH 2CH 3C CCH 3CH 2 C CHCH 31—丁炔 2—丁炔 1,3—丁二烯 1,2—丁二烯14. A,B 两化合物的分子式都是C 6H 12 ,A 经臭氧化并与锌和酸反应后的乙醛和甲乙酮,B 经高锰酸钾氧化只得丙酸,写出A 和B 的结构式。
