高中人教版化学必修一学案:2-1-1 物质的分类(附答案)
高中-化学-人教版-高中化学必修一2.1.1简单分类法及其应用 导学案(含答案)

第二章化学物质及其变化第一节物质的分类(第一课时简单分类法及其应用)【学习目标】1.通过讨论交流、小组讨论、思考交流,尝试进行简单分类,体会分类的目的和意义。
2.通过阅读教材、归纳小结,认识交叉分类法和树状分类法,知道两种分类法的特点。
从不同层次认识物质的多样性及元素可以组成不同种类的物质,能根据物质的组成和性质对物质进行分类。
3.通过练习书写、思考讨论、图示表示、分类开发,进一步理解单质、氧化物、酸、碱、盐的概念。
能从物质类别的角度认识同类物质具有相似性,一定条件下物质可以相互转化。
【学习重点】根据组成和性质对化学物质进行分类。
【学习难点】分类的思想的建立及其应用。
【自主学习】旧知回顾:现有下列物质:①NaCl②HCl③CaCl2④CuO⑤H2O⑥Fe2O3 ⑦盐酸⑧漂白粉(含有次氯酸钙和氯化钙等)⑨SO3⑩NO。
其中常温为固体物质的是①③④⑥⑧、为液体的纯净物是⑤、为气体的物质是②⑨⑩、含有氯元素的化合物是①②③、属于氧化物的是④⑤⑥⑨⑩、属于盐的是①③、属于碱性氧化物的是④⑥。
新知预习: 1.化学研究的对象是物质及其变化,分类是学习和研究化学物质及其变化的一种常用的科学方法。
对事物进行分类时,事先一般要设定分类的标准。
当分类标准确定之后,同类中的事物在某些方面的相似性可以帮助我们做到举一反三;对于不同类事物的了解可以使我们有可能做到由此及彼。
这就是分类法作为科学方法的意义。
2.HNO3既属于一元酸又属于含氧酸,这种分类方法是交叉分类法,化合物可以分为氧化物、酸、碱、盐等,这种分类方法是树状分类法。
【同步学习】情景导入:当我们来到一个陌生的大型商场购物时,面对琳琅满目、品种繁多的商品,我们是如何快速地找到自己所需要的商品的?一、简单分类法及其应用活动一、物质分类标准1.讨论交流:举出生活中一些应用分类法的例子,思考对它们分类的目的和意义。
【温馨提示】如图书馆中的图书分类收藏,大型商场中的物品分类,电脑中的文件分类等等。
化学人教版高中必修1高中化学必修一【2-1】(教案 习题 答案)
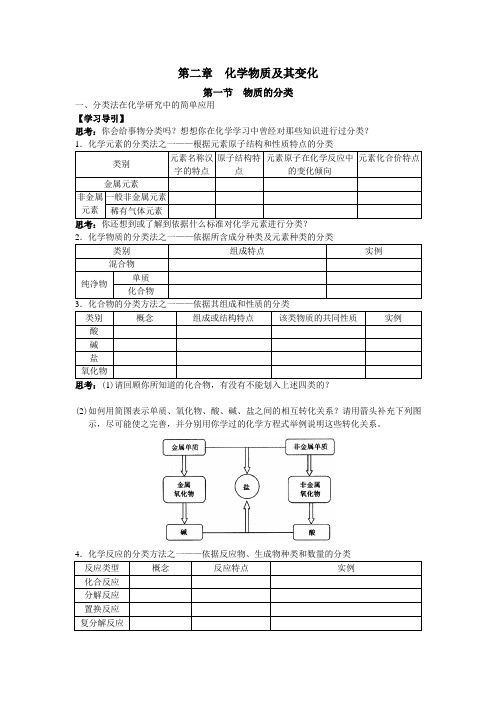
第二章化学物质及其变化第一节物质的分类一、分类法在化学研究中的简单应用【学习导引】思考:你会给事物分类吗?想想你在化学学习中曾经对那些知识进行过分类?思考:你还想到或了解到依据什么标准对化学元素进行分类?(2)如何用简图表示单质、氧化物、酸、碱、盐之间的相互转化关系?请用箭头补充下列图示,尽可能使之完善,并分别用你学过的化学方程式举例说明这些转化关系。
思考:请回顾你所学习过的化学反应,有没有不能划入上述四类的?你还知道哪些反应的分类方法?思考:分类法对化学学习有何帮助?请同学们思考、讨论课本24页的实践活动3。
【同步训练】1.与碱反应只生成盐和水的氧化物,叫做酸性氧化物,酸性氧化物也叫酸酐。
下列化合物中,属于硝酸的酸酐的是( )A.N2O3B.N2O4C.NO2D.N2O52.下列生活中的物质,可看作纯净物的是( )A.煤B.生铁C.蒸馏水D.矿泉水3.从元素组成上看,酸和碱的共同点是( )A.都含有原子团B.都含氧元素C.都含有氢元素D.都含有金属元素4.CO2、NO、H2O三者同属于下列的( )A.酸性物质B.碱性物质C.氧化物D.非金属元素5.下列各组物质中,硫元素的化合价相同的一组是( )A.H2S和SO2B.Na2S和SC.SO2和Na2SO4D.SO2和Na2SO36.下列物质中,不能和二氧化碳发生化合反应的是( )A.水B.生石灰C.氧气D.木炭7.对下列化学仪器进行分类:①试管,②酒精灯,③坩埚钳,④烧杯,⑤铁架台,⑥蒸发皿,⑦试管夹,⑧试剂瓶。
若把①②④⑧归入一类,则这一类仪器的共同特点是( ) A.可被加热B.玻璃制品C.量器D.颜色一样8.下列物质间的反应,一定不能生成盐的是( )A.酸与金属氧化物反应B.金属与氧气化合C.单质与化合物的置换反应D.盐与盐反应9.HCl、NaOH、NaCl具有的共同点是( )A.使石蕊溶液变色B.使酚酞溶液变色C.都含有Cl元素D.都是化合物10.连线题:请把左栏中的物质与右栏中其所属类别之间进行连线物质所属类别H2SO4含氧酸H2S无氧酸HCl一元酸HNO3多元酸11.很多食品包装中常常有一个小纸袋,内盛白色固体物质,标称“干燥剂”,其主要化学成分为生石灰。
人教版高中化学必修一学案《2-1 物质的分类》(第1课时)

第二章第一节物质的分类第1课时【学法指导】:仔细阅读教材第二章第一节内容,按要求自学【学习目标】:了解分类方法;了解分散系的概念;掌握分散系的分类方法和胶体的概念;【学习重点】:胶体的性质;【学习难点】:胶体的性质;【自学过程】:一、简单分类法和应用1、分类法便于我们对同类事物举一反三,在认识事物时采用多种分类方法,如_______________;在对同类事物进行再分类常采用____________________。
2、参考教材图2-2,将NaCl、Na2CO3、KCl、K2CO3进行分类,将分类结果写入右侧方框内:3、补充完善教材图2-3,举实例填入空格:单质:________、________;氧化物:________、_______;酸:________、_________;碱:________、__________;盐:_______、__________;混合物:__________、__________;二、分散系及其分类1、定义:分散系是把_______________________________________________________________所得到的体系;分散质属于________的物质,分散剂是起________作用的物质;例如,将NaCl 溶解到水中,NaCl是_________,水是________,得到的NaCl溶液时_________;再如粉尘漂浮在空气中,粉尘是________,空气是________。
2、分类:①按照________________________________可以有9种组合方式;②当分散剂是水或其他液体时,按分散质粒子的大小来分可以分为_________(粒子小于1nm)、________(粒子大于100nm)、__________(粒子____________)。
三、胶体1、外观:溶液均一透明,浊液浑浊,有些胶体也是均一透明的。
人教版高中化学必修一物质的分类导学案(含答案)

人教版(2019)高中化学新教材选择性必修1导学案1.1 物质的分类及转化第1课时物质的分类预习案一、物质的分类1、元素:元素是具有相同(即质子数)的一类原子的总称。
2、分子:能够独立存在并保持物质化学性质的最小微粒,由原子构成,呈电中性,具有一定的物理化学性3、同素异形体:同种元素形成的不同叫同素异形体。
形成方式:①,如O2和O3;②,如金刚石和石墨。
4、纯净物:由同种组成的物质。
5、混合物:由几种不同的单质或化合物组成的物质。
6、单质:由同种元素组成的称为单质,包括金属单质和非金属单质。
7、化合物:由组成的纯净物称为化合物,包括酸、碱、盐、氧化物等。
8、分类的方法(1)树状分类法:根据对象的共同点和差异,将对象分为不同的种类,而且形成具有一定从属关系的不同等级系统的一种分类方法。
应用树状分类法可以对同类事物进行再分类。
(2)交叉分类法:根据不同的分类标准对同一物质进行分类的一种方法。
在对物质进行分类时,采用交叉分类法能从不同角度对物质进行较全面的分析。
二、分散系与胶体的制备11、分散系:一种(或多种)物质分散到另一种(或多种)物质中所得到的体系,叫做分散系。
被分散的物质称为分散质,起容纳分散质作用的物质称为分散剂。
2、胶体的提纯:由于胶体粒子较大不能透过半透膜,而离子、小分子较小可以透过半透膜,利用此性质可以将胶体提纯。
3、胶体的制备(1)物理方法:研磨法。
如制豆浆。
(2)化学方法:利用水解反应、复分解反应等。
FeCl3+3H2O Fe(OH)(胶体)+3HClKI+AgNO3AgI(胶体)+KNO3探究案1、常见的混合物举例:①气体混合物②液体混合物③固体混合物2、常见物质的俗名3、分散系的分类分析指出下列分散系各自的分散质、分散剂,比较分散质、分散剂的存在状态4、溶液、胶体、浊液的比较限时训练案1.朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”。
高一化学人教版必修1教案:2.1物质的分类+

并进行比较前者:后者:
6、胶体的分类:
(1)、液溶胶:氢氧化铁胶体、碘化银胶体等
(2)、气溶胶:云、雾、烟尘等
(3)、固溶胶:红宝石、蓝宝石、土壤胶体等
7.胶体的性质
(1)渗析
应用
(2)丁达尔效应:的现象。
丁达尔效应的应用:利用丁达尔效应可以
比如:雾天行驶的汽车的灯光、早晨树林中出现阳光的光路、扫地时扬起灰尘,阳光从窗户射入,也会看到一条光柱,光柱中还可清晰地看见小灰尘在飞舞等。
(3)布朗运动:胶体的粒子可以做无规则的杂乱无章的运动。
(4)电泳现象:在外加电场的作用下,胶体的微粒在分散剂里向阴极(或阳极)作定向移动的现象。
原因:胶粒带有电荷(胶粒表面积很大,吸
附能力很强,能选择性地吸附溶液中的离子而带有电荷)。
说明:①电泳现象表明胶粒带电荷,但胶体都是电中性的。
②一般来说,金属氢氧化物、金属氧化物的胶体微粒吸附阳离子,带
正电荷,如Fe(OH)3胶体和Al(OH)3胶体微粒。
非金属氧化物、金属硫化物胶体微粒吸附阴离子,带负电荷,如As2S3
胶体、H2SiO3胶体的微粒。
③同种胶体的胶粒带相同的电荷。
④固溶胶不发生电泳现象。
凡是胶粒带电荷的液溶胶,通常都可发生电
泳现象。
气溶胶在高压电的条件也能发生电泳现象。
(4)胶体的凝聚:胶体是一种比较稳定的分散系。
由于胶体粒子可以通过吸附而带电荷,同一种胶粒带有相同的电荷,它们之间的相互排斥使得脱粒不容易聚集,胶粒所作的布朗运动也使胶粒不容易聚集成较大的颗粒而沉降。
但如果给予。
高一化学人教版必修1全册学案(附答案)

高一化学人教版必修1全册学案(附答案)本资料为woRD文档,请点击下载地址下载全文下载地址第二章化学物质及其变化教材分析一、本章内容概述本章包括物质分类法、胶体、电解质与离子反应、氧化还原反应基础四部分内容。
把物质分类法作为化学知识单独来教,在中学化学教学历史上是首次,体现了新课程的一种精神——学科教学不再单为学科发展服务,更关注学生综合素养的发展和提高。
胶体是从混合物(分散系)的分类切入的。
其实大家都清楚,胶体这部分知识相对比较独立,历史上教材编写者曾经分别尝试把它“掺杂”在元素化学(硅、胶体)中、置于高中化学最后(第3册选修中单独成为一个单元)。
现在又尝试把它置于高中化学的起始位置,努力实现尽快地与初中化学溶液部分的对接,也不失为一种有益的尝试。
离子反应、氧化还原反应是学习分类法后,从不同的视角对化学反应进行分类的具体应用。
二、本章在中学化学中的地位与作用本章在学科内容方面是同学们认识化学科学的起始章,具有非常重要的作用;为整个高中阶段的化学学习奠定重要的基础。
因此本章在全书中占有特殊的地位,具有重要的功能,是整个高中化学的教学重点之一。
.与初中的衔接作用与第1章相比,本章知识的衔接意义更大。
本章知识的每一部分,都可以在初中化学中找到它的“根”。
如前所述,有的是运用和巩固初中基础知识(元素与物质分类);有的属于对初中知识体系的补充(胶体对分散系概念的补充完善);有的属于初中知识的延伸发展(电解质是在电离概念的基础上提出的);而有的属于对初中基础概念的深入发展、提升、统一。
2.基础性、工具性作用物质分类法属于进一步学习化学的方法性工具;氧化还原反应、离子反应属于进一步学习元素化合物知识的学科工具,是学生深入认识化学反应本质的基础性知识。
3.值得注意的问题学习本章知识时要注意新旧知识的联系于对比,通过分析熟悉的物质,逐渐认识到有限的因素与庞大的物质家族之间的关系;同时应注意知识的迁移与和运用,通过对熟悉的物质及化学反应的分析,学会分析问题解决问题,并归纳总结出新概念的思路和方法。
人教版高中化学必修一2-1-1物质的分类.docx

高中化学学习材料一、选择(每题有1~2正确选项)1.下列各组物质,前者是单质后者为混合物的是()A.白糖、冰水混合物 B.铁粉、食醋 C.干冰、食盐 D.盐酸、空气2.按单质、氧化物、酸、碱、盐分类,下列各组物质中,两种物质类别相同的是()A.氧气、氧化镁 B.硫酸铜、氯化钠C.硫酸、碳酸钠 D.硝酸银、氢氧化钠3.下列各组中,前者属于后者的是()A.化合物、单质 B.元素、原子 C.氧化物、化合物 D.纯净物、化合物4.选项中的物质与其他不同的是()A.Fe B.Na C.Ag D.Si5.下列各组中的物质,按酸、碱、盐、氧化物分类属于同一类的是()A.Na、K2O、HNO3 B.CO2、CaCO3、NaOHC.SO2、SO3、H2SO4 D.NaOH、Mg(OH)2、Cu(OH)26. 下列各组,可用交叉分类法进行分类的是()A.Na2CO3、Na2SO4、K2CO3、K2SO4B.碳酸钙、氯化钙、纯碱、氯化钠C.干冰、一氧化碳、石墨、金刚石D.氢气、盐酸、苛性碱、小苏打7. 下列反应进行分类时(按初中的方法),既属于氧化反应又属于化合反应的是()A.Zn+H2SO4=ZnSO4+H2↑B.2KClO32KCl+3O2↑C.S+O2SO2D.H2+Cl22HCl8.下列反应既不属于化合或分解反应,也不属于置换或复分解反应的是()A. CH4 + 2O2=CO2 + 2H2O B.C + H2O(气)=CO + H2C.Cu2(OH)2CO3=2CuO + CO2 ↑+ H2O D.FeCl3 + 3NaOH=Fe(OH)3↓+ 3NaCl9.下列四个反应中有一个与其它三个不同,它是()A. 2Fe(OH)3 = Fe2O3 + 3H2O B.CaCO3 = CaO + CO2↑C.2NaHCO3 =Na2CO3 + CO2↑+ H2O D.2HCl+Ba(OH)2=BaCl2+2H2O10.关于物质分类正确的组合是()分类碱酸盐碱性氧化物酸性氧化物A Na2CO3H2SO4NaOH SO2CO2B NaOH HCl NaCl Na2O COC NaOH CH3COOH CaF2 CO SO2D KOH HNO3 CaCO3CaO SO311.下列反应属于化合反应的是()①Fe+S=FeS ②CaO+CO2=CaCO3 ③Fe+CuSO4=FeSO4+Cu④2HCl+CaCO3=CaCl2+H2O+CO2↑⑤4Fe(OH)2+O2+2H2O=4 Fe(OH)3A.①②③B.②③④C.③④⑤D.①②⑤12. 某物质经分析知,其中仅含一种元素,此物质()A、可能是纯净物也可能是混合物B、可能是单质也可能是化合物C、一定是纯净物D、一定是一种单质13、给物质分类时由于标准不同往往会出现()A.树状分类法B.环状分类法C.球状分类法D.交叉分类法14、人们把球分成篮球、排球、羽毛球等属于 ( )A.树状分类法B.环状分类法C. 球状分类法D.交叉分类法15、给物质分类的好处在于 ( )A.有利于认识事物B.有利于弥补事物的先天不足C.有利于人们开拓视野D. 有利于发现物质的有关规律,把握物质的本质属性和内在联系16、Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是()A.Na2CO3是碱B.Na2CO3是盐 C.Na2CO3是钠盐 D.Na2CO3是碳酸盐17、下列物质中既属于无机物,又属于酸的是()A.CH3CH2OH B.NaHSO4 C.CH3COOH D.H2SO418、下列物质①水、②空气、③硫酸、④碘酒、⑤NaHCO3、⑥CaO,其中属于混合物的是()A ①、②B ②、③C ②、④D ⑤、⑥二、非选择题1、(1)下列两组物质:①CO2、P2O5、CaO、SO2,②Cu、Mg、Zn、Al每组中有一种物质在某些化学性质或分类上与其他几种物质不同,这两种物质是①________,②________(2)在标准状况下,6.72LCH4和CO的混合气体的质量为6g,该混合气体中有__ mol的CH4,___ _g的CO。
2021-2022学年人教版高中化学必修一课堂学案:2.1物质的分类 第1课时 Word版含答案

第一节物质的分类第1课时简洁分类法及其应用[学习目标定位] 1.学会物质分类方法,会依据不同标准对物质进行分类。
2.生疏酸、碱、盐、氧化物等之间的转化关系。
3.了解分类的意义及应用。
一、物质的分类方法1.对物质进行分类,首先要确定分类的标准,然后按标准进行分类。
例如对下列化合物进行分类:①NaCl ②HCl③CaCl2④CuO ⑤H2O ⑥Fe2O3(1)依据通常状况下物质的存在状态为标准,可分为固体:①③④⑥、液体:⑤、气体:②。
(2)依据物质的元素组成为标准,可分为氯化物:①②③、氧化物:④⑤⑥。
(3)依据物质的组成和性质为标准,可分为酸:②、盐:①③、氧化物:④⑤⑥。
2.试从不同的角度对下列各组物质进行分类,将其类别名称分别填在相应的空格内。
3.有下列十种物质:①草木灰②纯碱③金刚石④苛性钠⑤生石灰⑥硫酸⑦碘酒⑧食盐⑨金属钠⑩O2和O3的混合气体。
回答下列问题:(1)只有一种元素组成的是③⑨⑩;只有两种元素组成的是⑤⑧。
(2)属于混合物的是①⑦⑩;属于纯洁物的是②③④⑤⑥⑧⑨。
(3)属于单质的是③⑨;属于化合物的是②④⑤⑥⑧。
(4)属于酸的是⑥;属于碱的是④;属于盐的是②⑧。
物质的分类方法(1)单一分类法:选定某一标准,对物质进行分类。
对于同一组物质,选用不同的分类标准,其分类结果不同。
(2)交叉分类法:用多种不同的单一分类法对物质进行分类。
(3)树状分类法:接受树状形式对同类物质进行再分类。
如依据物质的组成和性质分类:物质⎩⎪⎪⎨⎪⎪⎧纯洁物⎩⎪⎨⎪⎧单质⎩⎪⎨⎪⎧金属单质非金属单质化合物⎩⎪⎨⎪⎧氧化物酸碱盐混合物1.请按下列线索提示画出Fe、Cu、S、H2、HCl、NaOH、H2SO4、Ba(OH)2、NaHCO3、K2O、CuO、NaCl的树状分类图:答案Fe、Cu S、H2HCl、H2SO4NaOH、Ba(OH)2NaCl、NaHCO3K2O、CuO解析要正确填写树状分类图,必需首先明确各物质的组成和性质差异。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1、 分类是把____________________物体归类到一起的方法。
2、 对于若干种同样的物质,若分类的依据不同,则得到的分类结果_______________。
3、 运用分类的方法不仅能使有关化学物质及其变化的知识_________,还可以分门别类的
研究,发现物质变化的规律。
4、分类方法有_________________和__________________。
把以下物质分类:
H 2,CaO ,Ba(OH)2, Fe 2O 3,Al ,浑浊的河水,
CH 3CH 2OH ,NH 3·H 2O ,Ar ,NaHSO 4,Cu(OH)2,HCl ,HNO 3,H 2SO 4,CO 2,H 3PO 4,NaOH , CuSO 4,Cu 2(OH)2CO 3,NaHCO 3,空气,盐酸,CO ,CH 4,H 2CO 3,MgCl 2,MgSO 4
(1)属于单质的是:________________________________________________;
(2)属于稀有气体的是:___________________________________________________;
(3)属于有机化合物的是:_________________________________________________;
(4)属于氧化物:_________________________________________________________;
(5)属于酸:_____________________________________________________________;
(6)属于碱:_____________________________________________________________;
(7)属于盐:_____________________________________________________________;
(8)属于混合物:_________________________________________________________
氧化物分为:金属氧化物和非金属氧化物等。
1、酸:___________________________________________________________
二元酸 例子:______________________________________ 三元酸 例子:______________________________________ 一元酸 例子:______________________________________ 强酸 例子:______________________________________ 中强酸
例子:______________________________________
2、碱:____________________________________________________________
3、盐:电离时生成的阳离子是金属离子或(NH4+),阴离子是酸根离子的化合物。
盐分正盐,酸式盐,碱式盐等。
①正盐:电离时生成的阳离子是金属离子(或NH4+),阴离子是酸根离子的盐。
例子:__________________________________________________
②酸式盐:电离时生成的阳离子除金属离子(或NH4+)外还有H+,阴离子是酸根离子的盐。
例子:_____________________________________________________
③碱式盐:电离时生成的阳离子是金属离子(或NH4+),阴离子除酸根外还有OH-的盐。
例子:Cu2(OH)2CO3(碱式碳酸铜)
如交叉分类法:(课本24页)
[课堂练习2] 把以下的物质和分类用短线连起来。
物质分类
BaSO4可溶
NaOH 难溶
Na2SO4盐
Mg(OH)2碱
[课堂练习3]
把以下物质分类(酸:按酸性强弱再细分;碱按可溶性再细分)
H2SO4,NaOH,NH4HCO3,P2O5,Ba(OH)2,HNO3,NH4Cl,Mg(OH)2,KOH,NH3·H2O,CH3COOH,,HCl,H,Cu(OH),CaO,Fe(OH),Cu,H
物质的分类1第一课时学案答案:
一:
1.某些特征相似的
2.也不同
3.系统化
4.交叉分类法树状分类法
课堂练习
(1)H2 Al Ar
(2)Ar
(3)CH3CH2OH CH4
(4)CaO Fe2O3CO2CO
(5)HCl HNO3H2SO4H3PO4H2CO3
(6)Ba(OH)2Cu(OH)2NaOH NH3·H2O
(7)NaHSO4CuSO4Cu2(OH)2CO3NaHCO3MgCl2MgSO4(8)空气盐酸浑浊的河水
二:
1、在水溶液中电离生成的阳离子全部是H+的化合物
HNO3 HCl CH3COOH
H2SO4H2CO3 H2SO3
H3PO4
HCl HNO3H2SO4
H3PO4H2SO3
H2CO3CH3COOH
2、在水溶液中电离生成的阴离子全部是OH-的化合物
3、①Na2SO4
②NaHSO4NaHCO3NaHSO3
课堂练习3
氧化物:P2O5SO2H2O CaO
酸强酸:H2SO4HNO3HCl
中强酸:H3PO4
弱酸:H2CO3CH3COOH
碱可溶性碱:NaOH Ba(OH)2KOH NH3·H2O
不可溶性碱:Mg(OH)2Cu(OH)2Fe (OH)3
盐:NH4HCO3NH4Cl Cu2(OH)2CO3。
