碳载铂、钌催化剂对甲醇燃料电池阳极电催化性能的研究实验报告
生物甲醇燃料电池材料研究与性能优化

生物甲醇燃料电池材料研究与性能优化生物甲醇燃料电池是一种利用生物甲醇作为燃料的电池,其研究和性能优化一直是能源领域的热门话题。
本文将从材料研究和性能优化两个方面进行讨论。
一、材料研究生物甲醇燃料电池的核心是电极材料,其中阳极和阴极材料的选择对电池性能有着重要影响。
目前常用的阳极材料包括铂、铂合金和碳基材料等,而阴极材料则主要采用氧化物如二氧化铈、二氧化锆等。
在阳极材料方面,铂是一种优良的催化剂,但其昂贵的价格限制了生物甲醇燃料电池的商业化应用。
因此,研究人员致力于寻找替代材料,如过渡金属氧化物、过渡金属硫化物和非贵金属催化剂等。
这些材料具有较高的催化活性和较低的成本,可有效替代铂。
在阴极材料方面,氧化物是目前最常用的材料之一。
然而,氧化物在高温下容易发生晶格氧化、析氧和结构破坏等问题,导致电池寿命较短。
因此,研究人员正在探索新型阴极材料,如过渡金属氧化物的复合材料、过渡金属硫化物和有机金属框架材料等。
这些材料具有更好的稳定性和催化活性,能够提高生物甲醇燃料电池的性能和寿命。
二、性能优化除了材料研究外,性能优化也是生物甲醇燃料电池研究的重要方向之一。
性能优化主要包括提高电池的能量转化效率和减小电池的内阻。
提高能量转化效率是生物甲醇燃料电池研究的关键问题之一。
目前,研究人员通过改变电极结构、优化催化剂分散度和提高电子传输速率等方法来提高电池的能量转化效率。
此外,改进燃料供应系统和优化电解质的选择也可以有效提高能量转化效率。
减小电池的内阻是提高电池性能的另一个重要方面。
内阻主要包括电解质阻抗、电极/电解质界面阻抗和电子传输阻抗等。
研究人员通过优化电极材料的导电性能、改善电解质的离子传输速率和减小电极/电解质界面的电阻等方法来减小电池的内阻,从而提高电池的性能。
此外,研究人员还通过改进电池的结构、优化电池的工作温度和提高电池的稳定性等方法来进一步优化生物甲醇燃料电池的性能。
总结起来,生物甲醇燃料电池材料研究和性能优化是一个复杂而又关键的问题。
铂基催化剂在甲醇燃料电池中的应用研究

铂基催化剂在甲醇燃料电池中的应用研究甲醇燃料电池(Methanol Fuel Cell,简称MFC)作为一种新型的绿色能源技术,近年来备受关注。
而铂基催化剂作为MFC中重要的组成部分,其性能直接影响着MFC的效率和稳定性。
因此,对铂基催化剂在MFC中的应用进行深入研究具有重要意义。
首先,我们来了解一下MFC的基本原理。
MFC是一种利用甲醇和氧气反应产生电能的装置,其基本原理是利用催化剂促进甲醇的氧化反应和氧气的还原反应。
而铂基催化剂作为一种高效的催化剂,可以加速这两个反应的进行,从而提高MFC的能量转换效率。
然而,铂基催化剂在MFC中存在一些问题。
首先,铂是一种稀有金属,价格昂贵,限制了MFC的商业化应用。
其次,铂基催化剂在长时间运行过程中容易发生结构变化和中毒现象,降低了催化活性和稳定性。
因此,研究如何降低铂基催化剂的用量、提高其稳定性和延长使用寿命成为了当前研究的热点。
一种解决铂基催化剂稀有和昂贵问题的方法是合成非铂基催化剂。
近年来,研究人员开展了大量的工作,成功合成了一系列具有优异电催化性能的非铂基催化剂。
例如,以过渡金属氧化物、氮化物和硫化物等为主要成分的非铂基催化剂,具有较高的催化活性和良好的稳定性。
这些非铂基催化剂的研究为降低铂基催化剂的用量提供了新的思路。
另一方面,为了解决铂基催化剂在长时间运行过程中的结构变化和中毒问题,研究人员提出了一系列改性策略。
例如,通过调控铂基催化剂的形貌和晶相结构,可以提高其稳定性和抗中毒能力。
此外,也可以将铂基催化剂与其他材料进行复合,形成新的催化剂体系。
这些改性策略的研究为提高铂基催化剂的稳定性和延长使用寿命提供了新的途径。
除了合成非铂基催化剂和改性策略,还有一些其他的研究方向也值得关注。
例如,研究人员可以通过调控甲醇燃料电池的工作条件,如温度、压力和甲醇浓度等,来优化铂基催化剂的催化性能。
此外,也可以通过改变甲醇的供给方式,如直接注入或间接供给等,来提高铂基催化剂的利用效率。
炭载Pt-Ag双金属催化剂对甲醇氧化反应的电催化

2 结果与讨论
2 . 1 催化剂的形貌及晶体结构表征 图1 A和 1 B为典型的 P t A g / C和 P t A g / C样品的 T E M 图。由图 1可见, 球形纳米颗粒均匀分散 0 . 1 0 . 5 于炭载体表面, 没有明显的团聚现象。颗粒的平均尺寸通过统计平均获得, 对于每一个样品统计的颗粒 数目均大于 3 0 0 。P t A g / C和 P t A g / C样品的颗粒尺寸分别在( 5 1± 0 6 )n m 和( 5 4± 0 7 )n m , 其 0 . 1 0 . 5 尺寸分布柱状图如图 1 A ′ 和1 B ′ 所示, 其它 P t g / C样品的颗粒尺寸均在 5 0~ 6 0n m之间。 mA 图 2为系列 P t g / C样品的 X R D谱。从图 2可以看出, 4种催化剂样品均呈现面心立方晶体结构, mA 各特征衍射峰( 1 1 1 ) 、 ( 2 0 0 ) 、 ( 2 2 0 ) 和( 3 1 1 ) 均处于纯 A g ( 2 为3 8 1 ° 、 4 4 2 ° 、 6 4 4 ° 和7 7 4 ° ) 和纯 P t ( 2 θ θ 为3 9 8 ° 、 4 6 2 ° 、 6 7 4 ° 和8 1 2 ° ) 样品的特征衍射峰之间, 表明样品中存在 P t A g 合金纳米结构。选取 ( 2 2 0 ) 晶面特征峰, 通过 S c h e r r e r 公式计算了各样品的晶粒尺寸均在 5 0~ 6 0n m之间, 与T E M 照片得 到的颗粒尺寸相当。
第3 0卷 第 1期 2 0 1 3年 1月
应用化学 C H I N E S EJ O U R N A LO FA P P L I E DC H E M I S T R Y
直接甲醇燃料电池用碳气凝胶载铂催化剂的研究

h a t l i n i r o e re o t u p r n c r o eo e w r b ev d b E T eee to i ai - T e p ri e s ea d t eds e in d g e f e s p o tdo ab na r g l e eo s re y T M . h lco xd t n ma c z h ps l e o t e o w se au td b y l otmmer . e rs l s o st a : o e s e d s b t n o a b n a r g li r te e t l h n l a v lae y c c i v l c a t T e ut h w h t p r i i r ui fc r o eo e s ah rc n r - yh z t i o a
Zh n n Zh n Ka g Xio o g Z a g S e g h n a g Ni g u Ho g n ahn hn hn seg
( col f c ne B in o m n ao nvrt, eig10 4 ) Sho o i c , eigcm u i tnU i sy B in 0 04 Se j ci ei j
ie t e at l ie o t i rt e mal a d wel ip re Th z d,h p ri e sz f P s ah r s l n l s es d. e CV lt h ws h tP /c ro e le h bt h g e c d p o s o ta t a b n a mg x i i ih r c tlt ciiy ta t . aayi a t t h n P /C c v K e wo  ̄ y r drc t a o u lc l c r o eo e p r ie dsrb t n ie tmeh n lf e el s a b n a rg l oe sz it ui i o
铂催化剂在燃料电池上的应用研究

铂催化剂在燃料电池上的应用研究随着全球对环保和新能源的需求日益增长,燃料电池技术作为一种环保、高效的新型能源技术,受到了越来越多的关注。
而铂催化剂在燃料电池上的应用是其中非常重要的一部分内容,因为它起到了催化剂的作用,能够促进电化学反应,使燃料电池的效率和寿命都得到了极大的提高。
一、铂催化剂的基本原理铂催化剂是将铂纳米粒子嵌入各种载体中形成的一类材料,外形看起来像黑色或者灰色的粉末。
它的主要作用就是在燃料电池中提供一个催化剂的平台,使得电解过程能够更加高效地进行。
铂催化剂一般放置在燃料电池的阳极和阴极之间,可以扶持燃料和氧气之间的电化学反应,促进电子的传输和离子的交换。
二、铂催化剂在燃料电池上的应用铂催化剂在燃料电池上的应用非常广泛,其中最常见的就是作为燃料电池的阴极和阳极催化剂。
燃料电池的裂解过程中,需要将氢气、甲烷等燃料转化为电能,所以需要催化剂促进这些化学反应。
在这个过程中,阴极和阳极中的铂催化剂分别扮演着不同的角色。
在燃料电池的阴极催化剂中,铂通过激发氧气中的电子,使其与水的氢离子结合,产生水的同时,释放出电子。
电子被输送到电路中,形成电流,从而驱动载体进行工作。
而在燃料电池的阳极催化剂中,铂则可以将燃料的氢离子和电子结合在一起,从而形成水和电力。
除了在阴极和阳极中的催化剂,铂催化剂还可以用来增强燃料电池的稳定性和耐久性。
在传统的燃料电池中,存在着催化剂的失活现象,即铂颗粒随着时间的推移逐渐脱落或者氧化,使得燃料电池的效果会逐渐减弱。
但是,通过在铂催化剂表面进行修饰,可以增强铂与载体之间的粘合能力,从而减少铂颗粒的脱落和氧化,提高燃料电池的耐久性。
三、铂催化剂在燃料电池中的发展历程铂催化剂作为燃料电池的重要组成部分,其发展历程也非常值得关注。
早在20世纪80年代,铂催化剂就已经被广泛应用在燃料电池的电化学反应中。
但是,由于其高成本、不稳定等局限性,使得铂催化剂应用的范围受到了很大的限制。
介孔碳化钨提高铂电催化氧化甲醇活性
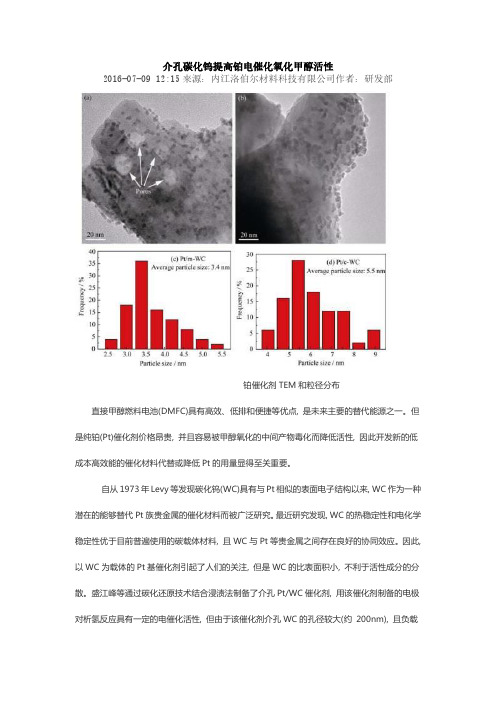
介孔碳化钨提高铂电催化氧化甲醇活性2016-07-09 12:15来源:内江洛伯尔材料科技有限公司作者:研发部铂催化剂TEM和粒径分布直接甲醇燃料电池(DMFC)具有高效、低排和便捷等优点, 是未来主要的替代能源之一。
但是纯铂(Pt)催化剂价格昂贵, 并且容易被甲醇氧化的中间产物毒化而降低活性, 因此开发新的低成本高效能的催化材料代替或降低Pt的用量显得至关重要。
自从1973年Levy等发现碳化钨(WC)具有与Pt相似的表面电子结构以来, WC作为一种潜在的能够替代Pt族贵金属的催化材料而被广泛研究。
最近研究发现, WC的热稳定性和电化学稳定性优于目前普遍使用的碳载体材料, 且WC与Pt等贵金属之间存在良好的协同效应。
因此, 以WC为载体的Pt基催化剂引起了人们的关注, 但是WC的比表面积小, 不利于活性成分的分散。
盛江峰等通过碳化还原技术结合浸渍法制备了介孔Pt/WC催化剂, 用该催化剂制备的电极对析氢反应具有一定的电催化活性, 但由于该催化剂介孔WC的孔径较大(约200nm), 且负载的Pt颗粒的粒径较大(约15nm), 对电化学性能的提高不是很明显。
陈赵扬等采用碳化还原并结合气相还原法制备的介孔Pt/WC催化剂也具有一定的电催化还原活性, 但是其中的Pt颗粒较大且团聚比较严重, 一定程度上限制了其进一步的应用。
浙江工业大学胡仙超等人采用硬模板法制备了介孔碳化钨(m-WC), 进一步还原铂的前驱体(H2PtCl6)得到Pt/m-WC催化剂。
采用X射线粉末衍射(XRD)、透射电子显微镜(TEM)和X 射线光电子能谱(XPS)等测试手段对样品的物相、结构和形貌进行了表征。
结果表明, 所制得的m-WC载体为单一的碳化钨相, 孔径为10~20nm, Pt/m-WC催化剂中Pt的粒径约为3.4nm, 主要以金属态形式存在, 相对比较均一的Pt纳米粒子均匀地分散在载体的表面和孔道中。
电化学测试结果表明, 与普通WC载Pt催化剂(Pt/c-WC)相比, Pt/m-WC催化剂具有较大的电化学活性表面积, 对甲醇呈现出更高的电催化氧化活性和更好的稳定性。
炭载Pt—P催化剂对甲醇氧化的电催化性能研究

度高 , 且 价格 便 宜 、 来 源 丰 富等优 点 而被广 泛研 究 。 研究 发 现 D MF C 阳极 催 化 剂 研 究 最 多 的是 P t 【 2 ] 以及 P t 基 复合 催 化 剂 [ 3 。 ] 。改 变 制 备 方 法 和 载 体 , 可
提高 单组 分 P t 催 化剂 的 活性 , 但 反 应 生成 的 中间产 物
果表明 P t - P / C催 化 剂是 一 类 具 有 潜 在 应 用 前 景 的 直
接 甲醇燃料 电池 阳极催 化 剂 。 关键 词 : 甲醇 ;P t — P / C催 化 剂 ; 电 催化 氧化 ; 直接 甲
醇 燃 料 电 池 中图分 类 号 : O6 4 文 献标 识码 : A D oI : 1 0 . 3 9 6 9 / i . i s s n . 1 0 0 1 — 9 7 3 1 . 2 O 1 3 . 2 0 . 0 1 4
杨改秀 等 : 炭载 P t — P催 化 剂 对 甲醇 氧 化 的 电催 化 性 能 研 究
文章 编 号 : 1 0 0 1 — 9 7 3 1 ( 2 0 1 3 ) 2 0 — 2 9 6 7 — 0 4
炭载 P t — P催 化 剂 对 甲醇 氧化 的 电催 化 性 能研 究
杨 改 秀 , 孔 晓 英 , 袁 振 宏 , 陈冠 益 , 陆天 虹 。 ,孙 永 明
2 . 3 n m。此 外 , 亦 用 多 种 电 化 学 测 试 手 段 测 试 了 P 的
掺 杂对 甲醇的 电催 化 氧 化性 能 的影 响 , 测试 结 果表 明 P t — P / C催 化 剂不 但 能够 增 强催 化 剂 对 甲醇 催 化 氧化 的活性 , 而且还 能 够提 高催 化 剂 的稳 定 性 。 该 测 试 结
燃料电池催化剂文献报告

燃料电池催化剂文献报告燃料电池是一种基于电化学原理的能量转化设备,可以将化学能直接转化为电能。
其中,燃料电池的催化剂在电池反应中起着至关重要的作用。
催化剂能够降低活化能,加速电化学反应速率,提高燃料电池的性能。
本文将综述燃料电池催化剂的研究进展和相关的文献。
燃料电池常用的催化剂包括铂(Pt)和铂合金,因为它们具有良好的电化学活性和稳定性。
然而,铂催化剂的昂贵导致燃料电池成本高昂,限制了其广泛应用。
因此,寻找替代的、廉价和高效的催化剂成为研究的热点。
以铂基催化剂为例,近年来的研究主要集中在改善催化剂的活性和稳定性。
一种常用的方法是通过合成纳米结构来增加催化剂的表面积。
研究表明,纳米颗粒的尺寸和形状对催化剂的活性和稳定性具有重要影响。
例如,较小尺寸的纳米颗粒通常具有较大的比表面积和较高的活性,但较小的尺寸也会导致较低的稳定性。
因此,研究人员通过调控催化剂纳米颗粒的大小和形状,寻找最佳的催化剂性能。
另外,改变催化剂的组成也是提高燃料电池性能的重要途径。
铂合金催化剂是一种常见的选择,通过与其他金属元素合金化可以提高催化剂的活性和稳定性。
例如,铂镍(Pt-Ni)合金催化剂在质子交换膜燃料电池中显示出较好的性能,因为镍的添加可以增加催化剂的氧气还原反应活性,并降低铂的用量。
此外,控制催化剂的表面结构和表面态也是改善催化剂性能的关键。
表面结构的控制可以通过合成方法、溶剂选择和添加剂等手段实现。
而催化剂的表面态可以通过调节电子结构和晶体缺陷来实现。
除了铂基催化剂,其他替代催化剂的研究也日益受到关注。
例如,过渡金属非贵金属(TM/NP)合金催化剂被认为是替代铂催化剂的有希望候选者。
这些非贵金属催化剂具有较低的成本、丰富的资源和良好的催化活性。
过渡金属硫化物、氮掺杂碳材料和杂化催化剂也是研究的焦点。
综上所述,燃料电池催化剂的研究在寻找更高效、廉价的催化剂方面取得了显著进展。
未来的研究将继续致力于优化催化剂的活性、稳定性和成本效益,以推动燃料电池技术的发展。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碳载铂、钌催化剂对甲醇燃料电池阳极电催化性能的研究学院:化学学院班级:化学03班姓名:艾丽莎学号:33090331碳载铂、钌催化剂对甲醇燃料电池阳极电催化性能的研究【实验目的】甲醇燃料电池阳极催化剂的合成及其电化学催化性能的表征,此实验过程设计无机合成、物理化学及电化学等学科方向内容,对同学熟练运用化学实验基本理论、基本方法和操作具有很好的促进作用。
燃料电池是一类连续地将燃料氧化过程的化学能直接转换为电能的电化学电池,直接甲醇燃料电池(DMFC)由于其结构简单、操作方便和比能量高等优点,具有十分诱人的应用前景,引起广泛的研究兴趣,已经成为燃料电池领域的研究热点。
把相关研究作为实验内容对同学开阔视野,培养科学的思维方式及勇于创新意识具有促进作用。
1. 了解碳载铂与铂钌阳极催化剂的制备方法。
2. 了解甲醇燃料电池的工作原理,掌握催化剂电催化性能的测试方法。
3. 了解甲醇燃料电池阳极电催化反应机理。
【实验原理】一.什么是燃料电池。
燃料电池(Fuel Cell, 简称FC)发电是继水力、火力和核能发电之后的第四类发电技术。
由于它是一种不经过燃烧直接以电化学反应方式将燃料的化学能转化为电能的发电装置,从理论上讲,只要连续供给燃料,燃料电池便能连续发电。
但是,与一般电池不同,FC所用的燃料和氧化剂并不是储存在电池内,而是储存在电池外。
在这一点上,与内燃机相似。
因此,FC又被形象地称为“电化学发电机”。
二.燃料电池的分类。
燃料电池的分类方式有很多种,可依据所用解质性、工作温度燃料电池的分类方式有很多种,可依据所用解质性、工作温度燃料电池的分类方式有很多种,可依据所用解质性、工作温度燃料的种类以及使用方式等进行分。
目前广为采纳法是燃料的种类以及使用方式等进行分。
目前广为采纳法是依据燃料电池中所用的电解质类型来进行分,即为六燃料:①碱性燃料电池(AFC)碱性燃料电池采用氢氧化钾溶液作为电解液,电池的工作温度一般在60 -220 ℃之间。
②质子交换膜燃料电池(PEMFC)质子交换膜燃料电池采用能够传导质子的聚合物膜作为电解质,比如全氟磺酸膜(Nafion 膜),其主链为聚四氟乙烯链,支链上带有磺酸基团,可以传导质子。
③磷酸燃料电池(PAFC)磷酸燃料电池是目前最为成熟的燃料电池,已经实现了一定规模的商品化。
其采用是100%的磷酸作为电解液,其具有稳定性好和腐蚀性低的特点。
④熔融碳酸盐燃料电池(MCFC)熔融碳酸盐燃料电池是一种中高温燃料电池,其电解质是Li2CO3-Na2CO3或者Li2CO3-K2CO3的混合物熔盐,浸在用LiAlO2制成的多孔膜中,高温时呈熔融状态对碳酸根离子具有很好的传导作用。
⑤固体氧化物燃料电池(SOFC)其是一种全固体的燃料电池,电解质是固态致密无孔的复合氧化物,最常使用钇掺杂锆简写为YSZ,这样的电解质材料在高温下具有很好的氧离子传导性。
⑥直接甲醇燃料电池(DMFC)直接甲醇燃料电池是近年来开发起的,用PEM 作为电解质的新型燃料电池。
其直接使用液体甲醇作为燃料,大幅度的简化了发电系统和结构。
三.甲醇燃料电池(DMFC)的工作原理。
直接以液态或气态甲醇为燃料的FC称为DMFC,直接甲醇燃料电池是质子交换膜燃料电池(PEMFC)的一种变种,它直接使用甲醇而勿需预先重整。
甲醇在阳极转换成二氧化碳、质子和电子,如同标准的质子交换膜燃料电池一样,质子透过质子交换膜在阴极与氧反应,电子通过外电路到达阴极,并做功。
DMFC的工作原理如图1所示。
图1 DMFC的工作原理图阳极反应:CH3OH + H2O → CO2 + 6H+ + 6e- E = 0.046V (1)阴极反应:3/2O2 + 6H+ + 6e-→ 3H2O E = 1.23V (2)电池反应:CH3OH + 3/2O2 → CO2 + 2H2O E = 1.18V (3)原理上,当阳极电位高于0.046V(vs.RHE)时,甲醇的电氧化反应应自发进行,同样,当阴极电位等于或略低于1.23V时,氧气还原反应也应自发进行。
表1列出了DMFC中反应物、产物和总反应的ΔH o298和ΔG o值,并由此可计算出DMFC在标准状态下的理论电压和理论能量转换效率。
表1 DMFC中反应物、产物和总反应的ΔH o298和ΔG o反应物或产物ΔH o298(kJ/mol) ΔG o(kJ/mol)CH3OH -239.1 -166.73/2O20 0CO2-393.51 -394.362H2O 2×-285.83 2×-237.16反应总值-726.07 -702.02DMFC在标准状态下的理论电压E o = -ΔG o/nF =1.21V (4)其中,F为法拉第常数,n为反应中包含的电子数。
DMFC在标准状态下的理论能量转换效率η= - ΔG o/ΔH o298 = 0.970 (5) 由上述的数据看出,DMFC的标准状态下的理论电压较高,理论能量转换效率也很高,但实际的能量转换效率要低很多。
尽管DMFC有很多的优点和良好的应用前景,并且经过近40年,尤其是最近10年的研究,其性能已经有了很大提高,但与商业化的要求仍有很大差距。
目前DMFC存在的主要问题是阳极催化剂对甲醇氧化的电催化活性低,而且常用的Pt催化剂还会被甲醇氧化的中间产物毒化。
因此,虽然甲醇的标准氧化还原电位是0.04V,但实际上,阳极极化可达到0.1-0.3V。
研制高效和抗中毒的甲醇氧化电催化剂,降低阳极极化是DMFC的研究热点之一。
目前性能较好、应用最多的阳极催化剂为碳载Pt-Ru催化剂。
四.甲醇燃料电池阳极催化剂的分类。
大量的研究实验表明铂催化剂对甲醇的氧化呈现出很高的活性,但随着极化过程的不断进行,CO毒化作用会使其活性大大降低,维持必须研制出适合DMFC的新型的电催化剂。
目前甲醇燃料电池阳极催化剂可以分为:(1)采用铂合金的催化剂Pt-Ru合金是最重要的铂基合金催化剂,其对甲醇的电催化的效果最好。
(2)以导电聚合物作为载体形成复合催化剂目前的催化剂大多是以C作为载体的,但是C在一定的电位下,尤其是在由多片MEA 组成的电堆中运行时容易出现反极化,导致C被氧化,生成的CO进而毒化Pt。
(3)金属氧化物催化剂Pt对甲醇的氧化具有很高的电催化活性,但在缺少含氧物种时,易被吸附的CO毒化,因此含氧丰富的高导电性和高催化活性的ABO3型金属氧化物作为甲醇氧化的阳极催化剂进入了研究者视野。
五.阳极催化剂的制备方法。
不同的催化剂制备方法对催化剂活性有很大影响,这主要是不同方法制备的催化剂的粒子大小、结晶度、合金化程度等都会不同。
研究制备电催化剂的方法有很多,如浸渍-液相还原法、电沉积法、气相还原法、凝胶-溶胶法、气相沉积法、高温合金化法、固相反应方法、羰基簇合物法、预沉淀法、离子液体法等。
1. 浸渍-液相还原法将Pt的可溶性化合物溶解后,与活性炭载体混合,再加入还原剂,如NaBH4、甲醛溶液、柠檬酸钠、甲酸钠、肼等,使Pt还原、沉积到活性炭上,干燥后,得到Pt/C催化剂。
用不同的还原剂,得到的催化剂性能会有很大的差别。
这种方法的优点是方法简便,缺点是制得的催化剂的分散性差,金属粒子的平均粒径较大。
2. 电化学沉积法可用循环伏安、方波扫描、恒电位、欠电位沉积等电化学方法将Pt或其它金属还原。
3. 气相还原法Pt或者其他金属的前驱体被浸渍或沉淀在载体上后,干燥,氢气高温还原可得Pt/C或二元金属复合催化剂。
4. 凝胶-溶胶法将Pt制成溶胶后,再吸附在活性炭上,可以得到分散性较好、均一度较高的Pt/C催化剂。
这种制备溶胶的过程极为复杂,条件苛刻,原料价格高,仅仅适用于实验室研究,而且采用这种方法获得的催化剂往往含有不同的杂质。
5. 气相沉积法在真空条件下将金属气化后,负载在载体上,就可得到金属催化剂。
这种方法制得的催化剂中金属粒子的平均粒径较小,可在2nm左右。
6. 高温合金化法这种制备方法适用于制备多元金属催化剂。
它的最大优点是利用氩弧熔等技术在高温下熔解多元金属,分散、冷却后,得到的多元金属复合催化剂的合金化程度很高,因而其电催化性能优异。
7. 固相反应方法由于固相体系中粒子之间相互碰撞的几率较低,反应生成的金属粒子的平均粒径较小,结晶度较低,因此,制得的催化剂的电催化性能较好。
8. 羰基簇合物法先把金属制备成羰基簇合物,并沉积到活性炭上,然后在适当的温度下用氢进行还原,可得到平均粒径较小的金属粒子。
9. 预沉淀法为了要制得金属粒子较小的催化剂,用预沉淀法来制备Pt/C催化剂。
10. 离子液体法用室温离子液体作溶剂,先把Pt、Ru 等催化剂的化合物溶解在离子液体中,并加入活性炭混合均匀,然后通氢气使Pt、Ru等还原和沉积到活性炭上。
由于离子液体的性质,使金属粒子不易聚集,平均粒径在3nm左右,因此电催化性能很好。
11. 喷雾热解法喷雾热解法制备催化剂步骤是把催化剂前驱体喷成雾状,并加热分解得催化剂。
催化剂制备的方法很多,还有很多的催化剂制备方法,如微波合成法、离子交换法、插层化合物法等。
由于有些方法工艺复杂,一般在实际的生产中不易应用。
六.玻碳电极的预处理方法和评价标准预处理方法:清洁处理,主要方法有三种,化学法①硝酸浸泡和擦洗。
②以氨水无水乙醇或乙酸乙脂1:1浸泡擦洗。
③也可用酒精擦洗后再以6NHCl或4NHO3浸泡。
电化学处理:即在+0.8V-(-1.8V(0.5MKcLPH7除O2I条件下)电压范围内反复极化次(复位-扫描)(阳极-阴极至阴极处)若严重污染和有麻坑,划痕可作机械处理,MgO粉(200目以上)放在湿绒布上,加少量水抛光。
也可根据电极情况把几种方法联合使用。
不宜长时间将电极浸泡再强酸强碱和有机溶剂中。
(玻碳电极抛光:现在1.0微米的磨料上磨,然后在0.3微米的磨料上抛光,然后转移到乙醇和去离子水中超声。
超声时间一般不要超过半小时。
)本实验中,将直径为3mm的玻碳电极先用金相砂纸(1#~7#)逐级抛光,再依次用1.0、0.3μm的Al2O3浆粉在麂皮上抛光至镜面,每次抛光后先洗去表面污物,再移入超声水浴中清洗,每次2~3min,重复三次,最后依次用1:1乙醇、1:1HNO3和蒸馏水超声清洗。
彻底洗涤后,电极要在0.5-1mol/L H2SO4溶液中用循环伏安法活化,扫描范围1.0~-1.0V,反复扫描直至达到稳定的循环伏安图为止。
评价标准:在0.20mol/LKNO3中记录1×10-3mol/L K3Fe(CN)6溶液的循环伏安曲线,以测试电极性能,扫描速度50 mV/s,扫描范围0.6 ~-0.1V。
实验室条件下所得循环伏安图中的峰电位差在80mV以下,并尽可能接近59mV,或ipa和ipc的绝对值的比近似等于1,电极方可使用,否则要重新处理电极,直到符合要求。
