Fe
以f,fe结尾的名词变复数

以f,fe结尾的名词变复数在英语中,有许多名词以f或fe结尾。
在变成复数形式时,它们的变化规则也不尽相同。
在本文中,我们将讨论这些名词的复数形式,以及它们的变化规则。
一、以f结尾的名词变复数1. 单词末尾只有f的名词在这种情况下,将f变成ves。
例如:leaf - leaves(叶子 - 叶子们)life - lives(生命 - 生命们)thief - thieves(小偷 - 小偷们)wife - wives(妻子 - 妻子们)2. 单词末尾有辅音+f的名词在这种情况下,先将f变成ves,然后再加s。
例如:calf - calves(小牛 - 小牛们)half - halves(一半 - 一半们)knife - knives(刀 - 刀们)self - selves(自己 - 自己们)shelf - shelves(书架 - 书架们)wolf - wolves(狼 - 狼们)二、以fe结尾的名词变复数1. 单词末尾只有fe的名词在这种情况下,将fe变成ves。
例如:knife - knives(刀 - 刀们)life - lives(生命 - 生命们)wife - wives(妻子 - 妻子们)2. 单词末尾有元音+fe的名词在这种情况下,只需要在末尾加s。
例如:cafe - cafes(咖啡馆 - 咖啡馆们)safe - safes(保险箱 - 保险箱们)wife - wives(妻子 - 妻子们)3. 单词末尾有辅音+fe的名词在这种情况下,先将fe变成ves,然后再加s。
例如:half - halves(一半 - 一半们)knife - knives(刀 - 刀们)leaf - leaves(叶子 - 叶子们)life - lives(生命 - 生命们)wife - wives(妻子 - 妻子们)总结在英语中,以f或fe结尾的名词在变成复数形式时,需要注意它们的变化规则。
在本文中,我们介绍了不同类型的名词的复数形式,并提供了一些例子。
常见元素符号

六、化学方程式计算步骤一解二设最后答,化学方程不能差,准确寻找质量比,纯量代入不掺假, 所有单位要一致,列出比例解决它。
七、金属活动顺序1、金属活动顺序表,钾钙钠镁铝锰锌,铬铁钴镍锡铅氢,氢后铜汞银铂金。2、钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金。 八、实验室制取氧气二氧化锰氯酸钾,一三混匀口略下,先查气密后装药,固定之后把热加。高锰酸钾加热时,管口还需塞棉花,气泡均匀才收集,先撤后熄莫忘记,向上排气管伸底,余烬火柴检验它。
2、钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金。
八、实验室制取氧气
二氧化锰氯酸钾,一三混匀口略下;
先查气密后装药,固定之后把热加。
高锰酸钾加热时,管口还需塞棉花;
气泡均匀才收集,先撤后熄莫忘记;
向上排气管伸底,余烬火柴检验它。
九、酸碱盐的溶解性
氢氧钾钠钡钙溶,盐酸除银和亚汞;
31. 二氧化锰,MnO , 13. 白磷,P , 24
32. 一氧化氮,NO , 14. 木炭,C ,
33. 二氧化氮,NO , 15. 红磷,P , 2
34. 四氧化三铁,FeO , 16. 人体中最多物质的化学式,HO , 34235. 氧化铁,FeO , 17. 氢氧化钙,Ca(OH) , 232
10、仪器的洗涤一般容器用水洗,内壁附物用刷洗,壁内若有不溶物,盐酸溶碱纯碱脂,仪器洗净有标准,水不成股不聚滴。 二、前二十种元素氢氦锂铍硼,碳氮氧氟氖, 钠镁铝硅磷,硫氯氩钾钙。
三、常见元素的化合价
1、钾钠银氢正一价,钙镁钡锌正二价,一二铜汞二三铁,三铝四硅五氮磷,二四六硫二四碳,金正非负单质零。
忌管头触器口。或,两管直立,莫触内壁,滴管悬空,滴入正中。 6、托盘天平的使用天平用前调零点,左物右码记心间,砝码要用镊子夹,由大到小顺序拿, 一般药品垫纸称,腐蚀药品杯中放,称完天平要复原,游码移回到零点。或,一放平、二调零,三加砝码四进行,砝码要用镊子取,左物右码须记清。
产地证CO,FA,FE,FF的诠释

2、FORM D 是东盟自贸区原产地证书。
3、FORM E 是中国—东盟自贸区使用的优惠性原产地证书。
4、FORM A 是具有法律效力的我国出口产品在给惠国税率基础上进一步减免进口关税的官方凭证。
5、FORM F 出口智利的“金质证书”。
6、一般产地证(C/O),一般原产地证是证明货物原产于某一特定国家或地区,享受进口国正常关税(最惠国)待遇的证明文件,它的适用范围是:征收关税、贸易统计、歧视性数量限制、反倾销和反补贴、原产地标记、政府采购等方面。
配额有广义和狭义之分。从广意义上说,配额是对有限资源的一种管理和分配,是对供需不等或者各方不同利益的平衡。例如,当某地旅游或者移民需求过旺时,采取配额制度可以缓解这种压力;当某种产品供不应求时,实行配额制可以调节不平衡;等等。
狭义的配额是指在国际贸易范畴内的定义,即一国(地区)为了保护本国产业不因进口产品过量而受损害,或者为了防止本国(地区)产品过度出口而主动或者被动地控制产品进出口数量或者价值。配额的方式多种多样,有人统计全球实施的配额有2500余种。根据不同的标准,配额有绝对配额与相对配额,关税配额与非关税配额,主动配额与被动配额等多种分类。
关于产地证CO,FA,FE,FF的诠释和办理
常பைடு நூலகம்的几种产地证书!
1、FORM C 为非多种纤维纺织品申明书,适用于主要价值或主要重量是属于麻或丝的原料,或其中所含毛重不超过17%的纺织品为多国家产地声明书(Multiple country declaration),声明商品的原材料是由几个国家产生的。
分享: [分享到微米] [分享到新浪Qing]
0
喜欢
f或者fe结尾的单词变复数口诀

f或者fe结尾的单词变复数口诀
名词单数变复数规律:一般以f 或fe结尾的词,将f 或fe变为v 再加es. 巧记:妻见小偷架下藏,手拿小刀想杀狼。
扩展资料
众数,或称复数,在语言学中是词素的其中一种,常和单数相对,在没有双数概念的语言中用于标示多于一个的`物件,在有双数概念的语言中则表示多于两个的名词数量。
在另外某些语言当中,用于标示非一个物件,包括多于一个物件和没有。
在许多的语言里,多数的名词都有众数,而另一部份的语言则缺乏,或通常不使用众数,如汉语、日语、越南语等。
能被2整除的数字叫复数。
有些语言透过外部屈折将名词变为众数,如英语;有些语言则同时透过外部屈折和内部屈折将名词转为众数,如德语、俄语、阿拉伯语;而另有一部份的语言则以黏着词尾来表达复数,如维吾尔语、土耳其语、藏语、匈牙利语等;另有一部分语言以孤立的词素来标明,如汉语、越南语、日语,虽然一般而言汉语和越南语的名词不做单复数之分。
cl2和fe反应现象

CL2和Fe反应现象概述在化学领域中,CL2和Fe反应是指氯气(CL2)与铁(Fe)之间发生化学反应的现象。
这个反应是氧化还原反应的一个例子,也是工业上常见的反应之一。
本文将详细介绍CL2和Fe反应的现象、反应方程式、反应机制以及相关应用。
反应现象当氯气与铁发生反应时,会产生明显的物理和化学变化,表现为以下几个方面的现象:1.颜色变化:氯气是黄绿色的气体,而铁是灰色或银白色的固体。
当氯气与铁接触后,铁会逐渐变成棕红色,并覆盖上一层氯化铁膜。
2.变薄:氯化铁膜会逐渐变薄,有时会脱落下来,暴露出新的金属表面。
3.反应速度:氯气与铁反应的速度较快,特别是在高温和潮湿环境下。
4.反应热量:氯气与铁反应是一个放热反应,反应时会释放大量的热能。
5.反应产物:氯气与铁反应的主要产物是氯化铁(FeCl2)。
反应方程式反应方程式可以用化学符号和方程式表示反应过程,对于CL2和Fe反应,反应方程式如下:2Cl2 + 2Fe -> 2FeCl2该方程式表示氯气(Cl2)与铁(Fe)反应生成氯化铁(FeCl2)。
根据方程式,2分子氯气与2个铁原子反应生成2分子氯化铁。
反应机制氯气和铁反应的机制涉及多个步骤,包括以下几个主要步骤:1.氯气分子的解离:氯气分子(Cl2)首先在反应条件下解离为两个氯离子(Cl)。
这个过程是一个典型的加入离解过程。
2.氯离子的吸附:氯离子吸附在铁表面,与铁原子形成氯化铁膜。
这个过程是快速进行的。
3.膜的形成和脱落:氯化铁膜逐渐形成,并覆盖在铁表面上。
在一些情况下,氯化铁膜会脱落,并暴露出新的铁表面。
4.继续反应:如果氯气继续存在,氯化铁膜将继续形成和脱落,反应将持续进行。
这个过程可以重复发生,直到氯气完全消耗为止。
应用领域CL2和Fe反应在工业和实验室中有广泛的应用,主要包括以下几个方面:1.漂白剂制造:氯气与铁反应产生氯化铁,氯化铁可以用作制造漂白剂的原料。
漂白剂广泛应用于纸张、织物等行业。
变价金属(Fe、Co、Ni、Cr、Mn等)及其化合物
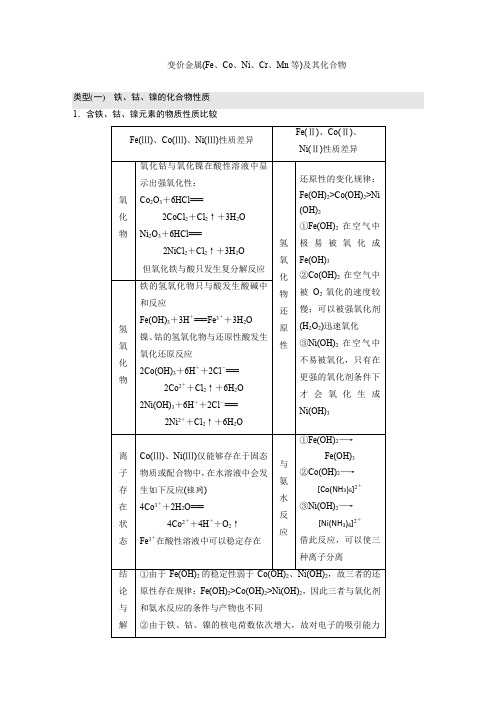
变价金属(Fe、Co、Ni、Cr、Mn等)及其化合物类型(一)铁、钴、镍的化合物性质1.含铁、钴、镍元素的物质性质比较2.铁、钴、镍盐溶液的氧化性与还原性(1)在酸性溶液中,Fe2+、Co2+、Ni2+分别是铁、钴、镍离子的稳定状态。
高价态的铁(Ⅵ)、钴(Ⅲ)、镍(Ⅳ)在酸性溶液中都有很强的氧化性,空气中的O2能将酸性溶液中的Fe2+氧化成Fe3+,但不能将Co2+、Ni2+氧化成Co3+和Ni3+。
(2)在碱性介质中,铁的最稳定价态是+3,而钴、镍的最稳定价态仍是+2,在碱性介质中,将低价态的Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)氧化成高价态比酸性介质中容易。
[对点训练]1.利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程图,回答下列问题:已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②沉淀Ⅰ中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:(1)浸出过程中Co2O3发生反应的离子方程式为_______________________________________________________________________________________________________________。
(2)NaClO3在浸出液中发生反应的离子方程式为______________________________________________________________________________________________________________。
(3)加入Na2CO3调pH至5.2,目的是__________________________________________;萃取剂层含锰元素,则沉淀Ⅱ的主要成分为______________________________________。
Fe化学性质

化学性质物理性质棕色或红褐色粉末或深棕色絮状沉淀。
密度3.4~3.9g/cm3。
化学性质具有两性但其碱性强于酸性,新制得的氢氧化铁易溶于无机酸和有机酸,亦可溶于热浓碱。
极强氧化剂,如次氯酸钠,在碱性介质中,能将新制的氢氧化铁氧化成+Ⅵ氧化态的高铁酸钠Na2FeO4。
加热时逐渐分解而成氧化铁和水。
不溶于水、乙醚和乙醇,溶于酸,在酸中的溶解度随制成时间的长短而定,新制的易溶于酸,若放置时间长,则难溶解。
氢氧化铁可用来制颜料、药物,也可用来做砷的解毒药等等。
低于500摄氏度时完全脱水成氧化铁。
加热分解。
氢氧化铁在烘干时易分解,但温度不高时不完全,也就是逐渐失水。
但在低于500摄氏度时能达到完全脱水成氧化铁。
没有一个明确的失水分解温度。
由可溶性Fe盐溶液加氨水沉淀来制取氢氧化铁或由氯化铁、硝酸铁溶液加入氨水沉淀而制得。
其粒子大小在1nm到100nm之间时会形成胶体。
胶状沉淀的水合氧化铁Ⅲ有较强的吸附性能。
氢氧化铁的两性电离:酸性:Fe(OH)3==(可逆)== H+ FeO+ H2OFeO +H2O ==(可逆)== [FeO2(OH)]+ H[FeO2(OH)] ==(可逆)== H+ FeO3碱性:Fe(OH)3+ 6H2O==(可逆)== [Fe(H2O)6]+ 3OH所以:氢氧化铁既是一种三元弱碱,又是一种三元弱酸。
其中H2O + FeO2又常写作[Fe(H2O)2(OH)4],[FeO2(OH)]又常写作[Fe(H2O)(OH)5],FeO3 又常写作[Fe(OH)6].用途可用来制颜料、药物,用作净水剂,也可用来做砷的解毒药等。
铁离子铁是一变价元素,常见价态为+2和+3。
铁与硫、硫酸铜溶液、盐酸、稀硫酸等反应时失去两个电子,成为+2价。
与Cl2、Br2、硝酸及热浓硫酸反应,则被氧化成Fe3+。
铁与氧气或水蒸气反应生成的Fe3O4,可以看成是FeO·Fe2O3,其中有1/3的Fe为+2价,另2/3为+3价。
为什么Fe基催化剂是最好的合成氨催化剂

为什么Fe基催化剂是最好的合成氨催化剂合成氨工业需要较低温度和压力下具有较高活性的催化剂。
90多年来,世界各国从未停止过合成氨催化剂的研究与开发。
目前,工业催化剂的催化效率在高温下已达90%以上,接近平衡氨浓度(因压力而异).侧如,在15 MPa及475℃下,A301催化剂的催化效率接近100%。
要提高催化剂的活性,就只有降低反应温度。
另一方面,工业合成氨的单程转化率只有15%~25%,大部分气体需要循环,从而增加了动力消耗。
为了提高单程转化率,也只有降低反应温度才有可能。
因此,合成氨催化剂研究总的发展趋势,就是开发低温高活性的新型催化剂,降低反应温度,提高氨的平衡转化率和单程转化率或实现低压合成氨。
近20多年来,随着英国BP公司钌基催化剂的发明和我国Fe1-x O基催化剂体系的创立,标志着合成氨催化剂进人了一个新的发展时期。
在合成氨反应中,速度控制步骤是N2的解离吸附;而解离N2的强键需要“敞开锅”式结构。
体心立方的Fe(111)面正构成这种表面结构,而其它两种晶面(100)和(110)则偏离此花样。
含有原子的类似于Fe(111)晶面的结构被认为是合成氨反应的活性中心.因此,合成氨反应被认为是结构敏感反应。
Al2O3的表面重构作用可以改变a-Fe的晶面结构.Bare等的研究结果表明,添加Al2O3并在水蒸气和O2中迅速退火之后,活性最低的Fe(110)面的活性几乎与Fe(111)面相同Strongin等的研究结果表明,Al2O3表面重构作用的机理是,Al2O3首先在表面生成FeAl2O4,然后以这种新的表面为模板,使a-Fe晶体生长向(111)或(211)面定向暴露在反应混合物中.经Al2O3表面重构后,(111),(100)和(110)面的活性基本相同,从而大大提高了活性。
通常认为,催化剂表面的碱中心有利于碱性NH3的脱附。
同样,氮原子具有孤对电子,是一种典型的Lewis碱;显然,催化剂表面的酸中心有利于N2的吸附,NH3 的脱附,特别是N2的吸附,有利于加速合成氨反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
配键 与 C O分 子 结 合 生 成 羰 基 化 合 物 , 如 诸 N( O4C( o F( o 5 . I ) a c ) e C ) 等 其中 F (O 5 C 、" e C ) 为五 配位化合物 , 其立体构型存 在三角双锥形 和四方锥 形两种可能构 型, 然而究竟属于哪种构 型, 分析 其 方法也为数不少, 如晶体场理论、 分子轨道理论 、 核 磁共振等 . 不过 , 这些方法虽有各 自的优点, 但同时 又存在许多不足之处 . 如采用晶体场理论虽可从晶 体场稳定化能的相对大小来推断, 但园受其他如配 位体等因素的影响而使结果偏离, 甚至背离实验结 果; 如采用分子轨道理论虽 能对配合物 的化学键作 比较全面的 阐述 , 既适用 于离 子型配合物 , 又适用 于共价键型配合物 , 由于该理论 的某些概念和计 但 算方法 比较复杂 而不易 被人 们所掌握 . 此, 为 本文
表 1 D 中。 3群 不动原子数 、 对特征标表 的 贡献夏所有原 子的运动情 况
由 击 R (算 所 解 的 不 : ()R 出 分 出 的 )
可约数 [ 结果如 表 4所示 . ,
表 4 c 的不可 的冀 情况 4群
DБайду номын сангаас 3
E 2 3 3 2 d 3 c C r h 3 0
0
23 s 1 一 2
—2
不 动的原 子数 6 对特 征标表 的贡献 3
.
2 一 j
—2
4 j
4
4 l
4
t.
1 8
从 而有
由
/i : 7 ,
有振动 = 4 A1+ 』2+ 2 4 1+ 2+ 5 , E
收稿 日 :01 0 2 期 20 — 4 0 作者简舟 : 余 毅(93)女, 1 ., 编辑 7
个c 0整体视为“ 一个原子”对特征标表的贡献 , ) 所
维普资讯
第1 期
余 毅 等 : (o5 c )分子 的立体构型研究
有原 子 的运 动如 表 1 所示 .
构 和性 质是人 们 认识 分 子 的重 要途 径 , 了解 分 子 是
2
一
专 0
0 一l
0
推知 : ( 3 ~ 2在 D 中, S) 3群 特征标 中各个对称
操 作 中不动 的原子 数 ( ( 0 子 枸型 中的 每一 c )分
结构和性质的重要方法 . 而群论是处理对称性的数
试 从群 论 、 价键 理论 结合 价 层 电子 对 互斥 理论 等 角 度 对 F(O) 分 子构型进 行 推 导说 明 . eC j
属于哪一种构 型, 则需先求 出简 正振 动表达 式 , 再
通过观测得到 的红外活性基频数 目与理论值相 比 较, 若与之相互吻合. 则属于此种构型 .
维普资讯
20 02年 1 月 第2卷 第 l 5 期
四川h  ̄ 唧 ( . N 1 i ) h仰 oScu N l 哑j ( 吐 ) c e f & 师范大学学报 v 岍 u 自然科学版 s 曲c
. 02 . 0
V . 5 2. . 1
若 F( O 5 子 为三 角 双 锥 形排 布式 , D ^ eC ) 分 属 3
群. 各对称操作对特征标表( 3群 的特征标表见表 D^
1的 贡献 计算 如下 : )
E: : ( +2 0 )= 3 ( 1 cs , E)=3 , 2 3 m= l+2 o1f : 0 ( 3 C :T cs2 ' , C )=0 , 3 : = l+2 olf =一 1 ( 2 cs8 ' , c )=一 1 ,
则 有一对 或 多 对孤 对 电子 , 如一 些过 渡金属 通 过
学工具 , 一组对称操作在数学上构成 一个群 , 它们
使分子从一种等价构型变为另一种等价构 型, 但相
应的 I m n -  ̄ 算符形式则不变 , I a 故利用群论 的有关 原理来分析分子对称性 而无需经过详 细计算 即可 获得一些 定性 的结 论【 . , 由于 F( 05 ec ) 为五配位化合物 , 其立体构型就 可能为三角双锥和四方锥形中的一种构型 , 但具体
r( o 5 ec ) 分子的 立体构 型研究
余 毅 余 , 江
( ( l[ 1 1J 师范大学学报》 自然科学版 )  ̄l ( 编辑部 , 四川 成都 60 6 ; 2  ̄J 师范大学 化学与生奇科学学院 , J成都 6 ∞6 ) 1 6 0 I l l[ 四J I J 6
摘要: 从群论方 法 、 价键 理 论 等角度 对金 属 羰基 化台 物 F ( o) e c 的立体构 型 进行 了推证 . 结果 表 明
F (O5 eC ) 的立体构型 为三 角双锥形 .
关键 词 : 论; 键理沦 ; 群 价 羰基化 合物 中图分类号 :g t O4 文 献标 识码 : 文章编 号 :11 ̄9 (o2o-o4o A 10. 52o )t 8-3 3 o
配位化合物结 构的研究 , 对于科研 、 生产 以及 化学的各个分支具有尤 为重要 的意义 _ 】配位化 】 . 合物是一类含有 中心金属 原子( 和若 干配 位体 M) () L 的化合 物( E ) 中心原 子 M通常是过渡金属 M . 元素的原子 ( 或离 子) 具有 空 的价轨道 . . 而配 体 L
O :T " m=一( +2 o lf )= l ( ^ h 1 cs8 ' , d ): 1 , 3 : :一( +2 o1i): 1 ( ): 1 1 cs8 , f , .
2 据 S根
一i 一迫 1 2
一
0
1 群 论 方 法
分子中, 原子 固定在其平衡位 置上 , 空间排 其 列 是 一对 称 的 图像 . 用 对称 性 原 理探 讨 分子 的 结 利
