fy青蒿素结构与性质-高考化学复习测试题20160115
全国高考热点透视之——青蒿素必考【含答案】

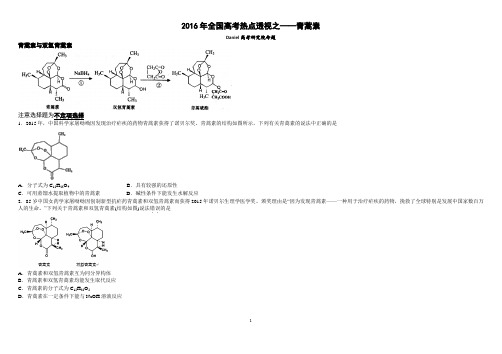
2016年全国高考热点透视之——青蒿素必考【含答案】-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN2016年全国高考热点透视之——青蒿素Daniel高考研究院命题青蒿素与双氢青蒿素注意选择题为不定项选择1.2015年,中国科学家屠呦呦因发现治疗疟疾的药物青蒿素获得了诺贝尔奖。
青蒿素的结构如图所示,下列有关青蒿素的说法中正确的是A.分子式为C15H22O4 B.具有较强的还原性C.可用蒸馏水提取植物中的青蒿素 D.碱性条件下能发生水解反应2.85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学医学奖。
颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家数百万人的生命。
”下列关于青蒿素和双氢青蒿素(结构如图)说法错误..的是A.青蒿素和双氢青蒿素互为同分异构体B.青蒿素和双氢青蒿素均能发生取代反应C.青蒿素的分子式为C15H22O5D.青蒿素在一定条件下能与NaOH溶液反应23.青蒿琥酯是治疗疟疾的首选药,可由青蒿素两步合成得到。
下列有关说法正确的是A.青蒿素分子式为C15H22O5B.青蒿素不能与NaOH溶液反应C.反应②原子利用率为100%D.青蒿琥酯能与氢氧化钠溶液反应可生成青蒿琥酯钠4.中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一。
下列说法不正确...的是A.从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种化学变化B.青蒿素的分子式为C15H22O5,它属于有机物C.人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段D.现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O元素5.某种药物青蒿素结构如右图所示,则下列说法正确的是3A.青蒿素易溶于水B.青蒿素的晶体为原子晶体C.青蒿素能与NaOH溶液反应D.青蒿素不能与NaOH溶液反应6.2011年我国女科学家屠呦呦因“发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得有诺贝尔奖“风向标”之誉的拉斯克临床医学奖。
2016年全国高考热点透视之——青蒿素必考【含答案】
2016年全国高考热点透视之——青蒿素Daniel高考研究院命题青蒿素与双氢青蒿素注意选择题为不定项选择1.2015年,中国科学家屠呦呦因发现治疗疟疾的药物青蒿素获得了诺贝尔奖。
青蒿素的结构如图所示,下列有关青蒿素的说法中正确的是A.分子式为C15H22O4B.具有较强的还原性C.可用蒸馏水提取植物中的青蒿素D.碱性条件下能发生水解反应2.85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学医学奖。
颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家数百万人的生命。
”下列关于青蒿素和双氢青蒿素(结构如图)说法错误..的是A.青蒿素和双氢青蒿素互为同分异构体B.青蒿素和双氢青蒿素均能发生取代反应C.青蒿素的分子式为C15H22O5D.青蒿素在一定条件下能与NaOH溶液反应3.青蒿琥酯是治疗疟疾的首选药,可由青蒿素两步合成得到。
下列有关说法正确的是A.青蒿素分子式为C15H22O5B.青蒿素不能与NaOH溶液反应C.反应②原子利用率为100%D.青蒿琥酯能与氢氧化钠溶液反应可生成青蒿琥酯钠4.中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一。
下列说法不正确...的是A.从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种化学变化B.青蒿素的分子式为C15H22O5,它属于有机物C.人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段D.现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O元素5.某种药物青蒿素结构如右图所示,则下列说法正确的是A.青蒿素易溶于水B.青蒿素的晶体为原子晶体C.青蒿素能与NaOH溶液反应D.青蒿素不能与NaOH溶液反应6.2011年我国女科学家屠呦呦因“发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得有诺贝尔奖“风向标”之誉的拉斯克临床医学奖。
2016新课标1高考压轴卷 化学 含资料

2016新课标乙卷高考压轴卷化学试题一、选择题:每小题6分.在每小题给出的四个选项中,只有一项是符合题目要求的.7.中国女药学家屠呦呦因研制新型抗疟药青蒿素和双氢青蒿素成果而获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素结构如图所示:下列关于青蒿素和双氢青蒿素的说法正确的()A.青蒿素的分子式为C15H22O5B.青蒿素和双氢青蒿素是同分异构体C.青蒿素和双氢青蒿素都能发生酯化反应D.青蒿素在稀硫酸催化条件下不能发生水解反应8.设N A为阿伏加罗常数的值,下列说法不正确的是()A.常温下,1L0.1mol•L﹣1NaClO溶液中阴离子总数大于0.1N AB.7.8gNa2O2中含有的阴、阳离子总数是0.3N AC.N2H2分子中各原子的最外层(除H外)均为8电子结构,1molN2H2中有共用电子对数目为3N AD.50mL18mol•L﹣1浓硫酸与足量铜反应,转移电子数小于0.9N A9.往含I﹣和Cl﹣的稀溶液中滴入AgNO3溶液,沉淀的质量m(沉淀)与加入AgNO3溶液体积V(AgNO3)的关系如图所示.则原溶液中的比值为()A. B.C. D.10.X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是()A.五种元素中,原子半径最大的是WB.Y与Z形成的化合物都可以和盐酸反应C.Y的简单阴离子比W的简单阴离子还原性强D.Z与Q形成的化合物水溶液一定显酸性11.已知高能锂电池的总反应式为:2Li+FeS═ Fe+Li2S[LiPF6.SO( CH3)2为电解质],用该电池为电源进行如图的电解实验,电解一段时间测得甲池产生标准状况下H24.48L.下列有关叙述不正确的是()A.从隔膜中通过的离子数目为0.4 N AB.若电解过程体积变化忽略不计,则电解后甲池中溶液浓度为4 mol/LC.A电极为阳极D.电源正极反应式为:FeS+2Li++2e﹣═ Fe+Li2S12.下列实验“操作和现象”与“结论”都正确的是( )0.1mol/L漏斗中加入碘水后再加入13.25℃时,用浓度为0.1000 mol•L-1的NaOH溶液滴定20mL 浓度均为0.1000 mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示。
2016年全国高考热点透视之——青蒿素必考【含问题详解】

2016年全国高考热点透视之——青蒿素Daniel高考研究院命题青蒿素与双氢青蒿素注意选择题为不定项选择1.2015年,中国科学家屠呦呦因发现治疗疟疾的药物青蒿素获得了诺贝尔奖。
青蒿素的结构如图所示,下列有关青蒿素的说法中正确的是A.分子式为C15H22O4 B.具有较强的还原性C.可用蒸馏水提取植物中的青蒿素 D.碱性条件下能发生水解反应2.85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学医学奖。
颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家数百万人的生命。
”下列关于青蒿素和双氢青蒿素(结构如图)说法错误..的是A.青蒿素和双氢青蒿素互为同分异构体B.青蒿素和双氢青蒿素均能发生取代反应C.青蒿素的分子式为C15H22O5D.青蒿素在一定条件下能与NaOH溶液反应3.青蒿琥酯是治疗疟疾的首选药,可由青蒿素两步合成得到。
下列有关说法正确的是A.青蒿素分子式为C15H22O5B.青蒿素不能与NaOH溶液反应C.反应②原子利用率为100%D.青蒿琥酯能与氢氧化钠溶液反应可生成青蒿琥酯钠4.中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一。
下列说法不正确...的是A.从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种化学变化B.青蒿素的分子式为C15H22O5,它属于有机物C.人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段D.现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O元素5.某种药物青蒿素结构如右图所示,则下列说法正确的是A.青蒿素易溶于水B.青蒿素的晶体为原子晶体C.青蒿素能与NaOH溶液反应D.青蒿素不能与NaOH溶液反应6.2011年我国女科学家屠呦呦因“发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得有诺贝尔奖“风向标”之誉的拉斯克临床医学奖。
《青蒿素》课后练习 有答案

《青蒿素:人类征服疾病的一小步》《一名物理学家的教育历程》课后作业2020-05一、阅读下面的文字,完成下列小题。
屠呦呦:获诺贝尔奖的“青蒿素之母”林晓娜①2015年10月5日,瑞典卡罗琳医学院宣布,中国药学家屠呦呦与另外两名海外科学家分享2015年诺贝尔生理学与医学奖,屠呦呦的突出贡献是创制新型抗疟药——青蒿素和双氢青蒿素。
当获奖消息传来时,屠呦呦已是一个耄耋高龄的老人。
她不是院士,没有海外留学经历,没有博士头衔,甚至被戏称为“三无科学家”。
②屠呦呦1930年12月生于浙江宁波,1951年考入当时的北京医学院药学系。
在大学里,她对植物化学、本草学和植物分类学表现出浓厚兴趣。
大学毕业后,她被分配到卫生部直属的中医研究院工作。
③1970年,屠呦呦参与一个大规模的研究项目。
该项目立项主要是由于战争需要。
越战期间,美军和越南部队在印度支那半岛的热带战场上均受到疟疾的困扰。
疟疾造成的非战斗减员比战伤减员高出四五倍,这使得军队战斗力严重受挫。
越南方面求助于我国。
在毛泽东主席、周恩来总理的关心之下,1967年5月23日,解放军总后勤部商请国家科委、卫生部等部门召开了疟疾防治药物研究工作协作会议。
此后,“523”就用以指代此次疟疾防治研究项目。
按照部署,“523”项目分临床研究、中医药、化学合成药三组。
屠呦呦加入了中医药组。
她与军事医学科学院的研究人员一同查阅历代医药记载,挑选其中出现频率较高的抗疟疾药方,并实验这些药方的效果。
④2009年,屠呦呦出版了《青蒿及青蒿素类药物》一书。
据此书记载,1971年10月她和同行们从中药青蒿中获得具有100%疟原虫抑制率的提取物,取得中药青蒿抗疟的突破;经去粗取精,于1972年11月8日得到抗疟单体——青蒿素。
1973年,青蒿素的抗疟功效在云南地区得到证实。
后来,山东中医药研究所、云南省药物研究所等单位也从黄蒿中获得青蒿素结晶。
同年,中医研究院中药研究所和中科院上海有机化学研究所等单位开始着手青蒿素化学结构的确定工作。
高考化学实验复习题及答案 (130)

高考化学实验复习题及答案34.青蒿素是一种有效的抗疟药。
常温下,青蒿素为无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157℃.提取青蒿素的方法之一是乙醚浸取法,提取流程如图1.请回答下列问题:(1)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率;操作Ⅱ的名称是蒸馏。
(2)用图2实验装置测定青蒿素的最简式,将28.2g青篙素放在装置C燃烧管中充分燃烧:①各装置的连接顺序从左到右依次为A、D、C、B、E(写各装置大写字母代号,每个装置限用一次)。
②装置D中的试剂是浓硫酸,装置E球型干燥管中碱石灰的作用是防止空气中二氧化碳和水蒸气进入装置E中U型管。
③已知青蒿素是烃的含氧衍生物,以上实验测量数据如表:实验B装置质量E(不含干燥管)装置质量实验前22.6g80.2g实验后42.4g146.2g 则青蒿素的最简式为C15H22O5。
【分析】(1)根据图1流程可知,先对青蒿进行干燥破碎,增大青蒿与乙醚的接触面积,提高青蒿素的浸取率,然后用乙醚对青蒿素进行浸取后,过滤,可得滤液和滤渣,提取液经过蒸馏后可得青蒿素的粗品,对粗品加95%的乙醇,浓缩、结晶、过滤可得精品;(2)为了能准确测量青蒿素燃烧生成的CO2和H2O,实验前应先通入氧气排出空气,防止干扰实验;进入装置C的氧气必须用装置D中浓硫酸干燥;C中青蒿素燃烧生成CO2和H2O;用装置B盛放的CaCl2或P2O5吸收生成的H2O,用装置E中碱石灰吸收CO2,装置E球型干燥管中碱石灰防止外界空气中CO2和H2O进入的装置,据此答题。
【解答】解:(1)根据乙醚浸取法的流程可知,对青蒿进行干燥破碎,可以增大青蒿与乙醚的接触面积,提高青蒿素的浸取率;操作Ⅱ分离相互溶解的液体,操作方法为蒸馏,故答案为:增大青蒿与乙醚的接触面积,提高青蒿素的浸取率;蒸馏;(2)①A为O2发生装置,进入装置C的O2必须用装置D中浓硫酸干燥;C中青蒿素燃烧生成CO2和H2O;用装置B盛放的CaCl2或P2O5吸收生成的H2O,用装置E中碱石灰吸收CO2,装置E球型干燥管中碱石灰防止外界空气中CO2和H2O进入的装置,所以装置的连接顺序为A、D、C、B、E,故答案为:D、C、B、E;②为了防止进入C装置的氧气中混有有水蒸气,需要D装置中盛放的浓硫酸进行干燥;装置F中的试剂为碱石灰,其作用是防止空气中二氧化碳和水蒸气进入装置E,故答案为:浓硫酸;防止空气中二氧化碳和水蒸气进入装置E中U型管;③由数据可知:m(H2O)=42.4g﹣22.6g=19.8g,则n(H2O)==1.1mol,m(CO2)=146.2g﹣80.2g=66g,则n(CO2)==1.5mol,青蒿素中氧原子的质量为:m(O)=28.2g﹣(2.2mol×1g/mol)﹣(1.5mol×12g/mol)=8g,n(O)==0.5mol,则N(C):N(H):N(O)=1.5:2.2:0.5=15:22:5,所以青蒿素的最简式为C15H22O5,故答案为:C15H22O5。
高三化学月考试题及答案-贵州贵阳市第一中学2016届高三上学期第三次月考理综化学试题

贵州省贵阳市第一中学2016届上学期第三次月考可能用到的相对原子量:H-1 C-12 N-14 O-16 Na-23 S-327. 2015年10月,中国科学家屠呦呦获得了2015年度诺贝尔生理学或医学奖,获奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”。
图4是青蒿素的结构,则下列有关青蒿素的说法不正确的是( )A.青蒿素分子式为C15H22O5B.青蒿素有-O-O-键具有较强的氧化性C.青蒿素易溶于水、乙醇、苯D.青蒿素在碱性条件下易发生水解反应8.下列实验操作过程中能引起结果偏低的是①用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,酸式滴定管未用标准液润洗②用量筒量取5.0mL溶液时,俯视读数③配置一定物质的量浓度的硫酸溶液,定容时仰视容量瓶的刻度线④用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,滴定前平视读数,滴定终点仰视读数A.③④B.②③C.①④D.①②9.设N A为阿伏伽德罗常数的值,下列叙述正确的是( )A.12.0g熔融的NaHSO4中含有的阳离子数为0.2N AB.标准状况下,0.1molCl2溶于水,转移电子数目为0.1N AC.1molCO2与含1molNaOH的溶液反应后溶液中HCO3-数为N AD.标准状况下,2.24LNH3和CH4的混合气体,所含电子总数为N A10.下列离子方程式正确的是( )A.向碘化亚铁溶液中通入足量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-B.碳酸氢钠溶液与过量的澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2OC.用浓盐酸配制的高锰酸钾溶液与过氧化氢反应:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2OD.硫酸氢钠溶液与氢氧化钡溶液以等物质的量混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O 11.将一定量的二氧化碳通入100毫升某浓度的氢氧化钠溶液中得到溶液X,若向X中逐渐加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示,则下列分析与判断不正确的是(不计二氧化碳溶解)A.若OA=AB,则溶液X为碳酸钠溶液B.若OA=0,则形成溶液X所发生反应的离子方程式为OH-+CO2=HCO3-C.若OA>AB,则溶液X中大量存在的阴离子为碳酸根离子和碳酸氢根离子D.若3OA=AB,则溶液X中c(NaHCO3)=2c(Na2CO3)12.将0.1摩尔镁、铝混合物粉末溶于200mL0.5mol/L的硫酸中,反应一段时间后,再加入150mL2mol/L的氢氧化钠溶液,待反应完全,此时溶液中大量存在的是A.Na+,Mg2+B.Na+,AlO2-C.Mg2+,AlO2-D.Al3+,Mg2+13.常温下,pH>7的某溶液中只含有Na+、CH3COO-、H+、OH-四种离子,下列描述正确的是A.该溶液只能由等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液混合而成B.该荣恶意一定由pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合而成C.该溶液中离子浓度一定为c(Na+)>c(CH3COO-)>c(OH-)>c(H+)D.加入一定冰醋酸,c(CH3COO-)可能大于、等于或小于c(Na+)26.(14分)氮及其化合物在生活、生产和科技等方面有重要的应用。
江苏省扬州市头桥中学高三化学月考试卷含解析

江苏省扬州市头桥中学高三化学月考试卷含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 2015年,中国科学家屠呦呦因发现治疗疟疾的药物青蒿素获得了诺贝尔奖。
青蒿素的结构如图所示,下列有关青蒿素的说法中正确的是A.分子式为C15H22O4B.具有较强的还原性C.可用蒸馏水提取植物中的青蒿素D.碱性条件下能发生水解反应参考答案:D根据有机物结构简式为青蒿素分子式为C15H22O5,A选项错误;青蒿素有—O—O—键,其中氧元素的化合价是—1价,具有较强的氧化性,B选项错误;青蒿素是有机物易溶于有机溶剂,应用有机溶剂提取青蒿素,C选项错误;青蒿素中含有酯基,能发生水解反应,D选项正确。
2. 已知在25℃时,下列反应的平衡常数如下:①N2(g)+02(g) 2NO(g) K1 =1×10-30②2H2(g)+02(g) 2H2O(g) K2 =2 xlO81③2C02(g) 2CO(g)+O2(g) K3 =4 x10一92下列说法正确的是()A.NO分解反应;No(g) N2(g)+02(g)的平衡常数为I xl0-30B.根据K2的值可以判断常温下H2和02很容易反应生成H20 C.常温下,NO、H20、C02三种物质分解放出02的倾向顺序为NO> H20> C02D.温度升高,上述三个反应的平衡常数均增大参考答案:C略3. 下列叙述正确的是()A.室温时饱和的二氧化碳水溶液,冷却到0℃时会放出一些二氧化碳气体B.氢氧化铁胶体是纯净物C.强电解质在水中溶解度一定大于弱电解质D.相同温度下,把水面上的空气换成相同压力的纯氧,100 g水中溶入氧气的质量增加参考答案:D略4.参考答案:D5. 常温下,下列各组离子在指定溶液中能大量共存的是A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+B.由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3-C.c(H+) / c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-D.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN-参考答案:C解析:A.pH=1酸性溶液中,Fe2+、H+、NO3-发生氧化还原反应,不能大量共存,故A错误;B.由水电离出的c(OH-)=1×10-13mol?L-1的溶液,为酸或碱溶液,该组离子HCO3-均不能共存,故B错误;C.c(H+) / c(OH-)=1012的溶液是酸性溶液,各离子可以共存,故C正确;D.Fe3+和SCN-不能共存,故D错误;故答案选C6. 用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
“青蒿素”结构与性质-高考化学复习测试题
编制:冯涌(QQ:1078875886)
青蒿素是我国药学家屠呦呦根据中医典籍从主要生长于我国的青蒿中提取的治疗疟疾的有效成分。
下图是屠呦呦在瑞典发表诺贝尔奖主题演讲时的画面,她的左边是诺奖主题演讲会的主持人卡罗林斯卡学院传染病学教授Jan Andersson先生,他在屠呦呦演讲的半个小时里双膝轮换一直跪在地上,为屠呦呦举着话筒。
Ⅰ.称取14.1mg青蒿素样品,如下图,在足量氧气中完全燃烧后,依次通过高氯酸镁和氢氧化钠固体粉末,燃烧产物被完全吸收,两种固体分别增重9.9mg和33.0mg 。
1
(1)计算确定青蒿素分子的最简式;
(2)能不能由此确定青蒿素的分子式?
Ⅱ.已知青蒿素中含有过氧键官能团(也称过氧基)。
称取1.41g青蒿素,完全溶解后在100mL容量瓶中定容、摇匀,取出25.00mL置于锥形瓶中,加入少量硫酸、足量的KI 和4滴淀粉溶液,锥形瓶中溶液呈蓝色。
向锥形瓶中滴入0.1250mol/L的Na2S2O3溶液20.00mL,蓝色恰好消失。
计算:
(1)该青蒿素溶液可能的浓度;
(2)青蒿素分子的最小摩尔质量。
Ⅲ.下面左图是主要生长在我国的植物青蒿茎和叶背面的照片,右图是某研究室通过晶体衍射测定得到的有关青蒿素分子结构中一些主要共价键的键长数据(单位:pm),图中元素符号右下角的数字是相应原子的编号。
(1)写出青蒿素的分子式。
现代化学快速、精确测定相对分子质量的仪器名称是。
(2)试分析在青蒿素分子中可能形成双键的原子及其编号。
(3)青蒿素的药用机理复杂。
试根据化学原理推测青蒿素能杀灭疟原虫最关键的原子及其编号。
Ⅳ.根据上述结构判断下列有关青蒿素的说法不正确的是:
A.含有醚键
B.由于青蒿素几乎不溶于水,水浸青蒿对治疗疟疾毫无作用
C.用乙醇浸取,挥发浓缩后可以结晶析出
D.受热易分解
E.能与碱反应
Ⅴ.双氢青蒿素的疗效更好。
青蒿素经还原剂处理,原来的双键加氢,得到双氢青蒿素。
写出双氢青蒿素的结构简式,并从理论上分析制备双氢青蒿素的困难所在。
“青蒿素”结构与性质-高考化学复习测试题
参考答案
Ⅰ.(1)C15H22O5;
(2)因为青蒿素的相对分子质量未知,故不能确定青蒿素的分子式。
Ⅱ.(1)0.05000/N mol/L(N为正整数);
(2)282g/mol。
Ⅲ.(1)C15H22O5;质谱仪;
(2)C12和O5;
(3)O1和O2。
Ⅳ. B.
Ⅴ.如图:
酯基稳定不易被还原,用强还原剂对酯基加氢还原时,
青蒿素中的过氧键(或称过氧基,有较强氧化性)易被破坏,
使青蒿素失去疗效。
