2017年浙江新高考化学无机推断题试题练习
浙江省丽水市新新高考化学易错易混推断题精粹含解析
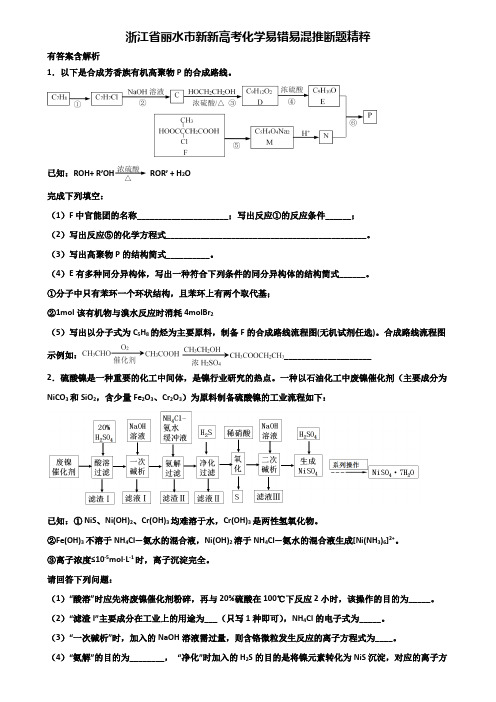
浙江省丽水市新新高考化学易错易混推断题精粹有答案含解析1.以下是合成芳香族有机高聚物P的合成路线。
已知:ROH+ R’OH ROR’ + H2O完成下列填空:(1)F中官能团的名称_____________________;写出反应①的反应条件______;(2)写出反应⑤的化学方程式______________________________________________。
(3)写出高聚物P的结构简式__________。
(4)E有多种同分异构体,写出一种符合下列条件的同分异构体的结构简式______。
①分子中只有苯环一个环状结构,且苯环上有两个取代基;②1mol该有机物与溴水反应时消耗4molBr2(5)写出以分子式为C5H8的烃为主要原料,制备F的合成路线流程图(无机试剂任选)。
合成路线流程图示例如:____________________2.硫酸镍是一种重要的化工中间体,是镍行业研究的热点。
一种以石油化工中废镍催化剂(主要成分为NiCO3和SiO2,含少量Fe2O3、Cr2O3)为原料制备硫酸镍的工业流程如下:已知:① NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物。
②Fe(OH)3不溶于NH4Cl—氨水的混合液,Ni(OH)2溶于NH4Cl—氨水的混合液生成[Ni(NH3)6]2+。
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
请回答下列问题:(1)“酸溶”时应先将废镍催化剂粉碎,再与20%硫酸在100℃下反应2小时,该操作的目的为_____。
(2)“滤渣I”主要成分在工业上的用途为___(只写1种即可),NH4Cl的电子式为_____。
(3)“一次碱析”时,加入的NaOH溶液需过量,则含铬微粒发生反应的离子方程式为____。
(4)“氨解”的目的为________,“净化”时加入的H2S的目的是将镍元素转化为NiS沉淀,对应的离子方程式为:________。
新高考化学高考化学压轴题有机合成与推断专项训练分类精编附解析

新高考化学高考化学压轴题 有机合成与推断专项训练分类精编附解析一、高中化学有机合成与推断1.麻黄素H 是拟交感神经药。
合成H 的一种路线如图所示:已知:Ⅰ.芳香烃A 的相对分子质量为92 Ⅱ. Ⅲ.(R 1、R 2可以是氢原子或烃基、R 3为烃基) 请回答下列问题:(1)A 的化学名称为_____________;F 中含氧官能团的名称为_________________。
(2)反应①的反应类型为______________。
(3)G 的结构简式为__________________________。
(4)反应②的化学方程式为______________________________________________。
(5)化合物F 的芳香族同分异构体有多种,M 和N 是其中的两类,它们的结构和性质如下: ①已知M 遇FeCl 3溶液发生显色反应,能和银氨溶液发生银镜反应,苯环上只有两个对位取代基,则M 的结构简式可能为____________________________________。
②已知N 分子中含有甲基,能发生水解反应,苯环上只有一个取代基,则N 的结构有___种(不含立体异构)。
(6) “达芦那韦”是抗击新型冠状病毒潜在用药,合成过程中要制备,参照上述合成路线,设计由和为原料制备的合成路线:________________________________________________________(无机试剂任选)。
2.华法林(物质F)是一种香豆素类抗凝剂,在体内有对抗维生素K 的作用,可用于预防血栓栓塞性疾病。
某种合成华法林的路线如图所示。
请回答下列相关问题。
(1)华法林的分子式是_________________。
物质E 中的含氧官能团名称是_____________。
(2)A →B 的氧化剂可以是__________(填标号)。
a .银氨溶液b .氧气c .新制Cu(OH)2悬浊液d .酸性KMnO 4溶液(3)C →D 的化学方程式是_______________________________________________。
2017年11月浙江省普通高校招生选考科目考试化学试题与答案

2017年11月浙江省普通高校招生选考科目考试化学试题与答案D们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。
下列说法正确的是A.Y的原子半径比X的大B.Q的最高价氧化物的水化物的酸性比Z 的强C.X、Y和氢3种元素形成的化合物中都只有共价键D.Q的单质具有半导体的性质,Q与Z可形成化合物QZ414.下列说法正确的是A.正丁烷和异丁烷均有两种一氯取代物B.乙烯和苯都能与H2发生加成反应,说明二者的分子中均含碳碳双键C.乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈D.乙醛能被还原成乙醇,但不能被氧化成乙酸15.下列说法正确的是A.花生油的主要成分是高级脂肪酸甘油酯,属于高分子化合物B.只有不同种类的氨基酸之间才能形成多肽C.向鸡蛋清的溶液中加入饱和硫酸钠溶液产生沉淀,加水后沉淀可溶解D.向淀粉溶液中加入硫酸溶液,加热后滴入几滴氢氧化铜悬浊液,再加热至沸腾,未出现红色物质,说明淀粉未水解16.已知:N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·molˉ1。
起始反应物为N2和H2,物质的量之比为1︰3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中NH3的物质的量分数如下表:物质的量分数温度400℃450℃500℃600℃压强20 MPa 0.387 0.274 0.189 0.08830 MPa 0.478 0.359 0.260 0.129下列说法正确的是A.体系中NH3的物质的量分数越大,则正反应速率越大B.反应达到平衡时,N2和H2的转化率之比均为1C.反应达到平衡时,放出的热量均为92.4 kJD.600℃,30 MPa下反应达到平衡时,生成NH3的物质的量最多17.金属(M)-空气电池的工作原理如图所示。
下列说法不正确...的是A.金属M作电池负极B.电解质是熔融的MOC.正极的电极反应:O2+4e‾+2H2O=== 4OH‾D.电池反应:2M+O2+2H2O===2M(OH)218.下列说法不正确...的是A.pH<7的溶液不一定呈酸性B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH‾)相等C.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl‾)=c(CH3COO‾) D.氨水和盐酸反应后的溶液,若c(Cl‾)=c(NH+4),则溶液呈中性19.根据Ca(OH)2/CaO体系的能量循环图:错误!错误!下列说法正确的是A.ΔH5>0 B.ΔH1+ΔH2=0C.ΔH3=ΔH4+ΔH5D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5=020.下列说法不正确...的是A.Mg2+和S2ˉ的最外电子层都形成了8个电子的稳定结构B.石英和金刚石都是原子间通过共价键结合形成的原子晶体C.浓H2SO4和H2O混合时放出热量与微粒之间的作用力有关D.H2O2易分解是因为H2O2分子间作用力弱21.在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙醇进料量(单位:mL·minˉ1)的关系如图所示(保持其他条件相同)。
专题25 无机综合推断-2017年浙江学考化学五次真题二年模拟分类汇编(解析版)

专题25 无机综合推断1.【2016年4月浙江省选考】下图中,固体A是铁锈的主要成分。
请回答:(1)白色沉淀E的化学式____________。
(2)写出A---B的化学方程式_____________________。
(3)写出C---D在溶液中发生氧化还原反应的离子方程式______________________。
【答案】BaSO4Fe2O3+3CO2Fe+3CO22Fe3++SO2+2H2O=2Fe2++SO42-+4H+【解析】A是铁锈的主要成分,A为氧化铁,与一氧化碳反应生成单质铁和二氧化碳,铁与氯气反应生成氯化铁,所以固体C为氯化铁,氯化铁与二氧化硫和水反应生成硫酸亚铁,硫酸亚铁溶液中加入氯化钡生成白色沉淀硫酸钡,则E是硫酸钡。
(1)白色沉淀硫酸钡的化学式BaSO4,故答案为:BaSO4;(2)一氧化碳还原氧化铁的化学方程式为:Fe2O3+3CO2Fe+3CO2,故答案为:Fe2O3+3CO2Fe+3CO2;(3)氯化铁与二氧化硫与水反应生成硫酸亚铁,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。
2.【2015年10月浙江省普通高校招生选考】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
请回答:(1)沉淀a中含有的单质是_____________。
(2)沉淀c的化学式是___________________。
(3)溶液A与H2O2溶液在酸性条件下反应的离子方程式是_________________________。
3.【浙江省2017届高三4月普通高校招生选考】为探究黑色固体X(仅含两种元素)的组成和性质,设计并完成如下实验:请回答:(1)X的化学式是________。
(2)固体甲与稀硫酸反应的离子方程式是___________。
备战高考化学无机非金属材料推断题综合经典题

备战高考化学无机非金属材料推断题综合经典题一、无机非金属材料练习题(含详细答案解析)1.赏心悦目的雕花玻璃通常是用某种物质对玻璃进行刻蚀而制成的,则这种物质是()A.盐酸B.氢氟酸C.烧碱D.纯碱【答案】B【解析】【详解】A、盐酸和二氧化硅不反应,不能用于在玻璃上进行刻蚀,故不选A;B、氢氟酸与二氧化硅易反应,生产四氟化硅气体,能在玻璃上进行刻蚀,故选B;C、二氧化硅与烧碱反应,但反应缓慢,不能用于在玻璃上进行刻蚀,故不选C;D、纯碱与二氧化硅在高温下反应,不能用于在玻璃上进行刻蚀,故不选D。
2.晶体是一类非常重要的材料,在很多领域都有广泛的应用。
我国现已能够拉制出直径为300 mm、重达81 kg的大直径硅单晶,晶体硅大量用于电子产业。
下列叙述正确的是()A.形成晶体硅的速率越快越好B.晶体硅有固定的熔沸点,研碎后就变成了非晶体C.可用X射线衍射实验来鉴别晶体硅和玻璃D.晶体硅的形成与晶体的自范性有关,而与各向异性无关【答案】C【解析】【分析】【详解】A.晶体的形成都要有一定的形成条件,如温度、压强、结晶速率等,但并不是说结晶速率越快越好,速率太快可能导致晶体质量下降,故A错误;B.晶体硅有固定的熔点,研碎后仍为原子晶体,故B错误;C.晶体与非晶体最本质的区别是组成物质的粒子在微观空间是否有序排列,x射线衍射可以看到微观结构,所以区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验,故C正确;D.晶体硅的形成与晶体的自范性有关,形成的晶体有各向异性,故D错误;故答案为C。
3.中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是__________________。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是________________;乘务员使用的无线通话机的芯片材料是________________。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与比例中的二氧化硅反应的化学方程式______________________________。
高考化学专题《无机非金属材料》推断题综合检测试卷含详细答案

高考化学专题《无机非金属材料》推断题综合检测试卷含详细答案一、无机非金属材料练习题(含详细答案解析)1.下列溶液中,不能存放在带玻璃塞的试剂瓶中的①碱石灰②NaCl③KNO3④CaO⑤CuSO4⑥NaOH⑦Na2CO3A.①④⑥⑦B.①③⑤⑥C.②③④⑦D.①⑥⑦【答案】A【解析】【分析】玻璃的主要成分中含有二氧化硅,能和二氧化硅反应的药品不能盛放在带有玻璃塞的试剂瓶中,据此分析解答。
【详解】①碱石灰为CaO和NaOH的混合物,能与二氧化硅反应生成具有黏性的硅酸盐和水,因此不能存放在带玻璃塞的试剂瓶中,符合题意;②NaCl与玻璃中的成分不发生反应,因此能存放在带玻璃塞的试剂瓶中,不符合题意;③KNO3与玻璃中的成分不发生反应,因此能存放在带玻璃塞的试剂瓶中,不符合题意;④CaO为碱性氧化物,溶于水生成的氢氧化钙能与二氧化硅反应生成具有黏性的硅酸盐和水,因此不能存放在带玻璃塞的试剂瓶中,符合题意;⑤CuSO4与玻璃中的成分不发生反应,因此能存放在带玻璃塞的试剂瓶中,不符合题意;⑥NaOH能与二氧化硅发生反应生成具有黏性的硅酸盐和水,因此不能存放在带玻璃塞的试剂瓶中,符合题意;⑦Na2CO3水解呈碱性,与二氧化硅反应生成具有黏性的硅酸钠,所以Na2CO3不能盛放在玻璃瓶中,符合题意;故答案为:A。
2.下列实验过程中,始终无明显现象的是()A.SO2通入Ba(NO3)2溶液中B.O2通入Na2SO3溶液中C.Cl2通入Na2SiO3溶液中D.NH3通入Ca(HCO3)2溶液中【答案】B【解析】【分析】【详解】A.二氧化硫被硝酸氧化为硫酸根离子,SO2通入Ba(NO3)2溶液中生成硫酸钡沉淀,故不选A;B.O2通入Na2SO3溶液中,Na2SO3被氧化为Na2SO4,无明显现象,故选B;C.Cl2通入Na2SiO3溶液中,氯气与水反应生成盐酸和次氯酸,盐酸和Na2SiO3反应生成硅酸白色胶状沉淀,故不选C;D.NH3通入Ca(HCO3)2溶液中生成碳酸钙沉淀和碳酸铵,故不选D;故选B 。
历年高考化学无机推断题集锦

历年高考化学无机推断题集锦高考复习面广量大,不少学生感到既畏惧,又无从下手。
同学们如何才能提高复习的针对性和实效性呢?下面来看看高考化学无机推断题,相信对你的复习有很大帮助~1.( 14分)下图是无机物A~N在一定条件下的转化关系(部分产物及反应条件未列出)。
其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
N中只含有两种元素,N可作为工业生产C的原料。
请填写下列空白:(1)在周期表中,组成单质G的元素位于第__________周期_______族。
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_________(填写序号)。
(3)反应⑩的离子方程式是:_______ ______。
(4)反应④ 的离子方程式是:___________________________________。
(5)将化合物D 与KNO3、KOH 共融,可制得一种"绿色"环保高效净水剂K2FeO4 (高铁酸钾).同时还生成KNO2和H2O 。
该反应的化学方程式是:________________________________________________________________(6 )现有1molN参加反应,假设各步反应均完全,生成C的质量为490g,生成G 的质量为224g,则反应①的化学方程式为_______________________。
2.(10分)无机框图下图为中学化学中几种常见物质的转化关系(部分产物已略去)。
已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做致冷剂。
(1)写出化学式F ,写出电子式G ;(2)鉴定G中阳离子的实验方法和现象__________________________________;(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式。
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目。
(完整版)2017年11月浙江选考化学试卷和答案

2017年11月浙江省普通高校招生选考科目考试化学试题2017.111.本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。
其中加试题部分为30分,用【加试题】标出。
2.可能用到的相对原子质量:H 1 C 12N 14O 16Na 23Mg 24Al 27 S 32Cl 35.5K 39 Mn 55 Fe 56Cu 64Ba 137选择题部分一.选择题(每小题只有1个正确选项符合题意。
每小题2分,共50分)1.下列属于氧化物的是A.Na2O B.Ca(OH)2C.HClO D.K2CO32.下列仪器名称为“蒸馏烧瓶”的是A.B.C.D.3.下列属于电解质的是A.镁B.酒精C.硫酸铜D.食盐水4.下列分散系属于悬浊液的是A.牛奶B.蔗糖溶液C.泥浆水D.氢氧化铁胶体5.下列不属于化石燃料的是A.煤B.石油C.天然气D.甲醇6.下列说法不正确...的是A.干冰可用于人工降雨B.碘酸钾可用作加碘食盐的添加剂C.碳酸钠是发酵粉的主要成分D.次氯酸钙是漂白粉的有效成分7.下列属于置换反应的是A.2FeCl3+Cu=CuCl2+2FeCl2B.2HClO光照2HCl+O2↑C.CuO+CO△Cu+CO2D.2Mg+CO2点燃2MgO+C8.下列表示不正确...的是A.氯原子的结构示意图:17828B.二氧化碳的结构式:O=C=O C.CH4的球棍模型:D.乙醛的官能团:-CHO9.下列物质的水溶液不能使酚酞变红的是A.NaOH B.Na2CO3C.NaCl D.NH310.下列方法(必要时可加热)不合理的是A.用澄清石灰水鉴别CO和CO2B.用水鉴别苯和四氯化碳C.用Ba(OH)2溶液鉴别NH4Cl、(NH4)2SO4和K2SO4D.用淀粉碘化钾试纸鉴别碘水和溴水11.下列说法正确的是A.18 8O表示中子数为10的氧元素的一种核素B.金刚石和石墨互为同素异形体,两者之间不能相互转化C.CH3COOH和CH3COOCH3互为同系物D.C6H14的同分异构体有4种,其熔点各不相同12.下列离子方程式不正确...的是A.氢氧化钠溶液与二氧化硅反应:SiO2+2OH-=2SiO-+H2O3B.碳酸钠溶液与氢氧化钡溶液反应:2CO-+Ba(OH)2=BaCO3↓+2OH-3C.酸性硫酸亚铁溶液在空气中被氧化:4Fe2++O2+4H+=4Fe3++2H2OD.氯气与氢氧化钠溶液反应:Cl2+2OH-=ClO-+Cl-+H2O13.Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
新高考化学27题——无机推断题
例1:浙江2015年9月份化学选考卷27题
某固体粉末中可能含有SiO2、Na2O、Ca0、Cu0、Fe2 03,某同学设计并完成如下实验:
请回答:
(1)步骤②中生成蓝色沉淀的离子方程式为。
(2)步骤⑤中生成的白色沉淀是(填化学式)。
(3)根据实验现象,固体粉末中一定存在的组分是(填化学式)。
例2:浙江2015年10月份化学选考卷27题
某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
请回答:
(1)沉淀a中含有的单质是。
(2)沉淀c的化学式是。
(3)溶液A与H2O2溶液在酸性条件下反应的离子方程式是。
例3:浙江2016年4月份化学选考卷27题
下图中,固体A是铁锈的主要成分。
请回答:
(1) 白色沉淀E的化学式________。
(2) 写出A---B的化学方程式____ ____。
(3) 写出C---D在溶液中发生氧化还原反应的离子方程式____ ____。
例4:浙江2016年10月份化学选考卷27题
为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如下实验:
请回答:
(1) X的组成元素为H、O和_______(用元素符号表示),化学式为__________。
(2) 写出经一步反应能得到X的化学方程式(要求非氧化还原反应)_________________。
练习1、(2017温州高二十校期末联考)
有一种埋在地下的矿物X(仅含四种元素),挖出后在空气中容易发黄,现探究其组成和性质,设计完成如下实验:
请回答:
(1)X的化学式_____________,挖出后在空气中容易发黄的原因___________________________。
(2)写出溶液分二等份,加KSCN无明显现象后,滴加双氧水的两个离子方程式:_____________________________,_________________________。
练习2、(2017湖州高三期末)
为探究无机盐X(仅含三种元素,摩尔质量为238g·mol-1,原子个数比为1:1:4)的组成和性质,设计并完成了如下实验:将11.9gX与水共热,生成一种气体单质和某强酸的酸式盐溶液A。
A的焰色
反应呈黄色, A中加入足量的BaCl2溶液,得到23.3g不溶于稀硝酸的白色沉淀。
请回答:
(1)X 的组成元素为Na和(用元素符号表示),其化学式为。
(2)X氧化能力极强,且对环境友好,可用于脱硫、脱硝。
在碱性条件下,X氧化SO32-的离子方程式。
练习3、(2017温州高三十校期末联考)
为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如下实验:
已知,各步反应所需试剂均过量,请回答:
(1)X的化学式为。
(2)写出X与稀硫酸反应的离子方程式。
(3)红色固体B的硫酸盐溶液与纯碱溶液反应能得到X,该反应的化学方程式为。
练习4、(2017宁波高三十校期末联考)
有两种常见元素组成的化合物A,经下述过程可以制备金属D,其中B为砖红色的固体氧化物,气体C 能使品红溶液褪色,所测气体体积已经转化成标况下体积。
试回答:
(1)C的化学式为。
(2)两部分A的质量比a:b= 。
(3)写出A和B反应生成C和D的化学方程式。
练习5、(2017杭州高三期末教学质量检测)
某同学用下列方案探究某带结晶水的不溶性盐X(仅含四种元素)组成。
请回答:
(1)X中的组成元素为H、O外,还包含___ ___(用元素符号表示),X化学式为__________。
(2)溶液Y久置在空气中发生的离子反应方程式_________ _________________。
练习6、(2017猜题卷)
氯化亚铜(CuCl)是一种重要的化工原料,容易被氧化,其合成流程如图所示。
Cu Cu NaCl H2O
Cl2
请回答:
(1)已知还原过程中的产物为Na[CuCl2],写出反应的化学方程式。
(2)合成结束后所得产品用酒精淋洗,让CuCl尽快干燥,原因是。
(3)在CuCl2热溶液中通入SO2气体也可以得到白色CuCl沉淀,写出该反应的离子方程式。
氯化还原稀释、过滤
CuCl。
