甲烷的性质
甲烷分子式

甲烷分子式甲烷分子式为CH4,是无色无味的气体,密度为0。
08g/L,熔点-122 ℃,沸点-182 ℃,临界温度-164 ℃,临界压力6。
67KPa,爆炸极限-4。
8~-12。
5%,自燃点448 ℃。
主要用途有制取天然气、城市煤气、及液化石油气等,也可作为燃料使用。
甲烷是天然气和沼气的主要成分。
甲烷易燃、易爆,甲烷与空气混合物的爆炸极限为12~15%,与氧气混合物的爆炸极限为18。
8~23%。
化学式:碳- 4,氢- 3,氧- 1,氮- 2,硫- 0。
5化学性质比较活泼,在空气中很容易被氧化成为甲醛,所以说甲烷是一种比较容易变成气体的一种天然气,还有就是它是一种非常常见的天然气,并且应用也非常广泛。
相关资料显示,我国目前已探明的天然气储量约占世界总储量的9。
7%,居第三位;其次是俄罗斯,约占世界总储量的10。
1%,居第四位。
根据“十五”计划安排,今后几年将进行大规模勘探开发工作。
到2010年,预测全国天然气消费量将达到1000亿立方米左右。
我国现阶段天然气生产仍处于起步阶段,对外依存度高达60%以上。
未来20年内,随着经济持续快速增长,能源需求不断增加,天然气供给缺口将逐渐扩大。
天然气中主要含一氧化碳、二氧化碳、氮气和水蒸气,此外,还含少量硫化氢、二氧化硫、甲烷、乙烷、丙烷、丁烷、戊烷、二甲醚、乙烯、乙炔、氢气、一氧化碳、二氧化碳、氨气、硫化氢、氯化氢等。
由于各地区原始条件差异甚大,因而形成了多种多样的天然气。
但是都具有以下特征:①含杂质少; ②热值高;③凝固点低;④流动性好;⑤相对密度小(0。
83-0。
86);⑥多数天然气的凝固点都在-161 ℃~-162 ℃之间。
煤在燃烧的过程中,除生成水蒸气、二氧化碳、一氧化碳、二氧化硫、氮氧化物等污染物外,还会产生大量的烟尘和粉尘,这些物质严重影响人们的健康。
近年来,许多研究者致力于煤的清洁利用技术的研究,试图通过改革传统的燃烧方法或采用新型的燃烧设备降低污染物的排放。
甲烷的物理性质和化学性质.

性质结构目标清华中学 文继明用途练习一、甲烷的分子结构甲烷分子是一个正四面体的非极性分子, 分子中四个C--H 键的键角均为'28109两种正四面体的比较'02810906044CH NH 与4P2)光照下与卤素反应2、化学性质:常况下甲烷的性质稳定不能使酸性高锰酸钾 溶液褪色1、物理性质::无色无味气体,比空气轻,难溶于水 二、甲烷的性质1)能燃烧 O H CO O CH 222422+−−→−+点燃甲烷与氯气在光照下的取代产物有:: Cl CH322Cl CH Cl CH CHCl CCl HCl同时还有取代反应:有机物分子中的原子或原子团被其 它的原子或原子团替换的反应。
卤代反应:有机物分子中的原子或原子团被卤素原子所取代的反应。
卤代反应属于取代反应 中的一种 。
22Cl CH 3CHCl 4CCl 空间结构Cl CH 3后退 请用鼠标点击2)光照下与卤素反应2、化学性质:常况下甲烷的性质稳定不能使酸性高锰酸钾 溶液褪色1、物理性质::无色无味气体,比空气轻,难溶于水 二、甲烷的性质1)能燃烧 O H CO O CH 222422+−−→−+点燃3) 高温下分解反应 242H C CH +−−→−高温三、甲烷的存在及用途1、存在:天然气、瓦斯气、沼气等的主要成分均是甲烷2、用途:颜料油漆实验用品医药橡胶工业甲烷燃料返回后退2CO 2H C 和取代反应:有机物分中的原子或原子团被其原子团替换的反应。
卤代反应:有机物分子中的原子或原子团被取代的反应。
卤代反应属于取代反应中的一种 。
22Cl CH 3CHCl ClCH 34CCl 小结4CH1、下列分子中,含有极性键且呈正四面体的是( )甲烷 白磷 氨气 二氯甲烷 2、将甲烷与氯气等体积混合后光照,其产物有( )种1 2 4 5 3、将甲烷与氯气等体积混合后光照,生成最多的是( ) 一氯甲烷 二氯甲烷 氯仿 氯化氢课堂练习A B C D A B C D A B C D3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有化学反应发生的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银 5、下列反应不是取代反应的是( ) A 、光照二氯甲烷与氯气的混合物生成氯仿 B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解课堂练习 答案3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有反应发生 的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银5、下列反应不是取代反应的是( )A 、光照氯仿与氯气的混合物B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解A 答案3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有反应发生 的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银5、下列反应不是取代反应的是( )A 、光照氯仿与氯气的混合物B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解A C 答案3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有反应发生 的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银5、下列反应不是取代反应的是( )A 、光照氯仿与氯气的混合物B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解A C D6、下列事实能说明甲烷分子呈正四面体的是()A、一氯甲烷只有一种结构答案B、二氯甲烷只有一种结构C、三氯甲烷只有一种结构D、四氯化碳只有一种结构7、能说明甲烷的稳定性好的事实是()A、甲烷不能使酸性高锰酸钾溶液褪色B、甲烷不容易液化C、甲烷分子的空间构型是正四面体D、由无水醋酸钠和碱石灰反应制甲烷时需要加热返回上页下页6、下列事实能说明甲烷分子呈正四面体 的是( )A 、一氯甲烷只有一种结构B 、二氯甲烷只有一种结构C 、三氯甲烷只有一种结构D 、四氯化碳只有一种结构7、能说明甲烷的稳定性好的事实是( )A 、甲烷不能使酸性高锰酸钾溶液褪色B 、甲烷不容易液化C 、甲烷分子的空间构型是正四面体D 、由无水醋酸钠和碱石灰反应制甲烷时需 要加热答案 B 下页上页 返回6、下列事实能说明甲烷分子呈正四面体 的是( )A 、一氯甲烷只有一种结构B 、二氯甲烷只有一种结构C 、三氯甲烷只有一种结构D 、四氯化碳只有一种结构7、能说明甲烷的稳定性好的事实是( )A 、甲烷不能使酸性高锰酸钾溶液褪色B 、甲烷不容易液化C 、甲烷分子的空间构型是正四面体D 、由无水醋酸钠和碱石灰反应制甲烷时需 要加热A B 下页上页 返回选做题已知答案已知请仿照上面的反应原理完成下列反应方程式选做题《甲烷》教学目标1、认识甲烷的分子组成及空间结构2、理解取代反应的概念3、掌握甲烷的重要性质4、了解甲烷的存在及重要用途。
甲烷

中文名: 甲烷;沼气;甲基氢化物;液化甲烷英文名: Methane别名: biogas;fire damp;marsh gas;methane gas;methane, compressed;methyl hydride分子结构:分子式: CH4分子量: 16.04物理化学性质性质描述:无色无臭的易燃气体相对密度0.5547(空气=1)沸点-164℃熔点-182.48℃临界温度-82.1℃临界压力4.54MPa自燃点537.78℃燃烧热(25℃)802.86kJ/mol微溶于水,溶于乙醇、乙醚等有机溶剂化学性质较稳定。
在一定条件下能发生卤化反应生成甲烷的卤代烃;经氧化而成醇、醛、酮、酸;经硝化而生成甲烷的硝基化合物;也能发生热解而生成烯、炔烃、燃烧时呈青白色火焰。
与空气的混合气体在燃点时能发生爆炸,爆炸极限为5.3%-14%。
安全信息安全说明:S9:保持容器在一个有良好通风放的场所。
S16:远离火源。
S33:采取防护措施防止静电发生。
其他信息产品应用:甲烷是重要的燃料和重要的化工原料。
以甲烷为主要成分的天然气,作为优质气体燃料,已有悠久的历史,其热值为882.0kJ/mol。
天然气被大规模开采利用,成为世界第三能源。
液化天然气的热值比航空煤油15%,用于汽车、海上快艇和超音速飞机,不但能担高速度。
而且可节省燃料。
除作燃料外,大、氢、乙炔、乙烯、甲醛、二硫化碳、硝基甲烷、氢氰酸和1,4-化可得二、二、三氯甲烷及四氯化碳。
生产方法及其他:在自然界中分布很广,是天然气、煤层气、沼气的主要成分,经分离可以取得。
1.从天然气分离天然气中含甲烷80%-99%,干天然气经清净后使用;湿天然气经清净后,用冷凝法、吸收法、吸附法分离出乙烷以上轻烃后使用。
2.从油田气分离石油开采时从油井中逸出天然气,其中干气含甲烷80%-85%;湿气含甲烷10%。
在加压和冷凝的情况下,可以液化用作化工原料。
3.从炼厂气分离各炼厂石油加工气体中含甲烷20%-50%。
甲烷的性质

6、在光照条件下,将等体积的甲烷和氯气 混合,得到的产物中物质的量最多的是( D) A、CH3Cl B、CH2Cl2 C、CCl4 D、HCl
7、下列叙述正确的是( B ) A、 有机物一定来自有机体内 B、 有机物与无机物可以相互转化 C、 CO属于有机物 D、 A-B + C-D A-C +B-D 一定属于复 分解反应
有机物的特点
种类繁多:3000万种以上 大多易燃烧:甲烷、酒精、汽油…
大多不溶于水而易溶于酒精、汽油等有机溶剂 大多数有机物熔点和沸点较低 大多反应慢、复杂、有副产物
反应用箭头不用等号
1
2
一. 甲烷的组成和结构 甲烷的分子式: CH4
H H C H
H H C H H
结构式
H
电子式
3
甲烷的立体结构
甲烷是正四面体结构,四个C—H键强度相同
球棍模型
比例模型
4
5
二、甲烷的性质
1.物理性质
6
2.化学性质
甲烷的烧
7
1 氧化反应(燃烧)
安静燃烧,淡蓝色火焰,
现象
放出大量的热。
点燃
CH4 + 2O2
CO2 + 2H2O
利用此性质,甲烷可作燃料 注意事项: 1、点燃前要验纯(瓦斯爆炸) CH4爆炸极限:4.9%~16% 2、写有机反应时连接号用“→” 3、 大多数的有机物燃烧后都生成 CO2和H2O
11
CH4 + Cl2
CH3Cl + Cl2
光
CH3Cl + HCl
CH2Cl2 + HCl CHCl3 + HCl
三氯甲烷又叫氯仿 (有机溶剂)
3.1甲烷的化学性质
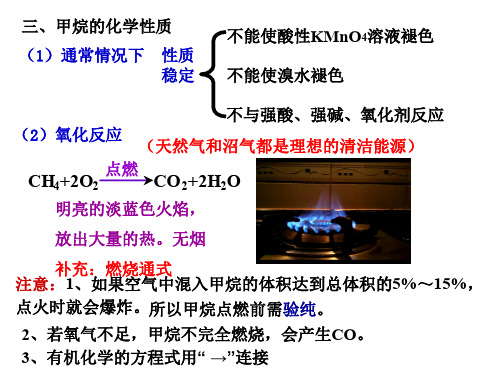
结构
课堂总结
总体: 性质较稳定
甲烷化 学性质
一定条件下
燃烧反应 列反应属于取代反应的是( A、D )
A、CH3CH2OH + HBr CH3CH2Br + H2O
B、2HI + Cl2
2HCl + I2
C、CH4 +2O2 点燃 CO2 + 2H2O
三、甲烷的化学性质
(1)通常情况下 性质 稳定
不能使酸性KMnO4溶液褪色 不能使溴水褪色
不与强酸、强碱、氧化剂反应 (2)氧化反应 (天然气和沼气都是理想的清洁能源)
点燃
CH4+2O2
CO2+2H2O
明亮的淡蓝色火焰,
放出大量的热。无烟
补充:燃烧通式 注意:1、如果空气中混入甲烷的体积达到总体积的5%~15%, 点火时就会爆炸。所以甲烷点燃前需验纯。
注意: 点燃甲烷前必须验纯,否则会爆炸。 CH4爆炸极限:5%~15.4%
(3)取代反应
实验现象(光亮处):
CH4和Cl2
颜色: 黄绿色变浅 水面: 水面上升
量筒: 壁上有油状液体 液面上有少量白雾
(水槽中有白色固体析出)
饱和食盐水 结论:
甲烷的取代反应
甲烷与氯气在光照条件下 发生了反应。
H
+
光照
109°28′
平面四边形
正四面体
例、下列事实能证明甲烷分子中是以C 原子 为中心的正四面体结构的是( B )
A CH3Cl只代表一种物质 B CH2Cl2只代表一种物质 C CHCl3只代表一种物质 D CCl4只代表一种物质
(4)甲烷的受热分解
①甲烷常温时很稳定,高温时可断键 ②甲烷的高温裂解反应方程式:
甲烷的性质

第一节
一、 甲烷的分子结构
甲烷
H
CH4
分子式 电子式
H C H H 结构式
填充模型
球棍模型
填充模型
经过科学实验证明甲烷分子的结构 是正四面体结构,碳原子9。50)。
二、甲烷的性质
物理性质:
甲烷是无色、无味的气体, 密度是0.717g/L(标准状况) 小于空气的密度,极难溶于水。
收集的方法:向下排空气法,排水法
甲烷是池沼底部产生的沼 气和煤矿的坑道所产生的气体 的主要成分。这些甲烷都是在 隔绝空气的情况下,由植物残 体经过微生物发酵的作用而生 成的。
化学性质:
通常情况下,甲烷稳定,如与强酸、强碱和强氧化剂 (三强)等一般不反应。在特定条件下甲烷能与某些物质 发生化学反应,如可以燃烧和发生取代反应等。 1、氧化反应 2、取代反应 3、受热分解
第一节 甲烷
1、有机物:绝大多数含碳的化合物都是有机化 大多数:熔沸点低、难 合物, 简称有机物。 溶于水、可以燃烧。
(个别简单的化合物如:CO﹑CO2和碳酸盐、碳酸氢盐
等虽含有碳元素,但它们的组成和性质与无机物相近,
一向把它们作为无机物。)
2、烃:仅含碳和氢两种元素的有机物 称为碳氢化合物,又称烃。 最简单的有机物、烃是什么?
思考与练习: 1mol CH4与Cl2混合在漫散光的照射下,
CH4与Cl2均无剩余,生成等物质的量的四种 有机物,参加反应的Cl2的物质的量为多少?
3、受热分解:
在隔绝空气的情况下,加热至10000C,甲烷 分解生成炭黑和氢气。
CH4 C + 2H2
三、应用:
三氯甲烷和四氯甲烷是工业上重要的溶剂。 氢气是合成氨和合成汽油等工业的原料;炭黑是橡 胶和染料的工业原料。
甲烷燃烧的化学方程式及性质

甲烷燃烧的化学方程式及性质
为了让大家更好的学习化学物品甲烷,下面由作者为你精心准备了“甲烷燃烧的化学方程式及性质”,持续关注本站将可以持续获取更多的考试资讯!
甲烷燃烧的化学方程式
完全燃烧:CH4+2O2=CO2+2H2O
不完全燃烧:2CH4+3O2=2CO+4H2O
甲烷的性质
1.甲烷的物理性质
甲烷是无色无味、极难溶于水、密度比空气小的气体。
2.甲烷的化学性质
(1)具有稳定性
通常情况下,甲烷性质比较稳定,与强酸、强碱不反应,与高锰酸钾溶液等强氧化剂也不反应。
(2)氧化反应——可燃性
将甲烷在空气中点燃,观察燃烧现象并检验燃烧产物。
甲烷的存在与用途
(1)甲烷的存在
甲烷是天然气、沼气、油田气和煤矿坑道气的主要成分。
我国的天然气主要分布在中西部地区及海底。
(2)甲烷的主要用途
以甲烷为主要成分的天然气和沼气都是理想的清洁能源。
甲烷还可用作化工原料。
归纳总结:
甲烷分子空间构型为正四面体形,碳原子位于中心,4个氢原子位于顶点,4个C—H键的。
表- 甲烷的理化性质及危险特性
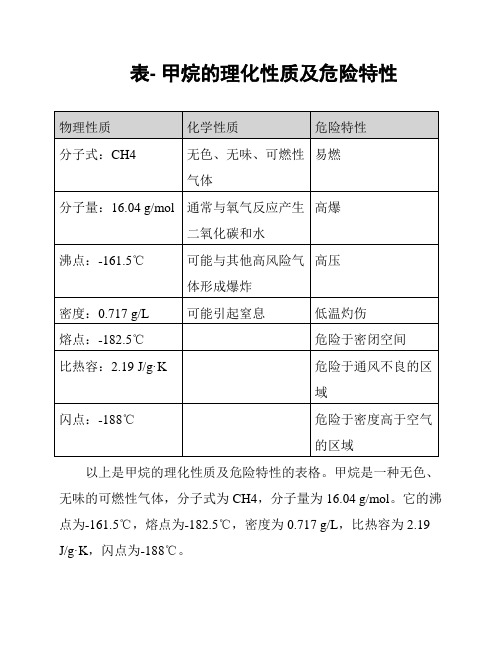
表- 甲烷的理化性质及危险特性
以上是甲烷的理化性质及危险特性的表格。
甲烷是一种无色、无味的可燃性气体,分子式为CH4,分子量为16.04 g/mol。
它的沸点为-161.5℃,熔点为-182.5℃,密度为0.717 g/L,比热容为2.19 J/g·K,闪点为-188℃。
甲烷在常温常压下与氧气反应产生二氧化碳和水,同时也可能与其他高风险气体形成爆炸。
它是易燃物质,具有高爆特性,并且可能引发高压、低温灼伤等危险。
甲烷还可能引起窒息,危险于密闭空间和通风不良的区域,以及密度高于空气的区域。
在处理甲烷时,需要注意其危险特性,并采取适当的安全措施以确保人员和环境的安全。
以上是关于甲烷的理化性质及危险特性的描述。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
甲烷甲烷分子式CH4。
最简单的有机化合物。
甲烷是没有颜色、没有气味的气体,沸点-161.4℃,比空气轻,它是极难溶于水的可燃性气体。
甲烷和空气成适当比例的混合物,遇火花会发生爆炸。
化学性质相当稳定,跟强酸、强碱或强氧化剂(如KMnO4)等一般不起反应。
在适当条件下会发生氧化、热解及卤代等反应。
甲烷在自然界分布很广,是天然气、沼气、坑气及煤气的主要成分之一。
它可用作燃料及制造氢、一氧化碳、炭黑、乙炔、氢氰酸及文字甲醛等物质的原料。
413kJ/mol、109°28′,甲烷分子是正四面体空间构型,上面的结构式只是表示分子里各原子的连接情况,并不能真实表示各原子的空间相对位置。
1.物质的理化常数:国标编号21007CAS号74-82-8中文名称甲烷英文名称methane;Marsh gas别名沼气分子式CH4 外观与性状无色无臭气体分子量16.04 蒸汽压53.32kPa/-168.8℃闪点:-188℃熔点-182.5℃沸点:-161.5℃溶解性微溶于水,溶于醇、乙醚密度相对密度(水=1)0.42(-164℃);相对密度(空气=1)0.55 稳定性稳定危险标记4(易燃液体) 主要用途用作燃料和用于炭黑、氢、乙炔、甲醛等的制造2.对环境的影响:一、健康危害侵入途径:吸入。
健康危害:甲烷对人基本无毒,但浓度过高时,使空气中氧含量明显降低,使人窒息。
当空气中甲烷达25%-30%时,可引起头痛、头晕、乏力、注意力不集中、呼吸和心跳加速、共济失调。
若不及时脱离,可致窒息死亡。
皮肤接触液化本品,可致冻伤。
二、毒理学资料及环境行为毒性:属微毒类。
允许气体安全地扩散到大气中或当作燃料使用。
有单纯性窒息作用,在高浓度时因缺氧窒息而引起中毒。
空气中达到25~30%出现头昏、呼吸加速、运动失调。
急性毒性:小鼠吸入42%浓度×60分钟,麻醉作用;兔吸入42%浓度×60分钟,麻醉作用。
危险特性:易燃,与空气混合能形成爆炸性混合物,遇热源和明火有燃烧爆炸的危险。
与五氧化溴、氯气、次氯酸、三氟化氮、液氧、二氟化氧及其它强氧化剂接触剧烈反应。
燃烧(分解)产物:一氧化碳、二氧化碳。
3.现场应急监测方法:4.实验室监测方法:气相色谱法《空气中有害物质的测定方法》(第二版),杭士平编可燃溶剂所显色法;容量分析法《水和废水标准检验法》第20版(美)5.环境标准:前苏联车间空气中有害物质的最高容许浓度300mg/m3美国车间卫生标准窒息性气体6.应急处理处置方法:一、泄漏应急处理迅速撤离泄漏污染区人员至上风处,并进行隔离,严格限制出入。
切断火源。
建议应急处理人员戴自给正压式呼吸器,穿消防防护服。
尽可能切断泄漏源。
合理通风,加速扩散。
喷雾状水稀释、溶解。
构筑围堤或挖坑收容产生的大量废水。
如有可能,将漏出气用排风机送至空旷地方或装设适当喷头烧掉。
也可以将漏气的容器移至空旷处,注意通风。
漏气容器要妥善处理,修复、检验后再用。
二、防护措施呼吸系统防护:一般不需要特殊防护,但建议特殊情况下,佩带自吸过滤式防毒面具(半面罩)。
眼睛防护:一般不需要特别防护,高浓度接触时可戴安全防护眼镜。
身体防护:穿防静电工作服。
手防护:戴一般作业防护手套。
其它:工作现场严禁吸烟。
避免长期反复接触。
进入罐、限制性空间或其它高浓度区作业,须有人监护。
三、急救措施皮肤接触:若有冻伤,就医治疗。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
灭火方法:切断气源。
若不能立即切断气源,则不允许熄灭正在燃烧的气体。
喷水冷却容器,可能的话将容器从火场移至空旷处。
灭火剂:雾状水、泡沫、二氧化碳、干粉。
第一部分:化学品名称化学品中文名称:甲烷化学品英文名称:methane中文名称2:沼气英文名称2:Marshgas技术说明书编码:51CASNo.:74-82-8分子式:CH4分子量:16.04第二部分:成分/组成信息有害物成分含量CASNo.甲烷74-82-8第三部分:危险性概述危险性类别:侵入途径:健康危害:甲烷对人基本无毒,但浓度过高时,使空气中氧含量明显降低,使人窒息。
当空气中甲烷达25%~30%时,可引起头痛、头晕、乏力、注意力不集中、呼吸和心跳加速、共济失调。
若不及时脱离,可致窒息死亡。
皮肤接触液化本品,可致冻伤。
环境危害:燃爆危险:本品易燃,具窒息性。
第四部分:急救措施皮肤接触:若有冻伤,就医治疗。
眼睛接触:吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:第五部分:消防措施危险特性:易燃,与空气混合能形成爆炸性混合物,遇热源和明火有燃烧爆炸的危险。
与五氧化溴、氯气、次氯酸、三氟化氮、液氧、二氟化氧及其它强氧化剂接触剧烈反应。
有害燃烧产物:一氧化碳、二氧化碳。
灭火方法:切断气源。
若不能切断气源,则不允许熄灭泄漏处的火焰。
喷水冷却容器,可能的话将容器从火场移至空旷处。
灭火剂:雾状水、泡沫、二氧化碳、干粉。
第六部分:泄漏应急处理应急处理:迅速撤离泄漏污染区人员至上风处,并进行隔离,严格限制出入。
切断火源。
建议应急处理人员戴自给正压式呼吸器,穿防静电工作服。
尽可能切断泄漏源。
合理通风,加速扩散。
喷雾状水稀释、溶解。
构筑围堤或挖坑收容产生的大量废水。
如有可能,将漏出气用排风机送至空旷地方或装设适当喷头烧掉。
也可以将漏气的容器移至空旷处,注意通风。
漏气容器要妥善处理,修复、检验后再用。
第七部分:操作处置与储存操作注意事项:密闭操作,全面通风。
操作人员必须经过专门培训,严格遵守操作规程。
远离火种、热源,工作场所严禁吸烟。
使用防爆型的通风系统和设备。
防止气体泄漏到工作场所空气中。
避免与氧化剂接触。
在传送过程中,钢瓶和容器必须接地和跨接,防止产生静电。
搬运时轻装轻卸,防止钢瓶及附件破损。
配备相应品种和数量的消防器材及泄漏应急处理设备。
储存注意事项:储存于阴凉、通风的库房。
远离火种、热源。
库温不宜超过30℃。
应与氧化剂等分开存放,切忌混储。
采用防爆型照明、通风设施。
禁止使用易产生火花的机械设备和工具。
储区应备有泄漏应急处理设备。
第八部分:接触控制/个体防护职业接触限值中国MAC(mg/m3):未制定标准前苏联MAC(mg/m3):300TLVTN:ACGIH窒息性气体TLVWN:未制定标准监测方法:工程控制:生产过程密闭,全面通风。
呼吸系统防护:一般不需要特殊防护,但建议特殊情况下,佩戴自吸过滤式防毒面具(半面罩)。
眼睛防护:一般不需要特殊防护,高浓度接触时可戴安全防护眼镜。
身体防护:穿防静电工作服。
手防护:戴一般作业防护手套。
其他防护:工作现场严禁吸烟。
避免长期反复接触。
进入罐、限制性空间或其它高浓度区作业,须有人监护。
第九部分:理化特性主要成分:纯品外观与性状:无色无臭气体。
pH:熔点(℃):-182.5沸点(℃):-161.5相对密度(水=1):0.42(-164℃)相对蒸气密度(空气=1):0.55饱和蒸气压(kPa):53.32(-168.8℃)燃烧热(kJ/mol):889.5临界温度(℃):-82.6临界压力(MPa):4.59辛醇/水分配系数的对数值:无资料闪点(℃):-188引燃温度(℃):538爆炸上限%(V/V):15爆炸下限%(V/V):5.3溶解性:微溶于水,溶于醇、乙醚。
主要用途:用作燃料和用于炭黑、氢、乙炔、甲醛等的制造。
其它理化性质:第十部分:稳定性和反应活性稳定性:禁配物:强氧化剂、氟、氯。
避免接触的条件:聚合危害:分解产物:第十一部分:毒理学资料急性毒性:LD50:无资料LC50:无资料亚急性和慢性毒性:刺激性:致敏性:致突变性:致畸性:致癌性:第十二部分:生态学资料生态毒理毒性:生物降解性:非生物降解性:生物富集或生物积累性:其它有害作用:该物质对环境可能有危害,对鱼类和水体要给予特别注意。
还应特别注意对地表水、土壤、大气和饮用水的污染。
第十三部分:废弃处置废弃物性质:废弃处置方法:处置前应参阅国家和地方有关法规。
建议用焚烧法处置。
废弃注意事项:第十四部分:运输信息危险货物编号:21007UN编号:1971包装标志:包装类别:O52包装方法:钢质气瓶。
运输注意事项:采用刚瓶运输时必须戴好钢瓶上的安全帽。
钢瓶一般平放,并应将瓶口朝同一方向,不可交叉;高度不得超过车辆的防护栏板,并用三角木垫卡牢,防止滚动。
运输时运输车辆应配备相应品种和数量的消防器材。
装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。
严禁与氧化剂等混装混运。
夏季应早晚运输,防止日光曝晒。
中途停留时应远离火种、热源。
公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。
铁路运输时要禁止溜放。
第十五部分:法规信息法规信息化学危险物品安全管理条例(1987年2月17日国务院发布),化学危险物品安全管理条例实施细则(化劳发[1992]677号),工作场所安全使用化学品规定([1996]劳部发423号)等法规,针对化学危险品的安全使用、生产、储存、运输、装卸等方面均作了相应规定;常用危险化学品的分类及标志(GB13690-92)将该物质划为第2.1类易燃气体。
用途:气体燃料、制炭黑、制氢气、四氯化碳灭火剂等.。
