实验室常用试剂缓冲液配制方法一览表
常用缓冲液的配制方法

1N
40.00
碳酸钠Na2CO3
106.00
1N
53.00
磷酸氢二钠Na2HPO4.12H2O
358.20
1N
358.20
磷酸二氢钾KH2PO4
136.10
1/15M
9.08
重铬酸钾K2Cr2O7
294.20
0.1N
4.9035
碘化钾KI
166.00
0.5N
83.00
高锰酸钾KMO4
158.00
GR.
ACS.
PA.
XЦ.
CP.
PUSS.
Puriss.
ЦДA.
LR.
EP.
Ц.
p.
pure
用途
纯度最高,杂质含量最少的试剂。适用于最精确分析及研究工作
纯度较高,杂质含量较低。适用于精确的微量分析工作,为分析实验室广泛使用
质量略低于二级试剂,适用于一般的微量分析实验,包括要求不高的工业分析和快速分析
4.2
2.65
7.35
5.4
8.60
1.40
4.4
3.70
6.30
5.6
9.10
0.90
4.6
4.90
5.10
5.8
9.40
0.60
(三)巴比妥钠-盐酸缓冲液(18℃)
PH
0.04M巴比妥钠溶液ml
0.2N盐酸
(毫升)
PH
0.04M巴比妥钠溶液ml
0.2N盐酸
(毫升)
6.8
100
18.4
8.4
100
0.1N
3.16
醋酸钠NaC2H3O2
82.04
各种缓冲溶液配制表-
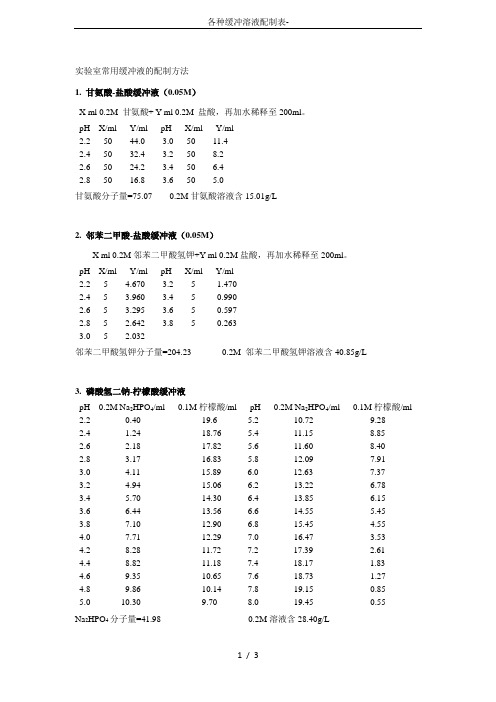
实验室常用缓冲液的配制方法1. 甘氨酸-盐酸缓冲液(0.05M)X ml 0.2M 甘氨酸+ Y ml 0.2M 盐酸,再加水稀释至200ml。
pH X/ml Y/ml pH X/ml Y/ml2.2 50 44.03.0 50 11.42.4 50 32.43.2 50 8.22.6 50 24.23.4 50 6.42.8 50 16.83.6 50 5.0甘氨酸分子量=75.07 0.2M甘氨酸溶液含15.01g/L2. 邻苯二甲酸-盐酸缓冲液(0.05M)X ml 0.2M邻苯二甲酸氢钾+Y ml 0.2M盐酸,再加水稀释至200ml。
pH X/ml Y/ml pH X/ml Y/ml2.2 5 4.6703.2 5 1.4702.4 53.960 3.4 5 0.9902.6 53.295 3.6 5 0.5972.8 5 2.6423.8 5 0.2633.0 5 2.032邻苯二甲酸氢钾分子量=204.23 0.2M 邻苯二甲酸氢钾溶液含40.85g/L3. 磷酸氢二钠-柠檬酸缓冲液pH 0.2M Na2HPO4/ml 0.1M柠檬酸/ml pH 0.2M Na2HPO4/ml 0.1M柠檬酸/ml 2.2 0.40 19.6 5.2 10.72 9.282.4 1.24 18.76 5.4 11.15 8.852.6 2.18 17.82 5.6 11.60 8.402.83.17 16.83 5.8 12.09 7.913.04.11 15.896.0 12.637.373.24.94 15.066.2 13.22 6.783.4 5.70 14.30 6.4 13.85 6.153.6 6.44 13.56 6.6 14.555.453.8 7.10 12.90 6.8 15.454.554.0 7.71 12.29 7.0 16.47 3.534.2 8.28 11.72 7.2 17.39 2.614.4 8.82 11.18 7.4 18.17 1.834.6 9.35 10.65 7.6 18.73 1.274.8 9.86 10.14 7.8 19.15 0.855.0 10.30 9.70 8.0 19.45 0.55Na2HPO4分子量=41.98 0.2M溶液含28.40g/LNa2HPO4·2H2O分子量=78.05 0.2M溶液含35.61gC6H8O7·H2O分子量=10.14 0.1M溶液含21.01g/L4. 柠檬酸-氢氧化钠-盐酸缓冲液pH 钠离子浓度/M 柠檬酸C6H8O7·H2O/g 氢氧化钠NaOH/g 浓盐酸HCl/ml 终体积/L2.2 0.20 210 84 160 103.1 0.20 210 83 116 103.3 0.20 210 83 106 104.3 0.20 210 83 45 105.3 0.35 245 144 68 105.8 0.45 285 186 105 106.5 0.38 266 156 126 10使用时可以每升中加入1g酚,若最后pH有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
实验室常用试剂和缓冲液配方

实验室常用试剂和缓冲液配方实验室中常用的试剂和缓冲液配方有很多种,下面将介绍一些常用的试剂和缓冲液的配方:一、试剂的配方1. Tris缓冲液:- 3 M Tris-Cl,pH 7.4(准备方法:将121.1 g Tris粉末溶解在800 mL去离子水中,使用HCl调节pH值至7.4,并将溶液体积加至1 L)2.NaCl溶液:-5MNaCl(准备方法:将287.7gNaCl溶解在800mL去离子水中,并将溶液体积加至1L)3.验血试剂:-4%NaOH溶液(准备方法:将40gNaOH溶解在900mL去离子水中,并将溶液体积加至1L)-5%CuSO4溶液(准备方法:将50gCuSO4溶解在900mL去离子水中,并将溶液体积加至1L)-2%K4[Fe(CN)6]溶液(准备方法:将20gK4[Fe(CN)6]溶解在900mL去离子水中,并将溶液体积加至1L)4.PBS缓冲液(磷酸盐缓冲液):-10×PBS缓冲液(准备方法:将80gNaCl,2gKCl,11.5gNa2HPO4,2gKH2PO4溶解在800mL去离子水中,并将溶液体积加至1L。
pH值可以调节至7.4左右)5. Tris-EDTA缓冲液(TE缓冲液):- 10 mM Tris-HCl,1 mM EDTA,pH 8.0(准备方法:将12.1 gTris溶解在800 mL去离子水中,然后加入0.37 g EDTA,使用HCl调节pH值至8.0,并将溶液体积加至1 L)二、缓冲液的配方1. Tris-HCl缓冲液:- 50 mM Tris-HCl,100 mM NaCl,1% Triton X-100,pH 7.4(准备方法:将6.05 g Tris,5.8 g NaCl,0.1 g Triton X-100溶解在800mL去离子水中,使用HCl调节pH值至7.4,并将溶液体积加至1 L)2. Tris-Borate缓冲液(TBE缓冲液):- 89 mM Tris,89 mM boric acid,2 mM EDTA,pH 8.3(准备方法:将10.81 g Tris,5.49 g boric acid,3.72 g EDTA溶解在800 mL去离子水中,使用NaOH或HCl调节pH值至8.3,并将溶液体积加至1 L)3. Tris-Glycine缓冲液:- 25 mM Tris,192 mM glycine,0.1% SDS,pH 8.3(准备方法:将3.03 g Tris,14.35 g glycine溶解在800 mL去离子水中,使用HCl调节pH值至8.3,并将溶液体积加至1 L)4. Tris-Acetate缓冲液(TAE缓冲液):- 40 mM Tris,20 mM acetic acid,1 mM EDTA,pH 8.3(准备方法:将4.84 g Tris,1.86 g acetic acid,0.37 g EDTA溶解在800 mL去离子水中,使用NaOH或HCl调节pH值至8.3,并将溶液体积加至1 L)5. Phosphate缓冲液:- 100 mM sodium phosphate,pH 7.0(准备方法:根据目标pH值使用磷酸二氢钠和磷酸氢二钠调节溶液pH至7.0,并将溶液体积加至1 L)以上只是一些常用的试剂和缓冲液的配方,并不是全部。
实验室常用试剂缓冲液配制方法一览表

实验常用试剂、缓冲液的配制方法1、1M Tris-HCl□组份浓度1 M Tris-HCl(pH7.4,7.6,8.0)□配制量1L□配置方法1. 称量121.1gTris置于1L烧杯中。
2. 加入约800mL的去离子水,充分搅拌溶解。
3. 按下表量加入浓盐酸调节所需要的pH值。
pH值浓HCl7.4 约70mL7.6 约60mL8.0 约42mL4. 将溶解定容至1L。
5. 高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tris溶液的pH 值随温度的变化差很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
2、1.5 M Tris-HCl□组份浓度1.5 M Tris-HCl(pH8.8)□配制量1L□配置方法1.称取181.7gTris置于1L烧杯中。
2. 加入约800mL的去离子水,充分搅拌溶解。
3. 用浓盐酸调pH值至8.8。
4. 将溶液定容至1L。
5. 高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tris溶液的pH值随温度的变化差异很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
3、10×TE Buffer□组份浓度100 mM Tris-HCl,10 mM EDTA (pH 7.4,7.6,8.0)□配制量1L□配置方法1. 量取下列溶液,置于1L烧杯中。
1 M Tris-HCl Buffer(pH7.4,7.6,8.0)100mL500 mM EDTA(pH8.0)20mL2. 向烧杯中加入约800mL的去离子水,均匀混合。
3. 将溶液定至1L后,高温高压灭菌。
4. 室温保存。
4、3 M 醋酸钠□组份浓度3 M 醋酸钠(pH5.2)□配制量100mL□配置方法1. 称取40.8gNaOAc•3H2O置于100~200mL烧杯中,加入约40mL的去离子水搅拌溶解。
2. 加入冰乙酸调节pH值至5.2。
3. 加入去离子水将溶液定容至100mL。
实验常用试剂缓冲液的配制方法

实验常用试剂缓冲液的配制方法
一、常用试剂和试剂配置
1、氯仿。
将1L 99.7%纯度的氯仿加入水中,调节pH值至7.4,溶解
即可得到0.5mol/L的氯仿溶液。
2、二氧化碳水。
将100mL弱碳酸氢氧化钠溶液(NaHCO3,0.5mol/L)加入1L水中,经过气泡交换,可制得CO2水。
3、磷酸盐缓冲液。
将200mL磷酸盐溶液(K2HPO4,0.5mol/L)加入800mL水中,调节pH值至7.2,搅拌均匀,即可得到0.2mol/L磷酸盐缓
冲液。
4、EDTA标准溶液。
将25.0g EDTA·4Na(C10H14N2O8Na2)加入
1000mL水中,热溶解,调节pH值至7.0,搅拌均匀,得到0.2mol/LEDTA
标准溶液。
5、肌酐标准溶液。
将10.0g肌酐(C10H13N3O8)=14.2H2O)加入
1000mL的水中,搅拌,调节pH值至7.4,搅拌均匀,即可得到0.1mol/L
的肌酐标准溶液。
二、缓冲液的配置
1、弱酸缓冲液。
将3.0mL 0.2mol/L磷酸钠溶液(Na2HPO4)加入到
97mL 0.2mol/L磷酸钙溶液(Ca(H2PO4)2)中,搅拌均匀,即可得到
0.2mol/L的弱酸缓冲液。
2、弱碱缓冲液。
将3.0mL 0.2mol/L磷酸氢氧化钠溶液(NaH2PO4)
加入到97mL 0.2mol/L碳酸氢钙溶液(Ca(HCO3)2)中,搅拌均匀,即可
得到0.2mol/L的弱碱缓冲液。
3、弱盐缓冲液。
常见缓冲溶液配制方法

常见缓冲溶液配制方法1.醋酸钠/醋酸酸性缓冲液醋酸钠/醋酸酸性缓冲液适用于pH范围为4.0-6.0的实验。
配制方法如下:- 准备质量浓度为0.1mol/L的醋酸钠溶液和0.1mol/L的醋酸溶液。
-根据所需pH值,按照相应的比例混合醋酸钠溶液和醋酸溶液即可。
2.磷酸/盐酸性缓冲液磷酸/盐酸性缓冲液适用于pH范围为1.0-3.0的实验。
配制方法如下:- 准备0.2mol/L的盐酸溶液。
- 准备分别为0.2mol/L和0.1mol/L的磷酸溶液。
-具体配制时,根据所需pH值,按照相应的比例混合盐酸溶液和磷酸溶液即可。
3.磷酸/氢磷酸二盐酸性缓冲液磷酸/氢磷酸二盐酸性缓冲液适用于pH范围为2.0-7.0的实验。
配制方法如下:- 准备0.2mol/L的盐酸溶液。
- 准备分别为0.2mol/L、0.1mol/L和0.05mol/L的氢磷酸二盐溶液。
-具体配制时,根据所需pH值,按照相应的比例混合盐酸溶液和氢磷酸二盐溶液即可。
4.磷酸盐缓冲液磷酸盐缓冲液适用于pH范围为5.0-8.0的实验。
配制方法如下:- 准备分别为0.2mol/L的梯度磷酸盐溶液。
-根据所需pH值,按照相应的比例混合相应浓度的磷酸盐溶液即可。
5.三氯乙酸/三氯乙酸钠酸性缓冲液三氯乙酸/三氯乙酸钠酸性缓冲液适用于pH范围为3.0-4.6的实验。
配制方法如下:- 准备质量浓度为0.2mol/L的三氯乙酸钠溶液和0.2mol/L的三氯乙酸溶液。
-根据所需pH值,按照相应的比例混合三氯乙酸钠溶液和三氯乙酸溶液即可。
以上是一些常见的缓冲溶液配制方法,具体的配制过程可能会因实验需求和具体试剂而略有不同。
在配制缓冲溶液时,一定要注意使用高纯度的试剂,并按照配制方法进行准确的实验操作。
缓冲液配制方法
25.5
5.8
42.3
4.5
8.7
5.2
28.8
5.9
43.7
4.6
11.1
5.3
31.6
4.7
13.6
5.4
34.1
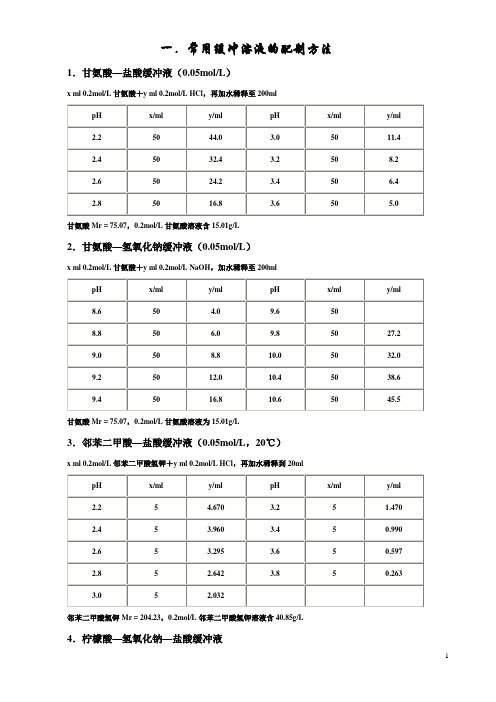
邻苯二甲酸氢钾Mr = 204.23,0.1mol/L溶液为20.42g/L
9.磷酸盐缓冲液
(1)磷酸氢二钠—磷酸二氢钠缓冲液(0.2mol/L)
pH
0.2mol/L
Na2HPO4/ml
pH
Na+浓度
/mol/L
柠檬酸/g
C6H8O7·H2O
氢氧化钠/g
NaOH(97%)
盐酸/ml
HCl(浓)
最终体积/L*
2.2
0.20
210
84
160
10
3.1
0.20
210
83
116
10
3.3
0.20
210
83
106
10
4.3
0.20
210
83
45
10
5.3
0.35
245
144
68
10
5.8
0.45
50
11.0
10.0
50
43.0
9.6
50
23.0
10.1
50
46.0
硼砂Na2B4O7·10H2O,Mr = 381.43,0.05mol/L溶液为19.07g/L
硼砂/ml
0.2mol/L
硼酸/ml
7.4
1.0
9.0
8.2
3.5
6.5
7.6
1.5
各种缓冲液配制方法

各种缓冲液配制方法缓冲液是一种用于调节溶液的pH值的溶液,常用于实验室中的生物化学和分子生物学实验中。
根据所需的pH范围和实验目的,可以使用不同的缓冲液配制方法。
以下是一些常见的缓冲液配制方法:1.磷酸盐缓冲液(PBS)磷酸盐缓冲液是一种常见的生物学实验中使用的缓冲液。
它的制备方法如下:-取一个容器,加入8克氯化钠(NaCl),0.2克磷酸二氢钠(NaH2PO4),和1.44克磷酸氢二钠(Na2HPO4)。
-加入适量的去离子水,搅拌溶解。
-将溶液转移到一个容量为1升的烧杯中。
-用去离子水补足体积至1升,并用1升体积瓶准确稀释至1升。
2. Tris缓冲液Tris缓冲液适用于pH 7-9范围内的实验。
制备方法如下:- 取一个容器,加入121.14克Tris(羟甲基氨基甲烷)。
-加入适量的去离子水,搅拌溶解。
-将溶液转移到一个容量为1升的烧杯中。
-用去离子水补足体积至1升,并用1升体积瓶准确稀释至1升。
3.醋酸盐缓冲液醋酸盐缓冲液适用于pH3-5范围内的实验。
制备方法如下:-取一个容器,加入20毫升醋酸钠三水合物(NaC2H3O2·3H2O)。
-加入6毫升醋酸。
-加入适量的去离子水,搅拌溶解。
-将溶液转移到一个容量为1升的烧杯中。
-用去离子水补足体积至1升,并用1升体积瓶准确稀释至1升。
4.磷酸缓冲液磷酸缓冲液适用于pH2-8范围内的实验。
制备方法如下:-取一个容器,加入0.126克磷酸二氢钾(KH2PO4)。
-加入0.680克磷酸二氢钠(Na2HPO4)。
-加入适量的去离子水,搅拌溶解。
-将溶液转移到一个容量为1升的烧杯中。
-用去离子水补足体积至1升,并用1升体积瓶准确稀释至1升。
5.碳酸氢盐缓冲液(HEPES缓冲液)HEPES缓冲液适用于pH6-8范围内的实验。
-取一个容器,加入10克HEPES。
-加入适量的去离子水,搅拌溶解。
-将溶液转移到一个容量为1升的烧杯中。
-用去离子水补足体积至1升,并用1升体积瓶准确稀释至1升。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验室常用试剂缓冲液配制方法一览表实验常用试剂、缓冲液的配制方法1、1MTri-HCl□组份浓度1MTri-HCl(pH7.4,7.6,8.0)□配制量1L□配置方法1.称量121.1gTri置于1L烧杯中。
2.加入约800mL的去离子水,充分搅拌溶解。
3.按下表量加入浓盐酸调节所需要的pH值。
pH值浓HCl7.4约70mL7.6约60mL8.0约42mL4.将溶解定容至1L。
5.高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tri溶液的pH值随温度的变化差很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
2、1.5MTri-HCl□组份浓度1.5MTri-HCl(pH8.8)□配制量1L□配置方法1.称取181.7gTri置于1L烧杯中。
2.加入约800mL的去离子水,充分搅拌溶解。
3.用浓盐酸调pH值至8.8。
4.将溶液定容至1L。
5.高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tri溶液的pH值随温度的变化差异很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
3、10某TEBuffer□组份浓度100mMTri-HCl,10mMEDTA(pH7.4,7.6,8.0)□配制量1L□配置方法1.量取下列溶液,置于1L烧杯中。
1MTri-HClBuffer(pH7.4,7.6,8.0)100mL500mMEDTA(pH8.0)20mL2.向烧杯中加入约800mL的去离子水,均匀混合。
3.将溶液定至1L 后,高温高压灭菌。
4.室温保存。
4、3M醋酸钠□组份浓度3M醋酸钠(pH5.2)□配制量100mL□配置方法1.称取40.8gNaOAc3H2O置于100~200mL烧杯中,加入约40mL的去离子水搅拌溶解。
2.加入冰乙酸调节pH值至5.2。
3.加入去离子水将溶液定容至100mL。
4.高温高压灭菌后,室温保存。
5、PBSBuffer□组份浓度137mMNaCl,2.7mMKCl,10mMNa2HPO4,2mMKH2PO4□配制量1L□配置方法1.称量下列试剂,置于1L烧杯中。
NaCl8gKCl0.2gNa2HPO41.42gKH2PO40.27g2.向烧杯中加入约800mL的去离子水,充分搅拌溶解。
3.滴加HCl将pH值调节至7.4,然后加入去离子水将溶液定容至1L。
4.高温高压灭菌后,室温保存。
注意:上述PBSBuffer中无二价阳离子,如需要,可在配方中补充1mMCaCl2和0.5mMMgCl2。
6、10M醋酸铵□组份浓度10M醋酸铵□配制量100mL□配置方法1.称量77.1g醋酸铵置于100~200mL烧杯中,加入约30mL的去离子水搅拌溶解。
2.加去离子水将溶液定容至100mL。
3.使用0.22μm滤膜过滤除菌。
4.密封瓶口于室温保存。
注意:醋酸铵受热易分解,所以不能高温高压灭菌。
7、Tri-HCl平衡苯酚□配置方法1.使用原料:大多数市售液化苯酚是清亮无色的,无需重蒸馏便可用于分子生物学实验。
但有些液化苯酚呈粉红色或黄色,应避免使用。
同时也应避免使用结晶苯酚,结晶苯酚必须在160℃对其进行重蒸馏除去诸如醌等氧化产物,这些氧化产物可引起磷酸二酯键的断裂或导致RNA和DNA的交联等。
因此,苯酚的质量对DNA、RNA的提取极为重要,我们推荐使用高质量的苯酚进行分子生物学实验。
2.操作注意:苯酚腐蚀性极强,并可引起严重灼伤,操作时应戴手套及防护镜等。
所有操作均应在通风橱中进行,与苯酚接触过的皮肤部位应用大量水清洗,并用肥皂和水洗涤,忌用乙醇。
3.苯酚平衡:因为在酸性pH条件下DNA分配于有机相,因此使用苯酚前必须对苯酚进行平衡使其pH值达到7.8以上,苯酚平衡操作方法如下:①液化苯酚应贮存于-20℃,此时的苯酚呈现结晶状态。
从冰柜中取出的苯酚首先在室温下放置使其达到室温,然后在68℃水浴中使苯酚充分溶解。
②加入羟基喹啉(8-Quinolinol)至终浓度0.1%。
该化合物是一种还原剂、RNA酶的不完全抑制剂及金属离子的弱螯合剂,同时因其呈黄色。
有助于方便识别有机相。
③加入等体积的1MTri-HCl(pH8.0),使用磁力搅拌器搅拌15分钟,静置使其充分分层后,除去上层水相。
④重复操作步骤③。
⑤加入等体积的0.1MTri-HCl(pH8.0),使用磁力搅拌器搅拌15分钟,静置使其充分分层后,除去上层水相。
⑥重复操作步骤⑤,稍微残留部分上层水相。
⑦使用pH试纸确认有机相的pH值大于7.8。
⑧将苯酚置于棕色玻璃瓶中4℃避光保存。
8、苯酚/氯仿/异戊醇□配置方法1.说明:从核酸样品中除去蛋白质时常常使用苯/酚/氯仿/异戊醇(25:24:1)。
氯仿可使蛋白(25:24:1)质变性并有助于液相与有机相的分离,而异戊醇则有助于消除抽提过程中出现的气泡。
2.配置方法:将Tri-HCl平衡苯酚与等体积的氯仿/异戊醇(24:1)均匀混合后,移入棕色玻璃瓶中4℃保存。
9、10%(W/V)SDS□组份浓度10%(W/V)SDS□配制量100mL□配置方法1.称量10g高纯度的SDS置于100~200mL烧杯中,加入约80mL的去离子水,68℃加热溶解。
2.滴加数滴浓盐酸调节pH值至7.2。
3.将溶液定容至100mL后,室温保存。
10、2NNaOH□组份浓度2NNaOH□配制量100mL□配置方法1.量取80mL去离子水置于100~200mL塑料烧杯中(NaOH溶解过程中大量放热,有可能使玻璃烧杯炸裂)。
2.称取8gNaOH小心地逐渐加入到烧杯中,边加边搅拌。
3.待NaOH完全溶解后,用去离子水将溶液体积定容至100mL。
4.将溶液转移至塑料容器中后,室温保存。
11、2.5NHCl□组份浓度2.5NHCl□配制量100mL □配置方法1.在78.4mL的去离子水中加入21.6mL的浓盐酸(11.6N),均匀混合。
2.室温保存。
12、5MNaCl□组份浓度5MNaCl□配制量1L□配置方法1.称取292.2gNaCl置于1L烧杯中,加入约800mL的去离子水后搅拌溶解。
2.加去离子水将溶液定容至1L后,适量分成小份。
3.高温高压灭菌后,4℃保存。
13、20%(W/V)Glucoe□组份浓度20%(W/V)Glucoe2□配制量100mL□配置方法1.称取20gGlucoe置于100~200mL烧杯中,加入约80mL 的去离子水后,搅拌溶解。
2.加去离子水将溶液定容至100mL。
3.高温高压灭菌后,4℃保存。
14、SolutionI□组份浓度25mMTri-HCl(pH8.0),10mMEDTA,50mMGlucoe(质粒提取用)□配制量1L□配置方法1.量取下列溶液,置于1L烧杯中。
1MTri-HCl(pH8.0)25mL0.5MEDTA(pH8.0)20mL20%Glucoe(1.11M)45mLdH2O910mL2.高温高压灭菌后,4℃保存。
3.使用前每50mL的SoliutionI中加入2mL的RNaeA(20mg/mL)。
15、SolutionII□组份浓度250mMNaOH,1%(W/V)SDS(质粒提取用)□配制量500mL□配置方法1.量取下列溶液置于500mL烧杯中。
10%SDS50mL2NNaOH50mL2.加灭菌水定容至500mL,充分混匀。
3.室温保存。
此溶液保存时间最好不要超过一个月。
注意:SDS易产生气泡,不要剧烈搅拌。
16、SolutionIII□组份浓度3MKOAc,5MCH3COOH(质粒提取用)□配制量500mL□配置方法1.量取下列溶液置于500mL烧杯中。
KOAc147gCH3COOH57.5mL2.加入300mL去离子水后搅拌溶解。
3.加去离子水将溶液定容至500mL。
4.高温高压灭菌后,4℃保存。
17、0.5MEDTA□组份浓度0.5MEDTA(pH8.0)□配制量1L□配置方法1.称取186.1gNa2EDTA2H2O,置于1L烧杯中。
2.加入约800mL的去离子水,充分搅拌。
3.用NaOH调节pH值值8.0(约20gNaOH)。
注意:pH值至8.0时,EDTA才能完全溶解。
4.加去离子水将溶液定容至1L。
5.适量分成小份后,高温高压灭菌。
6.室温保存。
18、1MDTT□组份浓度1MDTT□配制量20mL□配置方法1.称取3.09gDTT,加入到50mL塑料离心管内。
2.加20mL的0.01M的NaOAc(pH5.2),溶解后使用0.22μm滤器过滤除菌。
3.适量分成小份后,-20℃保存。
19、10mMATP□组份浓度10mMATP□配制量20mL□配置方法1.称取121mgNa2ATP3H2O,加入到50mL塑料离心管内。
2.加20mL的25mMTri-HCl(pH8.0),搅拌溶解。
3.适量分成小份,-20℃保存。
分子生物学实验常用培养基的配制方法1、Ampicillin□组份浓度100mg/mlAmpicillin(100mg/ml)□配制量50mL□配置方法1.称量5gAmpicillin置于50mL离心管中。
2.加入40mL灭菌水,充分混合溶解后,定容至50mL。
3.用0.22μm 滤膜过滤除菌。
4.小份分装(1mL/份)后,-20℃保存。
2、IPTG□组份浓度24mg/mLIPTG(24mg/mL)□配制量50mL配置方法1.称量1.2gIPTG置于50mL离心管中。
2.加入40mL灭菌水,充分混合溶解后,定容至50mL。
3.用0.22μm 滤膜过滤除菌。
4.小份分装(1mL/份)后,-20℃保存。
3、某-Gal□组份浓度20mg/mL某-Gal(20mg/mL)□配制量50mL□配置方法1.称取1g某-Gal置于50mL离心管中。
2.加入40mLDMF (二甲基甲酰胺),充分混合溶解后,定容至50mL。
3.小份分装(1mL/份)后,-20℃保存。
4、LB培养基□组份浓度1%(W/V)Tryptone,0.5%(W/V)YeatE某tract,1%(W/V)NaCl□配制量1L□配置方法1.称量下列试剂,置于1L烧杯中Tryptone10gYeatE某tract5gNaCl10g2.加入约800mL的去离子水,充分搅拌溶解。
3.滴加5NNaOH(约0.2mL),调节pH值至7.0。
4.高温高压灭菌后,4℃保存。
5、LB/Amp培养基□组份浓度1%(W/V)Tryptone0.5%(W/V)YeatE某tract1%(W/V)NaCl0.1mg/mLAmpicillin□配制量1L □配置方法1.称量下列试剂,置于1L烧杯中Tryptone10gYeatE某tract5gNaCl10g2.加入约800mL的去离子水,充分搅拌溶解。
3.滴加5NNaOH(约0.2mL),调节pH值至7.0。
