卡尔费休试剂
卡尔费休试剂处理方法

卡尔费休试剂处理方法卡尔费休试剂(Carrez试剂)是一种常用于沉淀蛋白质的化学试剂。
它由铁氰化钾(K4Fe(CN)6)和锌醋酸(CH3COOZn)组成,分别称为卡尔费休I试剂和卡尔费休II试剂。
卡尔费休试剂的处理方法主要用于去除溶液中的杂质和沉淀蛋白质,使得待测物质的浓度更加准确可靠。
我们来了解一下卡尔费休试剂的成分及其作用原理。
卡尔费休I试剂主要由铁氰化钾组成,其作用是与溶液中的金属离子(如Cu2+、Fe3+等)反应生成一种可沉淀的金属铁氰化物沉淀物。
卡尔费休II 试剂则由锌醋酸组成,其作用是与溶液中的蛋白质反应生成一种可沉淀的蛋白质沉淀物。
通过这两种试剂的配合使用,可以有效地去除溶液中的杂质和沉淀蛋白质。
接下来,我们将详细介绍卡尔费休试剂的处理方法。
首先,需要准备好卡尔费休I试剂和卡尔费休II试剂。
根据待测溶液的体积,按照一定的比例将两种试剂加入到溶液中。
一般情况下,卡尔费休I 试剂和卡尔费休II试剂的比例为1:1,即将等体积的两种试剂加入到待测溶液中。
加入试剂后,需要进行充分的搅拌混合,以保证试剂与溶液中的目标物质充分反应。
搅拌的时间可以根据具体实验要求来确定,一般情况下,数分钟的搅拌时间即可。
随后,待测溶液中的杂质和沉淀蛋白质将会与卡尔费休试剂反应生成沉淀物。
为了方便沉淀物的分离,可以通过离心的方式将沉淀物沉淀下来。
离心的参数可以根据实验要求来确定,一般情况下,离心速度为3000-5000 rpm,离心时间为5-10分钟。
经过离心后,可以观察到溶液中的沉淀物已经沉淀到离心管的底部。
此时,可以将上清液倒掉,只保留底部的沉淀物。
为了去除沉淀物中的残余试剂和杂质,可以使用适量的去离子水或缓冲液进行洗涤。
洗涤的次数可以根据具体实验要求来确定,一般情况下,3次洗涤即可。
将洗涤后的沉淀物溶解或重悬到适量的溶剂中,即可获得纯净的待测物质溶液。
这样处理后的溶液中将不再含有杂质和沉淀蛋白质,可以用于后续的实验操作。
卡尔费休试剂分子式

卡尔费休试剂分子式在化学领域,卡尔费休试剂是一种常用的化学试剂,其化学分子式为CFX。
它是一种强氧化剂,广泛应用于有机合成反应和分析实验中。
本文将深入探讨卡尔费休试剂的分子式、合成方法、性质以及应用领域。
一、卡尔费休试剂的分子式卡尔费休试剂的化学分子式为CFX。
其中,C代表碳元素,F代表氟元素,X则表示该试剂的具体结构和取代基。
卡尔费休试剂是一种有机氟化合物,常见的结构为R-C(F)(F)(F),其中R可代表有机基团。
二、卡尔费休试剂的合成方法卡尔费休试剂可以通过多种合成方法获得。
其中最常见的方法是选择性还原氟代化合物得到。
一种常用的合成方法是通过三氟化硼(BF3)与四氟化甲烷(CF4)反应生成卡尔费休试剂,反应方程式为:BF3 + CF4 → B(CF3)3此外,还可以通过卡尔费休试剂与氢氟酸反应生成硼氟酸铵(NH4BF4),再通过还原反应得到卡尔费休试剂。
这些合成方法都能够高效地得到纯度较高的卡尔费休试剂。
三、卡尔费休试剂的性质卡尔费休试剂具有许多独特的性质,这使得它在化学领域中有着广泛的应用。
以下将介绍几个重要的性质:1. 强氧化性:由于卡尔费休试剂中含有多个氟原子,它具有强烈的氧化性。
它可以与有机化合物中的氢原子发生氟化反应,将氢原子替换为氟原子,从而改变化合物的性质和反应活性。
2. 低毒性:相比于其他强氧化剂,卡尔费休试剂具有较低的毒性。
这使得它可以安全地在实验室中使用,并且不会对环境造成严重污染。
3. 耐热性:卡尔费休试剂在高温下依然稳定,可以在高温条件下进行化学反应。
这使得它在高温有机合成反应中具有重要的应用价值。
4. 溶解性:卡尔费休试剂在一些常见的有机溶剂中具有良好的溶解性,例如氯仿、二甲基甲酰胺等。
这方便了它的使用和配制。
四、卡尔费休试剂的应用领域由于卡尔费休试剂具有独特的性质,因此在化学领域中有着广泛的应用。
以下是一些典型的应用领域:1. 有机合成:卡尔费休试剂常用于有机合成反应中。
卡尔.费休试剂分类
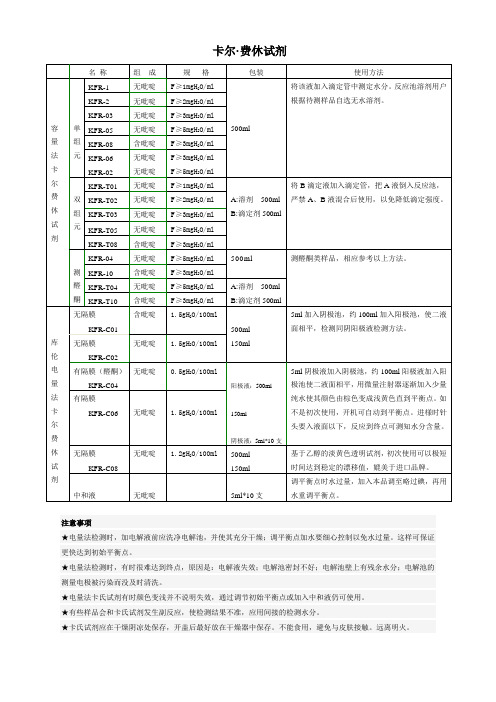
卡尔·费休试剂
注意事项
★电量法检测时,加电解液前应洗净电解池,并使其充分干燥;调平衡点加水要细心控制以免水过量。
这样可保证更快达到初始平衡点。
★电量法检测时,有时很难达到终点,原因是:电解液失效;电解池密封不好;电解池壁上有残余水分;电解池的测量电极被污染而没及时清洗。
★电量法卡氏试剂有时颜色变浅并不说明失效,通过调节初始平衡点或加入中和液仍可使用。
★有些样品会和卡氏试剂发生副反应,使检测结果不准,应用间接的检测水分。
★卡氏试剂应在干燥阴凉处保存,开盖后最好放在干燥器中保存。
不能食用,避免与皮肤接触。
远离明火。
卡尔费休水分滴定_介绍基础知识

卡尔费休水分滴定_介绍基础知识1.卡尔费休试剂:卡尔费休试剂是一种含有碘的化合物,常用的是氯化钠。
它与水分发生化学反应生成碘气,进而滴定测定水分的含量。
2.反应方程:水分与卡尔费休试剂反应的方程式如下:NaCl+H2O→NaOH+HClNaOH+I2→NaI+H2O3.滴定指示剂:卡尔费休水分滴定常使用淀粉指示剂。
淀粉在碘溶液中会形成淀粉-碘复合物,呈现蓝色。
滴定开始时,滴定瓶中的滴定试液呈现深蓝色,当滴定接近结束时,滴定溶液中的碘溶液消耗殆尽,反应中剩余的碘用于形成淀粉-碘复合物,产生蓝色。
4.滴定过程:卡尔费休水分滴定的具体步骤如下:-准备滴定管和滴定瓶,滴定管中放入一定量的卡尔费休试剂和淀粉指示剂。
-将待测水样溶液放入锥形瓶中,加入适量的酚酞指示剂。
酚酞指示剂的作用是增加滴定终点的清晰度。
-开始滴定,滴定试剂缓慢滴入锥形瓶中的水样溶液中,反应产生的气体逐渐排出。
-当滴定溶液呈现淡红色时,停止滴定,稍微搅拌瓶子使其均匀混合。
-继续滴定,每次滴加试剂1滴,直到溶液呈现深蓝色,停止滴定。
-记录滴定试剂的消耗量,并计算出水分的含量。
5.滴定计算:根据滴定试剂的消耗量可以计算出水分的含量。
卡尔费休试剂与水的摩尔比为1:1,所以滴定试剂的消耗量即为水分的含量。
卡尔费休水分滴定是一种简单、准确的水分分析方法,广泛应用于各个行业中。
它具有操作简单、结果可靠、灵敏度高等优点,成为水分分析的重要手段。
但需要注意的是,在进行卡尔费休水分滴定时,要保持滴定试剂的纯净性,避免被空气中的湿气或其它杂质污染,以保证分析结果的准确性。
另外,滴定过程中,滴定瓶和锥形瓶要充分摇动,以保证溶液充分反应。
卡尔费休试剂

有吡啶(无吡啶)电解液即卡尔-费休试剂,试剂分库仑(电量)法卡尔-费休试剂和容量(滴定)法卡尔-费休试剂两类。
库仑(电量)法卡尔-费休试剂,用于库仑(电量)法水分仪测试样品时使用。
试剂分有吡啶和无吡啶两种;包装有500ml和150ml两种方式。
有吡啶电解液是经典配方,但有吡啶的原因味比较难闻,毒性大一点。
无吡啶电解液没有吡啶成分,毒性小一点。
两种电解液性能完全一样。
该试剂不能测酮类物质,也不易连续大量测定醛类物质。
酮类物质可选用酮醛专用试剂。
容量(滴定)法卡尔-费休试剂,用于容量(滴定)法水分测定仪器使用。
容量(滴定)法卡尔-费休试剂,有吡啶成分,500ml包装,也可根据客户要求大包装发货。
滴定度2.6mgH2O/ml,滴定度也可根据客户要求配置。
卡尔费休库仑法试剂

卡尔费休库仑法试剂卡尔费休库仑法试剂是一种常用于测定水溶液中氧化还原电位的化学试剂。
它是由卡尔费休和库仑两位科学家于19世纪末独立发现并提出的。
卡尔费休库仑法试剂的主要目的是通过测定溶液中还原剂和氧化剂之间的电子转移来确定溶液的氧化还原电位。
卡尔费休库仑法试剂的主要成分是硫酸铜和硫酸铁。
在实际应用中,通常将这两种试剂按照一定的比例混合使用。
硫酸铜是一种强氧化剂,它能够将溶液中的还原剂氧化为高价态。
而硫酸铁则是一种强还原剂,它能够将溶液中的氧化剂还原为低价态。
通过测量溶液中还原剂和氧化剂之间的电子转移,我们可以获得溶液的氧化还原电位。
卡尔费休库仑法试剂的使用方法较为简单。
首先,我们需要准备好标准溶液和待测溶液。
标准溶液中含有已知浓度的还原剂或氧化剂,而待测溶液则是我们要进行氧化还原电位测定的样品溶液。
接下来,将标准溶液和待测溶液分别加入两个电极间的电解池中,然后加入适量的卡尔费休库仑法试剂。
在进行测定之前,我们需要将电解池与电位计连接起来,并进行校准。
校准完成后,可以开始进行氧化还原电位的测定。
在测定过程中,需要逐渐向待测溶液中滴加标准溶液,直至电位计显示的电位稳定。
通过记录滴加标准溶液的体积和对应的电位值,我们可以绘制出一条滴定曲线。
根据滴定曲线上的拐点,我们可以推断出溶液的氧化还原电位。
卡尔费休库仑法试剂在实际应用中具有广泛的应用价值。
它可以用于测定溶液中各种还原剂和氧化剂的浓度,用于分析水质中的氧化还原性质,以及用于研究氧化还原反应的动力学和机理等。
卡尔费休库仑法试剂是一种用于测定溶液中氧化还原电位的重要化学试剂。
它通过测量溶液中还原剂和氧化剂之间的电子转移来推断溶液的氧化还原电位。
在实际应用中,我们可以通过滴定曲线来确定溶液的氧化还原电位。
卡尔费休库仑法试剂具有广泛的应用领域,对于研究氧化还原反应和分析水质等方面具有重要作用。
卡尔费休试剂定义

卡尔费休试剂定义
卡尔费休试剂是一种常用于化学实验室中的碘量分析试剂。
它以法国化学家卡尔费休的名字命名,用于检测溶液中的碘含量。
卡尔费休试剂主要由淀粉、硫酸、碘化钾和亚硫酸钠等成分组成。
其工作原理是基于碘和淀粉的蓝色络合物的形成。
当卡尔费休试剂与含碘溶液混合时,溶液中的碘会与试剂中的碘化钾反应生成碘离子。
接着,碘离子与溶液中的淀粉结合,形成淀粉-碘络合物,从而产生一
种蓝色的颜色。
通过测量溶液中的蓝色强度,可以确定其中的碘含量。
通常,卡尔费休试剂用于测定含碘化物的水溶液中的碘含量,如海水中的碘离子含量、食盐中的碘含量等。
卡尔费休试剂具有以下特点:简单易用、快速可靠、灵敏度高。
它广泛应用于生化实验和环境监测等领域。
此外,卡尔费休试剂也被用于检测一些药品中的碘含量,如碘化钾溶液、碘酒等。
需要注意的是,卡尔费休试剂对于其他干扰物质的存在也会产生影响,因此在使用时需要对干扰物进行处理或选择其他更适合的试剂。
总而言之,卡尔费休试剂是一种常用的碘量分析试剂,通过与溶液中
的碘形成蓝色络合物来测定其中的碘含量。
它具有快速、可靠和灵敏度高等特点,在化学实验室和环境监测等领域得到广泛应用。
卡尔费休试剂处理方法

卡尔费休试剂处理方法介绍卡尔费休试剂是一种常用的化学试剂,广泛应用于实验室研究和工业生产中。
它具有很高的活性和反应性,但同时也存在一定的危险性。
因此,在使用完卡尔费休试剂后,正确的处理方法非常重要,以确保人员安全和环境保护。
卡尔费休试剂的特点卡尔费休试剂是一种强氧化剂,常用于氧化反应和催化剂的制备。
它具有以下特点:1. 高活性:卡尔费休试剂能够与许多物质迅速反应,产生剧烈的化学反应。
2.强氧化性:卡尔费休试剂具有很强的氧化能力,能够将其他物质氧化为更高的价态。
3. 易燃易爆:卡尔费休试剂与有机物接触时,可能引发火灾或爆炸。
卡尔费休试剂的处理方法正确处理卡尔费休试剂是确保实验室安全和环境保护的重要步骤。
以下是处理卡尔费休试剂的方法:1. 安全操作在处理卡尔费休试剂前,必须保证安全操作。
包括: - 戴上适当的防护手套、护目镜和实验室外套。
- 在通风良好的实验室中操作,避免试剂蒸气的积聚。
- 避免与其他化学物质混合使用,以免引发意外反应。
2. 储存和标记卡尔费休试剂应储存在密封的容器中,远离可燃物和易燃物。
每个容器都应标有试剂名称、浓度、储存日期和安全警示标志。
3. 废弃物处理处理卡尔费休试剂产生的废弃物时,应遵循以下步骤: 1. 将废弃物收集到密闭的容器中,以防止试剂挥发或泄漏。
2. 避免将卡尔费休试剂与其他化学物质混合处理,以免引发意外反应。
3. 将废弃物交给专门处理危险化学废弃物的机构进行处理,确保符合环境保护要求。
4. 紧急情况处理在紧急情况下,如卡尔费休试剂泄漏或意外事故发生时,应立即采取以下措施: 1. 立即远离泄漏区域,确保人员安全。
2. 切勿直接接触泄漏的试剂,以免引发意外反应。
3. 封锁泄漏区域,防止泄漏扩散。
4. 立即通知实验室主管或紧急救援人员,进行进一步处理。
结论卡尔费休试剂是一种高活性和强氧化性的化学试剂,在使用和处理时必须十分谨慎。
正确的处理方法包括安全操作、储存和标记、废弃物处理以及紧急情况处理。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
卡尔·费休水分测定原理与技术
卡尔·费休法简称费休法,是1935年卡尔·费休(KarlFj scher)提出的测定水分的容量分拆方法。
费休法是测定物质水分的各类化学方法中,对水最为专一、最为准确的方法。
虽属经典方法但经过近年改进,提高了准确度,扩大了测量范围,已被列为许多物质中水分测定的标准方法。
费休法属碘量法,其基本原理是利用碘氧化二氧化硫时,需要-定量的水参加反应:12十S02十2H2O=2HI十H2SO4
上述反应是可逆的。
为了使反应向正方向移动并定量进行,须加入碱性物质。
实验证明,吡啶是最适宜的试剂,同时吡啶还具有可与碘和二氧化硫结合以降低二者蒸气压的作用。
因此,试剂必须加进甲醇或另一种含活泼OH基的溶剂,使硫酸酐吡啶转变成稳定的甲基硫酸氢吡啶。
试剂的理论摩尔比为碘:二氧化硫:吡啶,甲醇=1:1:3:1
测定技术费休试剂的配制和标定。
通常,配制费休试剂时只有碘应严格依照化学计量,其它组分则是过量的,一般采用的摩尔比为碘:二氧化硫:吡啶:甲醇=1:3:10:50。
配制费休试剂所用各物质必须严格控制其含水量,一般不得超过0.1%,若进行微量分析时,不应超过数个ppm。
配制步骤取无水吡啶133mL与碘42.33g,置入具塞棕色试剂瓶中,振摇至碘全部溶解后,加入无水甲醇333ml。
难确称量试剂瓶重,通入经浓硫酸脱水的二氧化硫气体至试剂瓶增重32g,将瓶塞塞牢、摇匀,于暗处放置48h后标定。
依此配制的费休试剂的滴定度约为含水3-5g/mL。
当使用专用试剂瓶时,可在通二氧化硫至增重32g时,把液面的位置作一标记,以后每次配制,只需取一定量的各物质置入试剂瓶中,通入二氧化硫气体,使试剂溶液掖面升高至标记处即可,这样可省去费时的称重操作。
为使费休试剂稳定,有另一种配制方法,即先配成二组溶浓,在使用前混合。
一组为碘和甲醇溶液I;另一组为二氧化硫和吡啶溶液。
溶液I:取碘63p,置入试剂瓶中,加366mL无水甲醉,括至碘全部溶解。
溶液II:取100mL无水吡啶,置入试剂瓶小,准确称量,然后通入干燥的二氧化硫气体,使其增重32g。
新配制的费体试剂很不稳定,随放置时间增加,浓度逐渐降低。
在前二、三日内,淌定皮有显著下降,以后降低援慢,一周以后,滴定度每日约减少1%,之后则变化更趋缓慢。
滴定度开始迅速下降的原因主要是试剂中各组分所含残存水分的作用,随后滴定度缓慢下降的原因则是副反应的影响。
因此,费你试剂配制以后,应放置一用以上,用前标定
费休试剂的标定方法一般有纯水标定、含水甲酵标准溶液标定和稳定的结晶水合物标定三种。
(1) 纯水标定法取数个干燥具塞滴定瓶,加入25mL无水甲醇,用费休试剂滴定至终点。
这时滴定瓶内呈无水状态,随即用注射取样器迅速注入已准确称量的纯水30.00mg,在剧烈搅拌下,以费休试剂滴定至终点,求得每毫升费体试剂相当于水的质量M^。
(2)含水甲醇标准溶液标定法
(i)含水甲醇标准溶液的配制含水中醇标准溶液是用无水甲醉加入定还的燕螺水配成的。
无水甲醇应经过金届镁粉二次处理,然后蒸馏,把蒸出的甲醇立即用来配制。
取充分干燥的500mL存虽瓶,在瓶中加入无水甲醇400mL,用注射器(或小滴瓶)减员法准确称设蒸馏水0.2500,注入容量瓶中,迅速塞牢瓶塞,振荡均匀后,用元水甲醇稀释至刻
度。
即使经过多次处理的甲醇,也难免含有微量水分,因此必须对此值予以校正。
可在不断搅拌,保持利同条件下,用无水甲醇及配制好的含水醇分别滴定同量费休试剂,得到Va和Vb,然后求校正值F。
(ii)标定方法在于燥的滴定瓶中加入无水甲醇10mL,以费休试剂滴至终点。
然后准确量取一定量的含水甲醇标准溶液(含水量为Hmg),以费休试剂在不断搅拌下滴定。
由试剂的消耗量V(单位为mL)计算费休试剂的滴定度T(mg/mL):
以含水甲醇标准液标定费休试剂结果准确、操作简便,而且可进行反滴定。
但是,含水甲醇标准溶液比一般水溶液的膨胀系数更大,标定时须注明当时温度。
在使用中温度有明显差别时,须需对水甲醇标准溶液的体积予以校正。
当使用含水甲醇标准液反滴定时,更要注意这种温度对体积造成的影响。
(3)稳定的结品水合物标定法一般用于标定(费休试剂的结晶水合物有一水合草酸铵(NH4)2C2.H2O、三水合乙酸钠CH3C00Na·3H2:0、一水合柠檬酸和二水合酒石酸钠等。
其中以二水合酒石酸钠为最好,它的理论含水量为15.66%。
在150℃加热后含水量为15.652%,将其暴露于相对湿度为20一79%的空气中,此水合物增加重量为0.01一0.09%。
费休法终点判定费休法的滴定终点,对于无色试液可用目视法判定。
如果是带有颜色或呈浑浊状的试液,则需用水停滴走法或电位滴定法判定终点。
