卤代烃的消除反应
第章卤代烃消除反应
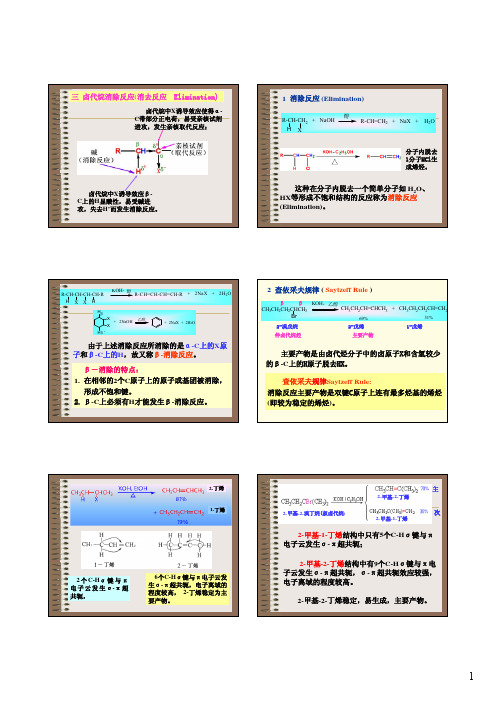
2-丁烯 1-丁烯
2 个 C-Hσ 键 与 π 电 子 云 发 生 σ-π 超 共轭,
6个C-Hσ键与π电子ቤተ መጻሕፍቲ ባይዱ发 生σ-π超共轭,电子离域的 程度较高, 2-丁烯稳定为主
要产物。
主
2-甲基-2-丁烯
2-甲基-2-溴丁烷(叔卤代烷)
次
2-甲基-1-丁烯
2-甲基-1-丁烯结构中只有5个C-Hσ键与π 电子云发生σ-π超共轭;
生成新的化合物。
3
小结 对E1反应而言,碳正离子的稳定性 叔碳正离子 > 仲碳正离子 > 伯碳正离子
对E2反应而言,生成的烯烃稳定性: 叔卤代烷 > 仲卤代烷 > 伯卤代烷
不论是E1机制和E2机制,不同卤代烷的消 除反应活性次序相同:
叔卤代烷 > 仲卤代烷 >伯卤代烷
五、卤烷的亲核取代反应与消除反应的关系
三 卤代烷消除反应(消去反应 Elimination)
卤代烷中X诱导效应使得αC带部分正电荷,易受亲核试剂 进攻,发生亲核取代反应;
卤代烷中X诱导效应βC上的H显酸性,易受碱进 攻,失去H+而发生消除反应。
1 消除反应 (Elimination)
R-CH-CH2 + NaOH 醇 HX
R-CH=CH2 + NaX + H2O
CH3CH2CH=CHCH3 + CH3CH2CH2CH=CH2
Br
69%
31%
2-溴戊烷
2-戊烯
1-戊烯
仲卤代烷烃
主要产物
主要产物是由卤代烃分子中的卤原子X和含氢较少 的β-C上的H原子脱去HX。
查依采夫规律Saytzeff Rule: 消除反应主要产物是双键C原子上连有最多烃基的烯烃 (即较为稳定的烯烃)。
消去反应详解

三、消去反应1.概念:有机物在适当的条件下,从一个分子中脱去一个小分子(如水、HX 等),生成不饱和(双键或三键)化合物的反应。
如:实验室制乙烯。
2.能发生消去反应的物质:醇、卤代烃;能发生消去反应的官能团有:醇羟基、卤素原子。
(1)卤代烃消去HX在卤代烃的消去反应中,碱是反应物,醇是提供反应环境的溶剂,因为生成的乙烯能溶于醇中,同时反应物中的碱能与HBr 发生反应,使反应不断向生成乙烯的方向移动。
对于2-溴丁烷来说,发生取代反应时,生成含取代基较多的烯烃,这样的烯烃对称性好,分子比较稳定。
也就是说主要从含氢原子较少的碳原子上消去氢原子。
在醇的消去反应中,浓硫酸既起催化剂的作用,又起脱水剂的作用,也能促进反应不断的向生成乙烯的方向进行。
(2)醇消去H 2O :CH 3CH 2OHC170/浓硫酸CH 2=CH2+H 2O3.反应机理:相邻消去发生消去反应,必须是与羟基或卤素原子直接相连的碳原子的邻位碳上必须有氢原子,否则不能发生消去反应。
如CH 3OH ,没有邻位碳原子,不能发生消去反应。
加成反应和消去反应是对立统一的关系:饱和化合物通过消去反应,生成不饱和的化合物,腾出空位子,再通过加成反应,引入所需要的官能团。
四、聚合反应聚合反应是指小分子互相作用生成高分子的反应。
聚合反应包括加聚和缩聚反应。
1.加聚反应:由不饱和的单体加成聚合成高分子化合物的反应。
反应是通过单体的自聚或共聚完成的。
加聚反应的复习可通过类比、概括,层层深入,寻求反应规律的方法复习。
发生加聚反应的官能团是碳碳双键:加聚反应的实质是:加成反应。
加聚反应的反应机理是:碳碳双键断裂后,小分子彼此拉起手来,形成高分子化合物。
Ⅰ.单烯烃的加聚CH 2 HBrNaOH 醇溶液CH 2 CH 2+ HBrCH 2(1)乙烯的加聚:(2)氯乙烯的加聚:(3)丙烯的加聚:(4)2-丁烯的加聚:小结:烯烃加聚的基本规律:Ⅱ.二烯烃的加聚二烯烃单体自聚时,单体的两个双键同时打开,单体之间直接连接形成含有一个新双键的链节而成为高分子化合物。
高二化学卤代烃消去反应的应用技巧学法指导

高二化学卤代烃消去反应的应用技巧消去反应是卤代烃的一个重要性质,通过消去反应可以向卤代烃中引入更活泼的官能团——碳碳双键或碳碳三键,从而合成其他烃的衍生物。
学习卤代烃的消去反应要注意抓反应实质、反应产物和有关实验。
一、逆向思维抓实质理解有机反应,要注意反应的实质:卤代烃消去反应时,断裂的是两种化学键——碳卤键和碳氢键,且不在同一个碳原子上,而是在两个相邻的碳原子上,因此并不是所有的卤代烃都能发生消去反应。
不能发生消去反应的卤代烃有两类:①只有一个碳原子的卤代烃,如Cl CH 3;②与连接卤原子的碳原子相邻的碳原子上没有氢原子的卤代烃,如Cl CCH )CH (233。
例1 下列卤代烃在KOH 醇溶液中加热不反应的是( )。
①Cl H C 56 ②Cl CHCH )CH (223③Cl CCH )CH (233④22CHBr —CHCl ⑤ ⑥22Cl CHA 、①③⑥B 、②③⑤C 、全部D 、②④解析:根据卤代烃消去反应的实质,分子中与连接卤素原子的碳原子相邻的碳原子上没有氢原子的卤代烃不能发生消去反应。
Cl CCH )CH (233不能发生消去反应;22Cl CH 也不能发生消去反应,因其分子中只有一个碳原子。
此外Cl H C 56若发生消去反应以后,将破坏苯环的稳定性,故Cl H C 56也不能发生消去反应。
答案:A二、触类旁通抓产物在理解卤代烃消去反应实质的基础上,要抓住不同卤代烃发生消去反应的生成物的规律:1、若与卤素原子所连碳原子相邻的两个以上碳原子上均连有氢原子,由于这些氢原子的排列方式不同,则发生消去反应的产物不止一种,这些产物互为同分异构体。
2、对于卤素原子连接在相邻两个碳原子上的二卤代烃,发生消去反应时有两种可能:形成一个碳碳三键或两个共轭的碳碳双键。
如4321R )R (CHClCHBrCH)R (CH R 发生消去反应,产物有两种:4321R )R (CCH C )R (CH R ≡、4321R )R (C CHCH )R (C R ==。
卤代烃发生消去反应的原理

卤代烃发生消去反应的原理
嘿,朋友们!今天咱就来讲讲卤代烃发生消去反应的原理,这可有意思啦!
你们想啊,卤代烃就好像是一群带着“小帽子”(卤素原子)的家伙。
比如说氯乙烷吧,它就是其中之一。
那消去反应是咋回事呢?这就像是一场奇妙的变身!
这些卤代烃们,在一定条件下,能把它们身上的“小帽子”给甩掉一个,同时和旁边的小伙伴连起来,变成一个新的家伙!就像氯乙烷,它能甩掉氯原子,然后碳和碳之间就连接起来形成双键啦!这多神奇啊!
咱打个比方,这不就像是一个人穿着一件旧外套,突然决定把外套脱掉,展现出一个全新的自己嘛!而且啊,不同的卤代烃发生消去反应的条件还不一样呢,有的需要强碱的帮忙,有的需要热一热。
这就好像每个人改变自己的方式不同,有的需要朋友鼓励,有的得自己好好想想。
“哎呀,那这个消去反应有啥用啊?”哈哈,用处可大啦!它能帮我们合成好多有用的化合物啊,就像是给我们盖房子提供了好多不同形状的砖头!比如说可以用来制备烯烃啊,这可是化工里很重要的东西呢。
咱再想想,如果没有卤代烃的消去反应,那得少了多少有趣的化学变化啊,那整个化学世界不就变得没那么精彩啦?所以说,卤代烃发生消去反应的原理真的是超级重要的呀!
总之,卤代烃的消去反应就像一场充满惊喜的魔法,让那些带着“小帽子”的家伙们发生奇妙的转变,为我们的化学世界增添了无数的可能和精彩!这就是卤代烃发生消去反应的神奇之处啊,你们觉得酷不酷呢!。
卤代烃发生消去反应实验的探索

一、卤代烃选择 二、反应温度控制
三、反应混合液的接触几率 四、碱的用量
一、卤代烃的选择,主要看两点:
所选卤代烃的沸点,最好高于70 ℃。 经试验,当温度低于70 ℃时,卤代烃 发生消去反应的速率非常慢、产生气 体的量很少,当温度高于70 ℃时,则 卤代烃发生消去反应的速率比较快、 产生气体的量比较多。溴乙烷的沸点是
38.4 ℃, 1-溴丙烷,其沸点是70 ℃
,
2、消去3.5 ℃,且生
成的氯乙烯是气态。
二、反应温度控制
反应温度的控制,主要考虑:尽 可能避免卤代烃及乙醇汽化。因 此,采用水浴加热,防止温度过 高,温度应控制在 71~75 ℃。
三、反应混合液的接触几率
要尽可能增大反应混合液的接触几 率,一是用锥形瓶代替大试管,二 是反应过程中要不断振荡锥形瓶。
四、碱的用量
1、加入氢氧化钠或氢氧化钾的物质 的量要大于卤代烃的物质的量
2、乙醇的用量适当,体积是卤代烃的1.5 倍。
实验步骤
步骤一:称取6 g 氢氧化钠固体,放入锥形瓶中, 向其中加入15 mL无水酒精,振荡约1分钟,向 其中加入10 mL 1,2-二氯乙烷,迅速用带导管的 单孔橡皮塞塞紧,将导管的另一端伸入倒置的 充满水的无色透明的塑料饮料瓶口中。
大学有机化学反应方程式总结卤代烃的取代反应与消除反应

大学有机化学反应方程式总结卤代烃的取代反应与消除反应大学有机化学反应方程式总结——卤代烃的取代反应与消除反应有机化学是研究碳为主体的有机化合物及其反应性质的学科。
其中,卤代烃是有机化合物中的一类重要化合物,它们在有机合成和医药领域具有广泛的应用。
卤代烃的取代反应和消除反应是有机化学中的基础反应之一。
本文将对这两种反应进行总结,并列举相关的反应方程式。
一、卤代烃的取代反应1. 氢氧离子的取代反应:卤代烃在碱性条件下可以发生醇和醚的生成反应。
具体反应方程式如下:R-X + OH- → R-OH + X-R-X + OR' → R-OR' + X-这种反应称为亲核取代反应,其中OH-或OR'为亲核试剂,R和X分别代表有机基团和卤素原子。
2. 氨或胺的取代反应:卤代烃与氨或胺反应可以生成相应的胺或胺盐。
具体反应方程式如下:R-X + NH3 → R-NH2 + HXR-X + RNH2 → R-NHR' + HX这种反应可以通过控制反应条件和反应物的选择来对生成物进行调控。
3. 芳香化合物的取代反应:芳香化合物的取代反应是有机化学中的重要反应。
卤代烃作为芳烃的取代试剂,可以发生芳香取代反应。
具体反应方程式如下:Ar-X + Nu- → Ar-Nu + X-Ar-X + Ar'-ONa → Ar-Ar' + X- + Na+这种反应可以引入不同的官能团和基团,从而改变芳香化合物的性质。
二、卤代烃的消除反应1. 亲电质消除反应:卤代烃在鹰式消除剂的作用下,发生亲电质消除反应。
具体反应方程式如下:R-X + Z → R-Z + X-其中,Z为鹰式消除剂。
这种反应可以生成亲电质和卤素离子。
2. 氢氧化物消除反应:卤代烃在碱性条件下,通过内消除反应,发生氢氧化物消除。
具体反应方程式如下:R-X + OH- → R-H + X-这种反应可以生成烯烃或炔烃等不饱和化合物。
【知识解析】卤代烃的化学性质

卤代烃的化学性质受官能团卤素原子(—X)的影响,卤代烃的化学性质比烷烃的活泼,既能发生消去反应,又能发生水解反应(取代反应)。
1.卤代烃的水解反应(取代反应)(1)条件:NaOH水溶液、加热。
(2)本质:水分子中的—OH取代了卤代烃中的—X。
R—X+NaOH R—OH+NaXR—CHX—CH2X+2NaOH R—CH(OH)—CH2OH+2NaX教材延伸(1)卤代烃的水解反应可用于制取醇,如CH3Cl+NaOH CH3OH+NaCl(制一元醇)、(制二元醇)、(制芳香醇)。
(2)卤代烃发生水解反应时量的关系:R—X~NaX~AgX↓,即1 mol一卤代烃通过反应可得到1 mol AgX(X=Cl、Br、I)沉淀,常利用此关系来定量测定卤代烃中卤素原子的含量。
2.卤代烃的消去反应(1)条件:强碱的醇溶液、加热。
(2)本质:从有机物分子中相邻的两个碳原子上脱去一分子的HX生成含不饱和键的烃。
(3)卤代烃发生消去反应的规律①与卤素原子相连的碳原子没有邻位碳原子的卤代烃不能发生消去反应,如CH3Cl。
②与卤素原子相连的碳原子有邻位碳原子,但邻位碳原子上无氢原子的卤代烃也不能发生消去反应,如。
③与卤素原子相连的碳原子有两个相邻的碳原子且相邻碳原子上均有氢原子(氢原子不等效)时,发生消去反应可生成不同的产物,如(或CH3—CH=CH—CH3↑)+NaBr+H2O。
名师提醒(1)发生消去反应必须具备的结构条件是分子中有β—H。
如中没有β-H,就不能发生消去反应(与X相连的C叫α-C,与α-C相邻的C叫β-C;α-C上连接的H叫α-H,β-C上连接的H叫β-H)。
(2)由于苯环的特殊结构(很稳定),卤代苯(如)不能发生消去反应。
(3)发生消去反应的有机产物有三种:(4)欲增加有机物分子中某些官能团(如—X、—OH等)的数目,可以先由原料发生消去反应生成含不饱和键的有机物,再由含不饱和键的有机物与卤素单质发生加成反应生成多卤代物,多卤代物还可继续发生水解反应以增加—OH的数目。
卤代烃的水解与消去反应对比探究

卤代烃的水解与消去反应对比探究卤代烃是指与一个或多个卤素原子结合的烃类物质,它们被广泛应用于日常的医药、农药、染料行业以及石油化工行业,影响着生活的方方面面。
卤代烃的水解和消去反应是其常见的两种反应,这俩种反应的比较在卤代烃的操作研究中起到至关重要的作用。
卤代烃水解反应是指如下化学方程式所示:RX+H2O→RH+XOH(其中R为烃基,X为卤烷基),其中烃基和卤烷基是反应产物,RX正是反应前的卤代烃物质。
卤代烃水解反应热力学特征以及反应活性是基于反应热力学性质进行比较的,它受到很多因素的影响,如形成卤烷基的元素催化剂的类型、卤族金属的种类、反应温度等。
消去反应是指RX→R+X的化学反应,消去反应的反应特性受到末端原子亲和力和反应温度的影响,一般情况下,它的活性能比水解反应大,并且它有很高的抗热性,可以在高温下进行反应,消去反应可以将水解反应产物进行分离,同时也可以通过消去反应对杂质进行处理。
由前述可知,尽管水解和消去反应都能够对卤代烃进行处理,但两种反应的特性有很大不同,它们的不同点在于:水解反应的活性较低,只能在低温下进行,并且受到多种因素的影响;消去反应的活性较高,可以在高温下进行,而且反应速率只受到反应温度和原子亲和力等因素的影响,可以比较准确地表示。
因此,在进行卤代烃的处理过程中,应该结合不同反应的特性,根据研究目的选择最合适的反应方式,以期获得最佳的反应效果。
事实上,卤代烃水解和消去反应的比较不仅仅可以探究卤代烃的操作研究,而且还能对现有的研究领域进行拓展,为后续的反应提供良好的参考。
综上所述,卤代烃的水解反应和消去反应是它的常见反应,它们的比较可以有助于揭示卤代烃的操作研究,同时也有利于拓展相关研究学科。
此外,在实际操作时,应根据项目需要,选择最合适的反应方式,以获得最佳反应结果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
E2反应的立体化学
内消旋-1,2-二溴-1,2-二苯基乙烷 顺-1-溴代二苯乙烯
RR or SS -1,2-二溴-1,2-二苯基乙烷
反-1-溴代二苯乙烯
卤代环己烷的E2反应
处于a-键上的Cl易发生反式消除,形成环己烯化合物。
处于e-键上的Cl不易发生反式消除,一般需要构象转化,转变成a-键后才 能发生消除。
卤代烃的1, 2-消除反应
主讲人 罗 钒 华中科技大学化学与化工学院
主讲内容
• 卤代烃的消除反应 • E2反应机理 • E1反应机理 • E1cb反应机理 • 亲核取代与消除反应的竞争
卤代烃的1,2-消除反应
卤代烃遇到具有碱性的亲核试剂时,除了可以发生亲核取代以外,也可以发生 1,2-消除反应。
反应机理:
卤素负离子离去生成中间体碳正离子,水分子夺取碳正离子β-氢,生成烯 烃。反应的决速步只与一个底物分子有关,是单分子过程,在反应动力学上是 一级反应。
E1反应的立体化学
对E1反应,-氢发生同面(syn)或反式(anti)消除,主要取决于反应条件: * 若中间体C+为紧密离子对,且X-担当碱,那么同面消除反应易进行。 * 若中间体C+为高度溶剂化, 那么发生同面和反式消除均有可能。
溶剂对E1反应的影响
3-氘-2-对甲苯磺酸丁酯
anti-消除产物
syn-消除产物
3-氘-2-对甲苯磺酸丁酯
syn-消除产物
对E1反应,由于过渡态已经有部分双键性质,所以能量最低的过渡态将是取 代最多的双键,即产物分布符合查依采夫(Zaitsev )规则。
反应条件对消除反应影响显著,例如:
E2 反应需要较强的碱,E1则不需要;E2 反应是立体专一性的,E1则不是。
E2反应:查依采夫(Zaitsev )规则---区域选择性
2-溴丁烷
2-丁烯 1-丁烯
2-溴-2-甲基丁烷
2-甲基-2-丁烯 2-甲基-1-丁烯
卤代烷脱卤化氢或醇脱水时,若分子中含有不同的β-H,生成的主要产物的双 键位于烷基较多的位置,即含H较少β碳提供氢原子,生成取代较多的稳定烯烃。
E1反应及其机理
E1cb反应机理
当-H具有较强酸性时,碱可以先攫取该质子,再发生C-X键的断裂。
卤代芳烃经E1cb反应发生的取代反应
反应机理
烯基卤的消除反应
反-3-溴- 4-辛烯
顺-3-溴- 4-辛烯 消除反应的机理(E2消除)
ห้องสมุดไป่ตู้
4-辛炔
顺-3,4-辛二烯
反-3,4-辛二烯
亲核取代反应 VS 消除反应
当卤代烷烃与亲核试剂(也是碱)处理时, SN2与E2反应是竞争进 行的;SN1与E1反应是一起竞争的。
* 碳正离子稳定性高,对SN1与E1反应都有利;位阻大有利于E1反应。
* 亲核试剂碱性强,有利于消除产物的生成。
课间提问(判断题)
判断下列说法是否正确。若正确在括号内划√,否则划X。 A)叔卤代烃与醇钠作用主要发生亲核取代反应。( ) B) 1,2-二溴-1,2-二苯基乙烷发生E2消除时生成反-1-溴代二苯乙烯 。( ) C)不论是E1还是E2反应都需要很强的碱。( ) D) 伯卤代烷和碱性较强的亲核试剂主要发生E2反应。( )
• 消除一般产生不饱和键; • 消除与加成(addition)互为逆过程; • 消除(Elimination)与取代经常
相伴相生,互相竞争;
卤代烃的不同1,2-消除反应途径
研究表明,卤代烃的消除反应主要途径包括:E2、E1、E1cb
C-H和C-X键同时断裂 C-X键先发生断裂 C-H键先发生断裂
2-溴丁烷的E2反应机理
饱和卤代烃的消除
2-溴丁烷
主
次
过渡态
E2反应的几何形态 (Geometry of Elimination)
同面消除
顺势共平面(syn) 重叠式构象,能量较高
反式共平面 交叉式构象 能量较低
反式过渡态
烯烃类产物
由于重叠式构象能量较高;另外,同面(syn)消除不符合轨道对称性的 匹配原理,C-H键与C-X键的断裂的同时,不利于C=C键的形成。因此卤代烷 的E2消除是反式(anti)消除。
SN2与E2反应
• 中心碳位阻小,有利于SN2反应;中心碳位阻大,有利于E2反应
* 亲核试剂碱性弱,亲核性强,有利于SN2反应;碱性强有利于E2反应 * 离去基团离去能力强,对SN2与E2反应都有利
SN1与E1反应
* 两种反应途经拥有相同的碳正离子中间体,因此离去基团离去 能力强,对SN1与E1反应都有利。
