环境腐蚀
世界各地自然环境腐蚀严酷度腐蚀等级
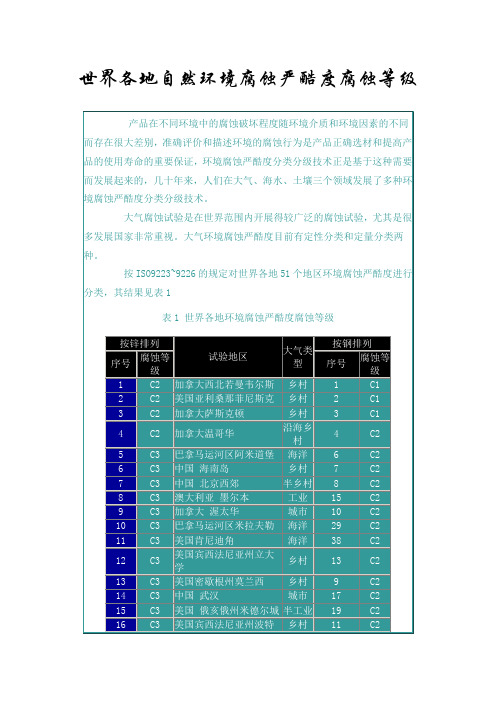
按ISO9223~9226的规定对世界各地51个地区环境腐蚀严酷度进行分类,其结果见表1
表1 世界各地环境腐蚀严酷度腐在不同环境中的腐蚀破坏程度随环境介质和环境因素的不同而存在很大差别,准确评价和描述环境的腐蚀行为是产品正确选材和提高产品的使用寿命的重要保证,环境腐蚀严酷度分类分级技术正是基于这种需要而发展起来的,几十年来,人们在大气、海水、土壤三个领域发展了多种环境腐蚀严酷度分类分级技术。
《环境腐蚀》课件

在这个PPT课件中,我们将深入探讨环境腐蚀的各个方面,包括定义、影响 因素、危害、评估方法、预防与控制以及案例分析。
什么是环境腐蚀?
1 定义
环境腐蚀指物质受到外界环境的侵蚀、破坏 的过程。
2 分类
环境腐蚀可分为化学腐蚀、物理腐蚀和生物 腐蚀三大类。
环境腐蚀的影响因素
化学成分
环境腐蚀的预防与控制
选材
选择耐腐蚀的材料,减少腐蚀风险。
保护涂层
使用防腐蚀涂层来保护物质表面。
阴极保护
利用阴极保护原理来防止腐蚀。
设计优化
在设计中考虑腐蚀预防措施,减少腐蚀的可能性。
环境腐蚀案例分析
1 铜腐事故
介绍一起铜腐蚀事故的原 因、后果和预防措施。
2 铜锈的形成和预防
探讨铜锈形成的机理,提 供预防铜锈的方法。
安全事故
某些情况下,腐蚀可能导致严 重的安全事故,威胁人身安全。
环境腐蚀的评估方法
1
动、静电位法
2
使用电化学方法测量物质表面的电位,
判断腐蚀程度。
3
电化学阻抗法
4
利用电化学原理来测量材料的腐蚀电流 并评估腐蚀程度。Fra bibliotek直接观察法
通过直接观察物质表面的腐蚀痕迹来评 估腐蚀程度。
重力法
通过测量物质的重量变化来评估腐蚀的 程度。
不同环境中的化学成分对腐蚀的程度有着重要 影响。
温度
高温会加速化学反应速率,从而增加腐蚀的风 险。
湿度
高湿度会增加环境中的水分,促进腐蚀的发生。
气流
强气流、酸雨等会加剧物质表面的腐蚀。
环境腐蚀的危害
物质损失
腐蚀导致物质表面损失,减少 材料的寿命。
腐蚀环境种类

环境种类大气腐蚀环境1.农村大气农村大气是最洁净的大气,空气中不含强烈的化学污染,主要含有有机物和无机物尘埃等。
影响腐蚀的因素主要是相对湿度、温度和温差.2.城市大气城市大气的主要污染物主要是城市居民生活所造成的大气污染,如汽车尾气、锅炉排放的SO2等。
实际上,很多大城市往往也是工业城市,或者是海滨城市,所以大气环境污染的相当复杂。
3.工业生产区大气工业生产区所排放的污染物含有大量的SO2、H2S等含硫化合物,所以工业大气环境最大的特征是含有硫化物。
他们易溶于水,形成的水膜成为强腐蚀介质,加速金属的腐蚀。
随着大气相对湿度和温差的变化,这种腐蚀作用更强。
很多石化企业和钢铁企业往往非常大,可以形成一个中等城市规模,大气质量相当差,对工业设备和居民生活造成的污染极其严重。
4.海洋大气其特点是空气湿度大,含盐分多。
暴露在海洋大气中的金属表面有细小盐粒子的沉降。
海盐粒子吸收空气中的水分后很容易在金属表面形成液膜,引起腐蚀。
在季节或昼夜变化气温达到露点是尤为明显。
同时尘埃、微生物在金属表面的沉积,会增强环境的腐蚀性。
所以海洋大气对金属结构的腐蚀性比内陆大气,包括乡村大气和城市大气要严重的多.海洋的风浪条件、离海面的高度等都会影响到海洋大气腐蚀性。
风浪大时,大气中的水分含盐量高,腐蚀性增加。
据研究,离海平面7~8m处的腐蚀最强,在此之上越高腐蚀性越弱。
雨量的大小也会影响腐蚀,频繁的降雨会冲刷掉金属表面的沉积物,腐蚀会减轻。
相对湿度升高会使海洋大气腐蚀加剧。
一般热带腐蚀性最强,温带次之,两级最弱。
中国最典型的处于海洋腐蚀环境中的是杭州湾跨海大桥,地处亚热带海洋性季风气候。
5.处于海滨的工业大气环境,属于海洋性工业大气,这种大气中既含有化学腐蚀污染的有害物质,又含有海洋环境的海盐粒子。
2种腐蚀介质的相互作用对混凝土的危害更大。
淡水腐蚀环境混凝土碳化模型国内外学者提出了许多混凝土碳化深度预测模型,这些模型大致可分为两类:一类是基于试验数据或实际结构的碳化深度实测值,采用数学统计或神经网络等方法拟合得到的经验模型;另一类为基于碳化反应过程的定量分析建立的理论模型。
第2章 腐蚀环境

常 用 金 属 材 料 的 耐 蚀 性
2.3
2.3.1定义:
大气腐蚀
大气腐蚀通常是指在常温下暴露在地球大气中的所发生的腐蚀。
常 用 金 属 材 料 的 耐 蚀 性
2.3.2大气腐蚀的影响因素:
1、湿度的影响
相对湿度 :空气中水蒸气含量与同温度下饱和水蒸气含量的比 值的百分数。
临界湿度——当湿度达到一定程度时,金属突然加速腐蚀时的 湿度值。 临界湿度以下腐蚀可以忽略,大于临界湿度,腐蚀随相对湿度 增加而增加。临界湿度取决于金属及其表面的污染程度。
常 用 金 属 材 料 的 耐 蚀 性
2、水膜中质点的影响
主要是:氧、硫化物、氯化物、灰尘等
3、温度的影响
注:影响大气腐蚀的最主要因素是水分!
常 用 金 属 材 料 的 耐 蚀 性
2.3.3大气分类
1、乡村大气:主要指SO2低。
2、城市大气:含SO2和烟尘。 3、工业大气:工厂区,不同工业会有不同污染。 4、海洋大气:很高的氯化物浓度 。
常 用 金 属 材 料 的 耐 蚀 性
2、海水腐蚀的影响因素:
(1)盐度 (2)pH值 (3)碳酸盐饱和度 (4)含氧量 (5)温度
常 用 金 属 材 料 的 耐 蚀 性 (6)流速
(7)生物的影响
①海生物附着不完整均匀时,附着层内外造成浓差电池; ②由于生物的生命活动,局部改变了海水介质成分; ③附着植物根的穿透和剥落,破坏了金属表面保护层。
土壤是土粒、水和空气的混合物。由于水中溶有各种盐类,故 土壤是一种腐蚀性电解质,金属在土壤中的腐蚀属于电化学腐蚀。 土壤中含有多种无机物质和有机物质,这些物质的种类和含量 既影响土壤的酸碱性,又影响土壤的导电性。土壤是不均匀的,因 此长距离的地下管道和大尺寸的地下设施,其各个部位接触的土壤 的结构和性质可能有较大的变化。土壤中还有大量微生物,对金属 腐蚀能起加速作用。
腐蚀环境分类

腐蚀环境分类
以下是 9 条关于腐蚀环境分类的内容:
1. 酸性环境腐蚀,这就好比食物放久了变酸一样,会慢慢侵蚀物品呢!像酸雨就是个典型例子,它能逐渐毁掉建筑和金属设施。
2. 碱性环境腐蚀呀,哎呀,就像碱性物质对皮肤的刺激似的,腐蚀性可不弱呢!比如一些碱性溶液如果不小心接触到金属,也会造成腐蚀哟!
3. 海洋环境腐蚀,那可真是像海水对船的不断冲击啊!你想想看,那些常年在海里的船只,是不是很容易生锈腐蚀呢?
4. 高温环境腐蚀,这可真是热得让人受不了,就好像把东西放在火上烤一样!像一些高温的工厂里的设备,就会遭受到这种腐蚀呢。
5. 潮湿环境腐蚀,这简直就像潮湿的天气让人浑身不舒服一样!像地下室那种潮湿的地方,金属物品很容易就被腐蚀啦!
6. 化学污染环境腐蚀,这不就是那些有害化学物质在搞鬼嘛!好比工厂排放的那些乱七八糟的化学物质,对周边环境造成严重腐蚀呢。
7. 土壤环境腐蚀,就好像土壤里藏着小恶魔在悄悄搞破坏呀!埋在土里的管道什么的,时间长了就会被腐蚀呢。
8. 大气环境腐蚀,那可不就是无时无刻不在的威胁嘛!就像空气中的一些成分在偷偷侵蚀着我们身边的东西一样。
9. 微生物环境腐蚀,这就像是微生物在悄悄发动攻击呢!像一些有微生物滋生的地方,真的会导致腐蚀哦!
我觉得腐蚀环境的分类真的很重要啊,了解这些能让我们更好地去应对和防范腐蚀带来的危害。
自然环境腐蚀
生物的生命运动改变了局部海水介质成分,加速腐蚀;
某些海生物生长时穿透表面保护层,破坏了保护膜,加速腐蚀
8.3 土壤腐蚀
多相性; 多孔性;不均匀性;固定性
一. 土壤腐蚀的电极过程及控制因素
金属在土壤中的电极电位取决于两个因素: 1. 金属的种类及表面性质 2. 土壤介质的物理化学性质
由于土壤是不均匀且相对固定的介质,因此土壤的理化性质在不同部位往 往不同
(2)湿膜的形成-金属表面形成可见水膜 其腐蚀历程类似于沉浸在水中条件下的腐蚀,但氧的补充情况比浸于水中好
8.1 大气腐蚀
二. 大气腐蚀过程和机理
2. 大气腐蚀的电化学特征 (1)阴极过程 大气腐蚀条件下,氧通过液膜传递速度快,液膜越薄扩散层的厚度越 薄,因而阴极上的氧去极化作用越容易进行,阴极过程的速度加快。 阴极过程主要是氧的去极化控制。 (2)阳极过程 当电极存在很薄的水膜时,阳离子水化困难,阳极过程受到阻滞, 在很薄的水膜下,氧易于到达阳极表面,促使阳极钝化作用,使阳极 过程受到强烈的阻滞
四. 防止大气腐蚀的措施
1. 提高材料耐蚀性 2. 控制环境
8.2 海水腐蚀
一. 海水的物理化学性质
1. 高盐度 2. 高电导率 3. pH值 4. 海水温度 5. 含氧量 6. 附着生物
海水的一项重要指标。盐度高,氯化物含量高 比江河高出两个数量级 中性,主要以氧去极化为主 不同地域变化范围大 不同环境,海水氧含量会在较大范围波动
8.3 土壤腐蚀
一. 土壤腐蚀的电极过程及控制因素
1. 阳极过程-铁在潮湿的土壤中阳极极化过程无明显的阻滞 腐蚀产物与土粒粘合,形成紧密层,有效阻碍阳极反应; 阳极钝化-氧易于到达金属表面时
2. 阴极过程-氧的去极化过程,受氧输送控制 氧的进入受阴极表面电解液(扩散层)的限制,还受阴极上面土壤层 的阻碍,输送氧的主要途径是氧在土壤气相中(孔隙)的扩散
第八章 环境腐蚀

2.
与腐蚀有关的重要微生物
1)喜氧菌(嗜氧菌)—有游离氧条件下能生存的菌类 铁细菌 氧化铁杆菌 20~25C, pH7~1.4 Fe2+Fe3++e 硫氧化菌 排硫杆菌、氧化硫杆菌、水泥崩解硫杆菌 28~30C, pH2.5~3.5 2S+3O2+2H2O2H2SO4 2)厌氧菌—在缺乏或几乎无游离氧下才能生存的菌类 硫酸盐还原菌 25~30C, pH7.2~7.5 3)有氧和无氧环境中都能生存—硝酸盐还原菌
在酸性很强的土壤中,氢的去极化;在某些情况下, 还有微生物参与阴极还原过程。
4. 影响土壤腐蚀的因素
电阻率
与土壤含水量、孔隙度有关,电阻率越大,土壤腐蚀越严重
透气性(孔隙度) —氧渗透和水分保存
透气性良好:加速腐蚀、生成保护性腐蚀产物并减缓腐蚀 透气性不良:减缓微电池腐蚀、易产生氧浓差电池而严重腐蚀
如:铁大气中生锈、铜产生铜绿…. 世界上60%以上钢材在大气环境中使用 大气腐蚀损伤占总腐蚀损失量 > 50% 某些功能材料(微电子电路)、文物等,
轻微大气腐蚀也不允许
以均匀腐蚀为主,包括点 蚀、缝隙腐蚀、电偶腐蚀 微动腐蚀、应力腐蚀及腐 蚀疲劳等
大气腐蚀特点:
液膜下的电化学腐蚀 大气环境不同, 腐蚀严重性不同
•
•
海水中有一定含氧量
海水为中性(pH~7.2-8.6),
特征: 阳极 Me → Men+ + ne阴极 O2+ 2H2O + ne- → 4OH 阳极溶解速度大,阴极氧去极化反应为控制步骤
低合金钢 —海洋环境常用金属材料 形成腐蚀产物覆盖层抑制海水腐蚀,可比碳钢耐腐蚀5倍
大量卤素离子
自然环境腐蚀

– 腐蚀速度下降(III区)
I II
III
IV
水膜厚度
• 水膜厚>1mm ,相当于金属全浸于电解质溶液,
腐蚀速度基本不变(IV区)
自然环境腐蚀
6.1.2 大气腐蚀条件
• 电化学腐蚀的特殊形式
– 金属表面在潮湿的大气中 吸附一层很薄的水膜 – 当水膜达到20~30分子层厚时 电解液膜
• 液膜来源
– 水分(雨雪)直接沉降; – 大气湿度或温度变化等原因引起的凝聚作用。
Fe → Fe2+ + 2e
• 阴极反应:Fe3O4/FeOOH界面上 8FeOOH + Fe 2+ + 2e → 3Fe3 O4 + 4 H 2 O
锈层内发生了Fe 3+→Fe 2+的还原反应 锈层参与了阴极反应过程
自然环境腐蚀
锈层形成后的腐蚀机理
• 大气干湿交替:锈层加速腐蚀 • 锈层干燥时
– 锈层和底部基体金属的局部电池成为开路 – 在大气中氧的作用下锈层内的Fe 2+重新氧化成为Fe 3+
大气腐蚀损失占总腐蚀损失量>50% • 对于某些功能材料(微电子电路)、文物、装饰
材料等,轻微大气腐蚀也不允许
自然环境腐蚀
大气腐蚀
• 大气腐蚀以均匀腐蚀为主
– 也包括点蚀、缝隙腐蚀、电偶腐蚀、微动腐蚀、 应力腐蚀及腐蚀疲劳等
• 大气腐蚀属于液膜下的电化学腐蚀
– 区别于浸于电解质溶液中的腐蚀
自然环境腐蚀
自然环境腐蚀
大气腐蚀条件
• 液膜的产生:结露
– 当金属表面处于比其温度高的空气中,空气中 的水蒸汽将以液体凝结于金属表面上
– 结露是发生潮大气腐蚀的前提 – 空气温度在5~50oC范围内,气温剧烈变化达
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属氧化膜 分层结构
金属氧化膜成长行为与耐腐蚀性
Fe高温氧化 Cu,Ni,Ti …
Fe中温氧化 Al,Cr, Zn …
Mg 氧化 ( V氧化物< 金属)
工业大气对腐蚀的影响 化学工业大气腐蚀性 》内陆沙漠地带大气腐蚀性 沿海工业城市大气腐蚀性 》内地很多倍。温度/湿度/工业大气 化学污染共同作用
SO2的腐蚀作用(酸雨),使腐蚀不断发展: Fe + SO2 + O2 = FeSO4 4FeSO4 + O2 +6H2O = 4FeOOH + 4H2SO4 4H2SO4 + Fe + O2 = 4FeSO4 + 4H2O
若能去除FeSO4, 腐蚀停止发展
含SO2
湿度的影响(临界湿度)
4.防止大气腐蚀措施
(1) 选材-Mn钢,不锈钢,Al, Ti, Fe+Cu+P+Cr+N; (2) 表面覆盖保护层-表面处理、电镀、有机物涂覆 (3) 防锈油、防锈液、气相缓蚀剂、包装封存 (4) 吸氧 Na2SO3+ H2O + O2 Na2SO4 (5) 去水(除湿)
阳极反应(金属/氧化膜界面): M Mn + ne;
阴极反应(氧化膜表面): 1/2 O2 + 2e O2— ;
• 氧化膜具电子导体和离子 导体特性,传输离子和电子, 使氧化膜增厚。
• 氧化速率决定于氧化膜中 物质的传输速率。
• 晶格缺陷/离子运动,表现 出离子电导性。离子传导是 氧化过程的控制步骤
H2O
吸附凝聚
H2O
OH-
Mቤተ መጻሕፍቲ ባይዱ
Mn+
ee
阴极反应:O2+ H2O + 4e 4OH— 阳极反应:Fe Fe2++2e
湿条件: 4Fe2O3 + Fe2++ 2e 3Fe3O4 干条件: 3Fe3O4 + 0.75 O2 4.5 Fe2O3
湿/干交替— 腐蚀不断发展
表面水膜厚/溶解氧与腐蚀 速度的关系 I- =100~1000A II- = 1000A~1m III- = 1m~1mm IV- > 1mm
(a) y2 = 2px
(b) y = 1gx
(c) y = a + bx
抛物线型 -较强保护性; 对数型 -强保护性; 直线型 -不具保护性。
氧化膜特征-耐蚀性
高耐蚀性氧化膜必要条件: (1) 膜致密, 完整覆盖 (体积氧化物/ 体积金属 > 1) (2) 膜的(热/化学)稳定性高; (3) 膜与基底金属的结合力强 (4) 膜具有一定的塑性和强度 (5) 膜与基底金属的热膨胀系数相近 (6) 膜的电导性低、对氧和金属离子的扩散系数低
高温/高压
第二阶段(氢侵蚀): 钢中H 与不稳定碳化物反应:
Fe3C +2H2 3Fe + CH4
脱碳-机械强度下降,CH4 -内压力, 裂纹, 鼓泡,破坏 不可逆。
防氢腐蚀措施: 降低含碳量( < 0.015%) (去碳作用);添加 Cr、Ti、Mo、W、V等, 生成稳定碳化物, 降低游离碳。
§6.2 大气腐蚀
3. 高温氢腐蚀
合成氨, 合成甲醇, 石油加氢等石化工业中, 发生高温、高压 下的氢脆腐蚀。氢气在常温常压下对碳钢发生明显腐蚀。
当T > 200-300℃, 压力 > 300大气压时,钢铁会发生严重 氢腐蚀 (机械强度急剧下降):
第一阶段(氢脆):
氢吸附,原子状态H进入(沿 晶界) 金属生成固溶体,无 化学反应,脆化可逆。
PbCO3.or PbO 覆盖在金属表面, 可阻止大气腐蚀的发展。
大气腐蚀机理
金属基底 微孔内
氧化物界面
氧化物外层
Fe Fe 2+ + 2e 3Fe 2+ + 2OH- +1/2O2 Fe3O4 +H2O 8FeOOH + 3Fe 2+ +2e 3 Fe3O4 + H2O 3 Fe3O4 +0.75 O2 + 4.5 H2O 9FeOOH
§6.3 海水腐蚀
海水—腐蚀性最强的天然环境介质,海水腐蚀十分普遍, 如 船舶、码头、海上平台、跨海大桥、海上设备、海水冷却、海 洋大气等。海洋腐蚀的控制是一个重大的实际问题。
1 海水特点 • 海水含盐分高 — 3.3%-3.8%(NaCl, MgCl2, MgSO4, CaSO4…) • 电导性强 — 2.3-3.0×10-2 -1cm-1 • 海水中Cl- (占总离子55%), 硫化物腐蚀性强 • 海水强对流, 充氧丰富, 接近饱和(随海水深度而变化) • 海水为中性(pH~7.2-8.6), 阴极反应:O2 + 2H2O + 4e 4OH-
大气腐蚀特点:
表面粗糙毛细作用, 化学颗粒, 范德华力等使金属表面形成水膜—大气腐 蚀基本条件。金属表面水膜厚和溶解氧对大气腐蚀关系密切。大气腐蚀 与表面腐蚀产物(膜)的保护性关系密切,比较稳定的表面腐蚀产物(膜), 如Fe--FeOOH, Cu-CuCO3.3Cu(OH), Al-Al2O3.3H2O, Pb-
2. 钢的脱碳 钢表面氧化时伴随“脱碳”过程, 表面层碳减少, 即: Fe3C + 1/2 O2 3Fe + CO Fe3C + CO2 3Fe + 2CO Fe3C + H2O 3Fe + CO + H2 Fe3C + 2H2 3Fe + CH4
• 反应产物气体, 脱碳 — 机械性能(强度、硬度…)下降 • 反应产物气体析出,表面膜破坏,腐蚀加剧
§6.1 干燥气体腐蚀
1. 高温氧化 高温氧化十分普遍, 如工业各种管式加热炉、涡轮机、金
属热加工等, 高温氧化反应式: x M +1/2 (yO2) MxOy
反应平衡决定于PO2和PMO, 空气中 PO2 :0.2 由PO2和PMO, 判定反应方向。
氧化膜的形成 氧化膜高温氧化
金属表面氧化膜成长电化学机理
大气腐蚀普遍, 约占60-70%。 化工大气腐蚀性强, 如硫酸 厂大气腐蚀达0.5mm/y; 联碱厂3-5 mm/y, 大气中O2, H2O直 接参与腐蚀反应 (电化学腐蚀)。
20亿/5年
重要因素
• SO2、SO3、H2S 生成HSO3, H2SO4,促进腐蚀
大 气
• 雷电暴雨电离N2 生成NH3(合成肥料), 促进腐蚀 (季裂)
污
• 盐粒(NH4)2SO4 ,(NH3 + SO3) 吸湿性和酸性
染
• 氯化物NaCl-吸湿和侵蚀性, 促进腐蚀
气 候
• -定厚度灰尘/ 微颗粒,吸附 H2O, SO3…促进腐蚀
条 • 湿度、日照、气温、风向、风速等均可影响大气腐蚀
件
含SO2
无SO2 T/D
大气腐蚀原理
O2 O2
化学凝聚
H2O
毛细管凝聚
