第10讲钠及其重要化合物
钠及其重要化合物知识点汇总

钠及其重要化合物知识点汇总钠是一种常见的金属元素,原子序数为11,在周期表中位于第三周期的左侧,是一种非常活泼的金属元素。
钠在生活中具有非常重要的作用,广泛应用于食品加工、制药、化学工业等领域。
本文将从钠的物理性质、化学性质、重要化合物等方面进行全面汇总,带领读者深入了解钠及其化合物。
一、钠的物理性质1. 外观:钠是一种银白色的金属元素,有一定的延展性和可塑性。
2. 密度:钠的密度较小,约为0.97g/cm³,是常见金属中密度最小的。
3. 熔点和沸点:钠的熔点较低,为97.8℃,沸点也不高,为883℃。
4. 导电性:钠是一种良好的导电金属,电子亦能良好地传导。
5. 可燃性:钠是一种极容易燃烧的金属元素,与水接触时可以迅速剧烈地反应,甚至能够产生爆炸。
二、钠的化学性质1. 与氧反应:钠与氧反应后能够生成氧化钠(Na2O)和过氧化钠(Na2O2)两种化合物。
其中,氧化钠能够与水反应,产生氢氧化钠(NaOH)。
2. 与酸反应:钠可以与酸反应,产生氢气和相应的钠盐。
例如,当钠与盐酸反应时可以产生氢气和氯化钠。
3. 与水反应:钠与水接触后可以迅速且剧烈地反应,产生氢氧化钠和氢气。
由于反应剧烈,钠和水一起使用时需要特别小心。
4. 氧化还原性:钠是一种良好的还原剂,可以将氧化性较强的物质还原。
例如,钠可以将氯气还原成氯化钠。
三、钠的重要化合物1. 氢氧化钠氢氧化钠(NaOH)是一种重要的化学品,也是钠最为重要的化合物之一。
氢氧化钠常常被用于金属清洗、纸浆生产、染料生产等行业。
2. 碳酸钠碳酸钠(Na2CO3)是一种常见的碳酸盐类化合物,广泛应用于玻璃制造、制药、生产洗涤剂等领域。
3. 氯化钠氯化钠(NaCl)是一种常见的盐类物质,是人体内必需的营养元素之一。
氯化钠广泛应用于食品加工、制盐和化学工业等领域。
4. 硫酸钠硫酸钠(Na2SO4)是一种重要的无机盐,在制造玻璃、纸张、化学品等方面具有广泛的应用。
2019版高考化学(人教版)练习:第三章 第10讲 钠及其化合物 Word版含解析

课时作业1.下列关于钠的叙述正确的是()A.钠在空气中燃烧生成Na2OB.根据反应Na+KCl 熔融NaCl+K↑,知Na的金属性强于KC.钠燃烧时发出黄色(透过蓝色钴玻璃)的火焰D.实验完毕后剩余的金属钠不能随意丢弃,应放回原试剂瓶解析:钠在空气中燃烧生成Na2O2,只有在常温下才生成Na2O,A错;反应Na+KCl熔融NaCl+K↑是利用了K的低沸点,B错;观察Na燃烧时的火焰不能透过蓝色钴玻璃,C错;实验用剩的金属钠应放回原试剂瓶,不能随意丢弃,以防失火,D正确。
答案:D2.钠及其化合物与人们的生活密切相关,某同学对其认识不正确的是()A.碳酸氢钠常用于治疗胃酸过多症B.Na2O2用作呼吸面具的供氧剂C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔D.金属钠着火时,使用泡沫灭火器来灭火解析:D项,Na燃烧生成的Na2O2能与CO2反应,因此金属钠着火时不能用泡沫灭火器灭火,应用沙土掩埋法灭火。
答案:D3.下列各组中的两种物质反应,反应条件(温度或反应物用量)改变,不会引起产物种类改变的是()A.Na和O2B.NaOH和CO2C.Na2O2和CO2D.Na2CO3和盐酸解析:钠与氧气在常温下与加热或点燃条件下生成的产物不同,常温下生成氧化钠,加热或点燃条件下生成过氧化钠,A项错误;氢氧化钠与少量二氧化碳反应生成碳酸钠,与过量二氧化碳反应生成碳酸氢钠,产物不同,B项错误;过氧化钠与二氧化碳反应生成碳酸钠和氧气,与量无关,C项正确;Na2CO3与少量盐酸反应生成NaHCO3和NaCl,与过量盐酸反应生成CO2,H2O和NaCl。
答案:C4.某固体物质只含有钠和氧两种元素,将它放在足量的水中产生两种气体,这两种气体又可以在一定条件下反应生成水。
则原固体物质的组成是()A.Na2O2与Na2O B.Na和NaOHC.Na2O2和Na D.Na和Na2O解析:由这两种气体在一定条件下反应生成水,可知为氧气和氢气,故原固体组成为Na2O2和Na。
高考复习方案(全国卷)2017版高考化学一轮复习第3单元金属及其化合物第10讲钠及其重要化合物教学案
第3单元金属及其化合物第10讲钠及其重要化合物考纲要求 1.了解钠的主要性质及其应用。
2.了解钠的重要化合物的主要性质及其应用。
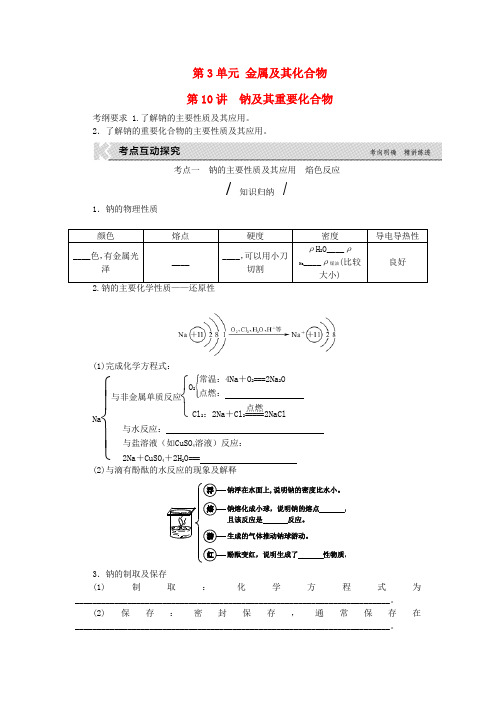
考点一钠的主要性质及其应用焰色反应知识归纳1.钠的物理性质颜色熔点硬度密度导电导热性____色,有金属光泽________,可以用小刀切割ρH2O____ρNa____ρ煤油(比较大小)良好(1)完成化学方程式:Na⎩⎪⎨⎪⎧与非金属单质反应⎩⎨⎧O2⎩⎪⎨⎪⎧常温:4Na+O2===2Na2O点燃:Cl2:2Na+Cl2=====点燃2NaCl与水反应:与盐溶液(如CuSO4溶液)反应:2Na+CuSO4+2H2O===(2)与滴有酚酞的水反应的现象及解释3.钠的制取及保存(1)制取:化学方程式为________________________________________________________________________。
(2)保存:密封保存,通常保存在________________________________________________________________________。
4.钠的用途(1)制取Na 2O 2等化合物。
(2)钠、钾合金(液态)可用于原子反应堆的导热剂。
(3)用作电光源,制作高压钠灯。
(4)冶炼某些金属,如:4Na +TiCl 4=====熔融4NaCl +Ti 。
5.焰色反应(1)概念:很多金属或它们的化合物在灼烧时都会使火焰呈现特殊颜色的现象。
属于元素的____________性质。
(2)操作步骤:铂丝――→酒精灯灼烧____色――→蘸取待测物――→酒精灯灼烧观察火焰颜色――→用 洗涤铂丝――→酒精灯灼烧无色 (3)常见元素焰色反应的颜色:钠元素:________;钾元素:________(透过________观察)。
■ 判断思考1.判断下列描述的正误(正确的打“√”,错误的打“×”)。
(1)钠表面自然形成的氧化层能够保护内层金属不被空气氧化( )(2)将一小块钠放入无水乙醇中,产生气泡,说明钠能置换出醇羟基中的氢( )(3)1 mol Na 被完全氧化生成Na 2O 2,失去2N A 个电子( )(4)电解熔融氯化钠或饱和食盐水都可得到金属钠( )(5)金属钠可保存在煤油中,也可保存在四氯化碳中( )(6)4Na +O 2,F2Na 2O 和2Na +O 2=====点燃Na 2O 2可说明相同的反应物在不同的条件下可能发生不同的反应( )(7)焰色反应是大多数金属元素的性质,属于化学变化( )(8)用洁净的铂丝对某溶液进行焰色反应,火焰呈黄色,则溶液中一定含有Na +,不含K+( )2.金属钠露置在空气中会发生什么样的变化?最终生成什么物质?(用示意图表示)典型例题1 下列说法正确的是( )A .2015·全国卷Ⅱ] 钠在空气中燃烧可生成多种氧化物,23 g 钠充分燃烧时转移电子数为N AB .2015·天津卷] 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na +,无K +C .2015·山东卷] 金属钠着火时使用泡沫灭火器灭火D .2013·新课标全国卷Ⅰ] 钠与CuSO 4溶液反应:2Na +Cu 2+===Cu ↓+2Na +图31012 按如图3101所示实验装置进行钠跟水反应的实验,据此判断下列说法正确的是( )A.打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应C.反应一段时间后,左端液面上升,进入长颈漏斗,a处有无色气体产生D.若用苯或酒精来代替煤油,可观察到相同的实验现象■ 变式训练1.关于钠的叙述中,不正确的是( )A.金属钠与水反应生成氢气,但是实验室中不能用金属钠与水反应制备氢气B.金属钠放在石棉网上加热时,先熔化成银白色小球,然后剧烈燃烧,发出黄色火焰C.金属钠在空气中放置生成氧化钠,在空气中燃烧生成过氧化钠D.金属钠与氧气反应的产物取决于氧气的用量2.把一小块金属钠放入下列溶液中,说法正确的是( )A.放入饱和NaOH溶液中:有氢气放出,恢复至室温后溶液的pH增大B.放入稀CuSO4溶液中:有氢气放出,有紫红色铜析出C.放入MgCl2溶液中:有氢气放出,有白色沉淀生成D.放入NH4NO3溶液中:有无色无味气体放出1.金属钠与可溶性盐溶液反应的思维模型2.金属钠与溶液反应现象分析的思维模板(1)共性:因为钠与不同溶液的反应均属于剧烈的置换反应,故有共同的现象产生:①浮:钠浮在液面上;②熔:钠熔化成光亮的小球;③游:在液面上不停地游动直至反应完全;④响:反应中不停地发出“嘶嘶嘶”的响声。
钠及其重要化合物

硫酸钠的安全性
硫酸钠是一种常见的钠化合物,常用于化工、农业和食品 等领域。其安全性相对较高,但仍需注意使用方式和暴露 量。
硫酸钠对皮肤和眼睛无刺激性和毒性,但吸入高浓度的硫 酸钠可能导致呼吸道刺激和呼吸困难。长时间吸入硫酸钠 还可能对肺部造成影响。
在化合物中通常呈+1价 钠与水反应生成氢氧化钠和氢气
钠的存在形式
01
自然界中,钠主要以化合物的形 式存在,如氯化钠(食盐)和碳 酸钠(纯碱)等
02
在人体内,钠主要以离子形式存 在,对维持人体正常生理功能具 有重要作用
02 钠的重要化合物
氧化钠
01
化学式:Na2O
02
性质:氧化钠是一种白色固体,具有吸湿性,与水反应生成 氢氧化钠。
氧化钠的安全性
01
氧化钠是一种常见的钠化合物,广泛应用于工业和日常生活中。其安全性主要 取决于使用方式和暴露量。
02
在正常条件下,低浓度的氧化钠对人体无害。然而,高浓度的氧化钠可能对皮 肤、眼睛和呼吸系统造成刺激。长时间接触高浓度的氧化钠还可能导致皮肤干 燥、脱屑和裂纹。
03
在工业环境中,应采取适当的防护措施,如穿戴防护服、戴化学防护眼镜和使 用呼吸器,以减少氧化钠暴露的风险。
氢氧化钠的安全性
氢氧化钠是一种强碱,具有腐蚀性和刺激性。其安全 性取决于使用方式和暴露量。
低浓度的氢氧化钠溶液(如家用清洁剂)通常对人体 无害,但高浓度的氢氧化钠溶液可能对皮肤、眼睛和
呼吸系统造成严重刺激和伤害。
在处理氢氧化钠时,应穿戴化学防护眼镜、化学防护 服和化学防护手套,并使用适当的呼吸器。储存和使
第10讲 常见金属及其重要化合物(课件)-2023届高考化学二轮复习(全国通用)

Cu+Cl2
CuCl2,2Cu+S
Cu2S
②铜在潮湿的空气中生锈。
2Cu+O2+H2O+CO2
Cu2(OH)2CO3
③将 Cu 与浓硫酸混合加热。
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
④Cu 与稀硝酸反应的离子方程式。
+2N
+
3Cu+8H
3Cu2++2NO↑+4H2O
HC +H+
HC
H2O+CO2↑
④用化学方程式表示呼吸面具中产生O2的原理。
2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2CO2═2Na2CO3+O2
(3)扫除易忘知识盲点。
钠能够置换出金属性比其弱的金属
①钠与盐溶液反应,不能置换出盐中的金属,钠与熔融的盐反应才可能置
换出盐中的金属。
⑤常用FeCl3溶液腐蚀铜板(用离子方程式表示)。
Cu+2Fe3+═Cu2++2Fe2+
⑥用离子方程式表示将氨水逐滴滴入CuSO4溶液的反应过程。
Cu2++2NH3·H2O═Cu(OH)2↓+2N+
Cu(OH)2+4NH3·H2O═[Cu(NH3)4]2++2OH-+4H2O
(3)知识盲点。
3+
Al
+3HC
Al(OH)3↓+3CO2↑
⑥用离子方程式分别表示
3+
高三化学一轮复习 第10讲 钠及其化合物 针对练习 答案+解析

高三化学一轮复习(十) 1.下列有关叙述正确的是()A.碳酸氢钠药片,该药是抗酸药,服用时喝些醋能提高药效B.分别将少量钠投入到盛有水和乙醇的烧杯中,可比较水和乙醇中氢的活泼性C.钾、钠、镁等活泼金属着火时,可用泡沫灭火器灭火D.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+[解析]醋酸能与碳酸氢钠反应产生二氧化碳,降低药效,A错;钠在水中反应的速度比在乙醇中的大,可比较二者氢原子的活性,B正确;钠、钾都能与水反应产生氢气,镁能在二氧化碳中燃烧,因而不能用泡沫灭火器灭火,C错误;钠的焰色反应为黄色,可掩盖钾的火焰的紫色,D项错误。
[答案] B2.(2017·武汉模拟)把一小块金属钠放入下列溶液中,说法正确的是() A.放入饱和NaOH溶液中:有氢气放出,恢复至室温后溶液的pH增大B.放入稀CuSO4溶液中:有氢气放出,有紫红色铜析出C.放入MgCl2溶液中:有氢气放出,有白色沉淀生成D.放入NH4NO3溶液中:有无色无味气体放出[解析]A项错误,饱和NaOH溶液中放入钠,钠与水反应消耗水且生成NaOH,恢复至室温会有部分NaOH晶体析出,同时生成氢气,由于溶液仍是饱和溶液,故溶液的pH不变;B项错误,钠与水反应生成氢气和NaOH,NaOH 与CuSO4反应会出现蓝色沉淀;C项正确,钠与水反应生成的NaOH与MgCl2反应生成Mg(OH)2白色沉淀;D项错误,钠与水反应放热,生成的NaOH与NH+4反应生成NH3·H2O,NH3·H2O部分分解产生的少量氨气会与氢气同时放出,故放出的气体有刺激性气味。
[答案] C3.(2017·衡水模拟)下列实验操作正确的是()[解析]A项,取出钠后先用滤纸吸干钠表面的煤油,再切,且烧杯中的水不能装满,错误;B项,二者与澄清石灰水均反应生成沉淀,错误;D项,K+的焰色反应不能直接观察。
[答案] C4.(2017·长沙长郡中学月考)为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。
高中化学精品课件:钠及其化合物复习

2.某同学用Na2CO3和NaHCO3溶液进行如图所示实验。下列说法不正确 的是 问A题.实1验:前碳p酸H氢(N钠a2C溶O液3)与>氯pH化(N钙a溶HC液O反3) 应得到的沉淀是碳酸钙吗?如果是,
√ 那B么.实碳验酸后根两来溶自液哪中里离?子种类完全相同
问需C题要.N满a22:C足O从什3溶沉么液淀条溶中件解生?平成衡的角沉度淀思比考N,aH碳C酸O3氢钠溶液与氯化钙溶液生成沉淀 溶液中生成的沉淀多
2.焰色反应 (1)焰色反应的概念 某些金属或它们的化合物在灼烧时都会使火焰呈现出特殊的颜色,属于 物理变化,是元素的性质。 (2)焰色反应的操作 铂丝―酒―灼精―烧―灯→无色――蘸―取―→待测物―酒―灼精―烧―灯→观察火焰颜色―用―洗盐―涤―酸→
铂丝―酒―灼精―烧―灯→无色
(3)常见元素的焰色 钠元素: 黄 色;钾元素: 紫 色(透过 蓝色钴玻璃 观察);铜元素: 绿色; 钡元素: 黄绿色;Ca元素: 砖红 色。
该电池负极材料是什么?能否把电极锂外层裹包的聚合物电 解质去掉?
三、探究过氧化钠的性质
向饱和 NaOH 溶液(滴加酚酞)中加入少量的过氧 化钠粉末,会有什么现象? 实验现象:有大量无色气泡产生,溶液红色褪去,并放出热量,有少量晶体析出。 问题 1:Na2O2 与水反应的氧化剂和还原剂是?
问题 2:为什么有晶体析出?恢复到室温后,溶液中的 c(Na+) 和 c(OH-)如 何变化?
问题 1:金属钠与氯化钾反应置换出单质钾是在水溶液中进行的吗?为什么? 问题 2:该反应的温度应该如何控制? 问题3:该反应的反应条件如何控制有利于钾的生成? 问题4:把钠分别投入饱和氢氧化钙溶液、硫酸铜溶液、氯化铵溶液中,会有 什么现象?
问题 5:2013 年 3 月,我国科学家公布了如下图所示的水溶 液锂 离子电池体系。
高一年级必修1化学方程式:钠及其重要化合物

高一年级必修1化学方程式:钠及其重要化合物化学的成就是社会文明的重要标志,查字典化学网为大家推荐了高一年级必修1化学方程式,请大家仔细阅读,希望你喜欢。
一、钠及其重要化合物
1、钠与非金属的反应
4Na +O2=2Na2O(白色) 2Na + O2 △ Na2O2 (淡黄色)
2Na +Cl2 点燃 2NaCl
2、钠与水反应:2Na + 2H2O = 2NaOH + H2 (浮、熔、游、响、红)
3、氧化钠过氧化钠
Na2O+H2O=2NaOH 2Na2O2+2H2O=4NaOH+O2
Na2O+CO2=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2
Na2O+2HCl=2NaCl+H2O 2Na2O2+4HCl=4NaCl+2H2O+O2
6、Na2CO3和NaHCO3
①、与酸的反应
Na2CO3+2HCl=2NaCl+H2O+CO2
NaHCO3+HCl=NaCl+H2O+CO2(反应速率更快)
②、与碱的反应
Na2CO3+Ca(OH)2=CaCO3+2NaOH
2NaHCO3+Ca(OH)2=CaCO3+Na2CO3+2H2O
NaHCO3+NaOH= Na2CO3+H2O
③、与盐的反应
Na2CO3+CaCl2=2NaCl+CaCO3
Na2CO3+BaCl2=2NaCl+BaCO3
④、相互转化
2NaHCO3 △ Na2CO3+H2O+CO2(加热分解)
Na2CO3+H2O+CO2=2NaHCO3 (向Na2CO3溶液中通入足量的CO2)
小编为大家提供的高一年级必修1化学方程式,大家仔细阅读了吗?最后祝同学们学习进步。
