二零二一年四川省眉山市高中化学教师公招考试学科专业试题解析版
高中化学老师招聘试题及答案

高中化学老师招聘试题及答案一、选择题(每题2分,共20分)1. 化学变化的本质特征是:A. 放出热量B. 产生气体C. 产生沉淀D. 新物质的生成2. 以下哪个元素属于碱金属?A. 锂(Li)B. 钠(Na)C. 钾(K)D. 铯(Cs)3. 根据原子结构,以下哪个元素的原子半径最大?A. 氢(H)B. 氧(O)C. 钠(Na)D. 氯(Cl)4. 以下哪个化合物属于共价化合物?A. 氯化钠(NaCl)B. 硫酸钠(Na2SO4)C. 氧化铁(Fe2O3)D. 水(H2O)5. 根据化学平衡原理,以下哪个条件可以促进正反应的进行?A. 增加反应物的浓度B. 减少生成物的浓度C. 降低温度D. 增加催化剂6. 以下哪个反应是氧化还原反应?A. 氢气燃烧生成水B. 碳酸钙分解生成氧化钙和二氧化碳C. 水的电解D. 二氧化碳与水反应生成碳酸7. 以下哪个是原子的核外电子排布规律?A. 能量最低原理B. 洪特规则C. 泡利不相容原理D. 所有以上8. 以下哪种物质不是有机化合物?A. 甲醇(CH3OH)B. 乙醇(C2H5OH)C. 丙酮(C3H6O)D. 碳酸氢钠(NaHCO3)9. 以下哪个元素的原子序数是26?A. 铁(Fe)B. 钴(Co)C. 镍(Ni)D. 铜(Cu)10. 以下哪个是化学键的类型?A. 离子键B. 共价键C. 金属键D. 所有以上答案:1. D2. A3. C4. D5. A6. A7. D8. D9. C10. D二、填空题(每空2分,共20分)1. 元素周期表中,第IA族元素的特点是_________。
答案:最外层只有一个电子2. 化学方程式中,平衡常数K的表达式是_________。
答案:生成物浓度幂次方乘积与反应物浓度幂次方乘积的比3. 氧化还原反应中,被氧化的物质是_________。
答案:失去电子的物质4. 根据分子间作用力,水的沸点比甲烷高是因为_________。
2021统考教师资格考试《高中化学学科与教学》考试真题

2021统考教师资格考试《高中化学学科与教学》考试真题一、真题及详解全国统考教师资格考试《化学学科知识与教学能力》(高级中学)真题及详解考试时间:120分钟考试总分:150分本试题为回忆版,部分题目不全。
一、单项选择题(本大题共20道小题,每题3分,共60分)1.为增强课程的适应性,我国当前基础教育课程实行的是()。
A.国家统一课程B.国家、地方、学校C.学校自主课程D.学科和活动课程【答案】B @~~【解析】我国基础教育实行三级课程管理,目的是要增强课程对地方、学校及学生的适应性。
其中,“三级”指的是国家、地方、学校。
2.下列不属于化学课程三维目标的是()。
A.能力和德育B.知识与技能C.过程与方法D.情感态度与价值观【答案】A @~~【解析】化学课程三维目标包括:知识与技能、过程与方法、情感态度与价值观。
3.图1是某高中化学教材中帮助学生理解有关电子迁移内容的类比图像,下列选项不属于类比图像核心的教学功能的是()。
图略A.迎合学生的认知规律B.降低认知难度C.解释抽象知识D.开发学生的想象力【答案】D @~~【解析】类比图像是高中化学教材的重要呈现形式,既有图像的直观化,形象化的特点,又能有效的促进知识迁移。
将不同的事物进行数据化统计形成一个具有形象、直观、有说服力的图标,再与有共同类别或特征的其他事物进行对比的工序。
这种方法符合学生的认知特点,能够形象的解释较为抽象的知识,直观化形象化地展示降低了学习的认知难度。
7.有关科学探究表述正确的是()。
A.科学探究既是学习内容又是学习方式B.探究教学要按照科学探究的八个要素依次开展教学活动C.科学探究必须由学生独立完成D.科学探究要在教室或实验室完成【答案】A @~~【解析】科学探究是通过科学实验、探究活动、我们身边的科学、科学人物、计算机应用、职业链接、概念图等多重呈现方式呈现。
从太空探索、能源利用、物质研究、地球探索、探索生命、生态系统等视角,强调科学实验和科学探究、研究性学习活动的过程体验,让学生从活动中学习、理解和应用科学知识。
2021-2022学年四川省眉山市中学高二化学测试题含解析

2021-2022学年四川省眉山市中学高二化学测试题含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 某烷烃的一种同分异构体只能生成一种一氯代物,则该烃的分子式不可能的是() A.C2H6 B.C5H12 C. C4H10 D.C8H18参考答案:C略2. 下列有关说法正确的是( )A.可用分液漏斗分离乙醛与水的混合物B.可用溴水一次全部鉴别出苯、乙醇、1-己烯、福尔马林和苯酚溶液C.提纯苯甲酸(含有食盐固体)可采用溶解、过滤、蒸馏的方法。
D.煤油、柴油、花生油、猪油的主要成分均为酯类。
参考答案:B3. 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图所示,其中的固体电解质是Y2O3﹣Na2O,O2﹣可以在其中自由移动.下列有关叙述正确的是()甲乙A.瓦斯分析仪工作时,电池电路中电子由电极b流向电极aB.电极b是正极,O2﹣由电极a流向电极bC.电极a的反应式为:CH4+5O2﹣﹣8e﹣=CO32﹣+2H2OD.当固体电解质中有1mol O2﹣通过时,电子转移4mol参考答案:C【考点】原电池和电解池的工作原理.【专题】电化学专题.【分析】瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3﹣Na2O,O2﹣可以在其中自由移动;通甲烷气体的为负极,通空气一端为正极,电池总反应为CH4+2O2=CO2+H2O,正极反应为:O2+4e﹣=2O2﹣,负极反应为:CH4+5O2﹣﹣8e﹣=CO32﹣+2H2O或CH4+4O2﹣﹣8e﹣=CO2+2H2O,结合原电池的原理和电极反应分析解答.【解答】解:A、该电池中a为负极,b为正极,电子从负极流向正极,所以电池外电路中电子由电极a流向电极b,故A错误;B、电极b氧气得电子,生成O2﹣,而电极a需要O2﹣作为反应物,故O2﹣由正极(电极b)流向负极(电极a),故B错误;C、选项中电荷不守恒,甲烷所在电极a为负极,电极反应为:CH4+5O2﹣﹣8e﹣=CO32﹣+2H2O,故C正确;D、1mol O2得4mol电子生成2molO2﹣,故当固体电解质中有1mol O2﹣通过时,电子转移2mol,故D 错误;故选C.【点评】本题考查了新型化学电池,是对于原电池原理的应用,主要理解电池电解质不是在水溶液中的氧化还原反应,电解质是固体,O2﹣可以在其中自由移动,是本题的关键.4. 将一定量的固体Ag2SO4置于容积不变的密闭容器中(装有少量V2O5),某温度下发生反应:Ag2SO4(s) Ag2O(s)+SO3(g),2 SO3(g) 2 SO2(g)+ O2(g),反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是()A.这10 min内氧气的平均反应速率为0.005 mol·mol-1·min-1B.SO3的分解率为20%C.容器里气体的密度为40g/LD.硫酸银与三氧化硫的化学反应速率相同参考答案:D略5. 下图是一种有机物的比例模型,该模型代表的有机物可能是()A.饱和一元醇 B.羟基酸 C.羧酸酯 D.饱和一元醛参考答案:B略6. 1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。
2021下半年教师资格考试《高中化学学科》真题及答案

2021下半年教师资格考试《高中化学学科》真题及答案2021年教师资格考试结束啦,在这里提前预祝考生们都能取得好成绩!2021下半年教师资格考试《高中化学学科》真题及答案一、单项选择题(20)1、……偶极矩阵为零的是 (3分)正确答案:题目空缺2、……表示阿伏伽德罗常数的值,下列叙述正确的是 (3分)正确答案:题目空缺3、……下列各组离子在指定溶液中一定能大量共存的是 (3分)正确答案:题目空缺4、……各组物质可按“甲→(O2)乙→(O2)丙→(H2O)丁”实现转化的组合是(3分)正确答案:B.①③④5、……盐酸克伦特罗能够发生的反应有 (3分)正确答案:D.全部可以6、……a的M电子层有1个电子,b,c的最外层电子数都为电子层数的两倍,c的最高化合价为最低化合价绝对值的3倍。
下列说法错误的是 (3分) 正确答案:D.b、c分别与氢形成的化合物均为极性共价化合物7、……反应前CO物质的量为1mol,平衡时CO物质的量为0.8mol。
下列说法正确的是 (3分)正确答案:B.8、……下列说法正确的是 (3分)正确答案:D.生成物释放的总能量大于反应物吸收的总能量时,该反应的△H<09、……溶液反应放出气体的有机物有(含立体异构) (3分)正确答案:C.4种10、……开始时,插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,至略高于U形管中的液面。
下列有关解释合理的是 (3分) 正确答案:A.导管内液面回升时,正极反应式为:11、……让学生“跳一跳才能摘到桃子”。
这种教学设计主要遵循的是 (3分)正确答案:A.最近发展区理论12、……当前化学课程倡导的主要学习方式是 (3分)正确答案:C.①③④13、……下列属于认知性学习目标的行为动词是 (3分)正确答案:D.解释、判断14、……倡导开展STS教育,STS是指 (3分)正确答案:A.科学、技术、社会15、……下列关于教育角色的说法不正确的是 (3分)正确答案:B.教师是学生学习的控制者16、……下列可作为化学课程资源的是①学生②博物馆③企业④实验室⑤科研人员⑥信息化媒体 (3分)正确答案:D.全部17、……硫酸铁溶液与铁粉反应,生成硫酸亚铁。
2024学年四川省眉山市高二化学第一学期期末考试试题含解析

2024学年四川省眉山市高二化学第一学期期末考试试题注意事项1.考试结束后,请将本试卷和答题卡一并交回.2.答题前,请务必将自己的姓名、准考证号用0.5毫米黑色墨水的签字笔填写在试卷及答题卡的规定位置.3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符.4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮擦干净后,再选涂其他答案.作答非选择题,必须用05毫米黑色墨水的签字笔在答题卡上的指定位置作答,在其他位置作答一律无效.5.如需作图,须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗.一、选择题(每题只有一个选项符合题意)1、某同学组装了如图所示的电化学装置电极I为Al,其他电极均为Cu,则A.电流方向:电极IV→→电极IB.电极I发生还原反应C.电极II逐渐溶解D.电极III的电极反应:Cu2++2e-==Cu2、有下列几种反应类型:①消去②取代③氧化④加成⑤还原⑥水解,用丙醛制取1,2﹣丙二醇(),按正确的合成路线依次发生的反应所属类型不可能是()A.⑤①④⑥B.⑤③⑥①C.⑤①④②D.④①④②3、化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大B.根据结构和组成相似的物质,沸点随相对分子质量增大而升高,推出NH3的沸点低于PH3C.根据价电子构型与化合价的关系,推出最外层电子数3个的元素一定是第ⅢA族元素D.根据反应物浓度越大反应速率越快,推出常温下相同的铝片中分别加入足量的浓硝酸和稀硝酸中,浓硝酸中铝片先溶解完4、通过强烈的相互作用形成金属键的微粒是A.阴阳离子 B.原子 C.分子 D.金属阳离子和自由电子5、用已知浓度的NaOH滴定未知浓度的盐酸,下列操作(其他操作正确)会造成测定结果偏高的是A.滴定终点读数时俯视度数B.酸式滴定管使用前,水洗后未用待测盐酸润洗C.锥形瓶洗净后未干燥D.碱式滴定管滴定前尖嘴部分有气泡,滴定后气泡消失6、在日本,金刚烷胺一直作为帕金森病的治疗药,并于1998年被批准用于流感病毒A型感染性疾病的治疗,金刚烷胺的合成路线如图所示。
四川省眉山市2021-2022高二化学上学期期末考试试题 理(含解析).doc

四川省眉山市2021-2022高二化学上学期期末考试试题理(含解析)1.化学与生产生活密切相关,下列说法不正确的是①盐碱地(含较多Na2CO3等)不利于作物生长,可施加石膏降低土壤的碱性②泡沫灭火器的化学原料为Na2CO3和Al2(SO4)3③锅炉水垢中的CaSO4常用Na2CO3溶液和酸除去④含氟牙膏不能减少龋齿,使人们的牙齿更健康⑤NaFe(SO4)2·H2O、KAl(SO4)2·12H2O均可作絮凝剂去除工业和生活废水中的悬浮物⑥在钢闸门上装锌块可以避免钢闸门遭受腐蚀A. ②④B. ①②⑥C. ①③D. ③④⑤【答案】A【解析】【详解】①石膏的成分为CaSO4∙2H2O,它能与Na2CO3反应,转化为难溶的CaCO3,从而降低土壤的碱性,①正确;②泡沫灭火器的化学原料为NaHCO3和Al2(SO4)3,②不正确;③锅炉水垢中的CaSO4与饱和Na2CO3溶液反应,可转化为CaCO3,再用酸溶解即可除去,③正确;④适当浓度的氟离子进入口腔后,与牙釉质的主要成分发生反应,生成坚固的氟磷灰石,因此含氟牙膏能减少龋齿,使人们的牙齿更健康,④不正确;⑤NaFe(SO4)2·H2O、KAl(SO4)2·12H2O均可作絮凝剂,它们的水解产物Fe(OH)3胶体、Al(OH)3胶体能吸附工业和生活废水中的悬浮物并使之沉降,⑤正确;⑥在钢闸门上装锌块,构成原电池,锌失电子,阻止钢闸门中的Fe失电子,从而保护钢闸门免遭腐蚀,⑥正确。
综合以上分析,②④不正确。
答案为:A。
2.已知N A是阿伏加德罗常数的值,下列说法正确的是A. 1 L 0.1 mol·L−1氯化铵溶液含有的NH4+数目为0.1N AB. 在密闭容器中充入3 mol H2与1 mol N2,充分反应后转移电子的数目为6N AC. 0.5 N A个CH4完全燃烧生成H2O和CO2,放出445.2KJ热量,则CH4的燃烧热为-445.2KJ/molD. 常温下,2L pH=2的硫酸溶液中含有的H+数目为0.02 N A【答案】D【解析】【详解】A.在水溶液中,NH 4+会发生水解,所以 1 L 0.1 mol·L −1氯化铵溶液含有的NH 4+数目小于0.1N A ,A 错误;B. 合成氨反应为可逆反应,在密闭容器中充入3 mol H 2与1 mol N 2,充分反应后转移电子的数目小于6N A ,B 错误;C. 0.5 N A 个CH 4(物质的量为0.5mol )完全燃烧,放出445.2kJ 热量,则1molCH 4完全燃烧放热不可能为445.2kJ ,且没有说明生成的水的存在状态,不能确定燃烧热的大小,C 错误;D. 常温下,pH=2的硫酸溶液中c (H +)=0.01mol/L ,2L 溶液中含有的H +数目为0.02 N A ,D 正确。
2021年教师资格《高中化学》真题及答案解析
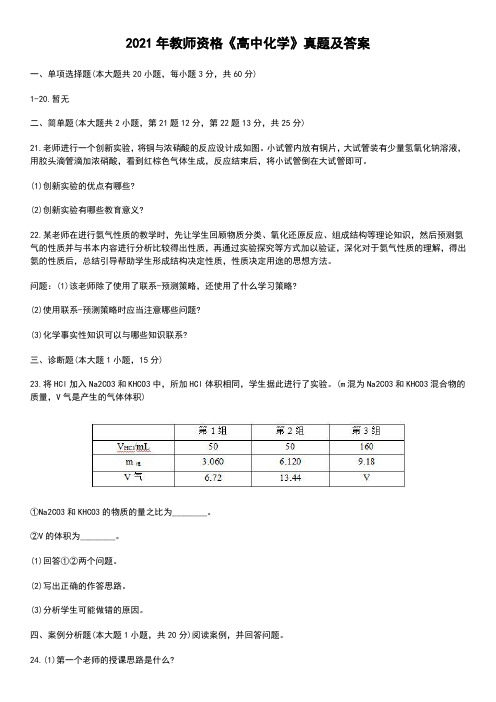
2021年教师资格《高中化学》真题及答案一、单项选择题(本大题共20小题,每小题3分,共60分)1-20.暂无二、简单题(本大题共2小题,第21题12分,第22题13分,共25分)21.老师进行一个创新实验,将铜与浓硝酸的反应设计成如图。
小试管内放有铜片,大试管装有少量氢氧化钠溶液,用胶头滴管滴加浓硝酸,看到红棕色气体生成,反应结束后,将小试管倒在大试管即可。
(1)创新实验的优点有哪些?(2)创新实验有哪些教育意义?22.某老师在进行氨气性质的教学时,先让学生回顾物质分类、氧化还原反应、组成结构等理论知识,然后预测氨气的性质并与书本内容进行分析比较得出性质,再通过实验探究等方式加以验证,深化对于氨气性质的理解,得出氨的性质后,总结引导帮助学生形成结构决定性质,性质决定用途的思想方法。
问题:(1)该老师除了使用了联系-预测策略,还使用了什么学习策略?(2)使用联系-预测策略时应当注意哪些问题?(3)化学事实性知识可以与哪些知识联系?三、诊断题(本大题1小题,15分)23.将HCl加入Na2CO3和KHCO3中,所加HCl体积相同,学生据此进行了实验。
(m混为Na2CO3和KHCO3混合物的质量,V气是产生的气体体积)①Na2CO3和KHCO3的物质的量之比为________。
②V的体积为________。
(1)回答①②两个问题。
(2)写出正确的作答思路。
(3)分析学生可能做错的原因。
四、案例分析题(本大题1小题,共20分)阅读案例,并回答问题。
24.(1)第一个老师的授课思路是什么?(2)第二个是采用到的教学策略是什么?(3)第三个是案例当中老师授课的优点是什么?五、教学计题(本大题1小题,共30分)25.根据下列材料回答问题。
(1)实验2-1的实验现象?(2)针对“二、离子反应及其发生的条件”从教学目标,教学方法,教学过程加以设计(不少于300字)。
参考答案一、单项选择题1.【答案】C。
乙醇使蛋白质变性,可以消毒。
高中化学招聘试题及答案

高中化学招聘试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于纯净物的是()A. 空气B. 蒸馏水C. 矿泉水D. 食盐水2. 根据质量守恒定律,化学反应前后()A. 元素种类不变B. 原子种类不变C. 原子数目不变D. 所有选项都正确3. 金属活动性顺序中,位于氢前面的金属能()A. 与酸反应生成氢气B. 与碱反应生成氢气C. 与盐反应生成氢气D. 不能与酸反应4. 以下化合物中,属于共价化合物的是()A. NaClB. CaOC. HClD. FeS5. 氧化还原反应中,得电子的物质是()A. 氧化剂B. 还原剂C. 催化剂D. 反应物6. 根据酸碱中和反应的原理,下列物质中属于酸的是()A. NaOHB. HClC. KOHD. NH3·H2O7. 原子结构中,决定元素化学性质的主要是()A. 质子数B. 中子数C. 电子层数D. 最外层电子数8. 以下物质中,属于非电解质的是()A. HClB. NaClC. H2OD. SO29. 根据化学平衡移动原理,当增大反应物浓度时,平衡会向()A. 正反应方向移动B. 逆反应方向移动C. 不移动D. 无法确定10. 以下物质中,属于强碱的是()A. NaOHB. NH3·H2OC. Ca(OH)2D. Mg(OH)2二、填空题(每空2分,共20分)1. 根据元素周期表,第IA族元素的原子最外层电子数是______。
2. 化学反应中,如果反应物的量不同,可能会导致产物的组成发生变化,这种现象称为______。
3. 根据化学键理论,离子键是由______作用形成的。
4. 金属铝与稀盐酸反应生成氢气和氯化铝,该反应的化学方程式为______。
5. 根据酸碱质子理论,能够接受质子的物质是______。
三、简答题(每题10分,共20分)1. 请简述什么是氧化还原反应,并举例说明。
2. 请解释什么是化学平衡,并说明影响化学平衡的因素。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、单选题(本题共15小题,试题中有且仅有一个选项符合题目要求。
)1.下列关于氮的固定的说法错误的是()
A.氮的固定包括人工固氮和自然固氮
B.工业合成氨属于人工固氮
C.自然固氮中氮元素被氧化
D.氮的固定中参与元素至少有两种
2.对化工生产认识正确的是()
A.海水提溴:一般需要经过浓缩、氧化、提取三个步骤
B.合成氯化氢:通入H
2的量略大于Cl
2
,可以使平衡正移
C.合成氨:采用500℃的高温,有利于增大反应正向进行的程度
D.侯德榜制碱法:析出NaHCO
3的母液中加入消石灰,可以循环利用NH
3
3.复合材料的使用使导弹的射程有了很大的提高,其主要原因在于( )
A.复合材料的使用可以使导弹能承受超高温的变化
B.复合材料的使用可以使导弹的质量减轻
C.复合材料的使用可以使导弹能承受超高强度的变化
D.复合材料的使用可以使导弹能承受温度的剧烈变化
4.下列说法正确的是()
A.将CO
2气体通入CaCl
2
溶液中,有白色沉淀生成
B.pH试纸如果事先用水润湿,不一定会对测定结果造成偏差
C.淀粉遇碘变蓝,所以可用加碘的食盐来检测马铃薯中是否含有淀粉
D.钙、铁、锌、碘元素都是人体必需的微量元素
5.化学与能源开发、环境保护、资源利用等密切相关。
下列说法正确的是()
A.无论是风力发电还是潮汐发电,都是将化学能转化为电能
B.乙醇和汽油都是可再生能源,应大力推广使用“乙醇汽油”
C.推广燃煤脱硫技术,可以防治SO
2
污染
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
6.综合利用海水可以为人类提供丰富的化学资源,下述说法不正确的是()
A.可以从海水中制取Br
2
B.可以从海水中制取金属Mg
C.可以从海水中直接提取NaCl
D.可以从海水中直接提取金属Na
7.“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。
某种兴奋剂的结构简式如右图所示,有关该物质的说法正确的是()
A.遇FeCl
3
溶液显紫色,因为该物质与苯酚属于同系物
B.该物质可以分别发生取代、氧化、消去、加聚、还原反应
C.1mol该物质浓溴水和H
2反应最多消耗Br
2
和H
2
分别为4mol、7mol
D.1mol该物质分别与NaOH和Na
2CO
3
反应最多消耗NaOH和Na
2
CO
3
分别为3mol、1.5mol
8.某单烯烃与H
2
加成后的产物是,则该烯烃的结构式可能有()
A.1种
B.2种
C.3种
D.4种
9.温度为T℃时,向2.0L恒容密闭容器中充入1.0molPCl
5,反应PCl
5
(g)⇌PCl
3
(g)+Cl
2
(g)经
一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是()
t/s 0 50 150 250 350
n(PCl
3
)/mol 0 0.16 0.19 0.20 0.20
A.反应在前50s的平均速率为v(PCl
3
)=0.0032mol•L﹣1•s﹣1
B.保持其他条件不变,升高温度,平衡时,c(PCl
3
)=0.11mol•L﹣1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl
5、0.20molPCl
3
和0.20molCl
2
,达到平衡前v(正)
>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl
5、2.0molCl
2
,达到平衡时,PCl
5
的转化率大于20%
10.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是()
A.过量新制的氯水滴到蓝色的石蕊试纸上,试纸先变红,说明氯水中含有H+
B.向氯水中滴加硝酸酸化的AgNO
3
溶液,产生白色沉淀,说明氯水中含有Cl﹣
C.向氯水中加入NaHCO
3
粉末,有气泡产生,说明氯水中含有H+
D.氯水能使有色花瓣褪色,说明氯水中含有Cl
2
11.下列有关碳和碳的化合物的说法中,错误的是()
A.金刚石和石墨物理性质不同,是因为它们的碳原子排列方式不同
B.一氧化碳、二氧化碳、葡萄糖都属于有机物
C.木炭、一氧化碳在一定条件下都能与氧化铜反应
D.大气中二氧化碳的消耗途径主要是绿色植物的光合作用
12.合金是一类用途广泛的金属材料.下列物质属于合金的是()
A.钢
B.铜
C.金刚石
D.四氧化三铁
13.设N
A
为阿伏加德罗常数的值,下列有关说法正确的是()
A.标准状况下,6.72LNO
2与水反应转移的电子数为0.1N
A
B.1molNa
2O和Na
2
O
2
混合物中含有的阴、阳离子总数是3N
A
C.1molCl
2与足量Fe反应转移电子数一定为3N
A
D.1L0.1mol/L的碳酸钠溶液中的阴离子总数等于0.1N
A
14.某溶液中含Fe3+、Cl-、Na+、SO
42-,其离子个数比为Fe3+∶Cl-∶Na+∶SO
4
2-=1∶2∶x∶2,则x的值
是()
A.1
B.2
C.3
D.4
15.下列说法正确的是()
A.食盐溶液静置会分层,上层比下层咸
B.“冰水混合物”是一种分散系
C.黄河入海口处三角洲的形成与胶体性质有关
D.电泳现象说明胶体带电
二、实验探究题
16.1942年,我国化工专家侯德榜以NaCl、NH
3、CO
2
等为原料制得纯碱,他的“侯氏制碱法”为世
界制碱工业做出了突出贡献。
回答下列问题:。
