设备变更申请表样
设备变更停止更改申请表

意见:签字: 年 月 日
审核五:需求部门主管副总(低风险批准,中、高风险审核)
意见:签字: 年 月 日
审核六:设备部经理(中风险审批、高风险审核)
意见:签字: 年 月 日
审核七:安全副总(高风险审核)
意见:签字: 年 月 日
审核八:设备副总(高风险批准)
意见:签字: 年 月 日
注:本表审批完成后,由申请部门留存,变更信息抄送设备部备案。
□控制方案更改,低、中、高风险审核,如无则由部门经理代)
意见:签字: 年 月 日
审核二:需求部门EHS(低、中、高风险审核,如无则由部门经理代)
意见:签字: 年 月 日
审核三:需求部门制造经理(低、中、高风险审核,如无则由部门经理代)
意见:签字: 年 月 日
设备变更停止/更改申请表
文件编号:QB/QCHX-GL-J-13-03保存期3年
变更停止/更改申请部门
变更编号
停止/更改发起日期
变更级别
□高□中□低
变更类型
□一般变更□重要变更□永久变更□紧急变更
□临时变更(时间: 年月 日-- 年月 日)
停止/更改原因
□停止 □更改原因:
控制方案
□申请终止变更,并恢复原状
变更申请表
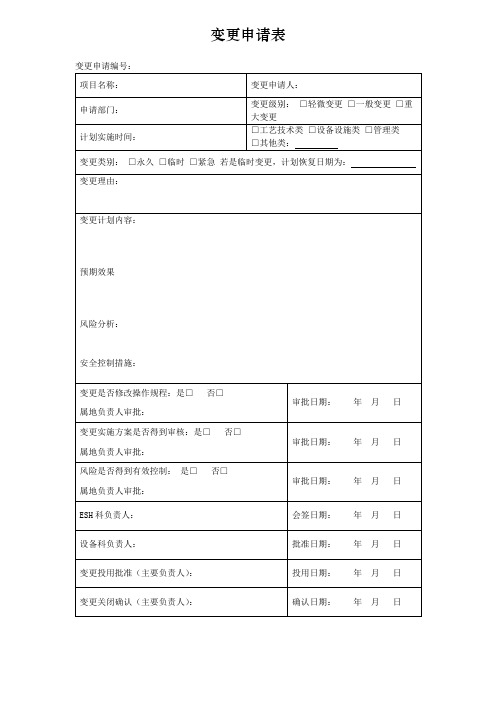
审批日期:年月日
变更实施方案是否得到审核:是□ 否□
属地负责人审批:
审批日期:年月日
风险是否得到有效控制:是□ 否□
属地负责人审批:
审批日期:年月日
ESH科负责人:
会签日期:年月日
设备科负责人:
批准日期:年月日
变更投用批准(主要负责人):
投用日期:年月日
变更关闭确认(主要负责人):
确认日期:年月日
变更申请编号:
项目名称:
变更申请人:
申请部门:
变更级别: □轻微变更 □技术类 □设备设施类 □管理类
□其他类:
变更类别: □永久 □临时 □紧急 若是临时变更,计划恢复日期为:
变更理由:
变更计划内容:
预期效果
风险分析:
安全控制措施:
变更是否修改操作规程:是□ 否□
工艺和设备变更申请审批表

变更的技术依据(预期改善的性质、实施变更的安全性、评审支持性的实验或工艺数据)
工艺设备变更详细说明(包括操作程序、试验日志、关键的工艺变量值等)
审查结论:
审查成员签字、日期 变更申请人: 技术专家: 安全环保专家: 技术负责人: 变更批准人: 注:以上内容由审查组和批准人填写
日期: 日期:
或工Байду номын сангаас数据)
工艺和设备变更申请审批表设计变更审批表员工职务变更审批表工艺变更申请单减免税申请审批表入户申请审批表工艺变更申请表退税申请审批表申请再生育审批表深圳入户申请审批表
工艺和设备变更申请审批表
编号: 装置 申请人 变更主题: 变更原因及目的: 变更内容: 申请日期 变更起止日期
是否需要工艺危害分析? 是(若是,请附上分析结果) 不是(请注明原因) 潜在的影响及控制措施 安全与健康 环境影响 产品效率 产能产量 质量 成本效益 其他影响 注:以上内容由工艺设备变更申请人填写。 未获得授权延期之前不得在变更截止日期后继续实施变更方案 变更带来的问题陈述:
特种设备使用状态变更申请表

以上第至号共台设备申请变更使用状态。(此表不够填写,可另附页)
安全责任声明:以上设备状态变更情况属实。在设备停用期间,我单位将严格执行设备停用管理制度,不擅自启用,对停用期间的设备安全负完全责任;在停用期满前,需重新启用的,我单位将按规定申请定期检验,经检验合格,具备使用条件后方才启用。
单位负责人(签字):年月日
填写说明:1、在用特种设备报停、报废、拆除、移装过户或改为常压,使用单位应当填写本表,在状态变更30日内向注册登记机关申请办理状态变更手续。2、本表一式四份,使用单位管理,检验机构,注册机构及当地监察机构各存一份。
特种设备使用状态变更申请表
申请单位(章)
申请ห้องสมุดไป่ตู้期
管理部门
工程部
联系人
联系电话/传真
电子邮箱
联系地址
邮编
变更状态类型
□报停□过户■启用
□注销□拆除
状态变更原因
使用状态变更设备清单
序号
设备类别
设备名称/型号
使用证编号或注册代码
出厂编号
变更前状态
变更后状态
变更日期
1
住宅电梯
在用
在用
2
住宅电梯
3
住宅电梯
4
5
变更申请及验收表

变更申请及验收表
XXX
变更申请表
变更名称
申请部门申请人
变更时间变更原因
变更原因、内容及技术依据(可附表):
变更风险分析情况(设备设施本质安全、工艺流程、安全管理):
风险分析人:年月日安全控制措施:
申请部门负责人意见:
申请部门负责人签字:年月日技术负责人意见:
技术负责人签字:年月日设备部意见:
设备部签字:年月日生产部意见:
生产部签字:年月日安全部意见:
安全部签字:年月日公司领导意见:
公司领导签字:年月日
XXX
变更验收表
验收变更的项目
组织验收部门
验收组人员
验收人(签字)
验收意见:
验收负责人签字:年月日主管领导审查意见:具名:年月日
需要沟通的部门(变更结果)
单元或部分具名单元或部分具名
变更所在部分
日期
所属部门
设备部
生产部
电仪。
变更申请变更确认表格式

风险评价情况:
预防/控制措施:
申请部门负责人意日期
公司分管领导意见:
签字、日期
变更的确认
组织确认部门
组织人
确认日期
与变更有关的措施实施情况确认意见或建议:
确认结论:
参加确认人员(签字):
说明:①此表由申请人填写;②部门、车间负责人批准后即可实施;③如果涉及到生产安全、产品质量风险、产品安全风险的变更,需经评估审核批准后才可实施;④此表最终应交生产部。⑤实际填写可根据内容加大行距或另附页。
变更申请/确认表
变更名称
变更类型
1.□新建、改建、扩建项目引起的技术变更;
2.产品有关的变更:□原料介质变更;□工艺流程及操作条件的重大变更;□工艺设备的改进和变更;□操作规程的变更;□工艺参数的变更;□公用工程的水、电、气、风的变更等。
3.设备设施的变更:□设备设施的更新改造;□安全设施的变更;□更换与原设备不同的设备或配件;□临时的电气设备等。
4.管理变更,主要包括:□法律法规、标准及其他要求的变更或更新;□人员的变更;□管理机构的较大变更;□管理职责的变更;
涉及产品
涉及车间
申请部门
申请人
申请日期
变更的提出
变更描述(至少包括:1.描述现行的操作流程和状态;2.描述变更的原因,应具体、清楚、完整;3.简述变更实施计划或方案、实施的过程变更希望达到的效果;4.变更可能带来的生产安全风险、产品质量风险、产品安全风险预测及拟采取控制措施。):
设备设施变更申请表

设备设施变更申请表
设备设施变更申请表
变更风险分析情况:(1通过经验判断、技术诊断或其他方法调查确定危险源
即危险因素存在于那个子系统中,对所需分析系统的生产目的、物料、装置及设备、工艺过程、操作条件以及周围环境等进行充分详细的调查了解;
2根据过去的经验教训及同类行业生产中发生的事故,或灾害情况,对系统的影响、损坏程度类比判断所要分析的系统中可能出现的情况,查找能够造成系统故障、物质损失和人员伤害的危险性,分析事故或灾害的可能类型;3对确定的危险源分类,制成预先危险性分析表;4识别转化条件,即研究危险因素转变成危险状态的触发条件和危险状态转变为事故或灾害的必要条件,并进一步寻求对策措施、检验对策措施的有效性;5进行危险性分级排列出重点和轻、重、缓、急次序以便处理; 6制定事故或灾害的预防性对策措施。
)
变更风险控制措施:(重要风险控制措施应包含防护用品佩戴情况、相关安全操作规程、制度执行情况、劳动纪律情况等)示例:1、对所有检修用的器械、工具进行检查,保证符合安全要求; 2、采取可靠的断电措施,切断需检修设备的电器电源; 3、检修使用的气防器材、消防器材、通讯照明设备等保证完好可靠;
4、检修现场用的爬梯、平台、盖板保证安全可靠;
5、对检修用的盲板进行逐个检查记录落实责任人;
6、移动式电器工具安装漏电保护器;
7、检修现场安装淋洗器配备冲洗用水;
8、处理检修现场设置围栏及警示标志;
9、清理现场易燃物品、障碍物及废弃物等; 10、保持检修现场消防通道、行车通道
畅通无阻; 12、作业人员穿戴好防护用品; 13、严格遵守劳动纪律,严禁在车间内吸烟、打电话等不安全行为;14、编制相关应急预案。
)。
医疗器械变更申请表

受理编号:第号《医疗器械经营企业许可证》变更申请表企业名称(盖章)企业法定代表人(负责人)联系人联系电话申请日期年月日受理单位:新疆维吾尔自治区食品药品监督管理局(收到申请日期)新疆维吾尔自治区食品药品监督管理局制填表说明一、申请企业应按照要求填表,内容应准确、完整,并使用钢笔(碳素笔)填写,不得涂改。
二、涉及变更企业名称、企业法定代表人、企业负责人、质量管理人(即质量管理机构负责人或者专职质量管理人员)等事项的,须填写表1相关栏目、表2和申报材料真实性的自我保证声明;涉及变更注册地址、仓库地址和经营范围等事项的,须填写本表全部相关栏目。
三、其他申报资料或证明文件,随本表一并报送(详见“实施《医疗器械经营企业许可证管理办法》规定”)。
四、填表注意事项:(一)个人简历应包括下列基本内容:姓名、性别、族别、出生年月、所学专业、学历、职称、主要工作经历(包括自参加工作以来至现在的工作经历,按照自何年何月至何年何月在何单位任何职的方式详细填写)、受教育情况(指接受大中专教育、有关法律法规及相关专业技术培训等);企业内质量管理人员的学历或者职称是否与所经营产品的要求相适应。
(二)任职文件应规范、统一编号,应明确被任命人员的姓名、职务、归属部门、任命时间等。
(三)存储条件的说明应包括仓库是否符合所经营医疗器械储存条件的要求,仓库是否按照《医疗器械经营企业现场检查验收细则》设置和配备了有关设施设备等。
(四)拟增加产品相应存储条件的说明应对产品储存的温湿度要求、通风、防尘、防潮、防鼠、防霉变等要求作出说明。
(五)企业申请日期应填写向食品药品监督管理部门报送的日期。
(六)本表所列各项内容填写不下时可另附页。
(七)按照要求无需填写相关内容的栏目,在该栏目中标注“/”或者“无”字样,申请表不得空项。
(八)本表及所附证明文件均应加盖企业公章,复印件还应标注“与原件相符”。
(九)申请书及其他申报资料,应统一使用A4纸,标明目录、页码并按顺序装订成册。
