化学方程式汇总(46个)
化学方程式汇总(46个)
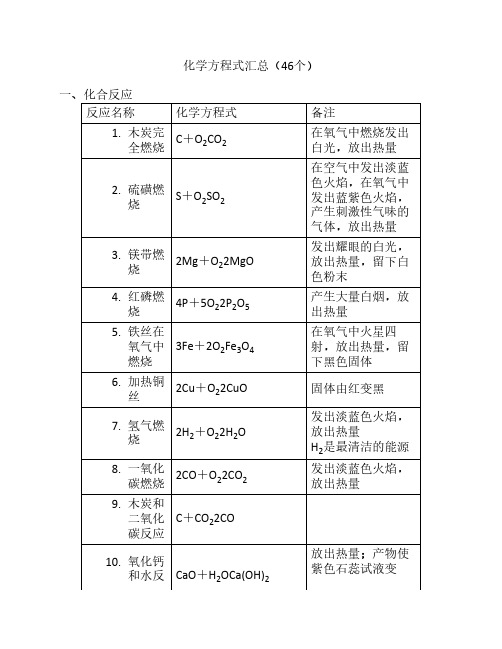
化学方程式汇总(46个)一、化合反应反应名称化学方程式备注1. 木炭完全燃烧C+O2CO2在氧气中燃烧发出白光,放出热量2. 硫磺燃烧S+O2SO2在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,产生刺激性气味的气体,放出热量3. 镁带燃烧2Mg+O22MgO发出耀眼的白光,放出热量,留下白色粉末4. 红磷燃烧4P+5O22P2O5产生大量白烟,放出热量5. 铁丝在氧气中燃烧3Fe+2O2Fe3O4在氧气中火星四射,放出热量,留下黑色固体6. 加热铜丝2Cu+O22CuO固体由红变黑7. 氢气燃烧2H2+O22H2O发出淡蓝色火焰,放出热量H2是最清洁的能源8. 一氧化碳燃烧2CO+O22CO2发出淡蓝色火焰,放出热量9. 木炭和二氧化碳反应C+CO22CO10. 氧化钙和水反CaO+H2OCa(OH)2放出热量;产物使紫色石蕊试液变应蓝,使无色酚酞试液变红11. 二氧化碳和水反应CO2+H2OH2CO3产物使紫色石蕊试液变红12. 硫酸铜粉末和水反应CuSO4+5H2OCuSO4·5H2O白色粉末变成蓝色晶体,放出热量CuSO4粉末用于检验物质是否含有水二、分解反应反应名称化学方程式备注13. 碳酸受热分解H2CO3H2O+CO2↑H2CO3不稳定14. 电解水2H2O2H2↑+O2↑正负极都产生气泡,负极产生的气体体积是正极产生气体的2倍负氢正氧,氢二氧一;工业上生产H215. 高温煅烧大理石或石灰石CaCO3CaO+CO2↑工业上生产CaO16. 过氧化氢在二氧化锰的催化作用下分解2H2O22H2O+O2↑产生大量气泡,放出热量实验室制取O217. 加热氯酸钾和二氧化锰的混合物2KClO32KCl+3O2↑实验室制取O218. 加热硫酸铜晶体CuSO4·5H2OCuSO4+5H2O蓝色晶体变成白色粉末,试管口产生无色液体三、置换反应反应名称化学方程式备注19. 木炭还原氧化铜C+2CuO2Cu+CO2↑产生红色固体20. 氢气还原氧化铜H2+CuOCu+H2O产生红色固体,试管口产生无色液体H2有还原性,用于冶炼金属21. 镁带在二氧化碳中燃烧2Mg+CO22MgO+C产生黑色和白色固体22. 锌粒和稀盐酸反应Zn+2HClZnCl2+H2↑实验室制取H223. 锌粒和稀硫酸反应Zn+H2SO4ZnSO4+H2↑实验室制取H224. 铁钉和稀盐酸反应Fe+2HClFeCl2+H2↑Fe元素从0价变成+2价25. 铁钉和稀硫酸Fe+H2SO4FeSO4+H2↑26. 铁丝和硫酸铜溶液反应Fe+CuSO4FeSO4+Cu铁丝表面产生红色固体27. 铜丝和硝酸银溶液反应Cu+2AgNO3Cu(NO3)2+2Ag铜丝表面产生银白色固体四、复分解反应反应名称化学方程式备注28. 氢氧化镁治疗胃“泛酸”Mg(OH)2+2HClMgCl2+2H2O29. 大理石或石灰石和稀盐酸反应CaCO3+2HClCaCl2+H2O+CO2↑实验室制取CO230. 硝酸银溶液和稀盐酸反应AgNO3+HClAgCl↓+HNO3产生白色沉淀31. 氯化钡溶液和稀硫酸反应BaCl2+H2SO4BaSO4↓+2HCl产生白色沉淀32. 硫酸铜溶液和氢氧化钠溶液反应CuSO4+2NaOHCu(OH)2↓+Na2SO4产生蓝色沉淀33. 氯化铁溶液和氢氧化钠溶液FeCl3+3NaOHFe(OH)3↓+3NaCl产生红褐色沉淀34. 碳酸钠溶液和石灰水反应Na2CO3+Ca(OH)2CaCO3↓+2NaOH35. 硫酸铜溶液和熟石灰制取农药波尔多液CuSO4+Ca(OH)2Cu(OH)2↓+CaSO436. 碳酸钠溶液和足量盐酸反应Na2CO3+2HCl2NaCl+H2O+CO2↑37. 氯化钠溶液和硝酸银溶液反应NaCl+AgNO3AgCl↓+NaNO3AgCl不溶于HNO338. 硫酸钠溶液和氯化钡溶液反应Na2SO4+BaCl2BaSO4↓+2NaClBaSO4不溶于HNO3五、其他反应反应名称化学方程式备注39. 甲烷燃烧CH4+2O2CO2+2H2O产生淡蓝色火焰40. 少量二氧化碳通入石灰水CO2+Ca(OH)2CaCO3↓+H2O产生白色沉淀;石灰水在空气中变质;石灰水用于检验CO241. 少量二氧NaOH在空气中变化碳和氢氧化钠溶液反应CO2+2NaOHNa2CO3+H2O质;NaOH溶液用于吸收CO242. 氢氧化钠溶液吸收二氧化硫SO2+2NaOHNa2SO3+H2ONa2SO3名称是亚硫酸钠43. 一氧化碳还原氧化铜CO+CuOCu+CO2产生红色固体尾气需要燃烧处理,防止CO污染空气44. 一氧化碳还原氧化铁3CO+Fe2O32Fe+3CO2工业炼铁的主要反应45. 盐酸除铁锈Fe2O3+6HCl2FeCl3+3H2O溶液变成棕黄色46. 硫酸溶解氧化铜固体CuO+H2SO4CuSO4+H2O溶液变成蓝色*固体小颗粒分散到气体中形成烟;小液滴分散到气体中形成雾。
有机化学方程式汇总(详)

39. 乙醇脱水(分子内、分子间) CH3CH2OH
CH2=CH2 ↑+H2O(消去反应)
2CH3CH2OH 浓 H2SO4 CH3CH2—O—CH2CH3+ H2O (取代反应)
140℃
40. 苯酚的电离方程式
电离 OH
O- + H+
41. 苯酚与 NaOH 溶液反应
OH + NaOH
ONa + H2O
4. 甲烷的热分解 CH4 高温 C+2H2
5. 烷烃的热分解 C4H10 △ C2H4+C2H6 C4H10 △ CH4 + C3H6
6. 乙烯实验室制法 CH3CH2OH
H2O + CH2=CH2 ↑
(浓硫酸:催化剂,脱水剂)
7. 乙烯的燃烧
点燃
CH2=CH2 + 3O2
2CO2 + 2H2O
8. 乙烯通入溴水中 CH2=CH2 + Br2
19. 乙炔通入溴水中 HC CH + Br Br
HCCH Br Br
1, 2 - 二溴乙烷
HCCH + Br Br
Br Br
Br Br HCCH
Br Br
1, 1 , 2 , 2 - 四溴乙烷
20. 乙炔与氢气的加成反应
催化剂 HC CH+ H2 △ H2C CH2
21. 乙炔水化制备乙醛
O
催化剂
NO2 2,4,6-三硝基甲苯
(TNT)
32. 甲苯和氢气的加成反应
CH3
CH3
Ni + 3 H2 △
33. 溴乙烷水解 CH3CH2Br + NaOH H2O,△ 4. 溴乙烷消去反应 CH3CH2Br +NaOH 醇 CH2=CH2↑ + NaBr + H2O
化学方程式部分汇总

化学方程式1.碳与氧气(不足)的反应2C+O2==== 2CO碳与氧气(充足)的反应C+O2==== CO22.一氧化碳与氧气的反应2CO+O2==== 2CO23.二氧化碳与碳的反应CO2+C==== 2CO4.碳酸氢钠与盐酸的反应NaHCO3+HCl==== NaCl+H2O+CO2↑5.碳酸钠与盐酸的反应Na2CO3+ 2HCl==== 2NaCl+ H2O+ CO2↑6.碳酸钙与盐酸的反应CaCO3+2HCl==== CaCl2+ H2O+ CO2↑7.碳酸氢钠与氢氧化钠的反应NaHCO3+NaOH==== Na2CO3 +H2O8.碳酸钠与氢氧化钙的反应Na2CO3+Ca(OH)2==== CaCO3↓+ 2NaOH9.碳酸氢钠(少量)与氢氧化钙的反应NaHCO3+ Ca(OH)2==== CaCO3↓+NaOH+ H2O 碳酸氢钠(过量)与氢氧化钙的反应2NaHCO3+ Ca(OH)2==== CaCO3↓+Na2CO3+2H2O10.碳酸氢钠加热的反应2NaHCO3==== Na2CO3+ H2O+CO2↑11.碳酸氢钙加热的反应Ca(HCO3)2==== CaCO3↓+H2O+CO2↑12.碳酸钙加热的反应CaCO3==== CaO+CO2↑13.二氧化碳(过量)通入氢氧化钙溶液中的反应Ca(OH)2+2CO2==== Ca(HCO3)2二氧化碳(少量)通入氢氧化钙溶液中的反应Ca(OH)2+CO2==== CaCO3↓+H2O14.氮气与氧气的反应N2+O2==== 2NO15.一氧化氮与氧气的反应2NO+O2==== 2NO216.二氧化氮与水的反应3NO2+ H2O==== 2HNO3+ NO17.氮气与氢气的反应N2+3H2========= 2NH318.氨气与水的反应NH3+H2O==== NH3?H2O19.氨气与盐酸的反应NH3+HCl==== NH4+Cl20.氨气与硫酸的反应2NH3+H2SO4==== (NH4+)2SO421.氨气与强酸的离子的反应NH3+H+ ==== NH4+22.氨的催化氧化的反应4NH3+5O2====== 4NO+6H2O23.碳酸氢铵加热的反应NH4+HCO3==== NH3↑+CO2↑+H2O24.氯化铵加热的反应NH4+Cl==== NH3↑+HCl↑25.碳酸铵加热的反应(NH4+)2CO3==== 2NH3↑+CO2↑+H2O26.氯化铵与氢氧化钙的反应2NH4+Cl+ Ca(OH)2==== CaCl2+2NH3↑+2H2O27.氯化铵与氢氧化钠的反应NH4+Cl+ NaOH==== NaCl+NH3↑+H2O28.碳酸氢铵与氢氧化钠的反应NH4+HCO3+2NaOH==== Na2CO3+NH3↑+2H2O29.碳酸氢铵与氢氧化钙的反应NH4+HCO3+Ca(OH)2==== CaCO3↓+NH3↑+2H2O30.硝酸的分解的反应4HNO3========= 4NO2↑+O2↑+2H2O31.铜与浓硝酸的反应Cu+4HNO3(浓)==== Cu(NO3)2+2NO2↑+2H2O32.铜与稀硝酸的反应3Cu+8HNO3(稀)==== 3Cu(NO3)2+2NO↑+4H2O33.铁与浓硝酸的反应Fe+6HNO3(浓)==== Fe(NO3)3+3NO2↑+3H2O34.铁与稀硝酸的反应Fe+4HNO3(稀)==== Fe(NO3)3+NO↑+2H2O35.碳与浓硝酸的反应C+4HNO3(浓)==== CO2↑+4NO2↑+2H2O36.一氧化氮与一氧化碳的反应2NO+2CO====== N2+2CO237.一氧化氮与氧气和水的反应4NO+3O2+2H2O==== 4HNO338.二氧化氮与氧气和水的反应4NO2+O2+2H2O==== 4HNO339.氢氧化钠吸收二氧化氮和一氧化氮的反应2NaOH+NO2+NO==== 2NaNO2+ H2O40.氨气(过量)与氯气的反应8NH3+3Cl2==== 6NH4+Cl+N2氨气(少量)与氯气的反应2NH3+3Cl2==== 6HCl+N241.二氧化氮生成四氧化二氮的反应2NO2==== N2O442.硫与铜的反应S+2Cu==== Cu2S43.硫与铁的反应S+Fe==== FeS44.硫与钠的反应S+2Na==== Na2S45.硫与铝的反应3S+2Al==== Al2S346.硫与汞的反应S+Hg==== HgS47.硫与氧气的反应S+O2==== SO248.硫与氢气的反应S+H2==== H2S49.硫与氢氧化钠的反应3S+6NaOH==== 2Na2S+Na2SO3+3H2O50.硫与浓硫酸的反应 S+2H2SO4(浓)==== 3SO2+2H2O51.黑火药点燃S+2KNO3+3C==== K2S+3CO2↑+N2↑52.二氧化硫(少量)与氢氧化钠的反应SO2+2NaOH==== Na2SO3+H2O二氧化硫(过量)与氢氧化钠的反应SO2+NaOH==== NaHSO353.二氧化硫与氢氧化钙的反应SO2+Ca(OH)2==== CaSO3↓+H2O54.二氧化硫与亚硫酸钙溶液的反应SO2+CaSO3+H2O ==== Ca(HSO3)255.二氧化硫与水的反应SO2+H2O==== H2SO356.二氧化硫与硫化氢的反应SO2+2H2S==== 3S↓+2H2O57.二氧化硫与氧气的反应2SO2+O2====== 2SO358.二氧化硫与过氧化钠的反应SO2+Na2O2==== Na2SO459.二氧化硫与氯水的反应SO2+ Cl2+2H2O==== H2SO4+2HCl60.三氧化硫与水的反应SO3+H2O==== H2SO461.亚硫酸与氧气的反应2H2SO3+O2==== 2H2SO462.亚硫酸钠与氧气的反应2Na2SO3+O2==== 2Na2SO463.浓硫酸与铜的反应 2H2SO4(浓)+Cu==== CuSO4+SO2↑+2H2O64.浓硫酸与碳的反应 2H2SO4(浓)+C==== CO2↑+2SO2↑+2H2O寿65.工业制备硫酸(初步) 4FeS2+11O2==== 8SO2+2Fe2O366.实验室制备硫酸(初步) Na2SO3+H2SO4(浓)==== Na2SO4+SO2↑+H2O67.硫化氢(少量)与氢氧化钠的反应H2S+2NaOH==== Na2S+2H2O硫化氢(过量)与氢氧化钠的反应H2S+NaOH==== NaHS+H2O68.硫化氢(少量)与氨气的反应H2S+2NH3==== (NH4+)2S硫化氢(过量)与氨气的反应H2S+NH3==== NH4+HS69.硫化氢与氧气(不足)的反应2H2S+O2==== 2S↓+2H2O 2H2S+O2==== 2S+2H2O 硫化氢与氧气(充足)的反应2H2S+3O2==== 2SO2+2H2O70.硫化氢与氯气的反应H2S+Cl2==== 2HCl+S↓71.硫化氢与浓硫酸的反应 H2S+H2SO4(浓)==== S↓+SO2↑+2H2O72.硫化氢的制备FeS+H2SO4==== FeSO4+H2S↑73.电解饱和食盐水(氯碱工业) 2NaCl+2H2O==== 2NaOH+H2↑+Cl2↑74.电解熔融状态氯化钠(制单质钠) 2NaCl==== 2Na+Cl2↑75.海水制镁(1) CaCO3==== CaO+CO2(2) CaO+H2O==== Ca(OH)2(3) Mg2+ +2OH2- ==== Mg(OH)2↓(4) Mg(OH)2+2HCl==== MgCl2+2H2O(5) MgCl2==== Mg+Cl2↑76.镁在空气中燃烧(与氧气的反应) 2Mg+O2==== 2MgO(与氮气的反应) 3Mg+N2==== Mg3N2(与二氧化碳的反应) 2Mg+CO2==== 2MgO+C77.镁与氯气的反应Mg+Cl2==== MgCl278.镁与水的反应Mg+2H2O==== Mg(OH)2+H2↑79.镁与盐酸的反应Mg+2HCl==== MgCl2+H2↑80.镁与氢离子的反应Mg+2H+ ==== Mg2+ +H2↑81.二氮化三镁与水的反应Mg3N2+6H2O==== 3Mg(OH)2↓+2NH3↑82.镁与溴水的反应(颜色退去) Mg+Br2==== MgBr2(产生气泡) Mg+2HBr==== MgBr2+H2↑83.溴与水的反应Br2+H2O==== HBr+HBrO84.溴与氢氧化钠的反应Br2+2NaOH==== NaBr+NaBrO+H2O85.溴与氢气的反应Br2+H2==== 2HBr86.溴与铁的反应3Br2+2Fe==== 2FeBr387.碘与铁的反应I2+Fe==== FeI288.溴与碘化钾的反应Br2+2KI==== 2KBr+I289.氯气与溴化钾的反应2KBr+Cl2==== 2KCl+Br2第四章90.硅与氧气的反应Si+O2==== SiO291.硅与氯气的反应Si+2Cl2==== SiCl492.硅与氢气的反应Si+2H2===== SiH493.二氧化硅与氟的反应Si+2F2==== SiF494.硅与碳的反应Si+C==== SiC95.硅与氢氧化钠溶液的反应Si+2NaOH+H2O==== Na2SiO3+2H2↑96.硅与氢氟酸的反应Si+4HF==== SiF4+2H2↑97.单质硅的制备(1.制备)SiO2+2C==== Si+2CO(2.提纯)Si+2Cl2==== SiCl4(3.提纯)SiCl4+2H2==== Si+4HCl98.二氧化硅与氢氧化钠的反应SiO2+2NaOH==== Na2SiO3+H2O99.二氧化硅与氧化钠的反应SiO2+Na2O==== Na2SiO3100.二氧化硅与碳酸钠的反应SiO2+Na2CO3==== Na2SiO3+ CO2↑ 101.二氧化硅与氧化钙的反应SiO2+CaO==== CaSiO3102.二氧化硅与碳酸钙的反应SiO2+CaCO3==== CaSiO3+CO2↑ 103.二氧化硅与氢氟酸的反应SiO2+4HF==== SiF4+2H2O104.硅酸的制备Na2SiO3+ CO2+H2O==== H2SiO3↓+ Na2CO3105.硅酸加热分解H2SiO3==== SiO2+H2O106.铝与氧气的反应4Al+3O2==== 2Al2O3107.铝与氯气的反应2Al+3Cl2==== 2AlCl3108.铝与盐酸的反应2Al+6HCl==== 2AlCl3+3H2↑109.铝与氢氧化钠的反应2Al+2NaOH+6H2O==== 2Na[Al(OH)4]+3H2↑110.铝与水的反应2Al+6H2O==== 2Al(OH)3+3H2↑111.铝与三氧化二铁的反应(铝热反应)2Al+Fe2O3==== 2Fe+Al2O3112.铝与二氧化锰的反应(铝热反应)4Al+3MnO2==== 3Mn+2AlO3113.氧化铝与盐酸的反应Al2O3+6HCl==== 2AlCl3+3H2O114.氧化铝与氢氧化钠的反应Al2O3+2NaOH+3H2O==== 2Na[Al(OH)4]115.电解氧化铝2Al2O3==== 4Al+3O2↑116.硫酸与与一水合氨的反应Al2(SO4)3+6NH3?H2O==== 2Al(OH)3↓+3(NH4+)2SO4117.氯化铝与一水合氨的反应AlCl3+3NH3?H2O==== Al(OH)3↓+3NH4+Cl118.氯化铝与氢氧化钠(少量)的反应AlCl3+3NaOH==== Al(OH)3↓+3NaCl119.氢氧化铝与氢氧化钠的反应Al(OH)3+NaOH==== Na[Al(OH)4]120.氯化铝与氢氧化钠(过量)的反应AlCl3+4NaOH==== Na[Al(OH)4]+3NaCl121.四羟基合氯酸钠与盐酸(少量)的反应Na[Al(OH)4]+HCl==== Al(OH)3↓+NaCl+H2O 122.氢氧化铝与盐酸的反应Al(OH)3+3HCl==== AlCl3+3H2O123.四羟基合氯酸钠与盐酸(过量)的反应Na[Al(OH)4]+4HCl==== AlCl3+NaCl+4H2O 124.四羟基合氯酸钠与氯化铝的反应3Na[Al(OH)4]+AlCl3==== 4Al(OH)3↓+3NaCl 125.向四羟基合氯酸钠中通入过量二氧化碳Na[Al(OH)4]+CO2==== Al(OH)3↓+NaHCO3 126.铜在潮湿空气中被腐蚀2Cu+O2+H2O+CO2==== Cu2(OH)2CO3127.铜与氧气的反应2Cu+O2==== 2CuO128.铜与氯气的反应Cu+Cl2==== CuCl2129.铜氧化在高温下转化4CuO==== 2Cu2O+O2↑130.硫酸铜与水的反应CuSO4+5H2O==== CuSO4?5H2O。
化学方程式汇总.

化学方程式汇总一、碱金属1.钠露置在空气中变暗:4Na + O2 = 2Na2O2.钠的燃烧(工业生产过氧化钠):2Na + O2Na2O23.钠与硫混合爆炸:2Na + S = Na2S4.钠投入水中:2Na + 2H2O = 2NaOH + H2↑5.钠投入硫酸铜溶液中:2Na + CuSO4 + 2H2O = Na2SO4 + Cu(OH)2↓+ H2↑6.过氧化钠与水反应:2Na2O2 + 2H2O = 4NaOH + O2↑7.过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3 + O28.碳酸氢钠与氢氧化钠溶液反应:NaHCO3 + NaOH = Na2CO3 + H2O9.碳酸氢钠溶液与盐酸反应:NaHCO3 + HCl = NaCl + H2O + CO2↑10.向碳酸钠溶液中逐滴加入盐酸:Na2CO3 + HCl(少量)= NaCl + NaHCO3盐酸足量时:Na2CO3 + 2HCl(足量)= 2NaCl + H2O + CO2↑11.少量石灰水与碳酸氢钠溶液反应:Ca(OH)2 + 2NaHCO3 = CaCO3↓+ 2H2O + Na2CO3离子方程式:Ca2+ + 2OH- + 2HCO3- = CaCO3↓+ 2H2O + CO32-12.足量石灰水与碳酸氢钠溶液反应:Ca(OH)2 + NaHCO3 = CaCO3↓+ H2O + NaOH离子方程式:Ca2+ + OH- + HCO3- = CaCO3↓+ H2O13.少量氢氧化钠与碳酸氢钙溶液反应:Ca(HCO3)2 + NaOH = CaCO3↓+ NaHCO3 + H2O离子方程式:Ca2+ + OH- + HCO3- = CaCO3↓+ H2O14.足量氢氧化钠与碳酸氢钙溶液反应:Ca(HCO3)2 + 2NaOH = CaCO3↓+ Na2CO3 + 2H2O离子方程式:Ca2+ + 2HCO3- +2OH-= CaCO3↓+ 2H2O + CO32-15.侯德榜制碱法:①向NaCl溶液中先通入NH3后通入CO2:NH3 + CO2 + NaCl + H2O = NaHCO3 ↓+ NH4Cl②碳酸氢钠受热分解:2NaHCO3Na2CO3 + CO2↑+ H2O16.向饱和碳酸钠溶液中通入二氧化碳气体:Na2CO3 + CO2 + H2O = 2NaHCO3↓二、卤素1.钠在氯气中燃烧:2Na + Cl22NaCl2.铜在氯气中燃烧:Cu + Cl2CuCl23.铁在氯气中燃烧:2Fe + 3Cl22FeCl34.铁与溴单质反应:2Fe + 3Br22FeBr35.碘与铁反应:Fe + I2FeI2 (Fe与I2反应时,Fe只能生成+ 2价)6.氯气与氢气混合光照:H2 + Cl22HCl(爆炸)7.工业制盐酸:H2 + Cl22HCl8.氯气与磷点燃:2P + 3Cl2(少量)2PCl3 (液) ;2P + 5Cl2(足量)2PCl5(固)9.氯气使湿润布条褪色(氯气溶解于水):Cl2 + H2OHCl + HClO10.次氯酸溶液见光:2HClO2HCl + O2↑11.氯气使湿润的碘化钾淀粉试纸变蓝:Cl2 + 2KI = 2KCl + I212.工业制漂白粉:2Ca(OH)2 + 2Cl2 = CaCl2 + Ca(ClO)2 + 2H2O离子方程式:Ca(OH)2 + Cl2 = Ca2++Cl-+ClO-+H2O13.漂白粉使用原理:Ca(ClO)2 + CO2 + H2O = CaCO3↓+ 2HClO14.向漂白粉溶液中通入足量SO2气体:Ca(ClO)2 + 2SO2 + 2H2O = Ca SO4 ↓+ 2HCl +H2SO4离子方程式:Ca2++2ClO-+2SO2 +H2O = CaSO4↓+SO42-+Cl-+4H+15.漂白粉固体久置变质:①Ca(ClO)2 + CO2 + H2O = CaCO3 + 2HClO;②2HClO2HCl + O2↑16.实验室制氯气:⑴4HCl(浓) + MnO2MnCl2 + Cl2↑+ 2H2O(这是最常用的);⑵2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O⑶KClO3 +6HCl = KCl + 3Cl2↑+ 3H2O⑷KClO+2HCl = KCl+Cl2↑+H2O17.工业制氯气(氯碱工业):2NaCl + 2H2OCl2↑+ H2↑+ 2NaOH18.实验室制氯气时尾气吸收(制84消毒液):Cl2 + 2NaOH = NaCl + NaClO + H2O19.氯气溶于热浓碱溶液:3Cl2 + 6KOH5KCl + KClO3 + 3H2O20.氯化钾与氯酸钾在酸性条件下生成氯气:5KCl + KClO3 + 3 H2SO4 = 3K2SO4 + 3 Cl2↑+ 3 H2O21.氯酸钾与盐酸生成氯气:6HCl + KClO3 = KCl + 3Cl2↑+ 3H2O22.氯离子检验:Cl- +Ag+ = AgCl↓(白色沉淀不溶于硝酸)23.溴离子检验:Br- +Ag+ = AgBr↓(浅黄色沉淀不溶于硝酸)24.碘离子检验:I - +Ag+ = AgI↓(黄色沉淀不溶于硝酸)25.氟气溶于水:2F2 + 2H2O = 4HF +O226.氟与氢气反应:F2 + H2 = 2HF27.碘与氢气反应:I2 + H22HI28.溴化银感光成像原理:2AgBr2Ag + Br2三、硫硫酸1.硫与铜共热:2Cu + SCu2S2.硫与铁共热:Fe + SFeS3.硫与氢气反应:H2 + SH2S4.硫在氧气中燃烧:S + O2SO25.硫与氢氧化钾溶液反应:3S + 6KOH2K2S + K2SO3 + 3H2O6.同元素的两种盐溶液遇酸生成该元素单质:2K2S +K2SO3 +3H2SO4 = 3S↓+3K2SO4 +3H2O7.硫化氢燃烧(O2不足):2H2S + O22S + 2H2O ;(O2充足):2H2S + 3O22SO2 + 2H2O8.氢硫酸露置在空气中变浊:2H2S + O2 = 2S↓+ 2H2O9.硫化氢隔绝空气加热:H2SH2 + S10.硫化氢与卤单质X2(Cl2、Br2、I2)反应:H2S + X2 = S↓+ 2HX11.硫化氢气体通入硫酸铜溶液:H2S + CuSO4 = CuS↓+ H2SO412.硫化氢与二氧化硫气体混合:2H2S + SO2 = 3S↓+ 2H2O13.硫化氢气体不能用浓硫酸干燥:H2S + H2SO4(浓) = S↓+ SO2 + 2H2O14.二氧化硫气体溶于水:SO2 + H2OH2SO315.实验室制二氧化硫气体:Na2SO3 + H2SO4 = Na2SO4 + SO2↑+ H2O16.实验室用碱液吸收硫化氢:H2S(少量) + 2NaOH = Na2S + 2H2O;H2S(过量) + NaOH = NaHS + H2O17.实验室用碱液吸收二氧化硫:SO2(少量) + 2NaOH = Na2SO3 + H2O;SO2(过量) + NaOH = NaHSO318.纯碱溶液吸收少量二氧化硫:SO2(少量) + 2Na2CO3+ H2O = Na2SO3+2NaHCO3纯碱溶液1:1吸收二氧化硫:SO2+ Na2CO3 = Na2SO3 + CO2纯碱溶液吸收过量二氧化硫:2SO2 + Na2CO3 + H2O = 2NaHSO3 + CO219.硫酸工业用氨水吸收二氧化硫及循环使用:①SO2 + 2NH3·H2O = (NH4)2SO3 + H2O;②(NH4)2SO3 + H2SO4 = (NH4)2SO4 + H2O + SO2↑20.二氧化硫通入氯水(SO2 与Cl2混合失去漂白性):SO2 + Cl2 + 2H2O = H2SO4 + 2HCl21.二氧化硫通入溴水(SO2使溴水褪色):SO2 + Br2 + 2H2O = H2SO4 + 2HBr22.二氧化硫使酸性高锰酸钾溶液褪色:5SO2 + 2KMnO4 + 2H2O = 2H2SO4 + K2SO4 + 2MnSO423.二氧化硫与稀硝酸:3SO2 + 2HNO3(稀)+ 2H2O = 3H2SO4 + 2NO24.亚硫酸钠与稀硝酸:3Na2SO3 + 2HNO3 = 3Na2SO4 + 2NO↑+ H2O25.亚硫酸钠溶液与卤单质X2(Cl2、Br2、I2)反应:Na2SO3 + X2 + H2O = Na2SO4 + 2HX26.亚硫酸盐放在空气中变质:2Na2SO3 + O2 = 2Na2SO427.二氧化硫与二氧化氮气体不共存:SO2 + NO2 = SO3 + NO28.浓硫酸与铜反应:Cu +2 H2SO4(浓)CuSO4 + SO2↑+ 2H2O29.浓硫酸与碳反应:C + 2H2SO4(浓)CO2↑+ 2SO2↑+ 2H2O30.浓硫酸与硫共热:S + 2H2SO4(浓)3SO2↑+ 2H2O31.工业制硫酸:①4FeS2 + 11O22Fe2O3 + 8SO2 ;也可以是S + O2SO2);②2SO2 + O22SO3 ;③SO3 + H2O = H2SO432.氧气与臭氧互相转化:3O22O3 ;2O33O233.臭氧使碘化钾淀粉试纸变蓝:O3 + 2KI + H2O = I2 + 2KOH + O234.双氧水与硫化氢:H2S + H2O2 = S↓+ 2H2O35.双氧水与二氧化硫:SO2 + H2O2 = H2SO436.双氧水与亚硫酸钠溶液:Na2SO3 + H2O2 = Na2SO4 + H2O37.双氧水与高锰酸钾酸性溶液反应:2KMnO4 + 5H2O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 5O2↑+ 8H2O38.双氧水与氯气:H2O2 + Cl2= 2HCl + O239.双氧水催化分解(实验室制氧气之一):2H2O22H2O + O2↑40.氯酸钾催化加热分解(实验室制氧气之二):2KClO32KCl + 3O2 ↑41.高锰酸钾加热分解(实验室制氧气之三):2KMnO4K2MnO4 + MnO2 + O2↑42.硫酸酸雨形成过程:SO2 + H2OH2SO3 ,2H2SO3 + O2 = 2H2SO443.硫代硫酸盐在酸性条件下自身氧化还原:Na2S2O3 + H2SO4 == Na2SO4 + SO2↑+ S↓+ H2O44.钙基固硫(煤的脱硫)消除二氧化硫污染:①CaO + SO2CaSO3;②2CaSO3 + O22CaSO4四、氮和磷1.工业合成氨:N2 + 3H22NH32.二氧化氮自身二聚:2NO2(棕色)N2O4(无色)3.自然界形成硝酸酸雨(雷雨发庄稼):①氮气与氧气放电N2 + O22NO;②一氧化氮被氧气氧化:2NO + O2 = 2NO2 ;③二氧化氮溶于水:3NO2 + H2O = 2HNO3 + NO4.工业制硝酸:①4NH3 + 5O24NO + 6H2O;②2NO + O2 = 2NO2 ;③3NO2 + H2O = 2HNO3 + NO5.镁在氮气中燃烧:3Mg + N2Mg3N26.氮化镁投入水中:Mg3N2 + 6H2O = 3Mg(OH)2 + 2NH3↑7.氮化镁与盐酸反应生成两种盐:Mg3N2 + 8HCl = 3MgCl2 + 2NH4Cl8.氨气溶于水显碱性:NH3 + H2ONH3·H2ONH4+ + OH-9.氨气与氯化氢的“白烟”实验:NH3 + HCl = NH4Cl10.氨气的催化氧化:4NH3 + 5O24NO + 6H2O11.工业制硝酸中尾气中NO2与NO共同与碱液反应:NO2 + NO + 2NaOH = 2NaNO2 + H2O12.二氧化氮与氢氧化钠溶液反应:2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O13.氨气与氯气反应:2NH3(少量) + 3Cl2 = N2 + 6HCl;8NH3(足量) + 3Cl2 = N2 + 6NH4Cl14.氯化铵受热:NH4ClNH3↑+ HCl↑15.碳酸氢铵分解:NH4HCO3NH3↑+ H2O + CO2↑16.实验室制氨气(常用碱石灰与氯化铵):2NH4Cl + Ca(OH)2 2NH3↑+ CaCl2 + 2H2O17.浓硝酸常显黄色原因:4HNO34NO2↑+ 2H2O + O2↑18.铜与浓硝酸(实验室制NO2):Cu + 4HNO3(浓) = Cu(NO3)2 + 2NO2↑+ 2H2O 19.铜与稀硝酸:3Cu + 8HNO3(稀) = 3Cu(NO3)2 + 2NO↑+ 4H2O20.银与稀硝酸:3Ag +4HNO3 (稀) = 3AgNO3 +NO ↑+2H2O21.少量铁与稀硝酸:Fe + 4HNO3(稀) = Fe(NO3)3 + NO↑+ 2H2O22.过量铁与稀硝酸:3Fe + 8HNO3(稀) = 3Fe(NO3)2 + 2NO↑+ 4H2O23.浓硝酸与磷共热:P + 5HNO3(浓)H3PO4 + 5NO2↑+ H2O24.浓硝酸与硫共热:S + 6HNO3(浓)H2SO4 + 6NO2↑+ 2H2O25.浓硝酸与碳共热:C + 4HNO3(浓)CO2↑+ 4NO2↑+ 2H2O26.工业用磷矿石制普钙:Ca3(PO4)2 +2H2SO4(浓)= 2CaSO4 +Ca(H2PO4)2 27.工业用磷矿石制重钙:Ca3(PO4)2 + 4 H3PO4 == 3 Ca(H2PO4)228.工业用磷矿石制磷酸:Ca3(PO4)2 + 3H2SO4(浓) = 3CaSO4 + 2H3PO429.五氧化二磷与热水反应:P2O5 + 3H2O2H3PO430.五氧化二磷与冷水反应:P2O5 + H2O = 2HPO3五、碳和硅1.工业制二氧化碳:CaCO3CaO + CO2↑2.硅的燃烧:Si + O2SiO23.工业制粗硅:SiO2 + 2CSi + 2CO↑4.粗硅精制:①Si + 2Cl2SiCl4 ;②SiCl4 + 2H2Si + 4HCl5.制金刚砂:SiO2 + 3CSiC + 2CO↑6.硅与氢氧化钠溶液反应:Si + 2NaOH + H2O = Na2SiO3 + 2H2↑7.硅与氢氟酸反应:Si + 4HF = SiF4↑+ 2H2↑8.二氧化硅与氢氧化钠溶液反应(强碱腐蚀玻璃):SiO2 + 2NaOH = Na2SiO3 + H2O9.氢氟酸雕刻(腐蚀)玻璃:SiO2 + 4HF = SiF4↑+ 2H2O10.工业制玻璃:SiO2 + Na2CO3Na2SiO3 + CO2↑;SiO2 + CaCO3CaSiO3 + CO2↑11.硅酸钠溶液中通二氧化碳气体:Na2SiO3 + CO2 + H2O = H2SiO3(胶体)+ Na2CO3 12.硅酸钠溶液中加入盐酸:Na2SiO3 + 2 HCl = H2SiO3(胶体)+ 2NaCl13.硅酸钠溶液与铵盐混合:Na2SiO3 + 2NH4Cl + 2H2O = H2SiO3↓+ 2NaCl + 2NH3·H2O14.工业制氢气:①C + H2OCO + H2 ,②CO + H2OCO2 + H215.工业制水煤气(煤的气化):C + H2OCO + H216.草酸使高锰酸钾溶液褪色:2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑+ 8H2O六、镁、铝、铁1.镁与水反应:Mg + 2H2OMg(OH)2 + H2↑2.镁在二氧化碳中燃烧:2Mg + CO22MgO + C3.镁与氯化铵等水解显酸性的盐溶液反应:Mg + 2NH4Cl = MgCl2 + 2NH3↑+ H2↑镁与氯化铜等水解显酸性的盐溶液反应:Mg + CuCl 2 + 2H2O = MgCl2 +Cu (OH)2↓+ H2↑4.氢氧化镁溶于氯化铵溶液:Mg(OH)2 + 2NH4Cl = MgCl2 + 2NH3·H2O5.铝与盐酸:2Al + 6HCl = 2AlCl3 + 3H2↑6.铝与氢氧化钠溶液:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑7.铝与氧化铁(铝热反应之一):2Al + Fe2O32Fe + Al2O38.氧化铝溶于盐酸中:Al2O3 + 6HCl = 2AlCl3 + 3H2O9.氧化铝溶于氢氧化钠溶液中:Al2O3 + 2NaOH = 2NaAlO2 + H2O10.氢氧化铝溶于盐酸中:Al(OH)3 +3HCl = AlCl3 +3H2O11.氢氧化铝溶于氢氧化钠溶液中:Al(OH)3 +NaOH = NaAlO2 +2H2O12.氢氧化铝的两种电离方式:Al3+ + 3OH-Al(OH)3H+ + AlO2- + H2O13.向氯化铝溶液中加入少量氢氧化钠溶液:AlCl3 + 3NaOH = Al(OH)3↓+ 3NaCl14.向氯化铝溶液中加入过量氢氧化钠溶液:AlCl3 + 4NaOH = NaAlO2 + 3NaCl + 2H2O15.向偏铝酸钠溶液中加入少量盐酸:NaAlO2 + HCl + H2O = Al(OH)3↓+ NaCl16.向偏铝酸钠溶液中加入过量盐酸:NaAlO2 + 4HCl = AlCl3 + NaCl + 2H2O17.向偏铝酸钠溶液中通入少量二氧化碳:2NaAlO2 + CO2 + 3H2O = 2Al(OH)3↓+ Na2CO318.向偏铝酸钠溶液中通入过量二氧化碳:NaAlO2 + CO2 + 2H2O = Al(OH)3↓+ NaHCO319.偏铝酸钠溶液与氯化铝溶液:3NaAlO2 + AlCl3 + 6H2O = 4Al(OH)3↓+ 3NaCl 20.实验室制取Al(OH)3 :Al2(SO4)3 + 6NH3·H2O = 2Al(OH)3↓+ 3(NH4)2SO421.工业生产铝(电解熔融的Al2O3):2Al2O34Al + 3O2↑22.铁与硫共热:Fe + SFeS23.铁在氧气中燃烧:3Fe + 2O2Fe3O424.氯气与铁点燃:2Fe + 3Cl22FeCl325.碘与铁反应:Fe + I2FeI226.铁与氯化铁溶液:Fe + 2FeCl3 = 3FeCl227.铁与高温水蒸汽反应:3Fe + 4H2O(g)Fe3O4 + 4H228.氯化铁溶液与铜:Cu + 2FeCl3 = CuCl2 + 2FeCl229.氯化铁溶液与硫化氢:2FeCl3 + H2S = 2FeCl2 + S↓+ 2HCl30.氯化铁溶液与碘化氢:2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl31.氯化铁溶液与二氧化硫:2FeCl3 + SO2 + 2H2O = 2FeCl2 + H2SO4 + 2HCl32.氯化亚铁与氯气:2FeCl2 + Cl2 = 2FeCl333.氯化亚铁酸性溶液与双氧水:2FeCl2 + 2HCl + H2O2 = 2FeCl3 + 2H2O34.氯化亚铁溶液在空气中变质:4FeCl2 + O2 + 4HCl = 4FeCl3 + 2H2O35.氯化亚铁与氢氧化钠溶液:FeCl2 + 2NaOH = Fe(OH)2↓+ 2NaCl36.氢氧化亚铁放空气中变色:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)337.氯化亚铁与铁氰酸钾(亚铁离子检验):3FeCl2 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2 ↓(蓝色) + 6 KCl38.氯化铁溶液与硫氰酸钾(铁离子检验):FeCl3 + 3KSCNFe(SCN)3(血红色溶液)+ 3KCl39.氯化铁溶液与氢氧化钠溶液(铁离子检验):FeCl3 + 3NaOH = Fe(OH)3↓(红褐色沉淀)+ 3NaCl40.除去氯化铜溶液中的氯化铁(沉淀转化):2FeCl3 + 3Cu(OH)2 = Fe(OH)3+ 3CuCl2 41.工业用氧化铁冶铁(与一氧化碳)反应:Fe2O3 + 3CO2Fe + 3CO242.氧化铜与碳:CuO + CCu + CO↑;CuO + COCu + CO243.重铬酸钾的酸碱性转化:K2Cr2O7+H2OK2CrO4+H2CrO4离子方程式:Cr2O72- + H2OCrO42- + 2H+七、有机反应方程式㈠、(取代反应)1.烷烃卤代(与氯气) :CH4 + Cl2CH3Cl + HCl2.卤代烃卤代:CH3Cl + Cl2CH2Cl2 + HCl ……3.苯的卤代(与液溴):+Br2 + HBr4.苯的硝化:+HNO3+ H2O5.工业制TNT :+3HNO3 +3H2O6.溴乙烷水解:CH3CH2Br + NaOHCH3CH2OH + NaBr7.乙醇脱水成乙醚:2CH3CH2OHC2H5OC2H5 + H2O8.乙醇与浓氢溴酸反应:CH3CH2OH +HBrCH3CH2 Br +H2O9.苯酚与浓溴水:+3Br2↓+3HBr10.乙酸与乙醇的酯化反应:CH3COOH + CH3CH2OHCH3COOCH2CH3 + H2O 11.乙酸乙酯水解(酸催化):CH3COOCH2CH3 + H2OCH3COOH + CH3CH2OH 12.乙酸乙酯水解(碱催化):CH3COOCH2CH3 + NaOHCH3COONa + CH3CH2OH 13.乙酸苯酚酯碱性条件下水解:CH3COOC6H5 +2NaOHCH3COONa +C6H5ONa+H2O14.皂化反应(以硬脂酸甘油酯为例):+ 3NaOH3C17H35COONa +15.纤维素与硝酸的酯化:[C6H7O2(OH)3]n +3n HNO3[C6H7O2(ONO2)3]n + 3 n H2O16.两分子乳酸自身成环反应:2 + 2H2O17.5 —羟基戊酸自身形成环酯:HO —CH2CH2CH2CH2COOH+ H2O18.乙二酸和乙二醇形成环酯(1:1):+ + 2H2O19 .两个丙氨酸自缩合形成二肽:2 + H2O㈡、加成反应(与氢气的加成反应也是还原反应)1.乙烯使溴水褪色:H2C = CH2 + Br2CH2BrCH2Br2.乙烯与氢气加成:H2C = CH2 + H2CH3CH33.乙烯与溴化氢加成:H2C = CH2 + HBrCH3CH2Br4.乙烯与水加成(工业制乙醇) :H2C = CH2 + H2OCH3CH2OH5.苯与氢气加成:+3H26.乙炔与氯化氢(1:1):CH≡CH + HClCH2 = CHCl7.乙炔与足量溴水:CH≡CH + 2Br2CHBr2 —CHBr28.1,3 —丁二烯与溴水完全加成:CH2 = CH —CH = CH2 +2Br29.1,3 —丁二烯与溴水(1,4 —加成):CH2 = CH —CH = CH2 + Br20.1,3 —丁二烯与溴水(1,2 —加成):CH2 = CH —CH = CH2 + Br211.乙醛与氢气加成:CH3CHO + H2CH3CH2OH㈢、消去反应1.溴乙烷消去:CH3CH2Br + NaOHCH2 = CH2↑+ NaBr + H2O2.1,2 —二溴乙烷消去:CH2BrCH2Br + 2NaOHCHCH↑+ 2NaBr + 2H2O3.乙醇消去(实验室制乙烯) :CH3CH2OHCH2 = CH2↑+ H2O㈣、氧化反应1.烃的含氧衍生物的燃烧通式:CxHyOz + (x + y/4 - z/2)O2 xCO2 + y/2H2O2.乙醇的催化氧化:2CH3CH2OH + O2 CH3CHO + 2H2O3.2 —丙醇的催化氧化:2CH3CH(OH)CH3 + O22CH3COCH3 + 2H2O4.乙醛的催化氧化:2CH3CHO + O22CH3COOH5.乙醛的银镜反应:CH3CHO + 2Ag(NH3)2OHCH3COONH4 + 2Ag↓+ 3NH3 + H2O乙醛银镜反应的离子方程式:CH3CHO +2Ag(NH3)2++2 OH-CH3COO-+ NH4+ +2Ag ↓+ 3NH3 + H2O6.甲醛的银镜反应:HCHO + 4Ag(NH3)2OH(NH4)2CO3 + 4Ag↓+ 6NH3 + 2H2O7.乙醛与新制氢氧化铜反应:CH3CHO + 2Cu(OH)2+NaOHCH3COONa + Cu2O↓+3H2O8.甲醛与新制氢氧化铜反应:HCHO + 4Cu(OH)2CO2↑+ 2Cu2O↓+ 5H2O㈤、聚合反应1.乙烯生成聚乙烯:nCH2 = CH22.氯乙烯生成聚氯乙烯:nCH2 = CHCl3.制顺丁橡胶:nCH2=CH—CH=CH24.制丁苯橡胶:nCH2=CH—CH=CH2+n5.由单体形成天然橡胶:n6.乙二醇的自身缩聚:nHO—CH2CH2—OH + (n - 1) H2O7.酚醛树脂的生成:n + nHCHO+ (n - 1)H2O8.制涤纶:n + nHOCH2CH2OH + (2n - 1)H2O㈥、其它反应1.实验室制乙炔:CaC2 + 2H2OCa(OH)2 +CHCH ↑2.葡萄糖发酵制酒精:C6H12O6(葡萄糖)2C2H5OH +2CO2↑3.证明醋酸强于碳酸(有气体生成):CH3COOH +NaHCO3CH3COONa +CO2↑+H2O4.碳酸强于苯酚(溶液变浑浊):CO2 +H2O +C6H5ONaNaHCO3 +C6H5OH5.丙氨酸与盐酸:+HCl6.丙氨酸与氢氧化钾:+KOH+ H2O7.乙醇和钠反应:2CH3CH2OH +2 Na 2CH3CH2ONa +H2↑最新文件仅供参考已改成word文本。
高中有机化学方程式汇总(全)(已免费)

光照 光照 光照 光照 高温 CaO△ 催化剂加热、加压 催化剂催化剂△ 催化剂 △ 催化剂 催化剂催化剂 催化剂△ 催化剂催化剂浓硫酸△ △CH 3 NO 2O 2N CH 3催化剂△高中有機化學方程式匯總1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 2 + H 2O CH 3CH 2OH10. CH 2 = CH 2 + HBr CH 3—CH 2Br11. CH 2 = CH 2 + H 2 CH 3—CH 312. nCH 2 = CH 2 [ CH 2—CH 2 ] n13. nCH 2=CH-CH=CH 2 [CH 2-CH=CH-CH 2] n14. 2CH 2 = CH 2 + O 2 2CH 3CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] nCl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)221. + Br 2 Br + HBr22. + HO -NO 2 NO 2 +H 2O23. + HO -SO 3H SO 3H+H 2O24. + 3H 2催化剂NaOH H 2O 醇△ 催化剂 △ 浓硫酸 170℃ 浓硫酸140℃OH Br Br OH 催化剂 △ 催化剂△△ △ 浓硫酸△ Br25. +3HO -NO 2 +3H 2O26. 3CH ≡CH →27. CH 3CH 2Br + H 2O CH 3CH 2OH + HBr28. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr29. CH 3CH 2Br+ NaOH CH 2 = CH 2 + NaBr +H 2O30. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑31. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O 32. CH 3CH 2OH CH 2 = CH 2↑+ H 2O 33.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 34. OH+NaOH ONa+H 2O35. OH+H 2O O -+H 3O +36. ONa+H 2O+CO 2 OH+ NaHCO 337. +3Br 2 ↓ +3HBr 38. CH 3CHO + H 2 CH 3CH 2OH39. 2CH 3CHO + O 2 2CH 3COOH 40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O41CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O 42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑43.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑45. CH 3COOH + NaOH CH 3COONa + H 2O46. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O47.CH 3COOH+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O 48. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+ 浓硫酸△+ 2H2O O OC — CO OCH2-CH249. nOHCH2CH2COOH→ [ OCH2CH2C ] n +H2O50. C6H12O6 (s)+ 6O2 (g)6CO2 (g)+ 6H2O(l)51. C6H12O62CH3CH2OH + 2CO252. C12H22O11+H2O C6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11+ H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n+ nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n+ nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2 C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2 C17H35COO-CH2 57. C17H35COO-CH2 CH2-OH C17H35COO-CH +3NaOH 3C17H35COONa+ CH-OHC17H35COO-CH2 CH2-OH 58. CH2OH COOHCH2OH COOH1.HClClCHClCH+−→−+324光2.3.4.5.6.7.8.9.10.11.12.13.14.15.16.17.18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
化学方程式汇总文字表达式

化学方程式汇总+文字表达式化学方程式汇总一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2点燃→氧化镁2. 铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热(4Fe + 3O2△2Fe2O3) 铁+氧气→四氧化三铁3. 铜在空气中受热:2Cu + O2加热 2CuO 红色金属变为黑色固体铜+氧气→氧化铜4. 铝在空气中燃烧:4Al + 3O2 2Al2O3银白金属变为白色固体铝+氧气→氧化铝5. 氢气中空气中燃烧:2H2 + O2点燃 2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料、最理想的燃料(资源丰富,热值高,无污染).6. 红磷在空气中燃烧:4P + 5O2点燃 2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量烟幕弹发令枪子弹磷—+氧气→五氧化二磷7. 硫粉在空气中燃烧: S + O2点燃 SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰,.氧气中蓝紫色火焰硫+氧气→二氧化硫8. 碳在氧气充分时燃烧:C + O2点燃 CO2剧烈燃烧、白光、放热、使石灰水变浑浊碳+氧气→二氧化碳9. 碳在氧气不充分时燃烧:2C + O2点燃2CO 产生能量少,污染大;煤炉中常见反应、生成物是空气污染物之一、煤气中毒原因碳+氧气→一氧化碳(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2点燃 2CO2CO还原金属氧化物实验中,尾气处理的反应一氧化碳+氧气→二氧化碳11. 甲烷在空气中燃烧:CH4 + 2O2点燃 CO2+ 2H2O 明亮的蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧甲烷+氧气→二氧化碳+水12. 酒精在空气中燃烧:C2H5OH + 3O2点燃 2CO2+ 3H2O 清洁能源、绿色能源酒精+氧气→二氧化碳+水13.光合作用:6H2O +6 CO2光照C6H12O6+O2↑二氧化碳+水→葡萄糖+氧气14.呼吸作用:C6H12O6+O2呼吸6H2O +6 CO2↑葡萄糖+氧气→二氧化碳+水二.几个分解反应:15. 水在直流电的作用下分解:2H2O 通电 2H2↑+ O2↑初中唯一的一个条件为“通电”的反应。
化学方程式汇总

2、钠与水反应3、钠与硫酸铜溶液4、过氧化钠与水反应5、碳酸氢盐溶液与强酸溶液混合6、碳酸氢盐溶液与醋酸溶液混合7、氢氧化钙溶液与碳酸氢镁反应8、向碳酸氢钙溶液中加入过量的氢氧化钠9、向碳酸氢钙溶液中加入少量的氢氧化钠10、澄清石灰水与少量小苏打溶液混合11、澄清石灰水通入少量CO212、澄清石灰水通入过量CO213、碳酸氢钠溶液与少量石灰水反应14、碳酸氢钠溶液与过量石灰水反应15、等物质的量氢氧化钡溶液与碳酸氢铵溶液混合16、碳酸钠溶液与盐酸反应17、向氢氧化钠溶液中通入少量的CO2¬18、过量的CO2通入氢氧化钠溶液中19、碳酸氢铵溶液中加入过量氢氧化钠溶液20、碳酸钙与盐酸反应21、碳酸钙与醋酸反应22、澄清石灰水与稀盐酸反应23、磷酸溶液与少量澄清石灰水24、磷酸溶液与过量澄清石灰水25、碳酸镁溶于强酸26、硫酸镁溶液跟氢氧化钡溶液反应27、硫酸溶液跟氢氧化钡溶液反应28、硫酸氢钠溶液与氢氧化钡反应至中性29、硫酸氢钠溶液与氢氧化钡反应至硫酸根完全沉淀30、硫酸铝溶液中加入过量氢氧化钡溶液31、氢氧化镁与稀硫酸反应32、铝跟氢氧化钠溶液反应33、物质的量之比为1:1NaAl合金置于水中34、氧化铝溶于强碱溶液35、氧化铝溶于强酸溶液36、氢氧化铝与氢氧化钠溶液37、氢氧化铝与盐酸溶液反应38、硫酸铝溶液与碳酸氢钠溶液39、硫酸铝溶液与碳酸钠溶液40、氯化铝溶液中加入过量氨水41、明矾溶液加热水解生成沉淀42、氯化铝溶液与偏铝酸钠溶液43、偏铝酸钠溶液中加入氯化铁溶液44、偏铝酸钠溶液中加入少量盐酸46、偏铝酸钠溶液中加入氯化铵溶液47、金属铁溶于盐酸中48、铁粉与氯化铁溶液反应49、铜与氯化铁溶液反应50、硫化亚铁与盐酸反应51、硫化钠与盐酸反应52、硫化钠溶液中加入溴水53、氯化亚铁溶液中通入氯气54、向硫酸铁的酸性溶液中通入足量的H2S55、氯化铁溶液中滴加少量硫化钠溶液56、硫化钠溶液中滴加少量氯化铁溶液57、氯化铁溶液中滴加少量碘化钾溶液58、氯化铁溶液与氢氧化钠溶液反应59、氯化铁溶液跟过量氨水反应60、氯化铁溶液与硫氰化钾溶液61、氯化铁溶液跟过量锌粉反应62、锌与稀硫酸63、锌与醋酸64、锌与氯化铵溶液65、氯化铁溶液加入碘化钾溶液66、硫酸亚铁溶液中加用硫酸酸化的过氧化氢溶液67、硫酸亚铁溶液中加用硫酸酸化的高锰酸钾溶液68、四氧化三铁溶于浓盐酸69、氧化铁溶于盐酸70、氧化铁溶于氢碘酸溶液71、用氯化铁与沸水反应制氢氧化铁胶体72、向溴化亚铁溶液通入足量的氯气73、向溴化亚铁溶液通入少量氯气74、向碘化亚铁溶液通入足量氯气75、向碘化亚铁溶液通入少量氯气76、碘化钾溶液中加入氯水77、碘化钾溶液中加入过量氯水78、溴化钠溶液中加入氯水79、亚硫酸溶液中加入氯水80、亚硫酸溶液中加入氯化铁81、亚硫酸溶液中加入双氧水82、氯气通入水中83、氯气通入碳酸氢钠溶液中84、亚硫酸钠溶液中加入溴水85、亚硫酸钠溶液中加入双氧水86、二氧化硫通入溴水中87、单质铁溶于过量稀硝酸中(NO)88、过量单质铁溶于稀硝酸中(NO)89、单质铜与稀硝酸反应90、单质铜与浓硝酸反应91、铜片插入硝酸银溶液92、用氨水吸收少量SO293、用氨水吸收过量的SO¬294、稀硝酸中通入SO295、浓硝酸中通入SO296、氯化铵与氢氧化钠两种浓溶液混合加热97、向次氯酸钙溶液中通入SO298、用碳酸钠溶液吸收过量SO299、硫酸铜溶液中通入硫化氢100、硫酸铜溶液中加入硫化钠溶液101、电解饱和食盐水102、电解硫酸铜溶液103、电解氯化铜溶液104、电解熔融氯化钠105、电解熔融氧化铝106、二氧化锰与浓盐酸共热107、氯气通入冷的氢氧化钠溶液中108、氯气通入热的氢氧化钾溶液中109、次氯酸钙溶液通入过量的二氧化碳110、次氯酸钠溶液中加入浓盐酸111、氯酸钾与浓盐酸112、硫化钠、亚硫酸钠混合液中加入稀硫酸113、NO2溶于水114、NO2通入亚硫酸钠溶液115、硫化钠的第一步水解116、碳酸钠的第一步水解117、氯化钡溶液与硫酸反应118、硫溶于热的氢氧化钠溶液119、醋酸钡溶液与硫酸反应120、醋酸与氢氧化钾溶液反应121、醋酸与氨水反应122、苯酚溶于氢氧化钠溶液123、苯酚与氯化铁溶液反应124、苯酚钠溶于醋酸溶液125、苯酚钠溶液中通入少量CO2 126、碳酸钠溶液中加入过量苯酚127、碳酸钙跟甲酸反应128、甲酸钠跟盐酸反应129、小苏打溶液与甲酸溶液反应130、Na2C2O4溶液中加入酸性高锰酸钾溶液131、酸性高锰酸钾溶液与双氧水132、酸性氯化亚铁溶液与双氧水133、SO2通入酸性高锰酸钾溶液134、乙烯通入酸性高锰酸钾溶液生成CO2 135、乙酸乙酯与氢氧化钠溶液136、硬脂酸甘油酯与氢氧化钠溶液137、氯乙烷在氢氧化钠溶液中水解138、硝酸银溶液中滴入少量氨水139、硝酸银溶液中滴加氨水至过量140、葡萄糖发生银镜反应141、硫酸铜溶液中加入氢氧化钠溶液142、硫酸铜溶液中加入少量氨水143、硫酸铜溶液中加入过量氨水144、硫酸锌溶液中加入少量氨水145、硫酸锌溶液中加入过量氨水146、甘氨酸与氢氧化钠溶液147、甘氨酸与盐酸溶液148、邻羟基苯甲酸与氢氧化钠溶液149、邻羟基苯甲酸与碳酸氢钠溶液150、邻羟基苯甲酸与碳酸钠溶液。
高中有机化学方程式汇总(全)(已免费)

高中有機化學方程式匯總1. CH4 + Cl 2光照CH3Cl + HCl2. CH3Cl + Cl 2光照CH2Cl2 + HCl3. CH2Cl + Cl 2光照CHCl 3 + HCl4. CHCl 3 + Cl2光照CCl4+ HCl5. CH4高温 C +2H26.C H催化剂 C H+ C H3418161688加热、加压4 ↑+ Na233CaOCH7. CH COONa + NaOH△CO8. CH2 = CH2 + Br2CH2Br—CH2Br9. CH2 = CH2 + H2O 催化剂CH3CH2OH22+ HBr催化剂CH3—CH2Br 10. CH = CH△22+ H2催化剂CH3—CH311. CH = CH△22催化剂[ CH 2—CH2]n12. nCH = CH13. nCH =CH-CH=CH2催化剂[CH -CH=CH-CH ]22 2 n14. 2CH2 = CH2 + O2催化剂2CH3CHO15. CH≡CH + Br 2CHBr = CHBr16. CHBr = CHBr+ Br 2CHBr 2- CHBr 217. CH≡CH + HCl催化剂H 2C = CHCl△18. nCH2 = CH[ CH2-CH ] nCl Cl19.CH≡CH + H 2O 催化剂 CH3CHO20.CaC2 + 2H2OCH ≡CH↑+ Ca(OH)221.催化剂Br + HBr + Br222.+ HO-NO2浓硫酸NO2+H2O△23.+ HO-SO3H △SO3H+H 2O24.+ 3H2催化剂△CH3CH325.+3HO-NO2催化剂O2N NO2+3H O226.→NO3CH≡ CH227. CH3CH 2Br + H2O NaOH CH 3CH2OH + HBr28. CH3CH 2Br + NaOH H 2O CH 3CH2OH + NaBr29. CH3CH 2Br+ NaOH醇CH2 = CH2 + NaBr +H 2O△30.2CH3CH 2OH+2Na2CH3CH2ONa + H2↑31.2CH3CH 2OH+O2催化剂2CH3CHO + 2H2O △32OH浓硫酸CH2= CH2↑+ H2O32. CH CH170℃33.C2H5OH+C2H5OH 浓硫酸C2H5OC2H5+H2O140℃34.OH+NaOH ONa+H2O35.OH+H2O O-+H3O+36.ONa+H2O+CO2OH+ NaHCO3OH OHBr↓Br+3HBr37.+3Br2Br催化剂CH3CH2OH 38. CH3CHO + H 2△催化剂2CH3COOH 39. 2CH3CHO + O2△40. CH3CHO+2Ag(NH 3)2 OH △↓ +3NH3+H2O CH3COONH 4+2Ag41CH3CHO+2Cu(OH)2△CH3COOH+Cu 2O↓ +2H 2O42. 2CH3COOH+2Na2CH 3COONa+H2↑43.2CH3COOH+Na2CO32CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3CH 3COONa+H 2O+CO 2↑45. CH3COOH + NaOH CH3COONa + H2O46. 2CH 3COOH + Cu(OH) 2(CH 3COO) 2Cu + 2H 2O 47.CH 3COOH+CH 3CH 2OH浓硫酸 CH 3COOCH 2CH 3 +H 2O△ 48. CH 3COOCH 2CH 3 +NaOH CH 3COONa+CH 3CH 2OH49. nOHCH 2CH 2COO H →[ OCH 2CH 2C ] n +H 2O 50. C 6 H 12O 6 (s) + 6O 2 (g)6CO 2 (g) + 6H 2O (l) 51. C 6 H 12O 6 催化剂2CH 3CH 2OH + 2CO 252. C 12H 22O 11+H 2O 催化剂 C 6H 12O 6+ C 6H 12O 6蔗糖 葡萄糖 果糖53. C 12H 22O 11 + H 2O 催化剂2C 6H 12O 6麦芽唐 葡萄糖54. (C 6H 10O 5)n + nH 2O催化剂 n C 6H 12O 6 淀粉葡萄糖 6 10 5 ) n 2 O 催化剂 6 12 6 55. (C H O + nH △n C H O 纤维素葡萄糖 56.C 17H 33COO-CH 2催化剂 C 17H 35COO-CH 2C 17H 33COO-CH +3H 2 加热、加压C 17H 35COO-CH C 17H 33COO-CH 2C 17H 35COO-CH 2 57. C 17H 35COO-CH 2CH 2-OH C 17H 35COO-CH +3NaOH3C 17H 35COONa+ CH-OH C 17H 35COO-CH 2O O CH 2-OH 58. CH 2OH COOH+CH 2OH COOHC — C 浓硫酸 O O 2 △光CH 2- CH 2 1.CH 4Cl 2 HCl CH 3 Cl CH 3Cl Cl 2光 HCl CH 2 Cl 2 2.3.4.5.6.7.8.CH 2CH CH CH 2Br29.10.11.12.13.14.15.16.17.HOCH 2 (CHOH ) 4 CHO2Ag (NH 3 ) 2 OH HOCH 2 (CHOH )4 COONH 42Ag3NH 3H 2O18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1 )、银镜反应( 2)、乙酸乙酯的水解( 3 )苯的硝化( 4)糖的水解(5 )、酚醛树脂的制取( 6)固体溶解度的测定凡是在不高于 100 ℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学方程式汇总(46个)一、化合反应反应名称化学方程式备注
在氧气中燃烧发出白光,放出点燃1. 木炭完全燃烧C+OCO 22热量在空气中发出淡蓝色火焰,在点燃2. 硫磺燃烧氧气中发出蓝紫色火焰,产生S+OSO 22刺激性气味的气体,放出热量发出耀眼的白光,放出热量,点燃3. 镁带燃烧2Mg+O2MgO 2留下白色粉末点燃4. 红磷燃烧产生大量白烟,放出热量2PO 4P+5O2525. 铁丝在氧气中燃在氧气中火星四射,放出热量,点燃FeO 3Fe+2O342烧留下黑色固体△加热铜丝固体由红变黑 2CuO 2Cu+O2发出淡蓝色火焰,放出热量点燃7. 氢气燃烧2HO 2H+O222H是最清洁的能源2点燃8. 一氧化碳燃烧发出淡蓝色火焰,放出热量2CO 2CO+O229. 木炭和二氧化碳高温 2CO C+CO2反应放出热量;产物使紫色石蕊试CaO+HOCa(OH) 10. 氧化钙和水反应 22液变蓝,使无色酚酞试液变红 11. 二氧化碳和水反CO+HOHCO 产物使紫色石蕊试液变红 2223应白色粉末变成蓝色晶体,放出12. 硫酸铜粉末和水热量CuSO+5HOCuSO·5HO 4242反应 CuSO粉末用于检验物质是否4含有水二、分解反应反应名称化学方程式备注△碳酸受热分解HCO不稳定HO+CO↑ HCO232223正负极都产生气泡,负极产生的气体体积是正极产生气体通电14. 电解水的2倍2H↑+O↑ 2H O222负氢正氧,氢二氧一;工业上生产H 215. 高温煅烧大理石或高温工业上生产CaO+CO↑ CaCO23石灰石
16. 过氧化氢在二氧化产生大量气泡,放出热量锰的催化作用下分2HO2HO+O↑ 22222实验室制取O 2解17. 加热氯酸钾和二
氧+3O↑ 实验室制取O 2322△化锰的混合物蓝色晶体变成白色粉末,试管△18. 加热硫酸铜晶体CuSO·5HOCuSO+5HO 4242口产生无色液体三、置换反应反应名称化学方程式备注高温19. 木炭还原氧化铜产生红色固体+2CuO2Cu+CO↑ 2产生红色固体,试管口产生△20. 氢气还原氧化铜无色液体Cu+HO H+CuO22H有还原性,用于冶炼金属221. 镁带在二氧化碳中点燃产生黑色和白色固体+C 2Mg+CO2燃烧ZnCl+H↑ Zn+2HCl实验室制取H 22. 锌粒和稀盐酸反应222ZnSO+H↑ Zn+HSO实验室制取H 23. 锌粒和稀硫酸反应42242FeCl+H↑ Fe+2HCl Fe元素从0价变成+2价 24. 铁钉和稀盐酸反应22FeSO+H↑ Fe+HSO 25. 铁钉和稀硫酸反应422426. 铁丝和硫酸铜溶液FeSO+Cu Fe+CuSO铁丝表面产生红色固体44反应27. 铜丝和硝酸银溶液Cu+2AgNOCu(NO)+2Ag 铜丝表面产生银白色固体332反应四、复分解反应反应名称化学方程式备注28. 氢氧化镁治疗胃“泛Mg(OH)+
2HClMgCl+2HO 222酸” 29. 大理石或石灰石和稀CaCO+2HClCaCl+HO+CO↑ 实验室制取CO 32222盐酸反应 30. 硝酸银溶液和稀盐酸AgNO+HClAgCl↓+HNO 产生白色沉淀33反应 31. 氯化钡溶液和稀硫酸BaCl+HSOBaSO↓+
2HCl 产生白色沉淀2244反应32. 硫酸铜溶液和氢氧化CuSO+2NaOHCu(OH)↓+NaSO 产生蓝色沉淀4224钠溶液反应 33. 氯化铁溶液和氢氧化FeCl+3NaOHFe(OH)↓+3NaCl 产生红褐色沉淀33钠溶液反应 34. 碳酸钠溶液和石灰水NaCO+Ca(OH)CaCO↓+2NaOH 2323反应
35. 硫酸铜溶液和熟石灰CuSO+Ca(OH)Cu(OH)↓+CaSO 4224制取农药波尔多液36. 碳酸钠溶液和足量盐NaCO+2HCl2NaCl+HO+CO↑2322酸
反应37. 氯化钠溶液和硝酸银AgCl不溶于NaCl+AgNO AgCl↓+NaNO 33HNO 溶液反应338. 硫酸钠溶液和氯化钡BaSO不溶于4NaSO+
BaClBaSO↓+2NaCl 2424HNO 溶液反应 3 五、其他反应反应名称化学方程式备注点燃39. 甲烷燃烧产生淡蓝色火焰CO+
2HO CH+2O2242产生白色沉淀;石灰水在CO+Ca(OH)CaCO↓+40. 少量二氧化碳通入石223空气中变质;HO 灰水2石灰水用于检验CO 241. 少
量二氧化碳和氢氧NaOH在空气中变质;CO+2NaOHNaCO+HO 2232化钠
溶液反应NaOH溶液用于吸收CO 242. 氢氧化钠溶液吸收二SO+2NaOHNaSO+HO NaSO名称是亚硫酸钠223223氧化硫产生红色固体△43. 一氧化碳还原氧化铜尾气需要燃烧处理,防止CO+CuOCu+CO 2CO污染空气高温44. 一氧化碳还原氧化铁工业炼铁的主要反应3CO+FeO2Fe+3CO 232FeO+6HCl2FeCl+3HO 45. 盐酸除铁锈溶液变成棕黄色2332CuSO+HO CuO+HSO溶液变成蓝色 46. 硫酸溶解氧化铜固体4224 *固体小颗粒分散到气体中形成烟;小液滴分散到气体中形成雾。
**“烟雾”表示固体小颗粒和小液滴同时分散到气体中时的情形。
