化学周期表PPT课件
合集下载
高中化学元素周期表ppt课件

30
2.10e-与18e-微粒 把握住书写的规律技巧是关键。
原子
分子
阴离子 阳离子
10e- Ne
HF、H2O、 NH3、CH4
F-、
O2-、
N3-、
OH-、
NH
2
Na+、 Mg2+、 Al3+、 H3O+、 NH
4
18e-
Ar
HCl、H2S、 PH3、SiH4、 F2、H2O2、 N2H4、C2H6、 CH3OH、CH3F
5
基础回归 元素的性质与原子结构的关系
1.元素的性质决定于电子层数 和 最外层电子
,
主数要决定于
最外层电。子数
2.同一主族的元素,从上到下,原子核外电子层数依
次 增多,原子半径逐渐 增,大失电子能力逐
渐 增强,得电子能力逐渐
,减金弱属性逐渐
,非金增属强性逐渐 。
减弱
特别提醒 同主族元素性质不一定相似,如第ⅠA族
HF、H2O、NH3、CH4等。 ④任何元素都有零价,但不一定都有负价或正价。如
F无正价,Na、Mg、Al等无负价。
9
2.元素、核素、同位素
10
3.元素的相对原子质量 (1)目前已发现的110多种元素中,大多数都有 同位素。 (2)一种天然存在的元素的各种核素分占的比例 不一定相同,但所占的百分比组成不变。 (3)元素的相对原子质量是按各种天然同位素原 子所占的一定百分比算出来的平均值。元素周期表 和相对原子质量表中的数值就是元素的相对原子质 量,而非核素(或原子)的相对原子质量。
材料;②在周期表中的
F、Cl、附S、近P等探 索 研 制 农 药 的 材 料 ;
③在 过渡元素中寻找催化剂和耐高温、耐腐蚀的合
2.10e-与18e-微粒 把握住书写的规律技巧是关键。
原子
分子
阴离子 阳离子
10e- Ne
HF、H2O、 NH3、CH4
F-、
O2-、
N3-、
OH-、
NH
2
Na+、 Mg2+、 Al3+、 H3O+、 NH
4
18e-
Ar
HCl、H2S、 PH3、SiH4、 F2、H2O2、 N2H4、C2H6、 CH3OH、CH3F
5
基础回归 元素的性质与原子结构的关系
1.元素的性质决定于电子层数 和 最外层电子
,
主数要决定于
最外层电。子数
2.同一主族的元素,从上到下,原子核外电子层数依
次 增多,原子半径逐渐 增,大失电子能力逐
渐 增强,得电子能力逐渐
,减金弱属性逐渐
,非金增属强性逐渐 。
减弱
特别提醒 同主族元素性质不一定相似,如第ⅠA族
HF、H2O、NH3、CH4等。 ④任何元素都有零价,但不一定都有负价或正价。如
F无正价,Na、Mg、Al等无负价。
9
2.元素、核素、同位素
10
3.元素的相对原子质量 (1)目前已发现的110多种元素中,大多数都有 同位素。 (2)一种天然存在的元素的各种核素分占的比例 不一定相同,但所占的百分比组成不变。 (3)元素的相对原子质量是按各种天然同位素原 子所占的一定百分比算出来的平均值。元素周期表 和相对原子质量表中的数值就是元素的相对原子质 量,而非核素(或原子)的相对原子质量。
材料;②在周期表中的
F、Cl、附S、近P等探 索 研 制 农 药 的 材 料 ;
③在 过渡元素中寻找催化剂和耐高温、耐腐蚀的合
初三化学元素周期表(完整版).pptx

57-71 La-Lu 镧 系
57
La
镧
58
Ce
铈
59
Pr
镨
60
Nd
钕
61
Pm
钷
62 Sm 钐 150.3 (shān)
63 Eu 铕 151.96 (yǒu)
64
Gd
钆
65
Tb
铽
66
Dy
镝
67 Ho 钬 164.9 (huǒ)
68 Er 铒 167.2 (ěr)
69 Tm 铥 168.9 (diū)
47.9 50.94
(guī) (lín) (liú) (lǜ) (yà) (jiǎ) (gài)
(tài) (fán)
65.38 69.72 72.5
(xīn) (jiā) (zhě)
83.8 85.467 87.62 88.906
(kè) (rú) (sī) (yǐ)
1
42
Mo
钼
43
Tc
锝
44 Ru 钌 161.0 (liǎo)
学海无 涯
初三化学元素周期表 原子序数 元素符号 元素名称 相对原子质量 元素名称读音
1 H 氢 1.0079 (qīng)
2 He 氦 4.0026 (hài)
3
Li
锂
4
Be
铍
5 B 硼 10.811 (péng)
6
C
碳
7
N
氮
8 O 氧 15.999 (yǎng)
9
F
氟
10
Ne
氖
11 Na 钠 22.9898 (nà)
钇
40 Zr 锆 91.22 (gào)
各种形式的元素周期表PPT课件

各种形式的元素周期表
化学元素周期表的简介
▪ 化学元素周期表是1869年俄国科学家门捷列夫(Dmitri
Mendeleev)首创的,他将当时已知的63种元素依原子量 大小并以表的形式排列,把有相似化学性质的元素放在同 一行,就是元素周期表的雏形。在周期表中,元素是以元 素的原子序排列,最小的排行最先。表中一横行称为一个 周期,一列称为一个族。
过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。刚嫁入门的那天,就被小姑
子号称“铁姑”狠狠地捏了一把,新娘一生气,当时就休克了。
▪
这下不得了,娘家要上告了。铁姑的老爸和她的哥哥夜入县太爷府,把大印假偷走一直往西跑,跑到一个仙人
住的地方。
▪
这里风景优美:彩色贝壳蓝蓝的河,一只乌鸦用一缕长长的白巾牵来一只鹅 ,因为它们不喜欢冬天,所以要去
美,小心累着)
▪
硼铝镓铟铊 碰女嫁音他 (看来新郎新娘都
▪
氮磷砷锑铋 蛋临身体闭
▪
氧硫硒碲钋 养牛西蹄扑
▪
氟氯溴碘砹 父女绣点爱 (父女情深啊)
▪
氦氖氩氪氙氡 害耐亚克先动
▪
钽 钨 铼 锇 ---- 但(见)乌(鸦)(引)来鹅
▪
铱 铂 金 汞 铊 铅 ---- 一白巾 供它牵
▪
铋 钋 砹 氡 ---- 必不爱冬(天)
▪
第七周期:钫 镭 锕 ---- 防雷啊!
口诀背诵
▪ 纵列
▪
氢锂钠钾铷铯钫 请李娜加入私访 (李娜什么时候当
皇上啦)
▪
铍镁钙锶钡镭 媲美盖茨被累(呵!想和比尔.盖茨媲
箭环 头形 连, 接有 着点 各像 族四
驱 车 的 跑 道 ,
很有创意的元素周期表2
化学元素周期表的简介
▪ 化学元素周期表是1869年俄国科学家门捷列夫(Dmitri
Mendeleev)首创的,他将当时已知的63种元素依原子量 大小并以表的形式排列,把有相似化学性质的元素放在同 一行,就是元素周期表的雏形。在周期表中,元素是以元 素的原子序排列,最小的排行最先。表中一横行称为一个 周期,一列称为一个族。
过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。刚嫁入门的那天,就被小姑
子号称“铁姑”狠狠地捏了一把,新娘一生气,当时就休克了。
▪
这下不得了,娘家要上告了。铁姑的老爸和她的哥哥夜入县太爷府,把大印假偷走一直往西跑,跑到一个仙人
住的地方。
▪
这里风景优美:彩色贝壳蓝蓝的河,一只乌鸦用一缕长长的白巾牵来一只鹅 ,因为它们不喜欢冬天,所以要去
美,小心累着)
▪
硼铝镓铟铊 碰女嫁音他 (看来新郎新娘都
▪
氮磷砷锑铋 蛋临身体闭
▪
氧硫硒碲钋 养牛西蹄扑
▪
氟氯溴碘砹 父女绣点爱 (父女情深啊)
▪
氦氖氩氪氙氡 害耐亚克先动
▪
钽 钨 铼 锇 ---- 但(见)乌(鸦)(引)来鹅
▪
铱 铂 金 汞 铊 铅 ---- 一白巾 供它牵
▪
铋 钋 砹 氡 ---- 必不爱冬(天)
▪
第七周期:钫 镭 锕 ---- 防雷啊!
口诀背诵
▪ 纵列
▪
氢锂钠钾铷铯钫 请李娜加入私访 (李娜什么时候当
皇上啦)
▪
铍镁钙锶钡镭 媲美盖茨被累(呵!想和比尔.盖茨媲
箭环 头形 连, 接有 着点 各像 族四
驱 车 的 跑 道 ,
很有创意的元素周期表2
初中化学元素周期表 PPT课件 图文

返回
锂
元素名称锂 元素符号Li 原子序数3 相对原子质量(12C = 12.0000)6.941 英文名称Lithium 物理性质:状态:软的银白色金属,是最轻的金属。
返回
铍
元素名称铍
返回
元素符号Be
原子序数4
相对原子质量(12C = 12.0000)9.012182
返回
氯
元素名称氯 元素符号Cl 原子序数17 相对原子质量(12C = 12.0000) 35.4527 英文名称Chlorine 物理性质:状态:黄绿色卤气。
返回
氩
元素名称氩 元素符号Ar 原子序数18 相对原子质量(12C = 12.0000)39.948 英文名称Argon 物理性质:状态:无色、无臭、无味的惰性气体。
返回
铝
元素名称铝 元素符号Al 原子序数13 相对原子质量(12C = 12.0000)26.981539 英文名称Aluminum 物理性质:状态:银色,轻质,非磁性的可锻金属。
返回
硅
元素名称硅 元素符号Si 原子序数14 相对原子质量(12C = 12.0000)28.0855 英文名称Silicon 物理性质:状态:硬的深灰色非金属。
返回
氮
元素名称氮 元素符号N 原子序数7 相对原子质量(12C =12.0000) 14.00674 英文名称Nitrogen 物理性质:状态:无色、无味、无臭的气体。
返回
氧
元素名称氧 元素符号O 原子序数8 相对原子质量(12C = 12.0000)15.9994 英文名称Oxygen 物理性质:状态:无色、无臭、无味的气体。
第一节元素周期表(共40张PPT)
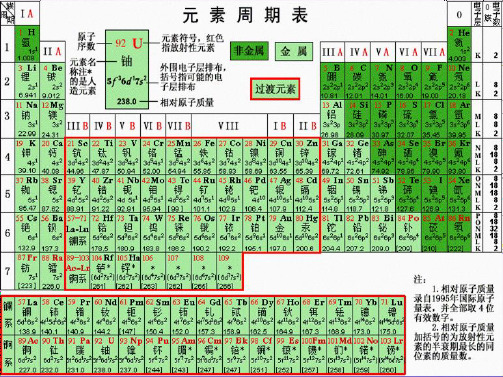
第ⅦA 族
与水缓慢反应
(2)原子结构特点 Cl2+H2O=HCl+HClO
静置后,液体分为两层。
通一过个以 12上C相质比量较同×,1点/思12考:钠和钾最的外性质层有 7个电子
静置后,液体分为两层。
和递变性。 (氧化性:Cl2 >I2)
核电荷数依次增多
不同点: 电子层数依次增多 上层无色,下层分别呈橙红色、紫红色
第一章 物质结构、元素周期律
第一节 元素周期表 一、元素周期表的结构
原子序数:依原子核电荷数由小到大的顺序给元素编号,这种
编号叫原子序数。
原子序数=核电荷数=质子数=核外电子数 (一)元素周期表的编排原则
1、横行: 把电子层数相同的各种元素按原子序数递增顺序
从左到右排列。
2、纵行: 把最外层电子数相同的各种元素按电子层数递增顺序 从上而下排成。
性逐渐增强,非金属性逐渐减弱。
2. 元素性质与原子结构有有密切的关系,主要与原子
核外的排布,特别是最外层电子数有关。原子结构
相似的一族元素,它们在化学性质上表现出相似性 和递变性。
1、砹(At)原子序数85,与F、Cl、Br、I同族,推测砹或
砹的化合物不可能具有的性质是( B)
A、砹易溶于某些有机溶剂 B、砹能与水剧烈反应
应越来越
,剧生烈成的氧化物越来越
。
最高复价杂氧化物对应水化物的碱性越来越 。
强
讨论1:Li与K 应如何保存? Li封存于固体石蜡中, 少量K保存于煤油中。
讨论2:碱金属与盐酸: 2R+2H+= 2R++H2 ↑ 讨论3:碱金属与盐溶液: 先与水反应
讨论4:Li+、Na+、K+、Rb+、Cs+也具有强还原性吗? 没有。 有较弱的氧化性。 氧化性: Li+ > Na+ > K+ > Rb+ > Cs+
51元素周期表(精品课件 ppt--高中化学

o (3)表中能形成两性 氧化物的元素是 ________(填名称),分 写出 元素的 氧化物与⑥、⑨最高价氧化物的水化物反 的 化学方程式: _______________________
o (4) 一个 方案,比 ⑦、⑩ 氧化性的强弱:
o ____________________________
o (2) 跟水起 烈反 ,放出________色 气体,同 使滴有紫色石蕊 液的溶液 ________色,因 ____________________________ ___________(写出离子方程式)。
o (3)碳酸 的水溶液使酚 液 ________色,因 ____________________________ ____________________________ ________________(用离子方程式表示 )。
o 三、核素 o 1.原子 o (1)原子 构:
o (2)有关粒子 的关系 o ① 量数(A)=________+________; o ②中性原子: 子数=________=
________;
o ③阳离子: 子数=核外 子数+ ________;
o ④阴离子: 子数=核外 子数- ________。
o A. 子数、中子数 o B. 子数、最外 子数 o C.中子数、最外 子数 o D.最外 子数、 量数 o 答案:B
o 2.(2008·四· 川高考)下列叙述中正确的是 o ()
o A.除零族元素外,短周期元素的最高化合价 在数 上都等于 元素所属的族序数
o B.除短周期外,其他周期均有18种元素 o C.副族元素中没有非金属元素 o D.碱金属元素是指第ⅠA族的所有元素 o 答案:C
o ③元素:具有相同________的同一 ________的 称。
o (4) 一个 方案,比 ⑦、⑩ 氧化性的强弱:
o ____________________________
o (2) 跟水起 烈反 ,放出________色 气体,同 使滴有紫色石蕊 液的溶液 ________色,因 ____________________________ ___________(写出离子方程式)。
o (3)碳酸 的水溶液使酚 液 ________色,因 ____________________________ ____________________________ ________________(用离子方程式表示 )。
o 三、核素 o 1.原子 o (1)原子 构:
o (2)有关粒子 的关系 o ① 量数(A)=________+________; o ②中性原子: 子数=________=
________;
o ③阳离子: 子数=核外 子数+ ________;
o ④阴离子: 子数=核外 子数- ________。
o A. 子数、中子数 o B. 子数、最外 子数 o C.中子数、最外 子数 o D.最外 子数、 量数 o 答案:B
o 2.(2008·四· 川高考)下列叙述中正确的是 o ()
o A.除零族元素外,短周期元素的最高化合价 在数 上都等于 元素所属的族序数
o B.除短周期外,其他周期均有18种元素 o C.副族元素中没有非金属元素 o D.碱金属元素是指第ⅠA族的所有元素 o 答案:C
o ③元素:具有相同________的同一 ________的 称。
元素周期表_课件PPT

人类在长期的生产活动和科学实践中,逐步认识了元 素间的内在联系和元素性质变化的规律性。那么同族元素 间有哪些规律存在呢?让我们一起走进丰富多彩的物质世 界,共同探讨元素的性质与原子结构的关系。
●梳理导引 1.碱金属元素原子的最外层都有______________个 电子,都是活泼的金属;且随核电荷数增加,电子层数逐 渐______________,原子半径逐渐______________,金属 性逐渐____________。 2.碱金属单质的物理性质:都有______________的 金属光泽,质______________,密度______________,熔 点____________,导电性和导热性都____________;随着 核电荷数增加,碱金属单质的熔、沸点逐渐____________, 密度逐渐____________[特殊的ρ(K)<ρ(Na)]。
4.比较元素金属性强弱的方法 (1)根据金属活动性顺序表判断。自左至右金属性减弱, 即失电子能力减弱,如:Zn>Cu。 (2)根据元素周期表判断。同周期,从左至右金属性减 弱 。 同 主 族 , 自 上 而 下 金 属 性 增 强 。 如 : Na>Mg>Al , Na<K。 (3)根据元素的单质与水(或酸)反应置换出氢的难易程 度判断。置换反应越易发生的元素金属性越强。如钾与水 比钠与水反应剧烈,则K>Na(金属性)。
溶液分上 下两层,下层呈 红棕色
Cl2+ 2NaBr===2NaCl+Br2
b.将少量新制的饱 和氯水加入盛有KI溶液 的试管,振荡后加CCl4, 振荡,静置
溶液分上 下两层,下层呈 紫红色
+I2
Cl2+2KI===2KCl
实验
c.将少量溴水加 入盛有KI溶液的试管, 振荡后加CCl4,振荡,
元素周期表ppt课件

元素周期表揭示了元素在生物地球化学循环中的作用,有助于理解 生态系统的物质循环和能量流动。
05
元素周期表的未来发展
新的元素发现与合成
合成新元素
随着科学技术的不断进步,科学家们 可能会合成更多超重元素,进一步丰 富元素周期表。
探索新元素特性
新元素的发现将有助于深入了解元素 的性质和行为,为科学研究和技术创 新提供更多可能性。
元素周期表的完善与修正
修正元素性质
随着新元素的合成和性质研究,元素周期表中的元素性质可能会得到修正和完 善。
调整周期表结构
根据新发现和研究成果,元素周期表的排列和分类可能会进行相应的调整和优 化。
元素周期表在未来的应用前景
科学研究
元素周期表在化学、物理、材料科学等领域的研究中发挥着重要作用,未来仍将 是科学家们的重要工具。
技术创新
元素周期表中的元素是许多技术和产品的关键组成部分,随着新元素的发现和应 用,将有助于推动技术创新和产业发展。
THANKS
感谢观看
材料分类与鉴别
元素周期表为材料分类和鉴别提 供了依据,有助于对不同材料进
行科学分类和鉴别。
在生命科学领域的应用
生物分子结构研究
元素周期表在解析生物分子结构中发挥了重要作用,例如蛋白质 和核酸的结构研究。
药物设计与研发
通过元素周期表,可以预测药物分子的性质和行为,有助于新药的 研发和优化。
生物地球化学循环
通过元素周期表,科学家可以了解材料的物理和 化学性质,从而在材料科学和工程领域进行有效 的应用。
促进化学和其他学科的发展
元素周期表为化学学科提供了基础框架,同时也 为其他学科提供了重要的参考和借鉴。
02
元素周期表中的元素
05
元素周期表的未来发展
新的元素发现与合成
合成新元素
随着科学技术的不断进步,科学家们 可能会合成更多超重元素,进一步丰 富元素周期表。
探索新元素特性
新元素的发现将有助于深入了解元素 的性质和行为,为科学研究和技术创 新提供更多可能性。
元素周期表的完善与修正
修正元素性质
随着新元素的合成和性质研究,元素周期表中的元素性质可能会得到修正和完 善。
调整周期表结构
根据新发现和研究成果,元素周期表的排列和分类可能会进行相应的调整和优 化。
元素周期表在未来的应用前景
科学研究
元素周期表在化学、物理、材料科学等领域的研究中发挥着重要作用,未来仍将 是科学家们的重要工具。
技术创新
元素周期表中的元素是许多技术和产品的关键组成部分,随着新元素的发现和应 用,将有助于推动技术创新和产业发展。
THANKS
感谢观看
材料分类与鉴别
元素周期表为材料分类和鉴别提 供了依据,有助于对不同材料进
行科学分类和鉴别。
在生命科学领域的应用
生物分子结构研究
元素周期表在解析生物分子结构中发挥了重要作用,例如蛋白质 和核酸的结构研究。
药物设计与研发
通过元素周期表,可以预测药物分子的性质和行为,有助于新药的 研发和优化。
生物地球化学循环
通过元素周期表,科学家可以了解材料的物理和 化学性质,从而在材料科学和工程领域进行有效 的应用。
促进化学和其他学科的发展
元素周期表为化学学科提供了基础框架,同时也 为其他学科提供了重要的参考和借鉴。
02
元素周期表中的元素
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
11
展示电子排布的周期表
2020年10月2日
12
演讲完毕,谢谢观看!
Thank you for reading! In order to facilitate learning and use, the content of this document can be modified, adjusted and printed at will after downloading. Welcome to download!
2020年10月2日
2
周期表的编排原则
按照原子序数递增的顺序从左到右排列
将电子层数相同的元素排成一个横行
把最外层电子数相同的元素(个别例外) 按电子层数递增的顺序从上到下排成纵行
2020年10月2日
3
周期表的结构
2020年10月2日
4
横的方面 7个周期(三短、三长、 (7个横行) 一不完全
周
7个主族:由短周期和长周期
期
元素共同构成的族(ⅠA~ⅦA)
表
7个副族:仅由长周期构成的族
(ⅠB~ⅦB)
纵的方面 (18个纵行)
Ⅷ族(3个纵行):Fe、Co、Ni等 9种元素
零族:稀有气体元素
2020年10月2日
5
同周期、同主族元素的递变规律
项目
同周期(左-右) 同主族(上-下)
原
核电荷数
依次增大
按周期元素数增加
子 最外层电子数
结
电子层数
构
原子半径
逐渐增多 相同
逐渐减小
相同 依次递增 逐渐增大
化合价
周期性变化
基本相同
元素的金属性和
非金属性
性 单质的氧化性还
质
原性
最高价化合物对 应水化物的酸碱
性
气态氢化物的 2020年10月稳2日定性
金属性减弱,非金属性增强 非金属性减弱,金属性增强
还原性减弱,氧化性增强 氧化性减弱,还原性增强
碱性减弱,酸性增强
酸性减弱,碱性增强
逐渐增强
逐渐减弱 6
决定
原子结构
反映
决定 反映
元素性质
反映 决定
元素在表中 台 型 元 素 周 期 表
2020年10月2日
8
扇形元素周期表
2020年10月2日
9
2020年10月2日
立 式 周 期 表
10
螺旋型周期表
2020年10月2日
汇报人:XXX 汇报日期:20XX年10月10日
13
元素周期表
2020年10月2日
1
1869年门捷列夫在继承和分析了 前人工作的基础上,对大量实验 事实进行了订正、分析和概括, 成功地对元素进行了科学分类。 他总结出一条规律:元素(以及 由它所形成的单质和化合物)的 性质随着相对原子质量的递增而 呈现周期性的变化。这就是元素 周期。
他还预言了一些未知元素的性质 都得到了证实。但是由于时代的局 限,门捷列夫揭示的元素内在联系 的规律还是初步的,他未能认识到 形成元素性质周期性变化的根本原 因。
